斑点追踪成像技术结合三维超声评价缺血性二尖瓣反流患者的乳头肌功能
孟 湘MENG Xiang
刘 昕2LIU Xin
斑点追踪成像技术结合三维超声评价缺血性二尖瓣反流患者的乳头肌功能
孟 湘1MENG Xiang
刘 昕2LIU Xin
目的应用斑点追踪成像(STI)及三维超声评价缺血性二尖瓣反流患者乳头肌的功能,并探讨缺血性二尖瓣反流(IMR)的影响因素,为临床预测IMR提供依据。资料与方法收集合并二尖瓣反流的缺血性心肌病患者76例为病例组,同时选取66例健康志愿者为正常对照组。两组受检者均行超声心动图及2D-STI检查,分别比较前后乳头肌的缩短率(AFS、PFS)、前后乳头肌(APM、PPM)到二尖瓣前瓣环的距离(APM-AMA、PPM-AMA)、二尖瓣瓣叶闭合面积(MLC)、乳头肌间距离(IPMD)、前后乳头肌相对于左心室前壁的角度变化(AngI、AngII)、前后乳头肌的纵向峰值应变(ALS、PLS)、纵向应变达峰时间(APT、PPT)及达峰延迟时间(DT)以及左心室舒张末期内径(LVIDD)、左心室舒张末期容积(LVEDV)、左心室射血分数(LVEF)。结果病例组与正常对照组LVIDD、LVEDV、LVEF相比,差异有统计学意义(P<0.05),两组AFS、PFS、IPMD、MLC、ALS、PLS及DT相比,差异有统计学意义(P<0.05)。ALS、PLS、AFS、PFS与LVEF呈正相关,与LVEDV呈负相关(P<0.05);MLC、IPMD、DT与LVEF呈负相关(P<0.05)。冠状动脉Gensini积分与ALS、PLS、MLC、AFS、PFS、IPMD有相关性,r值分别为-0.65、-0.78、0.54、-0.51、-0.57、0.49。经多元Logistic回归分析发现IPMD、MLC、PLS、DT与IMR有关联(P<0.05),OR值分别为1.26、1.32、1.37、1.52。结论 应用2D-STI技术能够准确评价心肌缺血导致的乳头肌功能障碍,并且IPMD及MLC增加、PLS减低、两组乳头肌运动不同步均为IMR的危险因素,该结果有助于临床预测IMR。
心肌缺血;二尖瓣闭锁不全;超声心动描记术,三维;斑点追踪成像;心室功能,左;乳头肌
缺血性二尖瓣反流(ischemic mitral regurgitation,IMR)指冠状动脉狭窄或闭塞致心肌供血不足引起的二尖瓣瓣叶闭合不良而出现反流[1],其对心功能影响较大,预后较差。既往研究均显示IMR是缺血性心肌病患者心力衰竭和死亡的危险因素,削弱单纯血运重建治疗的远期效果[2-3]。
二维斑点追踪成像(two-dimensional speckle tracking imaging,2D-STI)是利用斑点追踪原理在二维超声图像基础上选取一定范围感兴趣的心肌,测量心肌应变、应变率等,是一种客观、定量、实时、无创的评价局部心肌功能的新方法,可从纵向、径向对乳头肌形变进行评价[4]。本研究旨在应用2D-STI技术评价合并二尖瓣反流的缺血性心肌病患者的乳头肌功能,采用多元Logistic回归分析探讨IMR的影响因素,为临床预测缺血性心肌病患者二尖瓣反流提供较准确的依据。
1 资料与方法
1.1 研究对象 选择2015年9月-2016年3月于保定市第一中心医院心内科就诊的缺血性心肌病患者76例,其中男40例、女36例,年龄45~72岁。纳入标准:有心绞痛或心肌梗死病史;行冠状动脉造影显示冠状动脉狭窄>75%;行常规超声心动图检查伴有轻度及以上的二尖瓣反流者(反流面积/左心房面积>3.5%),窦性心律。排除标准:先天性心脏病、心肌病、心脏瓣膜病;心力衰竭;慢性阻塞性肺疾病。采集健康志愿者66例作为正常对照组,其中男35例、女31例,年龄43~68岁。入选标准:经常规体检排除心脏相关疾病及高血压、糖尿病等病史。所有入选对象均知情同意。两组临床资料见表1。
表1 两组临床资料比较(±s)

表1 两组临床资料比较(±s)
分组 例数 年龄(岁) 收缩压(mmHg) 舒张压(mmHg) 心率(次/分) 血脂(mmol/L)血糖(mmol/L)正常对照组 66 57.50±8.15 104.20±18.50 76.90±8.30 68.70±13.30 4.71±1.20 5.10±0.90病例组 76 56.40±7.63 124.40±17.90 81.10±11.50 71.80±14.40 5.24±1.40 5.40±0.80 t值 0.320 -2.460 -1.377 -0.820 -1.386 -1.039 P值 >0.05 >0.05 >0.05 >0.05 >0.05 >0.05
1.2 仪器和方法 采用GE Vivid E9彩色多普勒超声诊断仪,4V探头,频率1.5~4.0 MHz,5s探头,频率1.5~4.0 MHz,EchoPAC工作站对动态影像进行脱机分析。
1.2.1 二维测量 受检者取左侧卧位,平静呼吸状态下同步记录心电图,连续采集3个心动周期的心尖四腔、二腔及胸骨旁左心室长轴观二维动态灰阶图像,确保乳头肌能完整显现,必要时采用非标准切面。①测量两组乳头肌舒张末期及收缩末期长度,进而得出乳头肌缩短率(fractional shortening,FS);②乳头肌移位:测量收缩期前乳头肌尖端到二尖瓣前瓣环的距离(length between the anterolateral papillary muscle tips and the contralateral anterior mitral annular,APM-AMA)和后乳头肌尖端到二尖瓣前瓣环的距离(length between the posteromedial papillary muscle tips and the contralateral anterior mitral annular,PPM-AMA)(图1A);于左心室乳头肌短轴切面,收缩期测量乳头肌间距离(interpapillary muscle distance,IPMD)[5](图1B);以左心室腔中心为原点,测量前后乳头肌相对于左心室前壁的角度变化(AngI、AngII);③检查过程中在2D模式下显像完整、清晰的心尖四腔观图像后转换至4D模式,嘱患者呼气后屏气采集动态三维全容积图像,调节图像,使二尖瓣前后叶及瓣环所围成的面积清晰显像,选择“面积(剪切平面)”按键,扫描计录收缩末期二尖瓣瓣叶与瓣环水平所围成的面积,得到瓣叶闭合面积(mitral leaflet closure,MLC),以了解瓣叶牵拉程度(图1C)。以上数据均测量3次取平均值。

图1 健康志愿者。于收缩期心尖四腔心切面测量APM-AMA(箭,A);左心室乳头肌短轴切面测量IPMD(B);三维全容积图像测量MLC(C);前外侧乳头肌应变曲线(D)
1.2.2 乳头肌各应变值的测量 采用EchoPAC工作站,应用STI技术将感兴趣区(ROI)分别定位于前后乳头肌,得到两条应变曲线,结合心电图和心动周期进行分析,测量参数:前乳头肌纵向应变(anterior longitudinal strain,ALS)(图1D)、后乳头肌纵向应变(posterior longitudinal strain,PLS)、前乳头肌纵向应变达峰时间(anterior peak time,APT)、后乳头肌纵向应变达峰时间(posterior peak time,PPT)以及延迟时间(delay time,DT)。每个数值测量3次,取平均值。
1.2.3 冠状动脉狭窄的程度与范围 以冠状动脉Gensini积分来表示。根据冠状动脉狭窄程度计分:≤25%计1分,26%~50%计2分,51%~75%计4分,76%~90%计8分,91%~99%计16分,100%计32分;根据狭窄部位乘以不同系数:左主干×5.0;回旋支开口处×3.5;左前降支近段、回旋支近段×2.5;左前降支中段×1.5;第一对角支、第二对角支、回旋支钝缘支、远段、右冠状动脉近段、中段、远段、后降支×1.0;右冠状动脉左心室后支×0.5,Gensini积分为各冠状动脉分支积分之和[6]。
1.2.4 重复性检验 随机抽取15例患者,由2名副主任医师以相同的方法对APM-FS、PPM-FS、IPMD、 MLC、ALS、PLS及DT等参数进行测量分析,用于观察者间的重复性检验;由同一名检查者对同一患者的动态图像再次进行分析,用于观察者内的重复性检验。1.3 统计学方法 采用SPSS 19.0软件。两组间参数比较采用两独立样本t检验;相关性检验采用Pearson相关性分析;采用逐步回归法筛选自变量,进行多元Logistic回归分析IMR的影响因素。以Bland-Altman分析法进行重复性检验。P<0.05表示差异有统计学意义。
2 结果
2.1 正常对照组及病例组参数比较 两组年龄、性别、左心房内径(left atrial diameter,LAD)、左心房面积(left atrial area,LAA)差异无统计学意义(P>0.05);左心室整体重构指标:左心室舒张末期内径(left ventricular end-diastolic diameter,LVEDd)、左心室舒张末期容积(left ventricular end-diastolic volume,LVEDV)、左心室射血分数(left ventricular ejection fraction,LVEF)差异有统计学意义(P<0.05);二维参数AFS、PFS、IPMD、MLC、ALS、PLS、DT差异均有统计学意义(P<0.05)。见表2、3及图2。
表2 两组一般参数比较(±s)
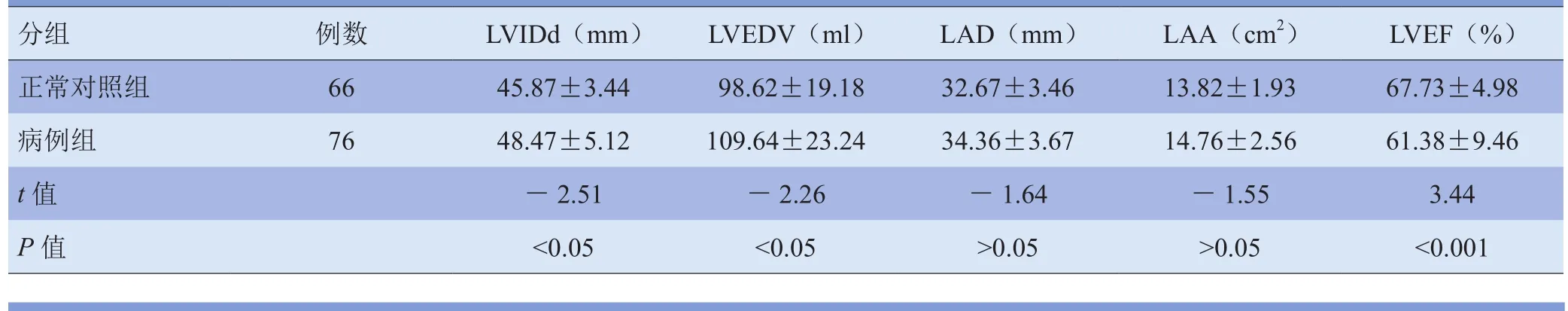
表2 两组一般参数比较(±s)
分组 例数 LVIDd(mm) LVEDV(ml) LAD(mm) LAA(cm2) LVEF(%)正常对照组 66 45.87±3.44 98.62±19.18 32.67±3.46 13.82±1.93 67.73±4.98病例组 76 48.47±5.12 109.64±23.24 34.36±3.67 14.76±2.56 61.38±9.46 t值 -2.51 -2.26 -1.64 -1.55 3.44 P值 <0.05 <0.05 >0.05 >0.05 <0.001
表3 两组二维测量及应变参数比较(±s)

表3 两组二维测量及应变参数比较(±s)
分组 例数 AFS PFS IPMD(mm) AngI AngII APM-AMA(mm)正常对照组 66 0.28±0.08 0.28±0.06 17.90±4.16 86.42±14.12 129.58±16.45 26.32±4.78病例组 76 0.20±0.09 0.21±0.04 23.80±8.19 90.10±16.54 136.58±14.45 27.29±4.32 t值 4.63 3.06 -3.72 -1.34 -1.29 -1.72 P值 <0.001 <0.01 <0.001 >0.05 >0.05 >0.05分组 例数 PPM-AMA(mm) MLC(cm2) ALS(%) PLS(%) DT(ms)正常对照组 66 25.12±4.69 1.30±0.35 -22.43±6.23 -22.94±5.45 19.30±5.57病例组 76 27.73±5.43 1.90±0.49 -16.80±5.88 -18.03±5.77 33.18±12.56 t值 -1.89 -5.70 -4.42 -3.92 -5.38 P值 >0.05 <0.001 <0.001 <0.001 <0.001
2.2 测量参数与左心室重构指标间的相关性 ALS、PLS、AFS、PFS、MLC、IPMD、DT与LVEF的相关系数分别为0.42、0.38、0.32、0.28、-0.36、-0.21、- 0.41(P<0.05),APM-AMA、PPM-AMA、AngI、 AngII与LVEF无相关性(P>0.05);ALS、PLS、AFS、PFS与LVEDV的相关系数分别为-0.25、-0.30、-0.21、-0.23,MLC、IPMD、DT、APM-AMA、PPMAMA、AngI、AngII无显著相关性(P>0.05)。而各参数与LVIDD无显著相关性(P>0.05)。
2.3 病例组乳头肌相关参数与Gensini积分的相关性病例组积分为(41.12±15.01)分。病例组AMP-AMA、PMP-AMA、AngI、AngII、DT与Gensini积分无相关性(P>0.05),ALS、PLS、MLC、AFS、PFS、IPMD与Gensini积分的相关系数分别为-0.65、-0.78、0.54、-0.51、-0.57、0.49(P<0.05)。
2.4 病例组相关参数行多元Logistic回归分析 将AFS、PFS、APM-AMA、PPM-AMA、IPMD、MCL、ALS、PLS、DT纳入方程,Logistic回归结果显示:IPMD及MLC增加、PLS降低、DT增加发生二尖瓣反流的风险更大(P<0.05)。见表4。
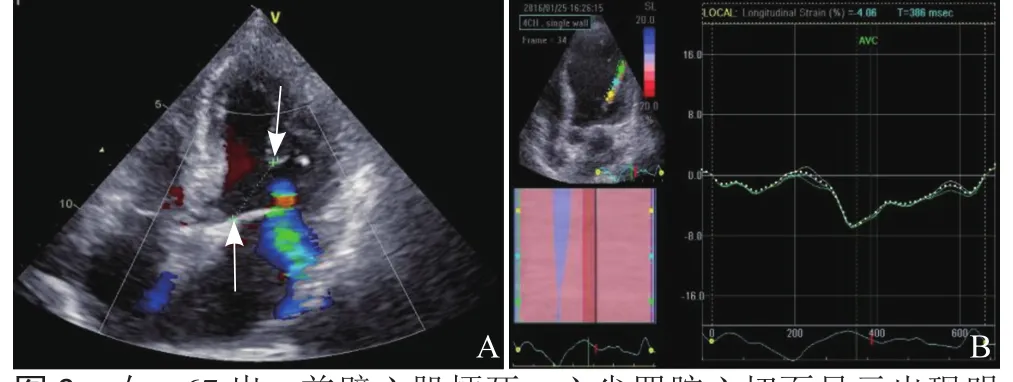
图2 女,67岁,前壁心肌梗死。心尖四腔心切面显示出现明显反流(A);前外侧乳头肌收缩功能减低,应变值降低(B)

表4 病例组IMR的影响因素
2.5 重复性检验 AFS、PFS、IPMD、MLC、ALS、PLS及DT等参数测量的观察者内和观察者间的变异系数分别约为3.48%、4.43%(APM-FS);3.52%、4.76%(PPMFS);3.73%、5.12%(IPMD);3.55%、4.80%(MLC);3.21%、4.98%(ALS);3.98%、5.21%(PLS);3.90%、4.12%(DT),测量重复性好。
3 讨论
心肌缺血可以影响二尖瓣装置的任一部分,以乳头肌、二尖瓣瓣环及左心室后壁最为常见。其中乳头肌功能不全是引起IMR最主要的原因[7]。乳头肌良好的功能可以保证牵拉住二尖瓣,防止瓣叶由于左心室收缩时压力迅速升高而脱入左心房侧,维持其正常功能。IMR目前仍然是缺血性心脏病最复杂、并且尚未解决的方面之一。IMR的发病机制复杂,虽然有多种治疗方法和措施,但缺乏统一的标准,远期的治疗效果仍处于探索阶段。目前针对二尖瓣反流的主要治疗方法是手术治疗,但是美国卫生实验研究院最近显示大约1/3的患者接受瓣环成形术后会出现二尖瓣反流复发[8]。因此深入了解IMR的发病机制有助于临床对患者实施个性化治疗,提高术后成功率,改善患者的生活质量。
本研究结果显示,病例组的PLS、ALS、APM-FS、PPM-FS减低,说明心肌缺血影响乳头肌时其收缩功能减低。二尖瓣装置中乳头肌做功最大,而且供应的血管多为冠状动脉终末支血管。当心肌缺血能量供应不足时,收缩功能易受到损害。此外,PLS、ALS、AFS、PFS与LVEF呈正相关、与LVEDV呈负相关,说明乳头肌收缩功能减低与左心室整体重构有关。病例组的MLC增加,心肌缺血累及乳头肌附近室壁时乳头肌位置改变,对二尖瓣的牵拉力增加,二尖瓣瓣叶闭合点下移,因此闭合面积增加。MLC与LVEF呈负相关,表明MLC同时也会受到左心室整体重构的影响,左心室整体重构致二尖瓣几何结构的改变,瓣环扩大,MLC增加。病例组的DT增大,说明缺血可以导致两组乳头肌运动不同步,这可能与两组乳头肌血供特点以及对缺血敏感程度不同有关。
本研究结果显示,病例组冠状动脉Gensini积分与PLS具有良好的相关性。因为乳头肌在收缩时承受着巨大的机械作用,加之两组乳头肌的供血特点:APM供血多来自左冠状动脉前降支的对角支和回旋支的边缘支双重供血,而PPM多由右冠状动脉的单支终支血管供应,故PPM对缺血更敏感,易受到缺血损害,随着冠状动脉狭窄程度的加重,收缩功能越差,应变值越低。IPMD与冠状动脉狭窄程度呈正相关,当心肌缺血早期不足以引起心脏形态学改变,常导致散在性心肌细胞营养不良、萎缩和纤维组织增生,随着缺血程度和范围加重,左心室发生形态学改变即局部重构,致乳头肌向外、向下、向后移位,IPMD增加。与Gensini积分作相关性分析发现2D-STI测得的ALS、PLS比二维超声心动图测得的AFS、PFS相关性好,表明2D-STI在评价乳头肌收缩功能方面优于二维超声心动图。
经Logistic回归分析结果显示,PLS降低、MLC及IPMD增加、DT增加为IMR的危险因素。二尖瓣瓣叶的正常闭合是由左心室压力和乳头肌牵拉力共同决定的,当PLS减低时,对二尖瓣的牵拉力减小,这两个力量不能平衡,则会导致二尖瓣瓣叶闭合不全。MLC的增加表明二尖瓣几何结构的改变对二尖瓣反流的发生有影响。Meris等[9]的研究发现二尖瓣闭合面积是预测二尖瓣反流程度的独立危险因素。最近研究也表明二尖瓣装置结构变形在缺血性二尖瓣反流发生机制中起着中心性作用[10]。乳头肌和腱索是直接连接二尖瓣的装置,在正常心脏结构中乳头肌平行于左心室长轴,垂直于瓣叶,平衡左心室作用在瓣叶表面的压力。当乳头肌移位时,IPMD会增加,导致其产生的张力不能垂直作用在瓣叶上,二尖瓣前后叶不能正常闭合,最终发生反流。DT的增加会使IMR发生的风险增大。Tigen等[11]运用2D-STI研究非缺血性扩张型心肌病患者二尖瓣反流机制中乳头肌运动不同步的重要性,得出与本研究一致的结果。此外,有研究将左心室整体运动同步性和二尖瓣反流进行研究,证明两者间具有密切关联[9,12-13]。二尖瓣在整个收缩期均保持严密的关闭状态,这不仅取决于二尖瓣、乳头肌结构及功能正常,也取决于乳头肌与室壁激动有适当的时间关系,乳头肌内含有丰富的浦肯野纤维,在等容收缩期左心室内压力增高时,乳头肌早已处在紧张状态,准备对作用于二尖瓣的压力予以支持,当心肌缺血后心肌发生不均匀复极化,乳头肌激动过早或过晚,均导致两组乳头肌不能同步收缩,就不能保证完整有效地牵拉住二尖瓣瓣叶。
本研究有一定的局限性:左心室乳头肌分为前、后两组,两组乳头肌多由多支组成,为了研究方便只选取其中较大支,而并未证明单支乳头肌和整体乳头肌的关系,有待进一步研究证实。此外,本研究未对IMR不同程度进行分组比较,进而分析随着IMR程度的加重各参数的变化情况,以及分析Gensini积分与IMR不同程度之间的关系,因此后期会针对性地进一步研究。
总之,本研究证实心肌缺血会导致乳头肌收缩功能损害及结构异常,并且随着冠状动脉缺血程度的加重,乳头肌的功能损害及结构变形也加重。同时探讨IMR的危险因素,有助于临床早期对乳头肌功能进行评估,对临床预测IMR具有重要的指导意义。
[1] Boyd JH. Ischemic mitral regurgitation. Circ J, 2013, 77(8): 1952-1956.
[2] Hickey MS, Smith LR, Muhlbaier LH, et al. Current prognosis of ischemic mitral regurgitation. Implications for future management. Circulation, 1988, 78(3 Pt 2): I51-I59.
[3] Rankin JS, Hickey MS, Smith LR, et al. Ischemic mitral regurgitation. Circulation, 1989, 79(6 Pt 2): 116-121.
[4] 何雪威, 宋则周, 郑哲岚, 等. 二维斑点追踪成像评价心尖肥厚型心肌病左心室局部功能. 中国医学影像学杂志, 2014, 22(6): 414-417.
[5] Silbiger JJ. Mechanistic insights into ischemic mitral regurgitation: echocardiographic and surgical implications. J Am Soc Echocardiogr, 2011, 24(7): 707-719.
[6] Gensini GG. A more meaningful scoring system for determining the severity of coronary heart disease. Am J Cardiol, 1983, 51(3): 606.
[7] 郭洁,杨军.超声心动图评价缺血性乳头肌功能不全的研究进展.医学综述, 2013, 19(20): 3769-3771.
[8] Sanz J, Weinsaft JW. Ischemic mitral regurgitation. J Am Coll Cardiol, 2014, 64(18): 1880-1882.
[9] Meris A, Amigoni M, Verma A, et al. Mechanisms and predictors of mitral regurgitation after high-risk myocardial infarction. J Am Soc Echocardiogr, 2012, 25(5): 535-542.
[10] Liang YJ, Zhang Q, Fang F, et al. Incremental value of global systolic dyssynchrony in determining the occurrence of functional mitral regurgitation in patients with left ventricular systolic dysfunction. Eur Heart J, 2013, 34(10): 767-774.
[11] Tigen K, Karaahmet T, Dundar C, et al. The importance of papillary muscle dyssynchrony in predicting the severity of functional mitral regurgitation in patients with non-ischemic dilated cardiomiopathy: a two-dimensional speckle-tracking echocardiograph study. Eur J Echocardiogr, 2010, 11(8): 671-676.
[12] Konstantinou DM, Papadopoulou K, Giannakoulas G, et al. Determinants of funcetional mitral regurgitation severity inpatients with ischemic cardiomyopathy versus non ischemicdilated cardiomyopathy. Echocardiography, 2014, 31(1): 21-28.
[13] 孔令秋, 伍洲, 席晶晶, 等. 扩张型心肌病患者二尖瓣乳头肌移位的超声研究. 中华超声影像学杂志, 2014, 23(12): 1013-1016.
(本文编辑 张晓舟)
Assessment of Papillary Muscle Function in Ischemic Mitral Regurgitation by Speckle Tracking Imaging Combined with Three-dimensional Ultrasonic Technology
PurposeTo evaluate papillary muscle function in ischemic mitral regurgitation (IMR) with two-dimensional speckle tracking imaging (2D-STI) and three-dimensional ultraphonic technology, and to investigate the primary factors influencing IMR so as to provide clinical information for the prediction of IMR.Materials and MethodsSeventy-six IMR patients were enrolled as research group and other 66 healthy volunteers as control group. Two groups were both examined by transthoracic echocardiography and 2D-STI. The parameters including fractional shortening of anterior and posterior papillary muscles (AFS, PFS), length of anterior or posterior papillary muscle tips to contralateral anterior mitral annular (APM-AMA, PPM-AMA), mitral leaflet closure (MLC), inter distance papillary muscle (IPMD), the angle between the anterior papillary muscle and the anterior LV free wall (Ang I) and the angle between the posterior papillary muscle and the anterior LV free wall (Ang II), anterior and posterior papillary muscle longitudinal strain (ALS, PLS) and peak time (APT, PPT), delay time (DT), left ventricular end-diastolic diameter (LVIDD), left ventricular end-diastole volume (LVEDV), and left ventricular ejection fraction (LVEF) were compared.ResultsCompared with control group, LVIDD, LVEDV, LVEF, AFS, PFS, IPMD, MLC, ALS, PLS and DT in research group were all significantly different (all P<0.05). ALS, PLS, AFS, and PFS had positive correlation with LVEF (P<0.05) and negative correlation with LVEDV (P<0.05). MLC, IPMD, DT had negative correlation with LVEF (P<0.05). ALS, PLS, MLC, AFS, PFS, IPMD were significantly correlated with Gensini score (r=-0.65, -0.78, 0.54, -0.51, -0.57, 0.49, respectively, P<0.05). The multivariant Logistic regression analysis showed that IMR was correlated with IPMD, MLC, PLS and DT (OR=1.26, 1.32, 1.37, 1.52, respectively, P<0.05).Conclusion2D-STI can accurately evaluate the papillary muscle dysfunction caused by myocardial ischemia. Moreover, the risk factors of IMR include increase of IPMD and MLC, decrease of PLS, and desynchronization of papillary muscles. These findings contribute to the clinical prediction of IMR.
Myocardial ischemia; Mitral valve insufficiency; Echocardiography, threedimensional; Speckle tracking imaging; Ventricular function, left; Papillary muscles
1. 河北承德医学院研究生学院 河北承德067000
2. 保定市第一中心医院超声科 河北保定071000
刘 昕
Department of Ultrasound, the First Central Hospital of Baoding, Baoding 071000, China
Address Correspondence to: LIU Xin
E-mail: lxlx001@126.com
R542.5;R445.1
2016-09-25
修回日期:2016-11-21
中国医学影像学杂志
2017年 第25卷 第3期:203-207
Chinese Journal of Medical Imaging
2017 Volume 25 (3): 203-207
10.3969/j.issn.1005-5185.2017.03.011

