热加工过程中棕榈油理化特性、脂肪酸与自由基的变化研究
姬彦羽,赵宏亮,魏 静,瞿兆蕙,曹 君,张伟敏,*
(1.海南大学食品学院,海南海口 570228;2.海南省产品质量监督检验所,海南海口 570203)
热加工过程中棕榈油理化特性、脂肪酸与自由基的变化研究
姬彦羽1,赵宏亮2,魏 静2,瞿兆蕙1,曹 君1,张伟敏1,*
(1.海南大学食品学院,海南海口 570228;2.海南省产品质量监督检验所,海南海口 570203)
以棕榈油(24 ℃)为原料,采用国标法测定棕榈油在不同温度(160、180、200 ℃)下常规理化指标(酸价、过氧化值、丙二醛值、p-茴香胺值和总氧化值)随时间的变化,在此基础之上,分别采用GC-MS法与电子自旋共振(ESR)法对180 ℃下棕榈油脂肪酸组成和自由基含量变化进行测定。结果表明,加热温度越高和加热时间越长棕榈油理化指标值越大,其中过氧化值呈现先上升后下降趋势。脂肪酸组成结果表明,棕榈油中饱和脂肪酸与不饱和脂肪酸比例约为1∶1,且随着加热时间延长,比例基本不变。ESR实验表明,加热时间越长,2-苯叔丁基硝酮(PBN)捕获的自由基量越多,棕榈油氧化程度越深。
棕榈油,热处理,脂肪酸组成,自由基
煎炸加工(Deep-fat frying process)是一种方便快速的食品烹调方式,广泛应用于食品加工中。在煎炸过程中,食品原料通常浸没在150~190 ℃油脂中进行加热[1]。棕榈油(Palm oil)因其色泽浅,热稳定性好,不易聚合,适用范围广,价廉物美等特点,已在世界范围内煎炸行业得到广泛应用。虽然如此,由于棕榈油中不饱和脂肪酸的存在,受煎炸过程中氧气、水、高温及食品组分的影响,不饱和脂肪酸发生一系列水解、氧化、热聚合的复杂反应,形成一些新的物质,如游离脂肪酸,过氧化物、聚合物和自由基等,使得棕榈油理化性质改变,进而引起煎炸油的品质发生变化。此外,脂肪酸的组成、顺式和反式脂肪酸的比例及生物活性物质的含量也都发生改变[2]。这些变化不仅严重影响了煎炸食品的品质,导致油炸食品的风味、感官品质、营养价值及贮藏时间随着煎炸时间的延长而逐渐降低,而且还会产生有毒有害物质影响人体健康[3-4]。
目前,有关煎炸和热处理对棕榈油品质影响研究主要集中于常规理化指标的影响,而有关棕榈油热处理过程中的丙二醛与自由基含量变化的分析很少。鉴于此,本研究以棕榈油为实验对象,采用国标法分析棕榈油热加工过程中(不同加热温度和时间)主要理化性质、脂肪酸组成和自由基含量的变化。在此基础上,探讨棕榈油热处理过程中脂肪酸组成与主要理化性质及其自由基含量变化之间的联系。以便为以后延长煎炸棕榈油使用寿命、减少煎炸食品在高温加热处理时劣变反应产生有害物质、开发煎炸油质量控制方法及手段提供理论基础和科学依据。
1 材料与方法
1.1 材料与仪器
新湖牌24 ℃餐饮专用棕榈油 茂名市广垦长晟粮油食品有限公司。
石油醚60-90,乙醇,浓盐酸,三氯甲烷,甲醇,EDTA-2Na,异辛烷,无水硫酸钠,冰醋酸,硫酸,正己烷 分析纯,西陇化工股份有限公司;氢氧化钾,过氧化氢(30%) 分析纯,广州化学试剂厂;酚酞,硫代巴比妥酸 分析纯,国药集团化学试剂有限公司;氯化亚铁,硫氰酸钾,还原铁粉,TCA,1,1,3,3-四乙氧基丙烷,p-茴香胺 分析纯,麦克林试剂;2-苯叔丁基硝酮(PBN):98%,百灵威科技有限公司。
EF-101V台式电炸炉 广州拓奇厨房设备有限公司;754NPC紫外可见分光光度计 上海奥谱勒仪器有限公司;HH-4数显恒温水浴锅、ZD-85气浴恒温振荡器 常州澳华仪器有限公司;HP6890/5975C GC-MS联用仪 美国安捷伦公司;JES FA200电子自旋共振仪 日本电子株式会社JEOL公司。
1.2 实验方法
1.2.1 样品处理 向电炸炉中添加适量棕榈油,分别设定在160、180、200 ℃下连续加热,按照杨美艳的方法[5],分别在0、0.25、0.5、1、2、4、8、12 h取样约50 mL,冷却至室温后,贮于棕色样品瓶中,-18 ℃下避光保存。
1.2.2 不同热处理对棕榈油理化性质的影响测定 酸价(AV)、过氧化值(POV)测定参考GB/T 5009.37-2003《食用植物油卫生标准的分析方法》,丙二醛值(MDA)测定参考GB/T 5009.181-2003《猪油中丙二醛的测定》,茴香胺值(PAV)测定参考GB/T 24304-2009《动植物油脂 茴香胺值的测定》,总氧化指数(TV)[6]计算公式为TV=2POV+PAV。实验均平行测定三次,计算平均值。
1.2.3 棕榈油热加工过程中脂肪酸组成的变化测定
1.2.3.1 样品甲酯化 称取样品约50 mg,放入密封瓶中,加1%硫酸甲醇溶液2 mL,在70 ℃恒温箱中加热1 h甲酯化后,加入2 mL正己烷萃取,超声震荡,静置,取出上层溶液,用纯水洗涤至中性,加入无水硫酸钠1 g(吸水),浓缩至2 mL备用。微量注射器注入1 μL甲酯化样品溶液。
1.2.3.2 色谱条件 色谱柱为ZB-5MSI 5% Phenyl-95% DiMethylpolysiloxane(60 m×0.25 mm×0.25 μm)弹性石英毛细管柱,柱温60 ℃,以6 ℃/min升温至150 ℃,保持7 min,运行54 min;汽化室温度250 ℃;载气为高纯He(99.999%);柱前压7.62 psi,载气流量1.0 mL/min;分流比20∶1,溶剂延迟时间:5.0 min。
离子源为EI源;离子源温度230 ℃;四极杆温度150 ℃;电子能量70 eV;发射电流34.6 μA;倍增器电压1358 V;接口温度280 ℃;质量范围29~500 amu。
1.2.3.3 对总离子流图中的各峰经质谱计算机数据系统检索及核对 Nist2005和Wiley275标准质谱图,用峰面积归一化法测定各成分的相对质量分数。
1.2.4 棕榈油热加工过程中自由基含量的变化分析
1.2.4.1 反应体系制备 将适量亲脂性自旋捕集剂PBN溶于无水乙醇,然后添加到棕榈油中,使PBN在棕榈油中的浓度为0.1 mg/g[7]。将添加PBN的棕榈油装入ESR光谱检测用4 mm石英离心管,在180 ℃下连续加热,以促使热氧化反应发生并产生自由基,分别在0、4、8、12 h取样,采用ESR光谱检测自由基信号强度。
1.2.4.2 ESR测定条件 中心磁场323.171 mT,扫描时间1 min,扫描范围200 G,微波频率9056.237 MHz,微波功率0.99800 MW,调制频率100.00 kHz,信号放大900倍,室温。
1.2.4.3 g值的确定 g值可以表征自由基的本质类型。通过测定ESR光谱的频率和磁域变化,为衡量产生的自由基类型,采用下列公式[8]进行计算:
g=hv/βH
式中:H为磁感应强度,Gs;v为微波频率,GHz;h为planck’s常数,6.62×10-34J·s;β为波尔磁场,9.27×10-24J/T。
1.3 数据处理
采用SPSS12.0软件对数据进行分析。采用GraphPad Prism 5.0软件和Origin 8.0软件对图表进行处理。
2 结果与分析
2.1 棕榈油热加工过程中酸价(AV)变化情况测定结果
棕榈油热加工过程中酸价(AV)的变化情况测定结果见图1。由图可以看出,棕榈油AV在160、180、200 ℃三个温度下均呈现出随着加热时间的延长而逐渐升高的趋势。三种加热温度连续12 h加热处理的棕榈油AV都没有超过GB 7102.1-2003《食用植物油煎炸过程中的卫生标准》中规定的酸价上限5 mg KOH/g,说明该棕榈油具有较好的热氧化稳定性。比较160、180、200 ℃下从初始酸价到4 h酸价的变化值,发现200 ℃(0.59 mg KOH/g)>180 ℃(0.43 mg KOH/g)>160 ℃(0.34 mg KOH/g)。然而,比较160、180和200 ℃下从8 h酸价到12 h酸价的变化值时,发现160 ℃(0.84 mg KOH/g)>180 ℃(0.69 mgKOH/g)>200 ℃(0.51 mg KOH/g)。说明在短时间的棕榈油氧化中,温度越高,酸价变化越大,然而在长时间的加热时,温度越高,酸价变化越小,推测其可能原因是因为高温比低温导致的氧化程度剧烈,并且比低温更快达到氧化平衡点。

图1 棕榈油热加工过程中酸价(AV)的变化情况Fig. 1 Effect of heat treatment on acid value(AV)of palm oil注:标有不同字母表示差异显著(p<0.05),图2~图5同。
2.2 棕榈油热加工过程中过氧化值(POV)的变化情况测定结果
棕榈油热加工过程中过氧化值(POV)的变化情况测定结果见图2。由图可知,棕榈油POV在160、180、200 ℃三个温度下随着加热时间的延长,其总体变化趋势并不完全一致。POV在180 ℃和200 ℃加热条件下随时间的延长呈现先上升而后下降趋势,这与杨滢[9]和方亚峰[10]的研究结果基本一致。结果表明温度越高,棕榈油POV也越大并达到POV最大点所需时间也越短。而棕榈油POV在160 ℃下随时间延长而呈逐渐升高趋势,这可能是因为热处理温度较低,氧化劣变不剧烈,过氧化值变化趋势也相对不太明显,因而棕榈油也能经受更长时间的加热。实验所选三种加热温度连续12 h加热处理的棕榈油POV也并未超过国际食品法典委员会制定的过氧化值标准限量值20 meq/kg。出现本实验这种情况的可能原因是,油脂在热加工过程中不饱和脂肪酸会发生自动氧化产生稳定性差的氢过氧化物而使过氧化值升高,继续受热又会导致其分解为小分子的醛、酮、酸等物质[11-13],从而又使过氧化值降低。由于油脂氧化产生的氢过氧化物同时存在着生成和分解两种作用,所以过氧化值反映的是油脂氧化和氧化分解的总趋势。过氧化值的大小则取决于氢过氧化物的生成和分解速率两者之间的快慢程度。当氢过氧化物生成速率大于分解速率,那么过氧化值呈上升趋势;反之,则下降[14-15]。因此,过氧化值只能反映棕榈油在高温处理初始阶段的氧化劣变情况,而不能将其看作衡量棕榈油氧化劣变程度的唯一指标。
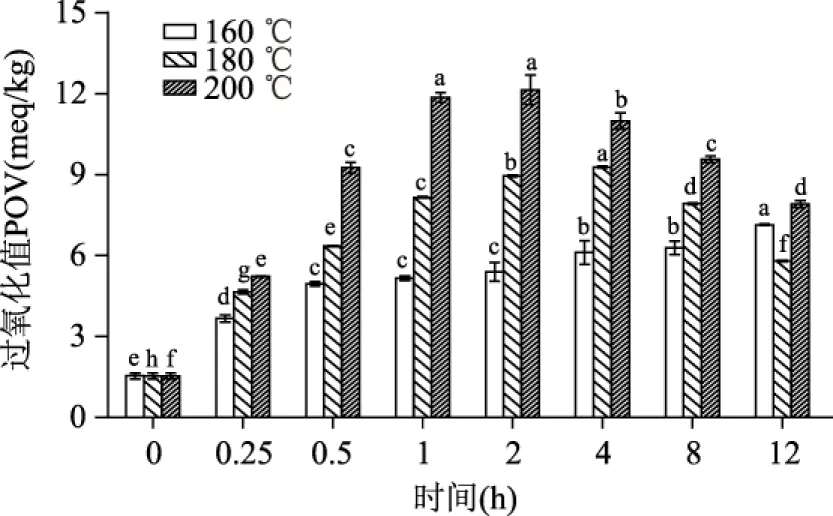
图2 棕榈油热加工过程中过氧化值(POV)的变化情况Fig.2 Effect of heat treatment on peroxide value(POV)of palm oil
2.3 棕榈油热加工过程中丙二醛(MDA)含量的变化情况测定结果
棕榈油热加工过程中丙二醛(MDA)的变化情况测定结果如图3所示。由图可知,MDA含量在160、180、200 ℃三个温度下均呈随着加热时间的延长而逐渐升高趋势。从0~12 h棕榈油MDA含量变化情况看,温度越高对MDA含量影响也越大。而在0~0.25 h范围内,三个加热温度下的MDA含量变化率最大,其变化值分别为6 μg%(160 ℃)、30 μg%(180 ℃)、49 μg%(200 ℃)。200 ℃下的变化值分别是160 ℃和180 ℃的8.17倍和1.63倍。说明温度越高,丙二醛生成的初始反应速率越大。从棕榈油MDA含量变化情况同样说明了棕榈油氧化变质程度随加热温度的升高和加热时间的延长而加剧,由于丙二醛具有较好的稳定性,因此能准确反映油脂的氧化程度[16-17]。

图3 棕榈油热加工过程中丙二醛值(MDA)的变化情况Fig.3 Effect of heat treatment on malondialdehyde value(MDA)of palm oil
2.4 棕榈油热加工过程中p-茴香胺值(PAV)的变化情况测定结果

图4 棕榈油热加工过程中p-茴香胺值(PAV)的变化情况Fig.4 Effect of heat treatment on p-anisidine value(PAV)of palm oil
棕榈油热加工过程中p-茴香胺值(PAV)的变化情况测定结果见图4。由图可以看出,棕榈油PAV在160、180、200 ℃三个温度下均随时间的延长而逐渐增加。PAV在0~1 h的变化趋势小于1~2 h。此外,三个温度对棕榈油PAV影响较显著。且温度越高对PAV的影响也越大,与丙二醛的影响结果基本相似。一般情况下,PAV越大,油脂中的醛类物质含量越高,油脂的氧化劣变程度越严重。所以PAV也可以作为衡量煎炸油劣变程度的一个重要标志。
2.5 棕榈油热加工过程中总氧化值(TV)的变化情况测定结果
棕榈油热加工过程中总氧化值(TV)的变化情况测定结果见图5。由图可知在160、180、200 ℃三个温度下,棕榈油TV的变化趋势类似于PAV的变化趋势,都是随时间的延长逐渐增加,且温度越高对棕榈油TV的影响也越大。TV常被用于评估脂类的氧化变质程度,它的优点是同时结合了一级氧化产物(氢过氧化物)与二级氧化产物(不饱和的醛类)的指标,更能全面的评价油脂氧化劣变程度[6]。
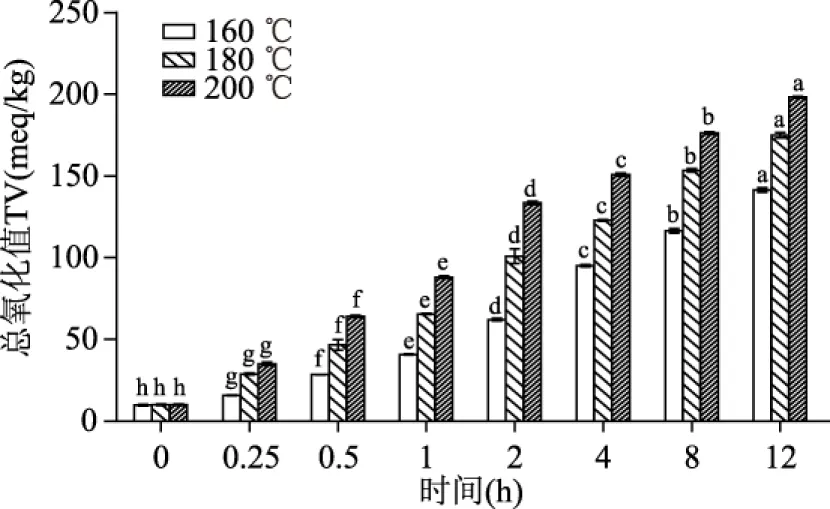
图5 棕榈油热加工过程中总氧化值(TV)的变化情况Fig.5 Effect of heat treatment on total oxidation value(TV)of palm oil
2.6 棕榈油热加工过程中脂肪酸组成的变化情况测定结果
根据理化指标分析结果,结合实际生活中常用的煎炸温度180 ℃,选择数据变化较为显著的0、4、8、12 h四个加热时间,研究不同加热时间对棕榈油脂肪酸组成变化的影响,以便进一步探讨热加工过程中棕榈油脂肪酸组成与理化性质变化之间的联系。具体结果见表1。

表1 棕榈油热加工过程中脂肪酸组成的变化情况(180 ℃)
由表1可以看出,未经热处理的棕榈油原料油,主要脂肪酸组成为棕榈酸42.63%、油酸28.19%,亚油酸22.27%以及硬脂酸4.050%和肉豆蔻酸1.31%,这五种脂肪酸共占棕榈油脂肪酸比例为98.450%。
通过比较0、4、8、12 h的棕榈油样品脂肪酸组成变化情况可以看出,以上五种脂肪酸均可检测到,脂肪酸组成具有一致性,并且总含量分别为98.45%、97.34%、97.07%和95.50%,呈逐渐下降趋势,说明随着加热时间的延长,棕榈油中脂肪酸氧化分解成其他小分子物质,导致脂肪酸总量的减少。且脂肪酸总含量减少幅度不是特别明显(减少2.95%)。未经热处理的棕榈油(0 h)饱和脂肪酸和不饱和脂肪酸比例接近1∶1,加热4、8、12 h的棕榈油样品中饱和脂肪酸和不饱和脂肪酸也基本比例接近1∶1,结果表明棕榈油随着加热时间延长,饱和脂肪酸和不饱和脂肪酸比例基本不变。说明棕榈油具有良好的氧化稳定性,适宜煎炸使用,这与曹亮[18]和季敏[19]的研究结果基本一致。
由表1还可以得出,棕榈油中多不饱和脂肪酸含量随着加热时间的延长,而呈逐渐下降趋势。这可能是因为多不饱和脂肪酸在热加工过程中不稳定,受高温影响而发生裂变、聚合等反应而氧化生成单不饱和脂肪酸和饱和脂肪酸,从而导致棕榈油中单不饱和脂肪酸和饱和脂肪酸的含量随加热时间的延长而不断增加,这与吴晓华[20]和徐婷婷[21]的研究结果相吻合。特别是从棕榈油中含量最多的棕榈酸、油酸、亚油酸含量随加热时间的变化情况来看,棕榈酸、油酸的含量随加热时间延长分别增加了2.39%和5.95%,而亚油酸含量则明显下降了11.96%,降幅为53.7%,这一变化趋势与王莹辉[22]研究结果相符。这说明了亚油酸的热稳定较差,容易发生热氧化等反应。随着加热时间的延长和亚油酸含量的降低,棕榈油主要理化指标(AV、POV、PAV、TV值、MDA含量)与自由基含量随之而升高,表明棕榈油中不饱和脂肪酸变化与理化性质及其自由基含量变化之间有内在联系。

图6 棕榈油热加工过程中自由基含量的变化情况(180 ℃)Fig.6 Effect of heat treatment on the free radical content of palm oil(180 ℃)
2.7 棕榈油热加工过程中自由基含量的变化情况测定结果
ESR的信号强度代表在共振条件下样品所吸收的总能量,即信号强度与样品中自由基含量即数目成正相关[23]。棕榈油热加工过程中自由基含量的变化情况如图6所示。由图可以看出,在自旋捕集剂PBN的捕集下,棕榈油自由基与PBN自旋加合所形成峰的形状在4、8、12 h三个时间点的峰形一致,峰的信号强度明显有差别。未加热棕榈油原料的ESR峰不明显,几乎没有,说明原料油中自由基含量少。从图还可以看出,随着加热时间的延长,ESR峰的信号强度明显增大,表明相同加热温度下(180 ℃),棕榈油中自由基含量随加热时间越长而提高,氧化程度越深。棕榈油在12 h连续热处理下,其不饱和脂肪酸减少了约6%,不饱和脂肪酸在自由基存在条件下,极易被氧化成次级产物,因此加热时间越长,由加热诱发的自由基数目越多,通过ESR检测到的自旋浓度越高。通过计算g值,可知棕榈油0、4、8、12 h的g值略有不同,说明PBN所捕集的自由基不是单一类型的,而是一些小分子自由基的总和,与陈家玉[7]研究结果一致。
3 结论与讨论
从本实验研究结果得出,棕榈油在160、180、200 ℃下连续加热过程中,棕榈油的酸价、过氧化值、丙二醛值、茴香胺值、总氧化值均呈上升趋势,其中过氧化值呈现先上升后下降趋势,且随温度升高理化指标变化越剧烈。ESR实验结果表明,棕榈油中自由基数量和含量随加热时间延长成逐步升高趋势。通过对棕榈油热加工过程中脂肪酸组成的变化情况分析,棕榈油中饱和脂肪酸与不饱和脂肪酸比例随加热时间延长而基本保持不变(始终接近1∶1),表明实验所选煎炸用棕榈油具有较好的氧化稳定性。但多不饱和脂肪酸(亚油酸)的含量却发生了较大变化,加热前后其含量减少了53.7%,表明亚油酸在热加工过程中发生了热氧化分解反应并与棕榈油主要理化性质及其自由基变化存在相关性。说明了亚油酸的变化不仅导致自由基数量和含量的升高,也使得棕榈油的酸价、过氧化值、丙二醛值、茴香胺值、总氧化值均呈上升趋势,从而影响棕榈油的品质和营养价值。
导致本实验结果的具体原因主要是:热处理条件下,油脂通过过氧化自由基和油脂分解从而生成各种短链的醛类、酮类、醚类、烃类和醇类等小分子化合物,发生酸败、氧化和分解等一系列反应。在高温加热过程中,不饱和脂肪酸发生氧化裂解生成活泼自由基开启油脂氧化的自由基链式反应。氧化初始阶段生成氢过氧化物,导致油脂过氧化值、酸价发生变化。氢过氧化物不稳定,在继续氧化过程中分解产生次级氧化产物,醛、酮、酸等小分子物质,对油脂的丙二醛值、茴香胺值产生影响。油脂氧化过程即包括初级氧化阶段和次级氧化阶段,不同阶段测定的指标不同,因此综合分析几种油脂理化指标更能准确反映油脂的氧化程度[24]。
此外,通过ESR实验也发现,由于PBN捕集剂只能捕集一些小分子自由基,并不能靶向捕集单一自由基,所以,在下一步的研究中可以尝试使用不同的自旋捕集剂,对目标自由基进行靶向捕集,从而实现检测棕榈油中某种单一自由基含量变化,有待于进一步深入研究。
[1]刘书香.棕榈油煎炸食品的质构及油脂肪酸与挥发性物质的变化研究[D].雅安:四川农业大学硕士研究生学位论文,2015.
[2]Andrikopoulos NK,Dedoussis GVZ,Falirea A,et al.Deterioration of natural antioxidant species of vegetable edible oils during the domestic deep-frying and pan-frying of potatoes[J]. International Journal of Food Sciences & Nutrition,2009,53(4):351-363.
[3]黄俊明,罗建波.油脂的热化学变化及其产物的毒性与检测[J].中国公共卫生,1993,9(4):166-168.
[4]周莉.食用油在煎炸中品质的变化及极性组分的快速检测技术研究[D].重庆:西南大学,2009.
[5]杨美艳. 食用油热加工过程中反式脂肪酸的形成与控制[D].南昌:南昌大学,2012.
[6]Shahidi F,Wanasundara U N. Methods for measuring oxidative rancidity in fats and oils[M]. Food Lipids:Chemistry,Nutrition and Biotechnology. 2002:387-403.
[7]陈家玉. 迷迭香提取物抗鱼油氧化酸败及其抗自由基活性的研究[D].广州:广东工业大学,2015.
[8]Thomsen M K,Lauridsen L,Skibsted L H,et al. Two types of radicals in whole milk powder. Effect of Lactose Crystallization,Lipid Oxidation,and Browning Reactions[J]. Journal of Agricultural and Food Chemistry,2005,53(3):1805-1811.
[9]杨滢,陈奕,张志芳,等. 油炸过程中3种植物油脂肪酸组分含量及品质的变化[J]. 食品科学,2012,23:36-41.
[10]方亚峰,周婷,陶丽媛,等. 食用油在持续煎炸过程中品质的变化与评价[J]. 粮食与食品工业,2016,02:32-34,39.
[11]Ramadan M F,Afify Amer M M,Mohamed A S. Correlation between physicochemical analysis and radical-scavenging activity of vegetable oil blends as affected by frying of French fries[J].J. Lipid Sci. Technol,2006(108):670-678.
[12]Dulkarim A B,Long S M,Lai O M,et al. Frying quality and stability of high-oleic Moringa oleifera seed oil in comparison with other vegetable oils[J].Food Chemistry,2007(105):1382-1389.
[13]Caiping S,Pamela W. Frying stability of high-oleate and regular soybean oil blends[J].Journal of the American Oil Chemists’ Society,2004,81(8):783-788.
[14]S. Esposto,A. Taticchi,I. Di Maio,et al. Effect of an olive phenolic extract on the quality of vegetable oils during frying[J].Food Chemistry,2015(176):184-192.
[15]Nadia Chammem,Salma Saoudi,Ines Sifaoui,et al.Improvement of vegetable oils quality in frying conditions by adding rosemary extract[J]. Industrial Crops and Products,2015(74):592-599.
[16]Supatcha Janporn,Chi-Tang Ho,Visith Chavasit,et al. Physicochemical properties of Terminalia catappa seed oil as a novel dietary lipid source[J]. Journal of Food and Drug Analysis,2015,23(2):201-209.
[17]Eunmi Koh,Jeonghee Surh. Food types and frying frequency affect the lipid oxidation of deep frying oil for the preparation of school meals in Korea[J].Food Chemistry,2015(174):467-472.
[18]曹亮. 茶油煎炸后品质变化及评价[D].哈尔滨:东北农业大学,2015.
[19]季敏,张剑,谢凤,等. 以棕榈油为基础的鱼制品煎炸用油及其氧化稳定性研究[J]. 粮食与油脂,2016,02:65-67.
[20]吴晓华. 棉籽油煎炸性能的研究[D].郑州:河南工业大学,2014.
[21]徐婷婷,李静,阚丽娇,等. 不同脂肪酸组成的食用油热氧化稳定性研究[J].食品工业科技,2013,24:93-97.
[22]王莹辉. 米糠油的煎炸应用研究[D]. 郑州:河南工业大学,2014.
[23]Paula Mariela González,María Belén Aguiar,Gabriela Malanga,et al. Electronic paramagnetic resonance(EPR)for the study of ascorbyl radical and lipid radicals in marine organisms[J]. Comparative Biochemistry and Physiology,Part A,2013(165):439-447.
[24]曹君,李红艳,邓泽元. 植物油氧化稳定性的研究进展[J]. 食品工业科技,2013,07:378-382,386.
Change of palm oil on physicochemical properties,fatty acid composition and free radical content during heat processing
JI Yan-yu1,ZHAO Hong-liang2,WEI Jing2,QU Zhao-hui1,CAO Jun1,ZHANG Wei-min1,*
(1.College of Food Science,Hainan University,Haikou 570228,China;2.Hainan Provincial Product Quality Supervision and Inspection Institute,Haikou 570203,China)
Palm oil(24 ℃),as raw material,was continuously heated at 160,180,200 ℃,and was sampled at different time points. Palm oil physicochemical indexes,including acid value(AV),peroxide value(POV),malondialdehyde(MDA),p-anisidine value(PAV),and total oxidation value(TV),were determined using the national standard method. In addition,the fatty acid composition and free radical content of palm oil were determined by GC-MS method and electron spin resonance(ESR)method,respectively. The results showed that the higher the heating temperature and the longer the heating time,the higher the values of the palm oil physical and chemical indicators. The peroxide value showed a trend of first increase and then decrease. The fatty acid composition showed that the ratio of saturated fatty acids and unsaturated fatty acids in palm oil was 1∶1,and the proportion was almost unchanged during the heating time.ESR experiments showed that the longer the heating time,the more free radicals captured by PBN,the greater the degree of oxidation of palm oil.
palm oil;heat treatment;fatty acid composition;free radical
2016-09-28
姬彦羽(1992-),女,硕士研究生,研究方向:热带特色食物资源开发与利用,E-mail:1054032161@qq.com。
*通讯作者:张伟敏(1979-),男,硕士,副教授,研究方向:热带特色食物资源开发与利用,E-mail:zhwm1979@163.com。
国家自然科学基金项目(31660495);海南省自然科学基金项目(20153076);海南省自然科学基金项目(314378)。
TS225.1
A
1002-0306(2017)05-0066-06
10.13386/j.issn1002-0306.2017.05.004

