用结晶—重结晶法制备高纯硝酸铈
乔 军,马 莹,王晶晶,杨启山,梁 超,阮 帅
(1.白云鄂博稀土资源研究与综合利用国家重点实验室,内蒙古 包头 014030;2.包头稀土研究院,内蒙古 包头 014030;3.瑞科稀土冶金及功能材料国家工程研究中心有限公司,内蒙古 包头 014030;4.内蒙古科技大学 化学与化学工程学院,内蒙古 包头 014010 )
用结晶—重结晶法制备高纯硝酸铈
乔 军1,2,3,马 莹1,2,3,王晶晶1,2,3,杨启山4,梁 超4,阮 帅4
(1.白云鄂博稀土资源研究与综合利用国家重点实验室,内蒙古 包头 014030;2.包头稀土研究院,内蒙古 包头 014030;3.瑞科稀土冶金及功能材料国家工程研究中心有限公司,内蒙古 包头 014030;4.内蒙古科技大学 化学与化学工程学院,内蒙古 包头 014010 )
研究了高纯硝酸铈的结晶法制备及重结晶法纯化除杂,采用正交回归试验法考察了硝酸铈结晶过程中料液初始酸度、结晶温度、陈化时间对产品质量的影响,以及母液回收利用情况。结果表明:采用结晶—重结晶法可以获得高纯硝酸铈产品,其中非稀土杂质质量分数小于1.5×10-5;确定了洁净硝酸铈制备工艺条件。热分解机制研究结果表明,硝酸铈的组成为Ce(NO3)3·6H2O。
结晶;重结晶;硝酸铈;制备;纯化
稀土化合物的纯度直接决定材料的特殊性能,不同洁净度的稀土材料可以制备出不同性能要求的陶瓷材料、荧光材料、电子材料等。目前,随着稀土提炼技术的发展,洁净稀土化合物呈现出良好的市场前景,高性能稀土材料的制备对洁净稀土化合物提出了更高要求。洁净硝酸铈是人工晶体材料[1-2]、功能板材[3]、电化学防腐保护膜[4-5]、有机反应催化[6]等材料的基质材料之一,同时也广泛应用于农业种植[7]等领域。目前,采用溶剂萃取、离子交换、沉淀法制备高纯稀土硝酸盐的研究较多[8-16],而利用结晶—重结晶法制备高纯度、高洁净度的硝酸铈的研究较少。试验研究了硝酸铈产品的化学结晶—重结晶法制备,同时采用热分析法确定其结晶水含量。
1 试验部分
1.1 原料试剂
碳酸铈:w(CeO2/REO)≥99.99%,包头新源稀土新材料有限公司产品,其化学成分见表1;硝酸:优级纯,天津化工试剂厂;纯水:电导率≥18.0 MΩ·cm。
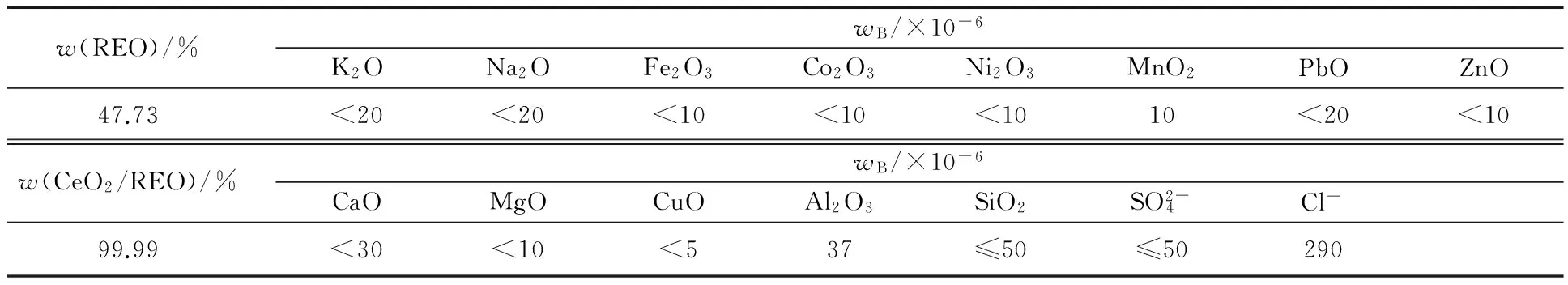
表1 碳酸铈原料的化学成分
1.2 分析方法
溶液中稀土浓度用EDTA络合滴定法测定,溶液酸度用氢氧化钠中和滴定法测定;硝酸铈中的钾、钠、钙、镁、铁、钴、镍、铝、铅、锌、铜等非稀土杂质元素采用等离子质谱法测定。
晶体形貌采用日本Hitachi公司S-3400N型扫描电子显微镜确定,产品TG-DSC曲线采用德国耐驰STA449F3型同步热分析仪测定(空气升温速度10 ℃/min,Al2O3),物相采用荷兰帕纳科全自动粉末衍射仪分析,产品结构采用德国傅丽叶全自动红外光谱仪确定。
1.3 试验原理和样品制备
对碳酸铈和硝酸反应得到的硝酸铈溶液进行加热浓缩、结晶,硝酸铈在晶体中富集,而非稀土杂质在母液中富集。试验工艺流程如图1所示。
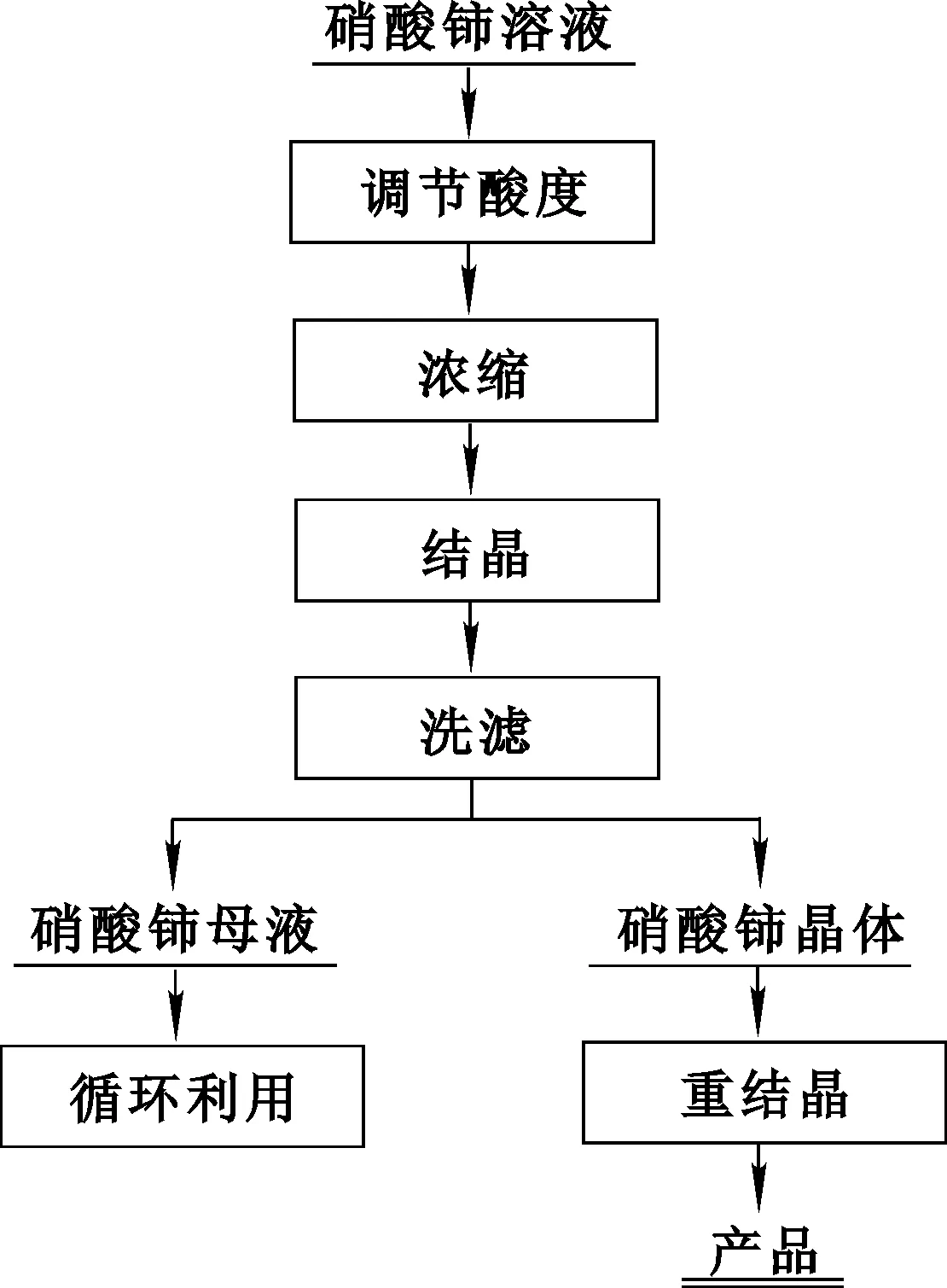
图1 结晶硝酸铈制备工艺流程
2 试验结果与讨论
2.1 正交回归试验设计及结果
试验选取料液酸度、结晶温度、陈化时间为影响因素,基准水平及变化间距见表2,正交回归试验结果见表3,硝酸铈收率方差分析结果见表4。
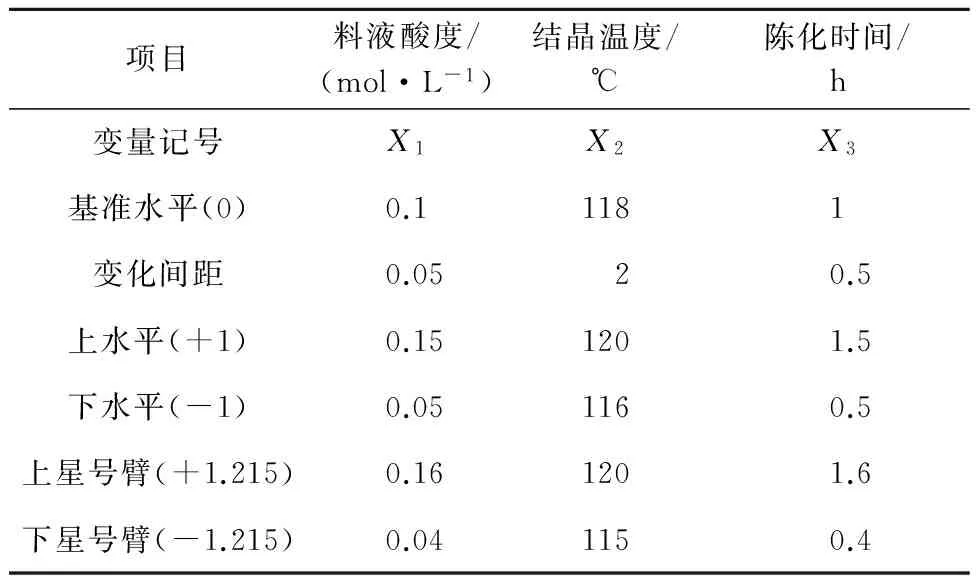
表2 基准水平及变化间距
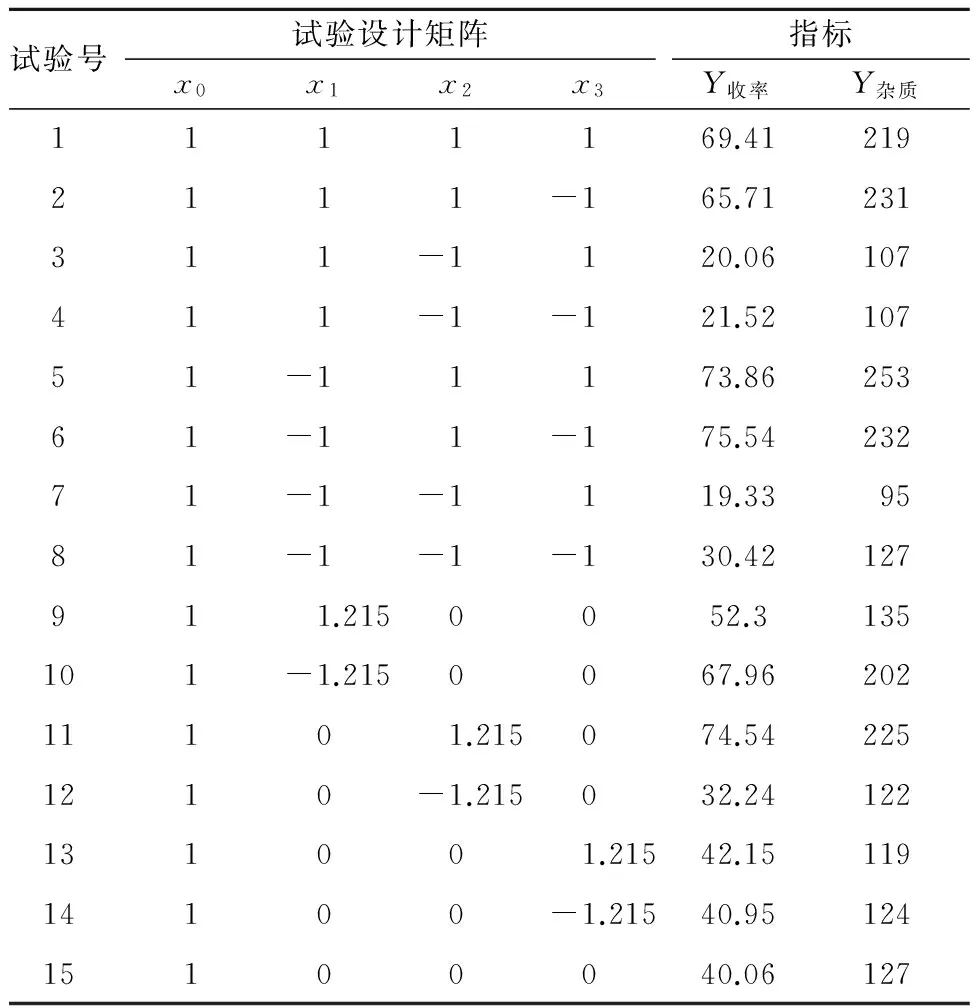
表3 正交回归试验结果

表4 硝酸铈收率方差分析结果

0.76x1x2+1.87x1x3+1.82x2x3+
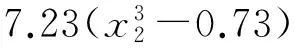
(1)
对每一项系数进行F检验,进而得到相应的简化方程(2);同理得到相应的简化方程(3):
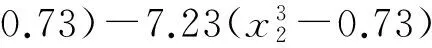
(2)

(3)
2.2 硝酸铈的结晶
2.2.1 结晶温度的影响
结晶温度对硝酸铈产品收率及非稀土杂质质量分数的影响试验结果如图2所示。

酸度/(mol·L-1):—▲—0.05 ;—●—0.10;—■—0.15。 图2 结晶温度对硝酸铈产品收率及非稀土 杂质质量分数的影响
由图2看出:随结晶温度升高,硝酸铈产品收率大幅度提高,酸度为0.05 mol/L条件下,结晶温度118 ℃时的收率为40%,122 ℃时的收率为80%,表明结晶温度越高,溶液越容易过饱和,析出的晶体量越大;随结晶温度升高,产品中非稀土杂质元素质量分数呈先缓后快的增大趋势,表明在较高的结晶温度下,非稀土杂质元素与稀土元素一起快速析出。
2.2.2 料液酸度的影响
料液酸度对硝酸铈产品收率及非稀土杂质质量分数的影响试验结果如图3所示。
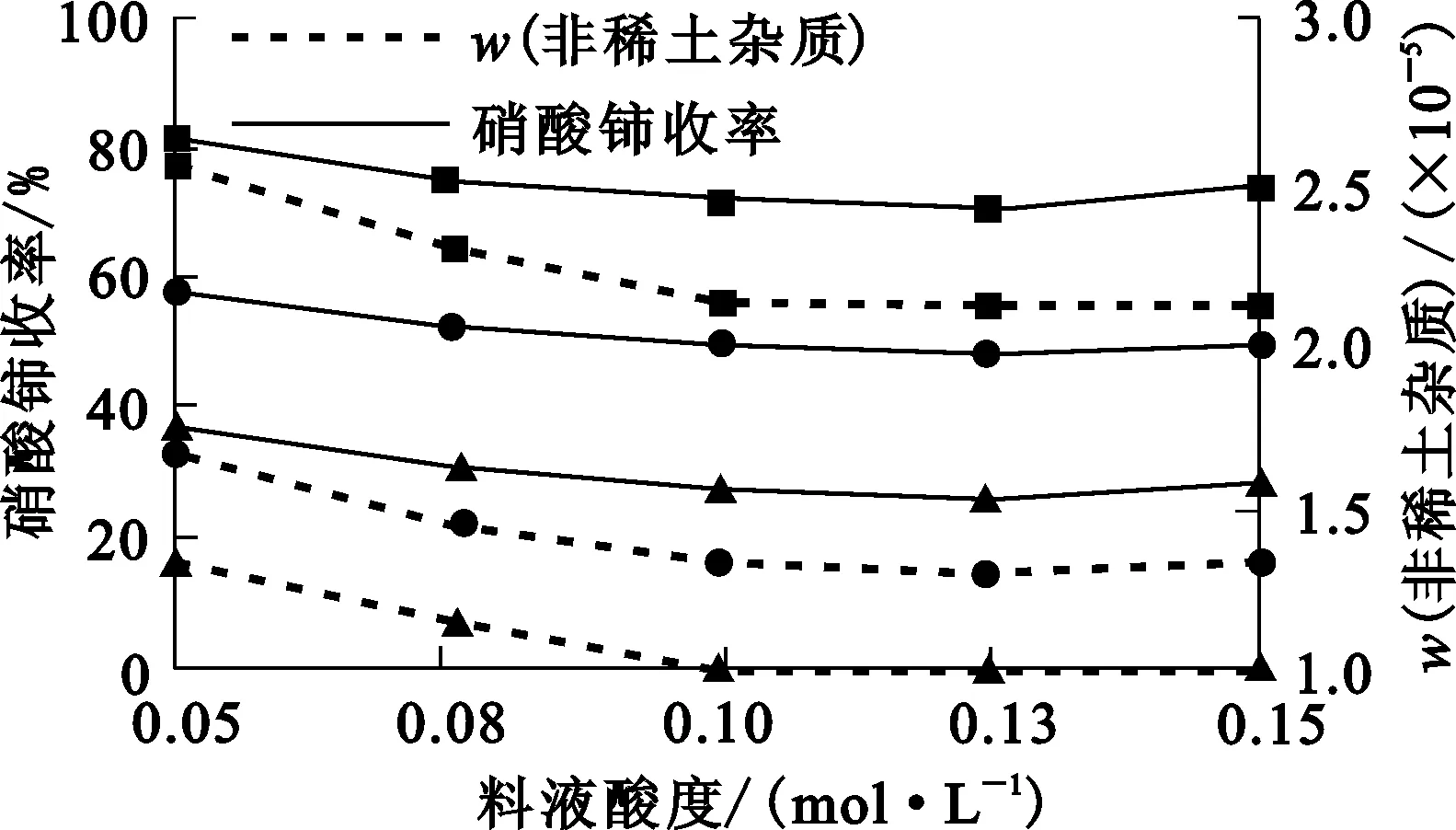
温度/℃:—▲—116 ;—●—118;—■—120。 图3 料液酸度对硝酸铈产品收率及非稀土 杂质质量分数的影响
由图3看出:随料液初始酸度增大,硝酸铈产品收率明显降低,因为料液酸度的改变会改变溶液的过饱和度,酸度升高,过饱和度降低,晶体析晶量减少,产品收率降低;随料液初始酸度增大,晶体中非稀土杂质元素质量分数减少,这是因为晶体在高酸度的过饱和溶液中析出时夹带的杂质元素更少。酸度过高,浓缩过程中的酸挥发现象加重,大部分氢离子被挥发掉,因此,适宜的料液酸度对去除非稀土杂质有利,但不宜过高。
2.2.3 陈化时间的影响
陈化时间对硝酸铈产品收率及非稀土杂质质量分数的影响试验结果如图4所示。
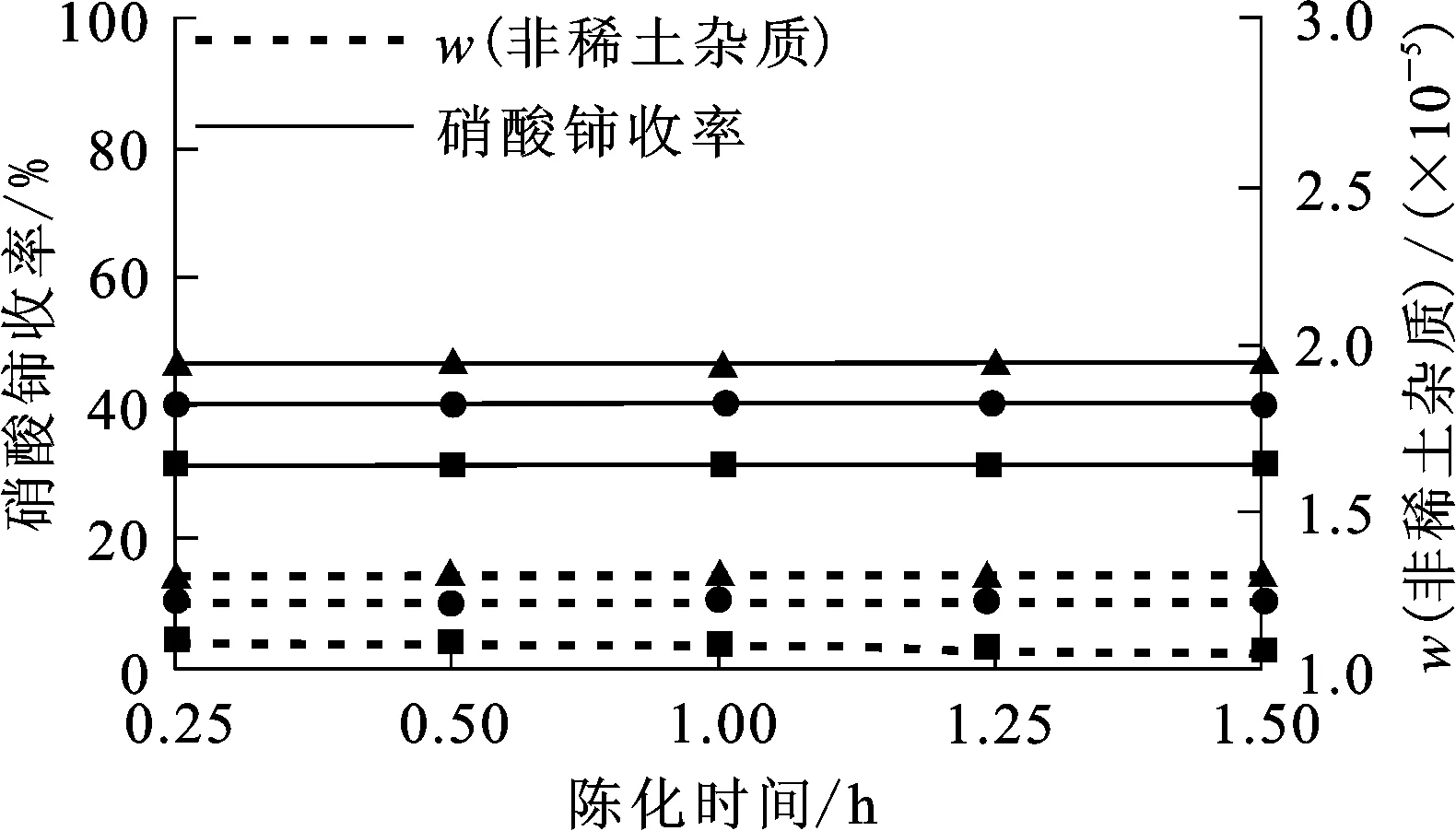
酸度/(mol·L-1):—▲—0.05 ;—●—0.10;—■—0.15。 图4 陈化时间对硝酸铈产品收率及非稀土 杂质质量分数的影响
由图4看出:陈化时间对硝酸铈晶体收率和非稀土杂质质量分数基本没有影响。试验中发现,随陈化时间延长,晶体颗粒在长大,而稀土总量和非稀土杂质质量分数变化不大,这可能是由于在晶体长大过程中,母液中的稀土元素及非稀土杂质元素也相应进入到晶体内部,在母液和晶体两相之间的分配达到平衡,不再发生变化。
方差分析和F检验结果表明:各因子的影响次序依次为结晶温度最显著,料液酸度较显著,陈化时间基本无影响。试验确定的适宜条件为:料液酸度0.10 mol/L,结晶温度118 ℃,陈化时间1 h。
2.3 硝酸铈母液的循环利用
控制溶液酸度、结晶温度进行结晶试验,结晶母液返回到硝酸铈溶液中循环利用。试验条件:料液酸度0.1 mol/L,结晶温度118 ℃,陈化时间1 h。硝酸铈母液循环次数对硝酸铈收率及非稀土杂质质量分数的影响试验结果如图5所示。

图5 母液循环次数对硝酸铈收率及非稀土 杂质质量分数的影响
由图5看出:母液不经循环,硝酸铈收率为70%;随母液开始循环,硝酸铈收率达90%左右。表明母液循环利用是可行的,循环使用到第4次后,晶体中杂质有明显富集,质量分数达2.06×10-5;母液循环到第5次后,杂质元素富集显著,尤其是Fe2O3(富集2倍)、Na2O(富集1.5倍)、CaO(富集2倍)、MnO2(富集2.5倍)、Al2O3(富集1.5倍)、PbO(富集2倍)等富集显著,杂质质量分数达2.73×10-5。试验中,结晶母液循环4次效果最佳,对硝酸铈的结晶行为和产品质量无明显影响。工业生产时的实际循环次数,随碳酸铈、硝酸等原料的质量变化而变化。当结晶母液中非稀土金属杂质质量分数超过规定要求后应回收其中的铈元素。
2.4 硝酸铈晶体的重结晶
对以结晶法获得的硝酸铈产品进行重结晶可以使产品中的非稀土杂质进一步降低,使产品更纯。取试验制备的硝酸铈晶体,于室温下加入超纯水搅拌溶解并调整酸度,再次进行加热浓缩、冷却,析出硝酸铈产品。硝酸铈晶体重结晶次数对硝酸铈收率、非稀土杂质质量分数的影响试验结果如图6所示。

图6 重结晶次数对硝酸铈收率及非稀土 杂质质量分数的影响
从图6看出,重结晶对硝酸铈收率没有明显影响,收率均稳定在70%以上,而杂质质量分数有效降低,产品得到净化。经过3次重结晶,产品中杂质元素总量由未经过重结晶时的2.5×10-5降为1.5×10-5左右,其中Na2O、CaO、MnO2、Al2O3、ZnO等元素去除效果明显。从工业生产角度考虑,重结晶次数不宜过多,以3次为最佳。
2.5 硝酸铈晶体的表征与分析
2.5.1 晶体的形貌
图7为硝酸铈晶体颗粒的形貌。可以看出:晶体特征非常明显,呈棱角分明的多面体结构,粒径在100 μm左右;一些小颗粒正在长大,晶体有粘接团聚现象。

图7 硝酸铈晶体的SEM照片
2.5.2 晶体的红外光谱分析
图8为所制备的硝酸铈晶体的红外光谱。可以看出:位于3 200~3 250 cm-1处的峰为含羟基基团结晶水的伸缩振动吸收峰,可以初步判断所制备的硝酸铈含有稳定的结晶水。

图8 硝酸铈晶体的红外光谱
2.5.3 晶体的XRD衍射分析
图9为硝酸铈晶体的XRD衍射分析图谱。该图谱与图谱库中的84-2198[Ce(NO3)3·5H2O]·H2O图谱相吻合,进一步表明所制备的硝酸铈晶体含有6个稳定结晶水。
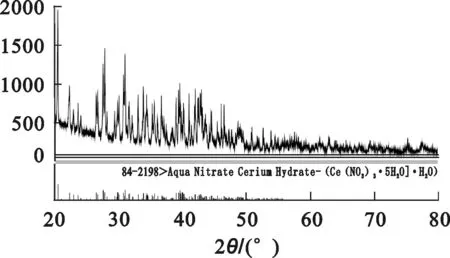
图9 硝酸铈晶体的XRD衍射图谱
2.5.4 晶体的热分解机制
图10为硝酸铈晶体的差热-热重曲线。由图10数据计算得到的硝酸铈的热分解数据见表5。
由图10和表5看出:硝酸铈的热分解过程可描述为7个阶段:第1阶段,脱去0.5个结晶水,得到Ce(NO3)3·5.5H2O;第2阶段,继续脱去0.5个结晶水,得到Ce(NO3)3·5H2O;第3阶段,继续脱去2个结晶水,得到Ce(NO3)3·3H2O;第4阶段,继续脱去2个结晶水,得到Ce(NO3)3·H2O;第5阶段,继续脱去1个结构水,得到Ce(NO3)3;第6阶段,无水硝酸铈分解,放出NO2和O2,得到Ce(NO3);第7阶段,脱去1个NO,得到CeO2。反应过程如下:
第1阶段,
[Ce(NO3)3·4.5H2O]·H2O+
0.5H2O↑;
(1)
第2阶段,

[Ce(NO3)3·4H2O]·H2O+
0.5H2O↑;
(2)
第3阶段,
[Ce(NO3)3·2H2O]·H2O+
2H2O↑;
(3)
第4阶段,

(4)
第5阶段,
Ce(NO3)3+H2O↑;
(5)
第6阶段,
2NO2↑+O2↑;
(6)
第7阶段,

(7)
峰1、峰2均为对称尖锐峰,表明分解过程为单纯的脱去结晶水过程。峰1脱去0.5个结晶水,吸热25.17 J/g,反应温度区间为57.5~73.8 ℃;峰2继续脱去0.5个结晶水,吸热27.6 J/g,反应温度区间为91.2~104.3 ℃;峰3为一个很小的对称尖锐峰,表明分解过程为脱去2个结晶水过程,吸热20.73 J/g,反应温度区间为163.2~189.7 ℃;峰4(由反应4、5两个阶段组成),表明分解过程为脱去2个结晶水和1个结构水,因脱去结构水需要吸收较大热量,总吸热82.73 J/g,反应温度区间为197.3~216.1 ℃;峰4(由反应6、7两个阶段组成),为无水硝酸铈发生分解反应,产生NO2、NO、O2,最后生成氧化铈,吸热349.7 J/g,反应温度区间为243.9~308.1 ℃,温度较高而且吸热值较大,说明分解反应不容易进行。
在这7个阶段中,理论累计失重率与实测累计失重率吻合较好,表明推断热分解机制正确,由此确定本工艺所得硝酸铈晶体的结构为[Ce(NO3)3·5H2O]·H2O,这与XRD分析结果以及现有文献一致[14]。
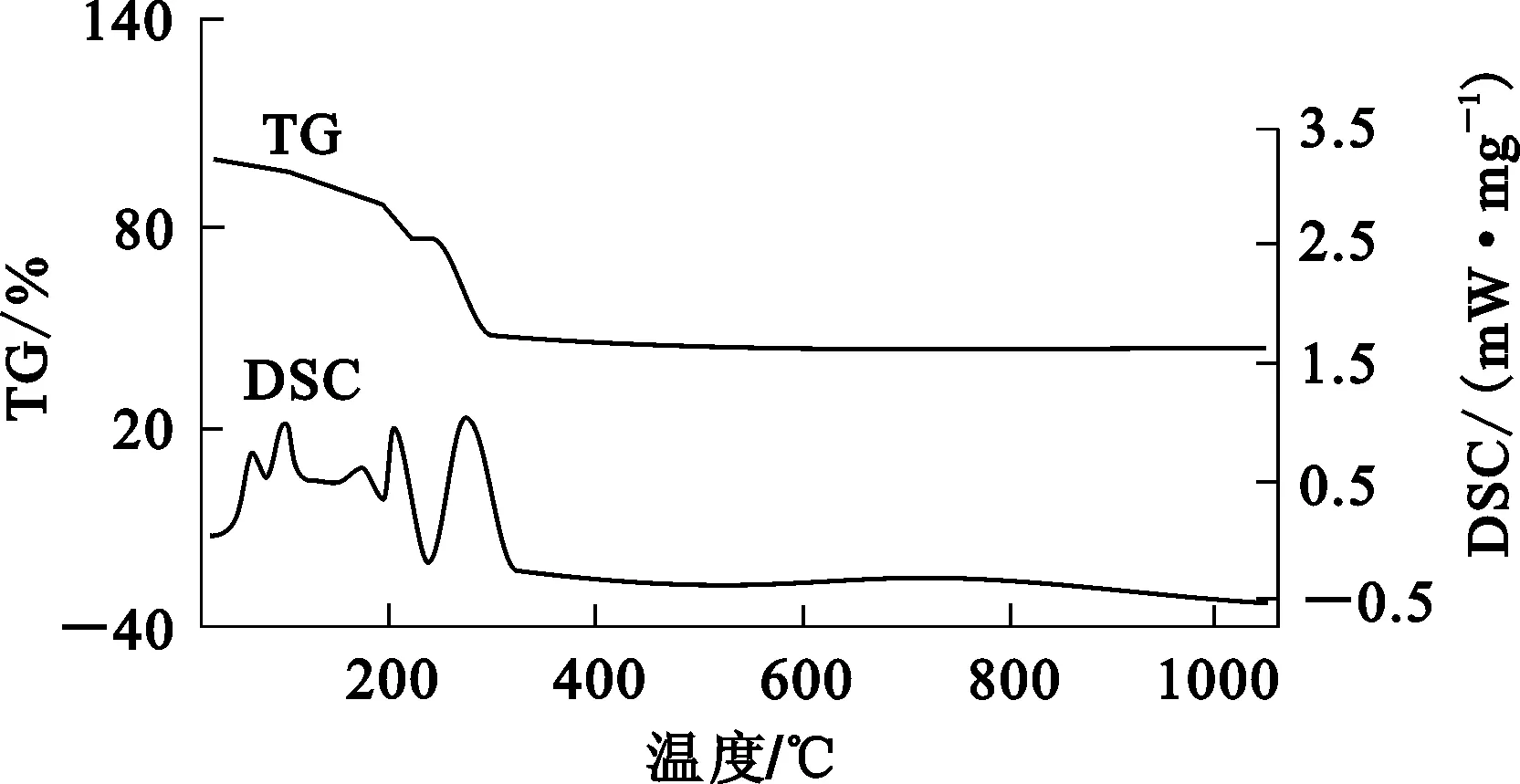
图10 硝酸铈晶体的TG-DSC曲线表5 硝酸铈的热分解机制分析

阶段理论失重率/%实测失重率/%理论残留率/%实测残留率/%反应温度/℃峰值温度/℃反应产物吸热量/(J·g-1)第1阶段2.082.3197.9297.6957.5~73.866.2Ce(NO3)3·5.5H2O25.17第2阶段4.154.5895.8595.4291.2~104.397.3Ce(NO3)3·5H2O27.60第3阶段12.4412.9687.5687.04163.2~189.7171.9Ce(NO3)3·3H2O20.73第4阶段20.7319.7579.2780.25第5阶段24.8823.5675.1276.44197.3~216.1205.6Ce(NO3)3·H2OCe(NO3)382.73第6阶段53.4654.9646.5445.04第7阶段60.3757.6039.6342.40243.9~308.1276.5Ce(NO3)CeO2349.70
2.5.5 硝酸铈晶体的化学分析
所得硝酸铈产品的化学分析结果见表6 。可以看出,所得晶体中,杂质质量分数很低,表明所得产品纯度很高。
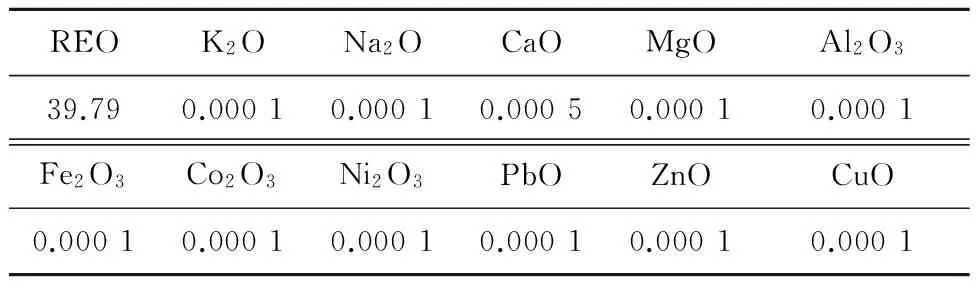
表6 硝酸铈产品的化学分析 %
3 结论
试验结果表明,采用化学结晶法及重结晶法制备洁净硝酸铈是可行的,在适宜料液酸度、结晶温度、陈化时间条件下可制得洁净硝酸铈产品,其中∑REO质量分数大于39.5%,收率大于70%,非稀土杂质质量分数小于1.50×10-5,母液可循环利用。该方法操作简单,产品质量稳定,母液可循环利用,易于实现产业化。
[1] 余祖孝,附青山,郝世雄,等.硝酸铈及热处理对化学镀Ni-W-P合金的性能影响[J].化学研究与应用,2015,27(5):696-699.
[2] 于美,马荣豹,刘建华,等.硝酸铈封闭对2A12铝合金己二酸-硫酸阳极氧化膜耐蚀性的影响[J].材料工程,2015,43(1):24-29.
[3] 洪尚坤 ,黎清宁,屈婧婧,等.硝酸铈添加剂对7075铝合金微弧氧化陶瓷膜特性的影响[J].中国表面工程,2014,27(6):116-121.
[4] 李向红,邓书端,木冠南,等.硝酸镧、硝酸铈在HCl介质中对铝的缓蚀作用[J].清洗世界,2007,23(2):1-4.
[5] 孙华,马洪芳,郭晓斐,等.硝酸铈对Ni-Co-P镀层组织结构和性能的影响[J].中国稀土学报,2014,32(2):228-233.
[6] 朱丽,李晔,张猛,等.硝酸铈改性赤泥制备除磷吸附剂[J].化工环保,2012,32(1):81-84.
[7] 郭淑华 .硝酸铈对南瓜组培苗生长影响的研究[J].安徽农业科学,2009,37(27):13022-13023.
[8] 肖方春.稀土溶液净化除杂[J].江西有色金属,1990(3):13-16.
[9] 张宝藏.稀土元素的提纯-稀土与非稀土元素的分离[J].稀土,1985(1):68-69.
[10] 冯宇川,潘有理,施朝英,等.沉淀除杂法提高稀土纯度的研究[J].江西师范科技学院学报,2006(4):115-117.
[11] 杨启山,赫文秀,杨卉,等.低杂质洁净硝酸铈制备工艺的研究[J].稀土,2013(5):35-40.
[12] 何水样,赵联营,刘羽纶.硝酸铈(Ⅲ)水合物热分解机理的研究[J].稀土,1988(4):33-37.
[13] 谭钦德,过伟,何明安,等.轻稀土硝酸盐及其水合物制备的研究[J].高等学校化学学报,1986,7(12):1067-1071.
[14] 高胜利,刘羽纶,杨祖培.稀土硝酸盐的制法、性质及结构[J].稀土,1990,11(4):23-28.
[15] 何水样,高胜利,杨祖培.重稀土水合硝酸盐的制备[J].稀土,1991,12(3):30-33.
[16] 乔军,马莹,王晶晶,等.氯化铈的结晶法制备及表征[J].湿法冶金,2016,35(6):492-497.
Preparation and Purification of Cerium Nitrate by Crystallization and Re-crystallization
QIAO Jun1,2,3,MA Ying1,2,3,WANG Jingjing1,2,3,YANG Qishan4,LIANG Chao4,RUAN Shuai4
(1.StateKeyLaboratoryforResearchandComprehensiveUtilizationofBaiyunOboRareEarthResources,Baotou014030,China;2.BaotouResearchInstituteofRareEarth,Baotou014030,China;3.NationalEngineeringResearchCenterofRareEarthMetallurgyandFunctionMaterials,Baotou014030,China;4.CollageofChemistryandChemicalEngineering,InnerMongoliaUniversityofScienceandTechnology,Baotou014010,China)
Preparation of high purity cerium nitrate by crystallization and re-crystallization was researched.By orthogonal regression experimental method,the effects of initial acidity of material liquid,temperature and aging time on the quality of cerium nitrate product were investigated,and the reutilization of mother liquors was studied.The results show that the high purity cerium nitrate can be obtained by the crystallization and re-crystallization.The total content of impurities in the product is less than 1.5×10-5.The reasonable process conditions for preparing aqua cerium hydrate nitrate are determined.The thermal decomposition mechanism shows that the composition of aqua cerium hydrate nitrate is Ce(NO3)3·6H2O.
crystallization;re-crystallization;aqua cerium hydrate nitrate;preparation;purification
2016-04-25
乔军(1970-),女,辽宁新民人,本科,高级工程师,主要研究方向为高纯稀土试剂的制备与研发。
TF802.6;TQ133.3
A
1009-2617(2017)01-0054-07
10.13355/j.cnki.sfyj.2017.01.013

