依巴斯汀对过敏性鼻炎免疫球蛋白及炎症因子水平的影响
张卫东
(郑州人民医院,河南郑州450003)
依巴斯汀对过敏性鼻炎免疫球蛋白及炎症因子水平的影响
张卫东
(郑州人民医院,河南郑州450003)
目的探讨依巴斯汀对过敏性鼻炎免疫球蛋白及炎症因子水平的影响。方法过敏性鼻炎患者88例,随机分为两组,每组44例。对照组采用氯雷他定及糖皮质激素治疗,观察组在对照组基础上加用依巴斯汀。治疗3个月。治疗前后晨起抽取空腹血检测免疫球蛋白、人血管内皮细胞粘附分子1和炎性因子。应用SPSS18.0软件,所获数据采用方差分析和t检验。结果两组治疗前IgM、IgG、IgA比较,P均>0.05。观察组治疗前后IgM、IgG、IgA比较,P均<0.0005;对照组治疗前后IgM比较,P>0.05;对照组治疗前后IgG、IgA比较,P均<0.0005。两组治疗后IgM、IgG比较,P均<0.0005;两组治疗后IgA比较,P>0.05。两组治疗前VCAM-1、IL-4、IL-10比较,P均>0.05。对照组治疗前后VCAM-1、IL-4、IL-10比较,P均<0.0005;观察组治疗前后VCAM-1、IL-4、IL-10比较,P均<0.0005。两组治疗后VCAM-1、IL-4、IL-10比较,P均<0.0005。结论过敏性鼻炎在常规治疗基础上加用依巴斯汀效果理想,有效的改善症状,改善机体免疫,降低炎症因子水平。
过敏性鼻炎/治疗;依巴斯汀/治疗应用;免疫球蛋白;炎症因子
过敏性鼻炎又称为变应性鼻炎,是鼻腔黏膜接触致敏原后引起的一种变态反应性疾病。表现为打喷嚏、流清涕、鼻痒、鼻塞等症状,严重影响我国居民健康。近年来,随着人们生存环境的改变及体质的下降,导致过敏性鼻炎发生率呈现上升趋势。常规方法以糖皮质激素治疗为主,药物能有效的改善患者症状,降低临床复发率[1]。但是,患者长期大剂量使用糖皮质激素容易产生耐药性,导致药物效果欠佳,难以达到预期的治疗效果。为此,我们自2015年11月—2016年11月间对过敏性鼻炎患者在氯雷他定及糖皮质激素的基础上加用依巴斯汀治疗了解免疫球蛋白及炎症因子水平的影响。现报道如下。
1 临床资料
1.1 一般资料过敏性鼻炎患者88例,随机分为两组,每组44例。对照组男26例,女18例,年龄19~55岁,平均年龄34.6岁,病程1~8年,平均4.1年。观察组男27例,女17例,年龄20~56岁,平均年龄35.1岁,病程1~9年,平均4.0年。两组一般资料比较,P>0.05,无显著性差异,具有可比性。
纳入标准:符合中华耳鼻咽喉科颈外科制定的关于《变硬性鼻炎诊断和治疗指南》中疾病相关标准;经过生化指标、影像学检查得到确诊。排除标准:(1)排除不符合纳入标准者。(2)排除合并有影响效应指标观测、判断其他生理或病理者。(3)排除合并严重心、肝、肾功能异常者。(4)排除合并过敏体质或对多种药物过敏者。
1.2 方法对照组采用氯雷他定及布地奈德吸入治疗:患者晨起空腹顿服10 mg氯雷他定每天1次;患者经口每次吸入400μg布地奈德,每天2次,连用12周(1个疗程)。观察组在对照组基础上加用依巴斯汀,每次口服2片,每天2次,连用12周(1个疗程),根据患者恢复情况酌情增减药物剂量。两组治疗前后清晨采集空腹静脉血采集5 ml静脉血,10 min离心,速度3000 rpm,测定免疫球蛋白、人血管内皮细胞黏附分子1(VCAM-1)及炎性因子水平。
1.3 统计学处理应用SPSS18.0软件,所获数据采用方差分析、t检验和χ2检验。
2 结果
2.1 两组治疗后症状改善时间比较见表1。
表1 两组治疗后症状改善时间比较(天
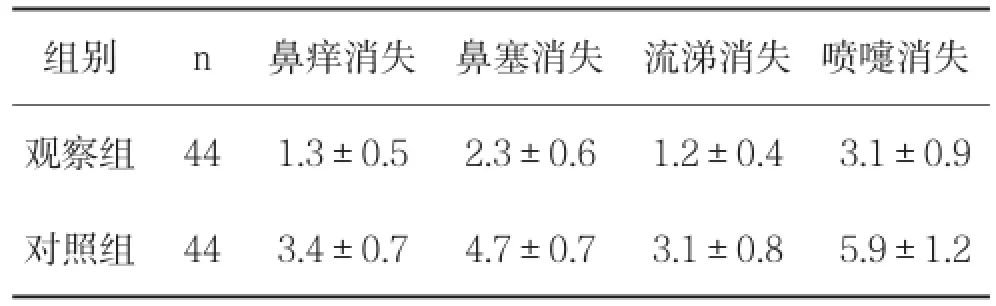
表1 两组治疗后症状改善时间比较(天
两组治疗后鼻痒消失、鼻塞消失、流涕消失、喷嚏消失比较,t=19.294、20.515、17.396、21.246,P<0.0005。
2.2 两组治疗前后免疫球蛋白水平比较见表2。
表2 两组治疗前、后免疫球蛋白水平比较(g/L

表2 两组治疗前、后免疫球蛋白水平比较(g/L
两组治疗前IgM、IgG、IgA比较,t=0.14425、0.49869、0.15809,P均>0.05。同组治疗前后IgM、IgG、IgA比较:观察组治疗前后IgM、IgG、IgA比较,t=4.8260、12.806、6.9176,P均<0.0005;对照组治疗前后IgM比较,t=1.0589,P>0.05;对照组治疗前后IgG、IgA比较,t=7.6817、6.0867,P均<0.0005。两组治疗后IgM、IgG比较,t=3.8931、5.4260,P均<0.0005;两组治疗后IgA比较,t=1.0836,P>0.05。
2.3 两组治疗前、后VCAM-1、IL-4和IL-10水平比较见表3。
表3 两组治疗前、后VCAM-1、IL-4和IL-10水平比较(μg/L

表3 两组治疗前、后VCAM-1、IL-4和IL-10水平比较(μg/L
两组治疗前VCAM-1、IL-4、IL-10比较,t=1.3190、0.41117、0.38866,P均>0.05。同组治疗前后VCAM-1、IL-4、IL-10比较:对照组治疗前后VCAM-1、IL-4、IL-10比较,t=9.1685、6.4803、10.786,P均<0.0005;观察组治疗前后VCAM-1、IL-4、IL-10比较,t=15.152、5.1715、27.224,P均<0.0005。两组治疗后VCAM-1、IL-4、IL-10比较,t=7.6571、8.8427、21.964,P均<0.0005。
3 讨论
过敏性鼻炎是一种机体免疫功能失调类疾病,常表现为鼻黏膜的充血水肿[2]。Th-2细胞主要参与细胞反应,过敏原入侵时会分泌出TL-4、IL-10等炎性物质[3]。过敏性鼻炎患者在一般情况下体内的Th-1和Th-2相对稳定是机体免疫系统正常的重要保证[4]。但当患者机体遭受过敏原侵袭的时候,Th-2的含量就会迅速上升,导致Th-1与Th-2相对比值的降低,大量的Th-2细胞进入机体的黏膜组织中分泌出大量的细胞因子,进入血液后,导致患者产生过敏反应[5]。
IL-4和IL-10在Th-2释放的细胞因子中数量最多,影响也最大[6]。另外,这两种细胞因子还可以激发肥大细胞的活性,使肥大细胞释放出炎性介质,造成鼻黏膜的水肿,分泌出大量黏性物质,这是造成过敏性鼻炎患者鼻塞、流鼻涕的最直接原因[7]。
VCAM-1作为一种细胞黏附因子,能够被嗜酸性粒细胞识别并结合,造成该细胞位置发生变化,引发过敏反应,过敏性鼻炎患者患病越严重,体内的VCAM-1含量越高,故在诊断和治疗中都可把VCAM-1水平做为判定标准[8]。
采用的布地奈德作为鼻喷药物,对患者病情有缓解作用。布地奈德进入呼吸道中会被黏附在呼吸道黏膜上,与受体结合后可以激发受体活力产生大量固醇类物质,这些物质进入细胞后会促进细胞产生分泌物改善炎症[9]。但过敏性鼻炎具有病程较长,易反复发作等特点,布地奈德鼻喷仅能在短时间内使病情得到控制,长期有效控制,还需要其他药物进行联合治疗[10]。
服用依巴斯汀对患者的病情有很好的抑制作用作用,且具有效果持久。本研究两组治疗前IgM、IgG、IgA比较,P均>0.05,无显著性差异。观察组治疗前后IgM、IgG、IgA比较,P均<0.0005,有非常显著性差异;对照组治疗前后IgM比较,P>0.05,无显著性差异;对照组治疗前后IgG、IgA比较,P均<0.0005,有非常显著性差异。两组治疗后IgM、IgG比较,P均<0.0005,有非常显著性差异;两组治疗后IgA比较,P>0.05,无显著性差异。两组治疗前VCAM-1、IL-4、IL-10比较,P均>0.05,无显著性差异。对照组治疗前后VCAM-1、IL-4、IL-10比较,P均<0.0005,有非常显著性差异;观察组治疗前后VCAM-1、IL-4、IL-10比较,P均<0.0005,有非常显著性差异。两组治疗后VCAM-1、IL-4、IL-10比较,P均<0.0005,有非常显著性差异。说明两种治疗方案均有较好的疗效,加用依巴斯汀对免疫功能及炎性因子效果更显著[11]。
[1]谢骊,刘涛,谭龙益.孟鲁司特联合布地奈德治疗过敏性鼻炎的疗效及其对患者tIgE与sIgE的影响[J].标记免疫分析与临床,2016,23(9):992-994.
[2]冉春涛.左西替利嗪联合依巴斯汀治疗慢性荨麻疹对实验室指标、临床症状积分的影响及临床疗效分析[J].河北医药,2016,38(7):1015-1017.
[3]张治成,杨晓,杨晓刚.意守式针灸疗法联合枸地氯雷他定治疗中重度间歇性过敏性鼻炎临床疗效及预后分析[J].重庆医学,2016,45(25):3542-3544.
[4]宋淑红,赵栋桉,周静芳,等.消瘾方加减联合依巴斯汀治疗慢性荨麻疹疗效评价及对IgE、IL-4和IFN-γ水平的影响[J].中国麻风皮肤病杂志,2015,17(4):229-231.
[5]宋淑红,朱翊,徐东宁,等.消瘾方加减联合依巴斯汀治疗慢性荨麻疹疗效及对血浆组胺水平的影响[J].现代中西医结合杂志,2016,25(3):323-325.
[6]张桂桃,粱利伟,宋德锋.鼻渊通窍颗粒联合盐酸非索非那定治疗过敏性鼻炎的疗效、预后及血清炎症因子水平分析[J].中国现代医学杂志,2016,26(13):122-125.
[7]卢湘云,孙伟忠,赖余胜,等.浙江嘉善儿童过敏性鼻炎患病状况、对生活学习的影响及发病因素调查分析[J].实用预防医学,2015,22(8):949-951.
[8]丁莲富,陈强,李岚,等.舌下特异性免疫治疗过敏性鼻炎/过敏性哮喘患儿IL-17和IL-35水平的变化及临床疗效[J].中国当代儿科杂志,2014,16(12):1206-1210.
[9]姚德志,黄磊瑛.舌下特异性免疫治疗对过敏性哮喘患者诱导痰中炎性因子、趋化因子、T细胞亚群含量的影响[J].海南医学院学报,2015,21(7):911-913.
[10]王敏,王向东,李颖,等.白细胞介素-1β在过敏性鼻炎小鼠的表达及其对鼻上皮细胞肿瘤坏死因子α诱导蛋白2的影响[J].中国耳鼻咽喉头颈外科,2014,21(6):315-318.
[11]池海超,陈觅,张杰.嗜酸乳酸杆菌对过敏性鼻炎模型大鼠血清中组胺、IL-5、IL-12及组织中ICAM-1的影响[J].重庆医学,2015,(31):4379-4381.
Ebastine for Allergic Rhinitis Immunoglobulin and the Influence of Inflammatory Factor Levels
Zhang Weidong
(The People's Hospital of Zhengzhou,Zhengzhou 450003,Henan)
ObjectiveTo observe the application result Ebastine in patients with allergic rhinitis and its impact on the body's immune globulin and inflammatory factor levels.Methods88 cases of allergic rhinitis patients,randomly divided into two groups,each group of 44 cases.The control group with loratadine and glucocorticoid therapy,observation group on the basis of control group and used in accordance with the basting.Treatment for 3 months.Extraction since morning fasting blood tests before and after the treatment of immune globulin,human vascular endothelial cells adhesion molecules 1 and inflammatory factors.Using SPSS18.0 software,the data obtained using analysis of variance and t test.ResultsThe two groups before treatment of IgM and IgG,IgA,P>0.05.Observation group of IgM and IgG,IgA comparison before and after treatment,P<0.0005.IgM comparison before and after the treatment,the control groupP>0.05.IgG, IgA comparison before and after the treatment,the control group,P<0.0005.IgM and IgG to compare the two groups after treatment,P<0.0005.IgA to compare the two groups after treatment,P>0.05.The two groups before treatment VCAM1, IL-4,IL-10,P>0.05.The control group before and after treatment,IL VCAM-1-4,IL-10,P<0.0005;Observation group before and after treatment,IL VCAM-1-4,IL-10,P<0.0005.Two groups after treatment VCAM1,IL-4,IL-0,P<0.0005.ConclusionAllergic rhinitis on the basis of conventional treatment combined with ebastine effect is ideal,effectively improve symptoms,improve the body's immune,lower levels of inflammatory cytokines,is worthy of popularization and application.
Allergic rhinitis/therapy;Ebastine/therapeutic use;Immune globulin;Inflammatory cytokines
R765.41
:A
:1008-4118(2017)01-0033-03
10.3969/j.issn.1008-4118.2017.01.011
2016-10-23

