替考拉宁和万古霉素治疗革兰阳性菌感染疗效及安全性比较
江学维,白 楠,倪文涛,马思锐,王 瑾,王 睿(.中国人民解放军总医院药物临床研究中心,北京 0085;.中国人民解放军总医院呼吸科,北京 0085;.沈阳药科大学生命科学与生物制药学院,辽宁 沈阳 006)
替考拉宁和万古霉素治疗革兰阳性菌感染疗效及安全性比较
江学维1,白 楠1,倪文涛2,马思锐3,王 瑾1,王 睿1(1.中国人民解放军总医院药物临床研究中心,北京 100853;2.中国人民解放军总医院呼吸科,北京 100853;3.沈阳药科大学生命科学与生物制药学院,辽宁 沈阳 110016)
目的:探讨替考拉宁与万古霉素治疗革兰阳性菌感染的临床疗效与安全性。方法:收集解放军总医院2012年1月–2016年4月期间住院病历数据库记载ICU和RICU分别应用替考拉宁和万古霉素两种药物治疗的临床病历,通过收集其人口学资料、基础疾病、伴随用药、用药疗程以及疗效、细菌清除和不良反应情况,通过SPSS 17.0分析比较两组药物的临床疗效及安全性。结果:在临床治疗有效率、细菌清除率方面,替考拉宁组的有效率和细菌清除率分别为32.3%和29.6%,与万古霉素组的有效率(38.7%)和细菌清除率(44.0%)相比差异无统计学意义,但替考拉宁具有低不良反应发生率的优势,差异具有统计学意义(P< 0.05)。两组患者的中青年患者与老年患者在临床疗效、细菌清除率和不良反应发生率方面差异无统计学意义,但不良反应发生率均为老年人大于中青年人。结论:替考拉宁治疗革兰阳性菌感染的疗效与万古霉素相当,但替考拉宁在相同条件下比万古霉素安全性更高。
替考拉宁;万古霉素;临床疗效;安全性
滥用抗菌药物使得病菌的耐药率大大增加,在革兰阳性致病菌中耐甲氧西林金黄色葡萄球菌(MRSA)与耐甲氧西林凝固酶阴性葡萄球菌(MRCNS)所占比例居高不下[1],使得攻克革兰阳性耐药菌成为焦点。万古霉素在抗革兰阳性耐药菌的突出疗效得到一致的好评,2014年CHINET显示未监测到耐万古霉素的细菌,而且由于和其他抗生素不存在交叉耐药性,万古霉素逐步成为对抗革兰阳性耐药菌的最后一道防线。但万古霉素不良反应发生率较高,尤其是肾毒性,在应用的同时需要经常监测临床血药浓度以防止因浓度过高而致的肾毒性。替考拉宁是由特定的游动放线菌经过发酵后提取而得的糖肽类抗菌药物,主要治疗各种严重的革兰阳性菌感染,如皮肤和软组织感染,泌尿道感染,呼吸道感染,骨和关节感染,败血症,心内膜炎及持续不卧床腹膜透析相关性腹膜炎,包括不能用青霉素类和头孢菌素类其他抗生素者,亦常用于MRSA。研究表明,替考拉宁治疗葡萄球菌属、屎肠球菌、粪肠球菌的敏感率高达100.0%、99.8%和98.1%[1],其中包括MRSA和MRCNS等高度耐药致病菌,成为继万古霉素之后,治疗革兰阳性菌重症感染强效有力的武器。国内外已有大量文献研究替考拉宁的抗菌疗效[2-4]。本研究通过对解放军总医院2012年1月– 2016年4月ICU与RICU应用替考拉宁与万古霉素抗感染的患者进行回顾性分析,比较其临床疗效与安全性。
1 材料和方法
1.1 资料来源
收集解放军总医院2012年1月– 2016年4月重症监护室/呼吸科重症监护室革兰阳性菌感染的患者资料。纳入标准:1)2012年1月– 2016年4月入住ICU和RICU并且年龄≥18周岁患者,男女不限;2)使用替考拉宁/万古霉素治疗的革兰阳性菌感染患者。排除标准:1)用药不足三天无法评价其疗效的患者;2)用药过程中存在替考拉宁、万古霉素交叉使用的;3)对替考拉宁或者万古霉素过敏的患者。
1.2 方法
查找符合纳入标准的患者病历,收集以下资料:1)患者的年龄、性别、住院天数;2)基础疾病、临床症状、体征、感染部位、停药时结局指标;3)用药选择、经验用药或目标用药、替考拉宁组是否使用负荷剂量、疗程;4)微生物检查结果、实验室检查结果;5)不良反应。
疗效指标:根据卫生部2004年颁布的《抗菌药物临床研究指导原则》分为“痊愈”、“显效”、“进步”、“无效”四级判定标准[5]。痊愈:症状、体征、实验室检查和病原学4项恢复正常;显效:病情明显好转,但上述4项有1项未完全恢复正常;进步:用药后有好转,但达不到显效标准;无效:用药72 h后病情无明显进步或有加重者;以痊愈和显效计算有效率。细菌学指标:完全清除、部分清除、未清除、不清楚。统计学方法:数据通过SPSS 17.0进行分析处理,计量资料用() 表示,临床有效率、细菌清除率和不良反应发生率采用χ2检验,P< 0.05为差异有统计学意义。
2 结果
2.1 一般资料
共检索符合入组标准的病历127例,男性83例,女性44例,无CRRT患者,两组间患者基本资料包括感染部位及数量、合并用药与药物的用法用量,差异无统计学意义,详见表1。

表1 两组患者一般资料Tab 1 The general information of patients between the two groups
2.2 疗效与细菌清除比较
本项研究共纳入病例127例,替考拉宁组78例(死亡19例),万古霉素组49例(死亡18例),其中死亡病例未纳入疗效统计,细菌学疗效中存在部分结果缺失。以治愈和显效例数计算有效率,以完全清除计算细菌清除率。两组临床疗效及细菌清除率差异无统计学意义(P> 0.05)。替考拉宁在治疗ICU和RICU革兰阳性菌感染的疗效与万古霉素相当。结果见表2。
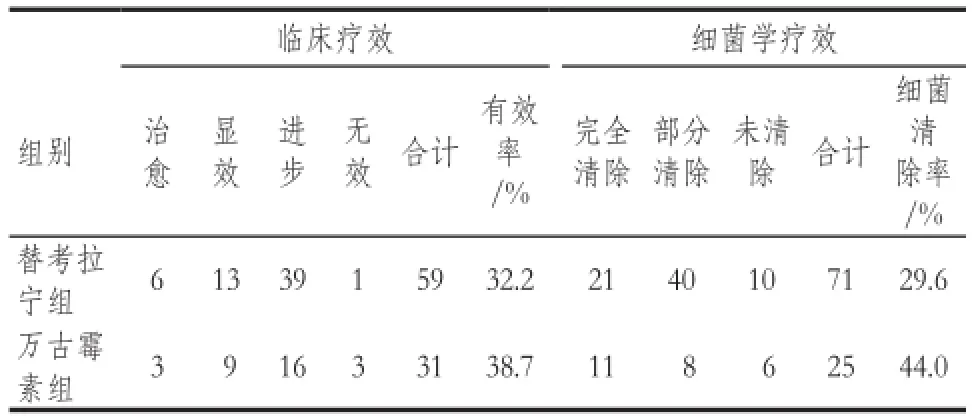
表2 两组患者临床疗效与细菌清除率比较Tab 2 Comparison of clinical efficacy and bacterial clearance rate between the two groups
2.3 不良反应
在不良反应方面,替考拉宁组出现4例不良反应,分别是肾毒性反应(2例)和胃肠道反应(2例)。万古霉素组出现13例不良反应,分别是肾毒性反应(5例)、胃肠道反应(3例)和皮疹(5例)。两药的不良反应发生率差异有统计学意义(P< 0.05)。替考拉宁组的不良反应发生率为5.1%,明显低于万古霉素组的26.5%,提示替考拉宁的不良反应发生率具有低于万古霉素的优势。
2.4 中青年组与老年组比较
本项研究包含老年患者(≥60岁)87例,其中替考拉宁组56例,万古霉素组31例;中青年患者40例,其中替考拉宁组22例,万古霉素组18例。替考拉宁组在治疗中青年革兰阳性菌ICU和RICU患者的有效率为28.6%,细菌清除率为15.0%,不良反应发生率为4.5%,对于老年患者的有效率为28.6%,细菌清除率为35.3%,不良反应发生率为5.4%。万古霉素组在治疗中青年革兰阳性菌ICU和RICU患者的有效率为26.7%,细菌清除率为22.2%,不良反应发生率为27.8%,对于老年患者的有效率为28.5%,细菌清除率为20.7%,不良反应发生率25.8%。两组试验的中青年患者与老年患者的临床疗效与细菌清除率差异无统计学意义,但不良反应发生率均为老年人大于中青年人。
3 讨论
在本项研究纳入的所有革兰阳性菌感染患者中,55.1%为肠球菌属感染,7.9%为MRSA感染,提示本院重症监护病房针对以MRSA为首的耐药革兰阳性菌控制得当。我院ICU和RICU病房具有严格的TDM制度,使用万古霉素后每1 – 2天都严格进行临床血药浓度监测,并根据谷浓度进行用药调整[6],且设计开发了住院患者药品不良事件主动监测与评估警示系统[7],结果显示不良反应发生率方面替考拉宁优势仍较为明显,仅为万古霉素的三分之一。
亚组分析中,60岁以上患者和中青年人组在临床有效率与细菌清除率差异无统计学意义(P> 0.05),不良反应发生率均为成年患者小于老年患者,且替考拉宁的发生率低于万古霉素。但替考拉宁组细菌清除率出现老年患者大于成年患者,万古霉素组临床有效率出现老年患者大于成年患者组的结果,考虑可能由于临床医生对于高年龄ICU和RICU患者更偏向使用文献报道较多的肾毒性较低的替考拉宁,因此可能影响最后的统计结果。
依据文献报道[8],替考拉宁的负荷剂量为400 mg,q 12 h,3次给药后改为维持剂量200 mg,q 24 h。本研究中替考拉宁组使用负荷剂量的病例数只有8例,导致有效率低于非负荷剂量组,但细菌清除率高于非负荷剂量组,考虑可能是临床医生在病情较重的患者选择使用负荷剂量替考拉宁,导致本研究的患者病情基线水平不一致而影响的结果。在多项试验中发现,使用负荷剂量的替考拉宁,并使其有效谷浓度维持在10 mg·L-1以上,患者的获益大大提高[9]。万古霉素负荷剂量为25 – 30 mg·kg-1[10],但在纳入病历中未找到使用负荷剂量的患者,因此无法统计其负荷剂量亚组的疗效与安全性。
本研究结果显示,住院期间伴有肾功能不全、心功能不全、脑部疾病、昏迷、感染性休克与应用机械通气的患者死亡率明显比其余患者死亡率高,差异具有统计学意义(P< 0.05)。有文献指出泌尿道插管为ICU患者死亡的高危因素[11],但本项研究并未得出同样的结果,原因可能为本研究病例主要来源于RICU,统计结果显示RICU病房患者泌尿道插管的概率较低,可能对结果存在一定影响。通过本研究结果,可见感染患者的生理状况、机体防御机能、意识障碍、基础疾病情况、是否有侵入性操作等单因素对生存状态有着重要影响。感染性休克为本组研究的高危因素,提示出现该症状时临床医生应予以足够的重视,有文献[12]报道称早期的指向性治疗(early goal directed therapy,EGDT)有助于降低感染性休克带来的高死亡率,推荐发生早期感染性休克的患者应尽早采用EGDT进行辅助治疗。
[1] 胡付品,朱德妹,汪复,等.2014年CHINET中国细菌耐药性监测[J].中国感染与化疗杂志,2015,15(5):401-410.
[2] 杨睿,鲁新华,张国俊.不同起始负荷剂量替考拉宁治疗革兰阳性菌下呼吸道感染的疗效与安全性评价[J].中华医院感染学杂志,2015,25(20):4673-4675.
[3] 张镇,严丽芳,冯春,等.血液病患者感染治疗中应用替考拉宁效果分析[J].中华医院感染学杂志,2016,26(16):3722-3726.
[4] 吴茱萸,唐思源.国产替考拉宁治疗革兰阳性球菌重症肺炎疗效分析[J].医药论坛杂志,2015,36(4):153-154.
[5] 高炜,高景,邢丽华,等.重症肺炎的抗菌药物降阶梯治疗策略与替考拉宁的临床应用[J].中华医院感染学杂志,2010,20(7):998-1000.
[6] 黄春燕,郭代红,朱曼.154例患者664次万古霉素血药浓度监测分析[J].中国药物应用与监测,2014,11(2):68-71.
[7] 朱曼,陈超,郭代红.万古霉素相关肾毒性的主动监测研究[J].中国药物应用与监测,2014,11(1):26-29.
[8] Ahn BJ, Yim DS, Lee DG,et al. Teicoplanin dosing strategy for treatment ofStaphylococcus aureusin Korean patients with neutropenic fever[J]. Yonsei Med J, 2011, 52(4): 616-623.
[9] 江学维,梁蓓蓓,王凯,等.替考拉宁药代动力学/药效学研究与给药方案优化[J].中国临床药理学杂志,2015,31(16):1662-1664.
[10] 翁心华,黄仲义,陈伯义,等.万古霉素临床应用中国专家共识(2011版)[J].中国新药与临床杂志,2011,30(8):561-573.
[11] 李冬梅,王超,刘荣,等.医院感染相关死亡危险因素分析[J].中华医院感染学杂志,2012,22(21):4707-4708.
[12] 贺鹤群,朱建华,叶继辉.重症肺炎的临床特征和死亡危险因素分析[J].实用医学杂志,2010,26(19):3532-3534.
Efficacy and safety of teicoplanin and vancomycin in the treatment of gram-positive bacterial infections
JIANG Xue-wei1, BAI Nan1, NI Wen-tao2, MA Si-rui3, WANG Jin1, WANG Rui1(1. Center of Clinical Medicine Research, Chinese
PLA General Hospital, Beijing 100853, China; 2. Department of Respiratory, Chinese PLA General Hospital, Beijing 100853, China; 3. College of Bioscience and Biopharmaceutics, Shenyang Pharmaceutical University, Shenyang 110016, China)
Objective: To evaluate the clinical efficacy and safety of teicoplanin and vancomycin in the treatment of gram-positive bacterial infections. Methods: By exploring the medical records databases of Chinese PLA General Hospital, the data was collected including the demographic data, underlying diseases, concomitant medication, course of treatment, treatment efficacy, bacterial clearance and adverse reactions of the patients who received teicoplanin or vancomycin in ICU and RICU wards from January 2012 to April 2016, the efficacy and safety were compared by SPSS 17.0. Results: The efficacy rate and bacterial clearance rate in teicoplanin group were 32.3% and 29.6%, respectively. There was no statistical significance when compared with vancomycin group (clinical efficacy rate and bacterial clearance rate were 38.7% and 44.0% respectively). While, teicoplanin had an advantage of low incidence of adverse reactions with statistical significance (P < 0.05). There was no statistical significance on the clinical efficacy and bacterial clearance rate between elderly patients and younger patients in both groups, while the incidence of adverse reactions was higher in elderly patients. Conclusion: The efficacy of treating gram-positive bacterial infections by teicoplanin was equivalent with vancomycin, while under the same conditions teicoplanin was safer than vancomycin.
Teicoplanin; Vancomycin; Efficacy; Safety
R978.1
A
1672 – 8157(2017)01 – 0010 – 03
十二五国家重大科技专项课题(2012ZX09303004-002)[通信作者] 王瑾,女,副主任药师,研究方向:临床试验管理及临床药理。E-mail:301jgb@sina.com
江学维,男,药师,研究方向:新药药代动力学研究。E-mail:15801679861@163.com

