油基体系中水合物分解过程的研究
宋光春,李玉星,王武昌
(中国石油大学(华东) 山东省油气储运安全省级重点实验室,山东 青岛 266580)
油基体系中水合物分解过程的研究
宋光春,李玉星,王武昌
(中国石油大学(华东) 山东省油气储运安全省级重点实验室,山东 青岛 266580)
采用自制的带视窗高压反应釜,以柴油、水、天然气为实验介质,先在含水率30%(w)的油基体系中生成天然气水合物,然后分别在不同加热温度、降压速率及抑制剂甲醇质量分数的作用下将其分解,分析水合物在3种不同分解过程中的宏观形态变化,并对分解速率和分解效率进行了比较。实验结果表明,油基体系中水合物的分解过程具有强剪切区分解较快、液相中水合物颗粒呈“缩核分解”等共性。3种分解过程中水合物形态变化的差别主要表现在水合物从壁面脱离的方式不同、液相中气泡产生的速率和数量不同以及分解过程中壁面是否有气体运移通道、体系中是否有冰相产生等。分解速率随加热温度、降压速率和抑制剂质量分数的增大而增加。在实验工况下,分解速率范围为6.40×10-4~ 2.09×10-1mol/min。
天然气水合物;分解;宏观形态变化;分解速率
在油气开采和输送过程中,由于高压和低温条件很容易形成气体水合物堵塞管道[1],阻碍正常生产[2]。因此,对油气输送管道内水合物分解过程的研究尤为重要[3-4]。目前,国内外学者对天然气水合物分解过程的研究多集中在分解理论和模型、多孔介质中水合物的开采分解及水合物储运等领域[5-8]。对油气输送管道或油水乳状液中水合物的分解研究则相对较少[9-10]。Peters等[11]和Boxall等[12]分别研究了两端降压法和直接电加热法对管道内水合物堵塞体的分解,但对管道内水合物分解的形态变化均未作详细描述。Lachance等[13]和Chen等[14]通过聚焦光束反射测量装置和颗粒显微录影设备对乳状液中水合物颗粒的分解特性进行了研究。但上述研究主要针对水合物颗粒的微观分解情况[15-17],对水合物在分解过程中的宏观形态变化仍需进一步分析。
本工作利用自行设计的实验装置,先在可视反应釜的油基环境内生成天然气水合物,然后分别通过加热、降压和注热力学抑制剂的方法将其分解,分析水合物在分解过程中的宏观形态变化,并将不同分解方式下水合物的分解速率和分解效率等参数进行比较,为油气输送管线水合物的防治技术提供了指导。
1 实验部分
1.1 实验材料
天然气:CH4,C2H6,C3H8的含量(φ)分别为90%,6%,4%,纯度不小于99.99%(φ);柴油:C7~C20,C24,C+28的含量(w)分别为92.74%,7.05%,0.21%,纯度不小于99.88%(w);甲醇:纯度不小于99.50%(w) 。
甲醇是工业中常用的水合物热力学抑制剂,可通过改变水分子与客体分子间的热力学平衡条件,使水分子间的作用能发生变化,破坏水合物晶体结构,即通过改变水合物相的化学位,抑制水合物生成或引发水合物分解[18]。
1.2 实验装置
采用自制的带视窗高压反应釜进行水合物的生成与分解实验。实验主要由供气系统、配-注液系统、反应釜系统、温控系统及采集分析系统组成。实验装置及流程见图1。其中,反应釜由不锈钢材料制成,容积990 mL,最大承压10 MPa,中部有圆形可视窗(φ 65 mm)便于采集实验过程中的照片。为加速水合物的生成,实验中使用磁耦合搅拌器,搅拌转速设定为200 r/min[19]。温度由恒温水浴调节,可快速开启,用于水合物形成和加热分解过程中的温度控制,温度范围-30~100 ℃,精度±0.05℃。热力学抑制剂由恒流泵注入,流量范围0.1~20 mL/min,工作压力0~20 MPa。实验过程中降压速率通过反应釜排气阀开度调节。反应釜上部和下部各有一个温度传感器,用于测量液相温度。反应釜上部与压力传感器相连,用于测量反应釜内压力。

图1 实验装置及流程Fig.1 Schematic diagram of experimental installation.
1.3 实验步骤及工况
首先进行反应釜清洗和气密性检测,随后用真空泵对反应釜抽真空并将含水率30%(w)的油基油水混合液抽入。开启搅拌器和恒温水浴,使溶液均匀混合并逐渐降温至2 ℃[20]。当体系温度维持恒定约30 min后,通入天然气至设定压力(6 MPa),开始水合物生成过程。当体系温度压力再次稳定约30 min后,认为生成过程基本结束。
水合物生成结束后再分别通过水浴加热、排气降压和注热力学抑制剂甲醇3种方式将其分解。当体系温度或压力维持恒定约30 min且反应釜内观察不到水合物存在时,分解过程结束。不同加热温度、降压速率和抑制剂甲醇质量分数下的分解条件见表1~3。

表1 加热分解条件Table 1 Conditions of the dissociation of natural gas hydrates through heating

表2 降压分解条件Table 2 Conditions of the dissociation of natural gas hydrates through depressurizing

表3 注甲醇分解条件Table 3 Conditions list of the dissociation of natural gas hydrates through adding methanol
2 水合物宏观形态变化分析
2.1 加热分解
实验3中的气相空间壁面处水合物的生成和分解见图2。
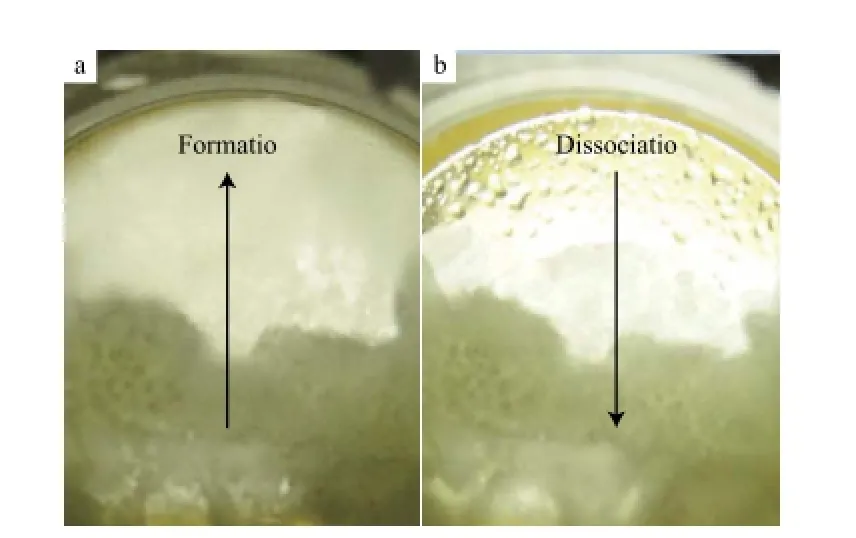
图2 实验3中气相空间壁面处水合物的生成和分解Fig.2 Formation and dissociation of natural gas hydrates on the wall(No.3).
由图2可见,气相壁面不同区域间水合物的分解顺序与生成顺序相反,即越晚生成水合物的区域其分解过程结束的越早,而最早生成水合物的区域其分解过程结束的一般相对较晚。这是由于水合物生成较早的区域,其水合物生成的驱动力往往较大,水合物生成量也较多,故该区域形成的水合物覆盖层较厚,因此当分解热在实验系统内均匀分布时,水合物覆盖层较薄的区域就会较早完成分解。
搅拌的剪切作用对反应釜内水合物的分解过程有重要影响。实验3中不同分解时刻搅拌剪切对水合物分解的影响见图3。由图3可见,对于附着在壁面上的水合物,强剪切区域(图3中红圈部分)的分解速率要明显快于其他区域的分解速率;对于分散在液相中的水合物,搅拌剪切能使其更快离散为水合物小颗粒而加速分解。
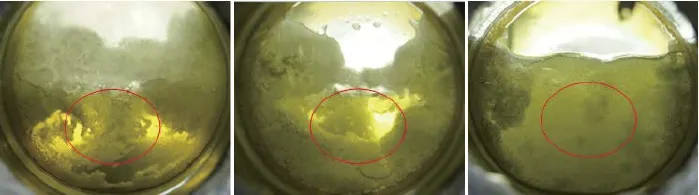
图3 实验3中搅拌剪切对水合物分解的影响Fig.3 Influence of magnetic stirrer on the hydrate dissociation(No.3).
附着在气相壁面上的水合物在加热分解时的分解形态与其生成量大小有关。实验3中气相壁面水合物的分解形态见图4。由图4可见,当生成量较小时,水合物层较为疏松,其在吸热后直接转化为水和气,观察不到水合物从壁面上脱离的现象。当生成量较大时,致密的水合物层会先变疏松,随后以水合物块的形式脱离壁面进入液相,最终在搅拌剪切的作用下转化为水合物颗粒并完成分解。

图4 实验3中气相壁面水合物的分解形态Fig.4 Dissociation morphology of hydrates in gas phase on the wall(No.3).
实验3中液相中水合物分解产生的气泡见图5。液相中水合物受热分解产生气体和解离水,其中,解离水在搅拌剪切的作用下重新分散进入油相,气体则在液相中重新溶解。当溶液被天然气溶解饱和后,水合物分解产生的气体就会在液相中生成气泡,如图5a所示。小气泡在升力作用下逐渐上浮,若上浮过程中不发生聚集,气液分界面处就会形成小气泡层,如图5b所示。若上浮过程中发生聚集,小气泡就会转化为大气泡,如图5c所示。另外,当液相壁面附着的水合物层较为致密时,最外层水合物分解产生的小气泡会因移动受阻而黏附在壁面上并发生聚集,直到聚集成为较大气泡后才得以脱离壁面,如图5d所示。
油基体系中水合物颗粒在分解时表现出明显的“缩核”特征,水合物的“缩核”分解过程见图6。由图6可见,在油水混合液中,水合物颗粒分解后会在颗粒外表面形成一层水膜,随着分解的不断进行,水膜逐渐增厚,膜内的水合物核则变得越来越小,直到最后水合物核完全消失,水合物颗粒最终转化为小液滴[14]。

图5 实验3中液相中水合物分解产生的气泡Fig.5 Bubbles generated by the hydrates dissociation in liquid phase(No.3).

图6 油基体系中水合物的“缩核”分解Fig.6 Schematic diagram of the shrinking model of the hydrates in an oil-based system.
2.2 降压分解
同加热分解类似,反应釜油基体系中水合物的降压分解也具有气相壁面水合物分解顺序与生成顺序相反、强剪切区分解较快、液相中水合物颗粒呈“缩核”分解的特征。此外,水合物的降压分解还包含其他特征,根据这些特征建立管道内水合物降压分解的宏观物理模型,如图7所示。降压分解过程中液相中气泡产生的数量更多且移动、聚集的速率更快。这是由于降压时气体的溶解度也随之降低,因此分解产生的天然气能更快在液相中溶解饱和并形成气泡。同时,由于气相空间压力的降低,气泡产生后向气相移动的推动力也不断增加,因此气泡移动和聚集的速率明显加快。

图7 管道内水合物降压分解的宏观物理模型Fig.7 Macro physical model of the dissociation of the hydrates in pipeline by depressurizing.
壁面水合物层有气体运移通道产生。由于降压分解产生的气泡数量多、移动速率快,故当壁面上附着的水合物层因分解而变得疏松后,气泡的连续上移和冲击就会导致一条贯穿整个壁面水合物层的气体运移通道产生,如图8所示。随着气泡在移动过程中的增长和聚集,这些通道也变得越来越宽,这大幅减少了分解过程的传质阻力,促进了分解气的排出。最后,相邻通道间的水合物层将会从壁面上脱离进入液相,从而实现最终分解。
不同于加热分解,降压分解时外界没有热量输入,故水合物的吸热分解和排气降压的节流效应都会导致温降。因此,当水合物分解量较大、分解速率较快时,反应釜内温度急剧下降,降至冰点以下时,解离水就会结冰并覆盖在水合物表面,进而形成冰/水合物混合体。冰/水合物混合体与纯水合物的比较见图9。由图9可见,冰/水合物混合体因表面覆盖冰层而密度降低,故可悬浮在液相上部。除密度不同外,相较于细泥沙状的纯水合物,冰/水合物混合体呈现出较为蓬松的絮状,这是由冰/水混合体在上浮和聚集的过程中裹挟入油水混合液导致的。另外,由图9还可观察到,除冰/水合物混合体外,釜内其他区域的水合物均已分解完毕。这是因为表面冰层形成后,水合物的分解变为冰-水合物移动边界的消融问题[23],冰的存在增加了水合物分解过程传热和传质的阻力,水合物的分解产生了自我保护效应[24]。同时,冰对压力的变化不敏感,压力的下降并不会造成冰的快速分解。两者的共同作用导致了冰/水合物混合体分解速率的降低。
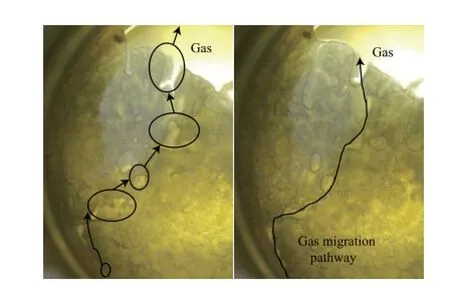
图8 实验4中降压分解时产生的气泡和气泡运移通道Fig.8 Bubbles generated by depressurizing dissociation and their migration pathway(No.4).

图9 冰/水合物混合体与纯水合物的比较Fig.9 Comparison between the ice/hydrates mixture and the pure hydrates.
2.3 注抑制剂分解
反应釜油基体系中水合物的注抑制剂分解同样具有强剪切区分解较快、液相中水合物颗粒呈“缩核”分解的特征,但壁面上及液相中水合物的分解过程与加热和降压分解存在较大不同,具体表现为水合物首先沿着抑制剂注入后的流动路径分解,如图10所示。注入抑制剂后气相壁面上附着的水合物多以块状或层状的形式快速、大片地脱落进入液相空间,整个脱落过程中观察不到水合物层有明显由致密逐渐变疏松的现象,且无明显的气泡产生。当直接接触到抑制剂的部分水合物都已大量分解时,其他部位的水合物才开始缓慢分解且其分解过程中的形态变化与加热和降压分解过程更为类似。

图10 实验7中水合物沿抑制剂注入后的流动路径分解Fig.10 Dissociation of the hydrates along the flow path(marked by red lines and arrows) of methanol in experiments(No.7).
3 分解动力学分析
3.1 评价参数定义
为了更好地对水合物分解效果进行分析比较,定义了3个表征水合物分解过程的动力学参数:分解时间(从分解开始起到分解结束所经历的时间,t)、分解速率(单位时间内分解产生的气体的物质的量,v)、分解效率(η)。分解速率计算式见式(1)。

式中,Δn为分解前后反应釜内气体的物质的量的变化量(降压分解时则为生成前后反应釜内气体物质的量的变化量),mol,可由Peng-Robinson方程计算得到。
加热分解效率(ηH)为单位过热度作用下水合物分解产生的气体的物质的量,计算式见式(2)。

式中,Δθ为过热度,℃。
降压分解效率(ηD)为单位压降下水合物分解产生的气体的物质的量,计算式见式(3)。

式中,Δp为压力降,MPa。
注抑制剂分解效率(ηI)为单位抑制剂浓度作用下单位时间内水合物分解产生的气体的物质的量,计算式见式(4)。

式中,w为抑制剂质量分数,%。
3.2 分解速率和分解效率
在各组实验中,虽然水合物的生成条件基本一致,但由于生成过程随机性较大,因此水合物的生成量并不相同,故分解时间不能直接用来比较不同方法下水合物的分解情况。不同实验的分解速率和分解效率见表4。
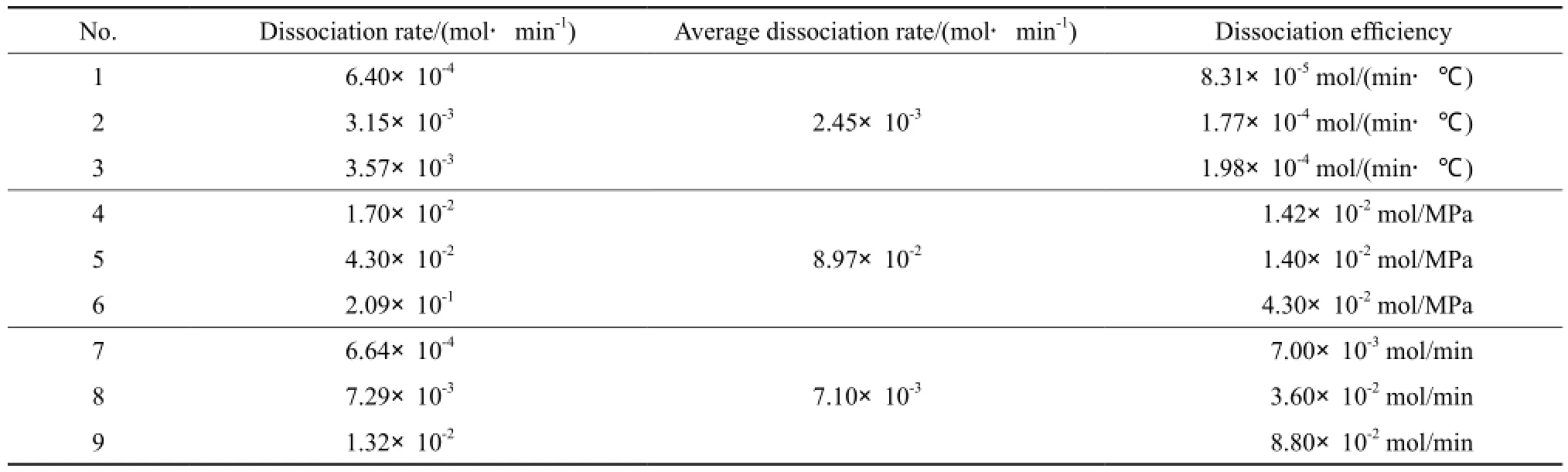
表4 分解速率及分解效率Table 4 Dissociation rate and dissociation efficiency of the natural gas hydrates
结合表1~4可知,水合物的分解速率随加热温度、降压速率和抑制剂质量分数的增大而增加。说明水合物的分解速率跟分解驱动力有关,分解驱动力越大,分解速率越高。其中,加热法的平均分解速率约为2.45×10-3mol/min,降压法的平均分解速率约为8.97×10-3mol/min,注抑制剂法的平均分解速率约为7.10×10-3mol/min。在实验工况下,实验中的分解速率范围为6.40×10-4~ 2.09× 10-1mol/min。
由表4还可知,采用加热法和注抑制剂法时,分解效率随加热温度和抑制剂质量分数的增大而增加。采用降压法分解水合物时,当降压速率分别为0.02 MPa/s和0.05 MPa/s时,分解效率几乎相同。根据对水合物形态变化的分析可知,这是由于降压速率为0.05 MPa/s时釜内温度过低,解离水结冰覆盖在水合物表面阻碍了水合物的进一步分解,从而导致分解效果大幅减弱。由于不同分解方法对分解效率的定义不同,故不同方法间分解效率的比较没有意义。
4 结论
1)油基体系中水合物的加热、降压和注抑制剂分解存在强剪切区分解较快、液相中水合物颗粒呈“缩核”分解等共性。
2)采用不同方法分解时水合物的宏观形态变化具有不同的特点,表现为水合物从壁面上脱离的方式不同、气泡产生的速率和数量不同以及壁面上是否有气体运移通道、体系中是否有冰相产生等。
3)分解速率随加热温度、降压速率和抑制剂质量分数的增大而增加。在实验工况下,分解速率范围为6.40×10-4~ 2.09×10-1mol/min。
[1] Sloan E D. Clathrate hydrates of natural gases [M].3rded. New York:Marcel Dekker,2007:1-5.
[2] Sloan E D. Fundamental principles and applications of natural gas hydrates[J].Nature,2003,426(6964):353-363.
[3] Hammerschmidt E G. Formation of gas hydrates in natural gas transmission lines[J].Ind Eng Chem,1934,26(8) :851-855.
[4] Sloan E D. Natural gas hydrates in fl ow assurance[M].3rded. New York:Elsevier Science Ltd,2010:1-36.
[5] Yousif M H,Sloan E D. Experimental investigation of hydrate formation and dissociation in consolidated porous media[J]. SPE Res Eng,1991,6(4):452-458.
[6] Zhao Jiafei,Lü Qin,Li Yanghui,et al. In-situ visual observation for the formation and dissociation of methane hydrates in porous media by magnetic resonance imaging[J].Magn Reson Imaging,2015,33(4):485-490.
[7] Fan Shuanshi,Zhang Yuzhen,Tian Genlin,et al. Natural gas hydrate dissociation by presence of ethylene glycol[J].Energy Fuels,2006,20(1):324-326.
[8] Kamath V A,Mutalik P N,Sira J H,et al. Experimental study of brine injection and depressurization methods for dissociation of gas hydrate[J].SPE Form Eval,1991,6(4):477-484.
[9] 史博会,王莹,吕晓方,等. 流动体系水合物分解研究进展[J].油气储运,2014,33(7):685-691.
[10] Boxall J,Greaves D,Mulligan J,et al. Gas hydrate formation and dissociation from water-in-oil emulsions studied using PVM and FBRM particle size analysis[C]//Proceedings of the 6thinternational conference on gas hydrates. British Columbia:Vancouver,2008.
[11] Peters D J,Selim M S,Sloan E D. Hydrate dissociation in pipelines by two-sided depressurization experiment and model[J].Ann N Y Acad Sci,2006,912(1):304-313.
[12] Boxall J,Hughes T,May E. Direct electrical heating of liquid-filled hydrate blockages[C]//Proceedings of the 7thinternational conference on gas hydrates. Scotland:Edinburgh,2011.
[13] Lachance J W,Sloan E D,Koh C A. Effect of hydrate formation/dissociation on emulsion stability using DSC and visual techniques[J].Chem Eng Sci,2008,63(15):3942-3947.
[14] Chen Jun,Liu Jun,Chen Guangjin,et al. Insights into methane hydrate formation,agglomeration,and dissociation in water + diesel oil dispersed system[J].Energy Convers Manage,2014,86(14):886-891.
[15] Gupta A,Moridis G J,Kneafsey T J,et al. Modeling pure methane hydrate dissociation using a numerical simulator from a novel combination of X-ray computed tomography and macroscopic data[J].Energy Fuels,2009,23(12):5958-5965.
[16] Ilhan S,Kahruman C,Yusufoglu I. Characterization of the thermal decomposition products of ammonium phosphomolybdate hydrate[J].J Anal Appl Pyrol,2007,78(2):363-370.
[17] Lee J D,Susilo R,Englezos P. Methane-ethane and methanepropane hydrate formation and decomposition on water droplets[J].Chem Eng Sci,2005,60(15):4203-4212.
[18] Hajar D,Ali H. Thermodynamic modeling of gas hydrate formation conditions in the presence of organic inhibitors,salts and their mixtures using UNIQUAC model[J].Fluid Phase Equilib,2015,39(4):101-117.
[19] Englezos P,Kalogerakis N,Dholabhai P D,et al. Kinetics of formation of methane and ethane gas hydrates[J].Chem Eng Sci,1987,42(1):2647-2658.
[20] Makogon Y F. Hydrates of hydrocarbons[M].Tulsa:Penn Well,1997:23-29.
[21] 万丽华,李小森,李刚. 热盐水分解甲烷水合物实验研究[J].现代化工,2008,28(7):47-50.
[22] 李淑霞,郝永卯,陈月明. 多孔介质中天然气水合物注热盐水分解实验研究[J].太原理工大学学报,2010,41(5):680-684.
[23] Takeya S,Shimada W,Kamata Y,et al. In situ X-ray diffraction measurements of the self-preservation effect of CH4hydrate[J].J Phys Chem A,2001,105(42):9756-9759.
[24] Handa Y P. A Calorimetric study of naturally occurring gas hydrates[J].Ind Eng Chem Res,1988,27(5):872-874.
(编辑 王 馨)
Study on dissociation of natural gas hydrate in oil-based systems
Song Guangchun,Li Yuxing,Wang Wuchang
(Key Laboratory of Oil-Gas Storage and Transportation Safety,China University of Petroleum(East China),Qingdao Shandong 266580,China)
Natural gas hydrates were formed in oil-based systems containing 30%(w) water in an autoclave equipped with visual windows,and then the dissociation processes of the hydrates through heating,depressurizing or adding methanol inhibitor were analyzed. The experimental results indicated that the common characters of the processes were the fast dissociation in strong shearing areas and the shrinking core dissociation in liquid phase. The hydrates exhibited different macro morphological changes when they dissociated through the three pathways,which included the ways that the hydrates fell off from the tube wall,the number of gas bubbles and their formation rates,whether or not there were migration pathways on the wall,and where or not there was ice phase in the systems. The dissociation rates increased with temperature rise,increasing depressurizing rate and increasing methanol concentration. The dissociation rate of the natural gas hydrates was in the range of 6.40×10-4-2.09×10-1mol/min in the experiments.
natural gas hydrate;dissociation;macro-morphological change;dissociation rate
1000-8144(2017)03-0348-08
TQ 026
A
10.3969/j.issn.1000-8144.2017.03.015
2016-09-19;[修改稿日期]2016-12-15。
宋光春(1992—),男,山东省泰安市人,博士生,电话 18660255608,电邮 UpcNGH_sgc@163.com。联系人:李玉星,电话 13370809333,电邮 lyxupc@163.com。
国家自然科学基金项目(51006120);高等学校博士学科点专项科研基金项目(20110133110004)。

