基于肿瘤标志物mRNA表达检测的指导性化疗治疗对NSCLC患者近远期疗效的影响
谢峰+陈昌南+林云笑
【摘要】 目的:探討基于肿瘤标志物mRNA表达检测的指导性化疗治疗对非小细胞肺癌(NSCLC)患者近远期疗效的影响。方法:选取2012年1月-2014年12月笔者所在医院确诊治疗的NSCLC患者100例,依据随机数字表法随机分为指导组和常规组,每组50例,常规组给予诺维本联合顺铂方案化疗治疗,指导组给予基于肿瘤标志物mRNA表达检测的指导性化疗(采用液相芯片技术检测肿瘤组织多种标志物mRNA后并依此选择化疗方案)治疗,随访2年,统计分析所有患者治疗效果、不良反应,治疗后0.5、1、2年的累积生存情况。结果:指导组治疗有效率明显高于常规组,差异有统计学意义(P<0.05);指导组不良反应发生率明显低于常规组,化疗疗程明显高于常规组,差异均有统计学意义(P<0.05);指导组治疗后0.5、1、2年累积生存率均明显高于常规组,差异均有统计学意义(P<0.05)。结论:基于肿瘤标志物mRNA表达检测的指导性化疗治疗可有效提高NSCLC患者的治疗疗效,且可有效减少药物毒副作用而提高耐受性,有利于改善生存预后水平,值得临床作进一步推广。
【关键词】 肿瘤标志物; mRNA表达; 指导性化疗; 非小细胞肺癌; 近远期疗效
Near and Forward Future Curative Effect of Based on mRNA Expression of Tumor Markers Detection Guidance Chemotherapy Treatment in Patients with NSCLC/XIE Feng,CHEN Chang-nan,LIN Yun-xiao.//Medical Innovation of China,2017,14(11):024-027
【Abstract】 Objective:To discuss the near and forward future curative effect of based on mRNA expression of tumor markers detection guidance chemotherapy treatment in patients with non-small cell lung cancer(NSCLC).Method:A total of 100 patients with NSCLC were selected from January 2012 to December 2014 in our Hospitals.According to the random distribution,all patients were divided into steering group and conventional group,
50 cases in each group.Conventional group was given novy this combined cisplatin chemotherapy,steering group was given based on mRNA expression of tumor markers detection guidance chemotherapy(used liquid chip technology to detect a variety of tumor markers mRNA and chemotherapy regimens in this choice) treatment,followed up for 2 years,statistical analyzed all of the patients after treatment efficacy,adverse reactions,the accumulation of 0.5,1, 2 yearss survival condition.Result:The therapeutic response rate of steering group was significantly higher than that of conventional group,there was statistically significant difference(P<0.05).The incidence adverse reactions rate of steering group was significantly lower than that of conventional group,the chemotherapy treatment course of the former was significantly higher than that of the latter,there was statistically significant difference(P<0.05).0.5,1,2 yearss cumulative survival rates after treatment of steering group were significantly higher than those of conventional group,there were statistically significant differences(P<0.05).Conclusion:Based on mRNA expression of tumor markers detection guidance chemotherapy treatment can effectively improve the treatment of patients with NSCLC curative effect,and it can effectively reduce side effects of drugs and improve patients tolerance,it is helpful to improve survival in patients with prognostic level,its worth of further clinical promotion.
【Key words】 Tumor markers detection; mRNA expression; Chemotherapy guidance; Non-small cell lung cancer; Near and forward future curative effect
First-authors address:The Peoples Hospital of Xinhui District in Jiangmen City,Jiangmen 529100,China
doi:10.3969/j.issn.1674-4985.2017.11.007
非小细胞肺癌(NSCLC)是临床上常见的癌症之一,其发病机制尚未明确,与吸烟、环境污染等因素有关,约60%以上的患者被发现时已处于中晚期,手术治疗疗效欠佳,因此化疗已成为该疾病主要的治疗方式之一[1]。有研究表明,常规化疗治疗虽可有效缓解患者的病情进展,但其临床疗效存在较为明显的差异,且副作用较明显,不利于患者顺利完成整个治疗。而国内外大量临床研究证实,某些肿瘤基因的mRNA表达情况与化疗药物疗效密切相关,提示在患者进行药物化疗前应进行相关基因表达水平检测,以确保化疗疗效的有效性[2-5]。对此,本研究通过给予患者基于肿瘤标志物mRNA表达检测的指导性化疗治疗,探讨其对患者近远期疗效的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取2012年1月-2014年12月笔者所在医院确诊治疗的NSCLC患者100例,依据随机数表法分为指导组和常规组,每组50例。指导组:男38例,女12例,依据分化程度分为高分化10例,中分化24例,低分化16例,依据组织类型分为鳞癌24例,腺癌26例,年龄45~64岁,平均(56.13±10.28)岁;常规组:男35例,女15例,依据分化程度分为高分化12例,中分化23例,低分化15例,依据组织类型分为鳞癌22例,腺癌28例,年龄45~65岁,平均(55.78±10.72)岁。本次研究已经笔者所在医院伦理委员会审批且通过,两组患者性别、分化程度、组织类型、年龄等一般资料比较,差异均无统计学意义(P>0.05),有可比性。
1.2 纳入与排除标准 纳入标准:(1)经临床症状、病史、实验室、病理学等证实为NSCLC[6];(2)化疗疗程2个或以上、预计生存期>3个月者;(3)患者或其家属签署知情同意书。排除标准:(1)伴有心、肝、肾等重要器官原发性严重性疾病者;(2)有精神病病史或沟通交流障碍者;(3)中途退出本次研究者[7-8]。
1.3 方法 常规组患者给予诺维本(法国 Pierre Fabre Medicament Production-Aquitaine Pharm International公司,注册证号 H20140083,1 mL∶10 mg)联合顺铂(江苏豪森药业股份有限公司,国药准字H20040813,30 mg∶6 mL)3周方案化疗治疗,持续4~6疗程,指导组患者给予基于肿瘤标志物mRNA表达检测的指导性化疗,即行常规经支纤镜或CT引导下穿刺活检或脱落细胞等方法收集癌变组织标本,送广州益善医学检验所采用分支DNA液相芯片技术行肿瘤组织ERCC1、TYMS、RRM1、TUBB3、TOP2A基因mRNA表达水平检测并依此选择化疗方案,对ERCC1 mRNA高表达者、RRM1 mRNA和TUBB3 mRNA低表达者选择吉西他滨(哈尔滨誉衡药业股份有限公司,国药准字H20040958,0.2 g)联合多西他赛(江苏恒瑞医药股份有限公司,国药准字H20080366,1.5 mL∶60 mg)3周方案,其中TYMSmRNA低表达非鳞癌者选择培美曲塞(南京先声东元制药有限公司,国药准字H20090135,0.5 g)、TUBB3 mRNA低表达者选择多西他赛、TOP2AmRNA高表达者选择依托泊苷(四川升和药业股份有限公司,国药准字H20045483,
5 mL∶100 mg)方案、RRM1 mRNA低表达者选择吉西他滨,对ERCC1 mRNA低表达者选择联合顺铂3周方案,其中RRM1 mRNA低表达者选择吉西他滨、TOP2A mRNA高表达者选择依托泊苷方案、TUBB3 mRNA低表达者选择多西他赛、
TYMS mRNA低表达非鳞癌者选择培美曲塞化疗,均化疗4~6疗程。
1.4 观察指标 所有患者每2个化疗疗程后进行1次超声或CT等影像学、血尿常规等检查,并通过电话、复诊等方式随访2年,统计分析所有患者治疗疗效、不良反应、治疗后0.5、1、2年的累积生存情况;其中疗效评估为,2个月瘤体最大相互垂直的直径乘积(DD2)增大>25%为恶化(PD),2个月DD2缩小<50%或增大<25%且持续时间>1个月为稳定(SD),DD2缩小>50%为部分缓解(PR),瘤体消失且持续时间>1个月为完全缓解(CR),治疗有效率=(CR例数+PR例数)/总例数×100%,不良反应包括恶心、骨髓抑制、脱发、呕吐。
1.5 统计学处理 采用SPSS 20.0软件进行数据处理,计量资料以(x±s)表示,比较采用t检验,计数资料用率(%)表示,比较采用 x2检验,以P<0.05为差异有统计学意义。
2 结果
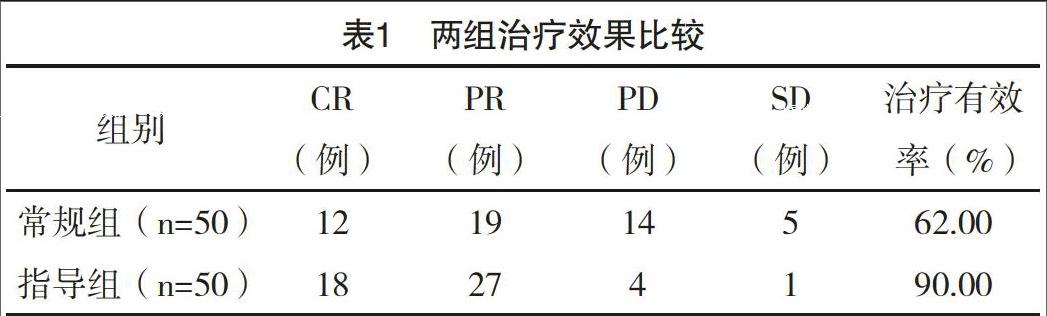
2.1 两组治疗效果比较 指导组治疗有效率明显高于常规组,差异有统计学意义( x2=10.746,P<0.05),见表1。
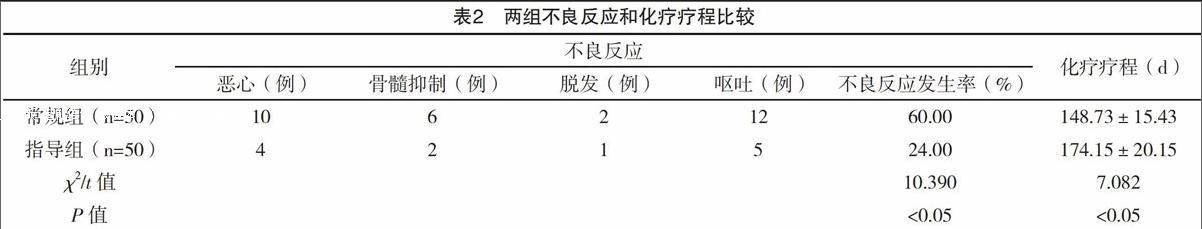
2.2 两组不良反应和化疗疗程比较 指导组不良反应发生率明显低于常规组,化疗疗程明显高于常规组,差异均有统计学意义(P<0.05),见表2。
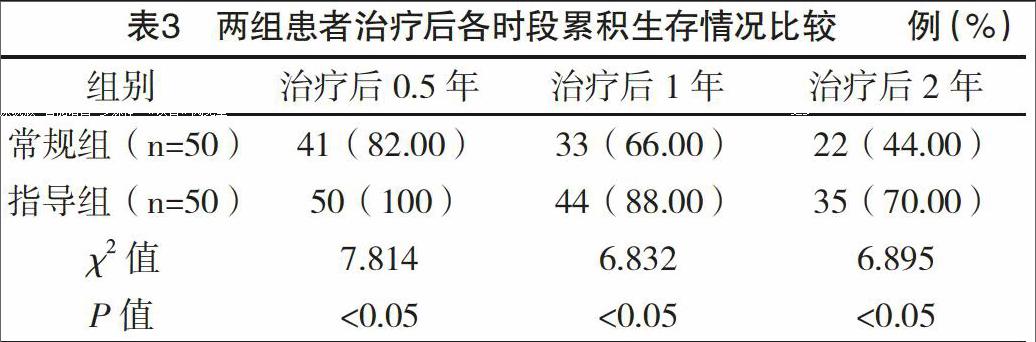
2.3 两组治疗后各时段累积生存情況比较 指导组治疗后0.5、1、2年的累积生存率均明显高于常规组,差异均有统计学意义(P<0.05),见表3。
3 讨论
NSCLC是世界上最常见的一种恶性肿瘤,且多数患者发现时已处于中晚期,可导致胸部胀痛、痰血、呼吸困难等症状,甚至死亡,其常用的治疗方法为化疗治疗,可有效缓解患者的临床症状[9-10]。有研究显示,常规化疗治疗虽可有效抑制患者肿瘤的增长,但只有部分患者明显受益,且副作用较明显,易使患者不能耐受而影响治疗的顺利的进行,导致疗效欠佳,故选择合理有效的化疗方案具有重要的临床意义[11-12]。而有研究表明,ERCC1是核苷酸外切修复家族中的成员,参与DNA链的损伤修复过程,其表达水平与铂类药物耐药的发生发展有关,RRM1则是DNA合成通路限速酶RR中的一个亚基,可作为吉西他滨的主要作用靶点,其高表达与后者疗效成负相关。而多数研究表明,TYMS表达水平与抗代谢类药物(培美曲塞等)疗效密切相关,高表达者疗效差,TUBB3表达水平则与抗微管类(紫杉醇类、长春碱类等)化疗方案疗效负相关[13-15],高表达者疗效差,且TOP2A表达水平与依托泊苷疗效正相关,提示在治疗中应依此谨慎选择化疗方案[16-20]。
对此,本研究通过给予患者讨基于肿瘤标志物mRNA表达检测的指导性化疗治疗,发现指导组患者治疗有效率、化疗疗程明显高于常规组(P<0.05),前者治疗后0.5、1、2年的累积生存率明显高于后者(P<0.05),表明该疗法可有效提高患者的近远期疗效;这可能是由于在常规化疗治疗中,药物虽可通过其抗肿瘤作用有效抑制肿瘤的生长,但由于肺癌的发生发展与某些基因的改变、多种细胞因子的正负性调节等有关,使不同患者对化疗药物的适应性和耐药性存在差异,导致药物未能有效在部分患者体内发挥应有的抗肿瘤作用,进而使治疗疗效欠佳,甚至诱发多重耐药,导致治疗失败,从而影响患者的近远期疗效。而在本研究治疗中,可能通过先对患者进行多种肿瘤标志物mRNA表达的检测,可有效评估不同患者对各种化疗药物的适应性和耐药性,并依此选择更优良的化疗方案,有利于使药物在进入体内后避免多重耐药的情况发生并发挥良好的抗肿瘤作用,进而有效抑制肿瘤的增长,从而提高患者的治疗疗效。此外,本研究还发现指导组患者不良反应发生率明显低于常规组,表明该疗法可有效减少药物对患者的毒副作用;这可能是由于化疗药物一般都具有较强的毒性,常规化疗方案在治疗部分不适应的患者时,易由于疗效欠佳而过度治疗,进而增加患者的治疗痛苦。而在本研究治疗中,可能由于通过有效评估患者化疗药物的耐药情况,对患者实施针对性的化疗方案,如多药联合或单药化疗等,可有效依据患者实际需求进行化疗,进而避免不当化疗的发生,有利于减少化疗的毒副作用。
综上所述,基于肿瘤标志物mRNA表达检测的指导性化疗治疗可有效提高NSCLC患者的治疗疗效,且可有效减少药物毒副作用而提高患者的耐受性,有利于改善患者的生存预后水平,值得临床作进一步推广。
参考文献
[1]尹志永,杨大勇,杨立丰,等.切除修复交叉互补基因1、核糖核苷酸还原酶M1亚基和3型β微管蛋白分子检测指导晚期非小细胞肺癌个体化治疗的临床效果[J].中国医药导报,2016,13(2):81-84.
[2]王展,李湘平,陈娟,等.ERCC1 rs1046282与肺癌铂类联合化疗毒副反应的相关性研究[J].中国临床药理学与治疗学,2015,50(8):923-927.
[3] Gong W,Zhang X,Wu J,et al.RRM1 expression and clinical out-come of gemcitabine-containing chemotherapy for advanced non-small-cell lung cancer:A meta-analysis[J].Lung Cancer,2012,75(3):374-380.
[4]李铁志,石彦涛,高少林,等.ERCC1、RRM1与BRCA1蛋白联合检测在非小细胞肺癌治疗中的价值分析[EB/OL].中国医学前沿杂志(电子版),2015,7(12):36-39.
[5] Pesta M,Kulda V,Fiala O,et al.Prognostic significance of ERCC1,RRM1 and BRCA1 in surgically-treated patients with non-small cell lung cancer[J].Anticancer Res,2012,32(11):5003-5010.
[6]陆舜,纪文翔,虞永峰.2014版《NCCN非小细胞肺癌临床实践指南》更新解读[J].中国医师进修杂志,2015,38(5):318-320.
[7]江波,涂长玲,何文杰,等.晚期非小细胞肺癌RRM1表达与吉西他滨疗效的相关性分析[J].肿瘤防治研究,2013,40(1):68-71.
[8] Rose M C,Kostyanovskaya E,Huang R S.Pharmacogenomics of Cisplatin Sensitivityin Non-small Cell Lung Cancer[J].Genomics Proteomics Bioinformatics,2014,12(5):198-209.
[9]余晶晶,祝兰兰,张伟,等.ERCC1和BRCA1基因在非小细胞肺癌术后辅助化疗患者预后中的作用[J].重庆医科大学学报,2013,38(5):517-522.
[10] Jett J R,Carr L L.Targeted therapy for non-small cell lung cancer[J].Am J Respir Crit Care Med,2013,188(8):907-912.
[11]孙运祥,何续逊,卢景彤,等.联合检测ERCC1、RRM1及β-tubulinⅢ基因表達用于指导晚期非小细胞肺癌个体化化疗的探讨[J].实用医学杂志,2013,29(15):2499-2501.
[12]许柏松,冯耘.联合检测蛋白ERCC1、Rad51和P53的表达与预测晚期非小细胞肺癌铂类药物化疗疗效的相关性研究[J].中国医药科学,2014,4(23):30-33.
[13]伍青,朱彦君,徐彪.多靶标检测平台分析肺腺癌患者不同分化程度中ERCC1、TYMS、RRM1、TUBB3基因表达及意义[J].现代肿瘤医学,2013,21(4):764-767.
[14] Simon G R,Schell M J,Begum M,et al.Preliminary indication of survival benefit from ERCCI and RRM I-tailored chemotherapy in patients with advanced nonsmall cell lung cancer:evidence from an individual patient analysis[J].Cancer,2012,118(9):2525-2531.
[15]文亢,李俊,李东斌.BRCA1、RRM1及ERCC1基因多态性与非小细胞肺癌化疗疗效相关性分析[J].浙江临床医学,2016,18(3):428-430.
[16]孟庆雨,王述民,许世广,等.ERCC1、TYMS、RRM1、TUBB3表达与非小细胞肺癌化疗疗效的相关性和意义[J].中国肿瘤,2013,22(8):661-665.
[17] Shimizu T,Nakanishi Y,Nakagawa Y.Association between expression of thyrnidylate synthase,dihydrofolate reductase,and glyci namide ribonucleotide formyltransferase and efficacy of pemetrexed in advanced non-small cell lung cancer[J].Anticancer Res,2012,32(10):4589-4596.
[18]白娟,郑玲,李茨,等.联合检测ERCC1、BRCA1、RRM1表达在非小细胞肺癌选择化疗方案中的意义[J].现代肿瘤医学,2016,24(21):3410-3413.
[19] Papadaki C,Sfakianaki M,Ioannidis G.ERCC1 and BRAC1 mRNA expression levels in the primary tumor could predict the effectiveness of the second-line cisplatin-based chemotherapy in pretreated patients with metastatic non-small cell lung cancer[J].
J Thorac Oncol,2012 (4):663-671.
[20]阳诺,马辉,冼磊,等.BRCA1、RRM1和TUBB3基因在非小细胞肺癌中的表达及其与化疗的關系[J].微创医学,2014,9(4):389-393.

