液质联用测定芍药甘草汤中3种有效成分的含量*
徐 玉 石镇东 郑小伟
浙江中医药大学基础医学院 浙江 杭州 310053
中药研究
液质联用测定芍药甘草汤中3种有效成分的含量*
徐 玉 石镇东 郑小伟#
浙江中医药大学基础医学院 浙江 杭州 310053
目的:采用高效液相色谱联用三重四级杆质谱(HPLC-MS/MS)测定芍药甘草汤中芍药苷、甘草酸及甘草次酸三种成分的含量。方法:色谱柱采用Eclipse Plus C18(2.1mm×50mm,1.8mm);流动相为0.1%甲酸乙腈和0.1%甲酸水溶液,流速设定为0.3mL·min-1,柱温为35℃,进行梯度洗脱。根据待检测化合物的性质,优化相关定量分析的质谱参数,多重反应监测(MRM),进行数据的采集。结果:芍药甘草汤中芍药苷、甘草酸及甘草次酸的含量分别为:160.46±3.82mg·ml-1,115.66±3.13mg·ml-1,8.34±0.34mg·ml-1。结论:本实验精密性良好,重现性高,分析方法准确,定量数据可靠。
HPLC-MS/MS 芍药甘草汤 芍药苷 甘草酸 甘草次酸
芍药甘草汤是《伤寒论》中配伍严谨、药简效佳的经典方剂,为后世医家所推崇。本方仅由芍药、甘草两味中药组成,具有柔肝止痉、缓急止痛的功效[1]。对芍药甘草汤入血原型成分进行测定,发现芍药甘草汤的药效物质基础为芍药苷、甘草酸、甘草次酸[2]。本文采用高效液相色谱联用三重四级杆质谱(HPLC-MS/MS)同时测定芍药甘草汤中芍药苷、甘草酸和甘草次酸的含量,为芍药甘草汤药效物质研究提供理论基础。
1 实验仪器及材料
1.1 实验仪器:1290 HPLC-6460 QQQ/MS(Agilent,美国);BS124S电子分析天平(赛利多斯科学仪器有限公司);Milli-Q Biocel纯水仪(美国Millipore公司);SHB-Ⅲ循环水式多用真空泵(郑州长城科工贸有限公司);RV10旋转蒸发仪(德国IKA公司);Freezone 6L冷冻干燥机(英国Labconco公司)。
1.2 实验材料:甲酸(色谱级)购于阿拉丁公司;甲醇和乙腈(均为色谱级)均购于美国Tedia公司;白芍、炙甘草来自浙江中医药大学饮片厂;芍药苷、甘草酸和甘草次酸标准品均购于中国药品生物制品检定所。
2 实验方法
2.1 供试品制备:将白芍、炙甘草各12g,打碎后,加以500ml水侵泡1h,煎煮2h,重复煎煮2次,合并滤液,浓缩至150ml,-20℃保存备用。
2.2 对照品溶液配制:精密称取对照品芍药苷2.42mg、甘草酸1.97mg、甘草次酸2.36mg分别置于2ml容量瓶中,制成对照品母液;所得芍药苷浓度为1.21mg·ml-1,甘草酸0.985mg·ml-1,甘草次酸1.18mg·ml-1。
2.3 标准曲线绘制:精密吸取不同比例的对照品母液,混合得到对照品混合溶液,然后将对照品混合溶液定容至2ml,得到系列浓度对照品溶液,用于标准曲线绘制,所得对照品浓度见表1。
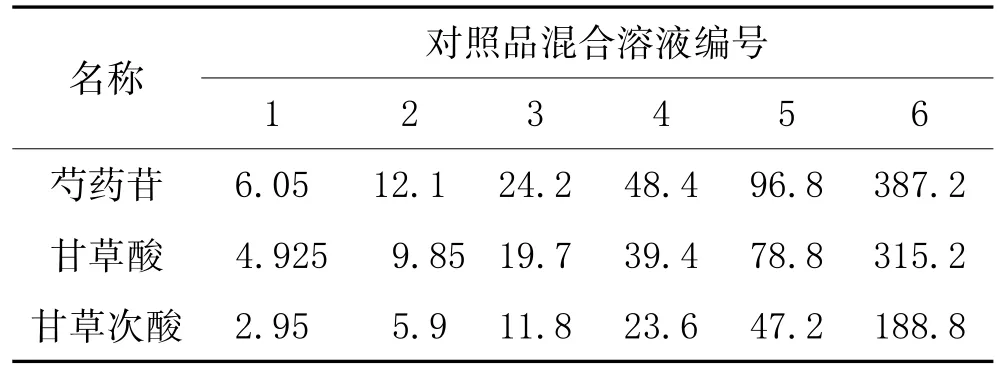
表1 对照品浓度(g·ml-1)
2.4 供试品前处理:取芍药甘草汤提取药液20ml,采用冷冻干燥后,残留物使用10ml色谱级甲醇超声溶解0.5h,溶液5000r·min-1×5min离心,取上清液使用0.22μm有机滤膜过滤,滤液可进行液质分析。
2.5 色谱质谱条件优化:经过对色谱条件的优化,最终确定的色谱条件:色谱柱为Eclipse Plus C18(2.1× 50mm,1.8mm);柱温为35℃;流动相(A为0.1%甲酸水溶液,B为0.1%甲酸乙腈);洗脱梯度(起始为5%B,保持1min,6min内增加至15%B,在11min内增加到22%B,在30min内升高到65%B,在32min内增加至95%B,保持1min,后运行时间设定为3min);流速设定为0.3ml·min-1;进样量为5ml。质谱条件为:氮气干燥气流速为9L/min,温度设定为350℃,雾化气压力为3.1bar,毛细管电压设定为3500V。检测方式为多重反应监测(MRM),数据采集速率为2spectrum/s,优化后的质谱参数见表2。
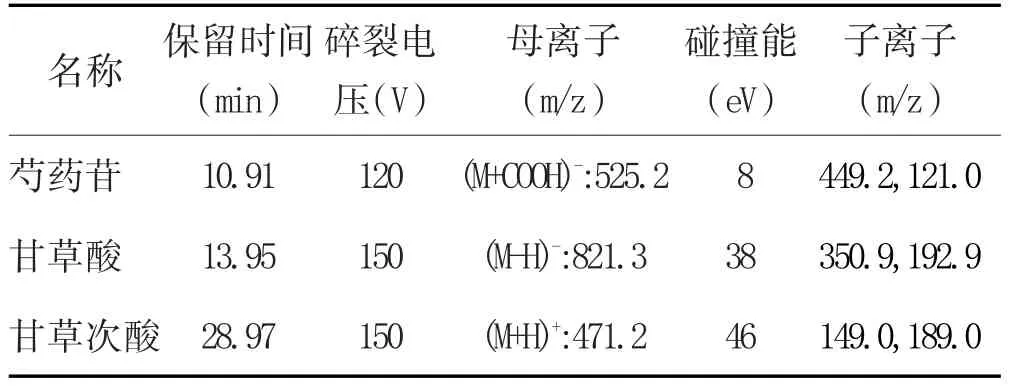
表2 优化后的化合物质谱参数
3 方法学考察和结果
3.1 色谱质谱条件优化:使用乙腈-水二元系统,使用优化的梯度洗脱程序,良好分离了芍药甘草汤中复杂成分。质谱条件优化过程中,主要优化了干燥气流速,毛细管电泳,碎裂电压以及碰撞能等,对于离子相应有较大影响的质谱参数。以芍药苷为例说明优化程中,首先是使用全扫面(Scan)模式找到芍药苷离子峰[M+COOH]-:m/z 525.2,使用负离子选择离子检测(SIM)和子离子扫描(PS)优化m/z525.2的碎裂电压和碰撞能为120V和8eV;再分析子离子扫描得到的二级质谱结果(图1),确定芍药苷的定量碎片离子m/z 449.2和m/z 121.0,并建立最终的多重反应检测(MRM)的定量方法。甘草酸和甘草次酸的质朴定量方法通过相同过程建立。

图1 芍药苷(A)、甘草酸(B)和甘草次酸(C)二级质谱图
3.2 标准曲线绘制:对照品按“2.3”方法处理,进样分析,所得标准曲线如表3,相关系数R2均大于0.997,表明标准曲线线性关系良好。

表3 线性方程结果,定量限和检测限
3.3 精密度、重复性及回收率实验:吸取一定浓度对照品,按“2.5”条件连续进样6次,测定3种对照品的浓度,分别计算相对标准偏差(RSD)。其结果均小于4%,表明方法稳定,精密度、重复性及准确度良好。见表4。
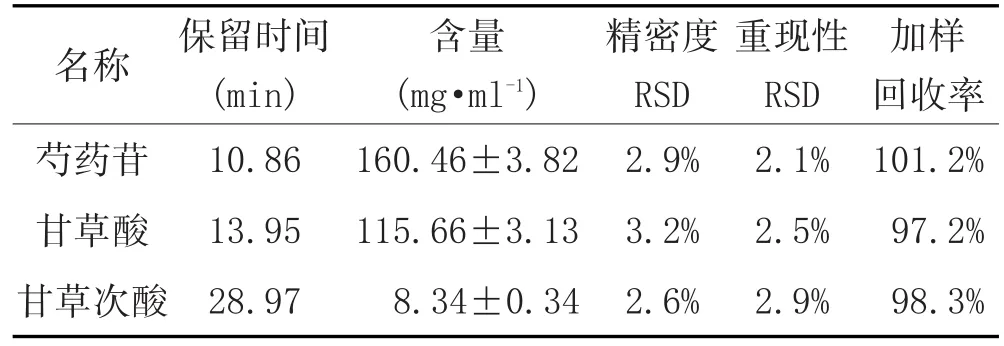
表4 有效成分定量结果
3.4 检测限和定量限:取已知浓度的标样溶液,按照“2.5”方法进样分析;以10倍信噪比为定量限,以3倍信噪比为检测限,得到定量限和检测限结果见表3。
3.5 样品含量测定:分别精密吸取芍药甘草汤供试品,按照“2.4”供试品处理方法处理,进样测定,平行进样3次。采用外标法计算芍药苷、甘草次酸及甘草酸的含量,结果见表4(n=3)。
4 结论
使用现代分析技术建立能被广泛接受的质量控制方法,可以使传统中药的应用变得有理有据[3]。本文采用HPLC/MS-MS同时测定芍药甘草汤中芍药苷、甘草酸和甘草次酸的含量。优化了毛细管电压、雾化器压力、干燥气温度和流速等离子源参数;使用全扫描找到目标化合物母离子,然后使用选择离子监测、自离子扫描分别优化了碎裂电压和碰撞能等质谱参数,建立了精密性良好、重现性高、准确的分析方法,定量测定了芍药甘草汤中芍药苷、甘草酸、甘草次酸的含量,这有助于芍药甘草汤的质量控制。
[1]高秀飞,胡婵娟,陈晓洁.芍药甘草汤加减治疗乳腺癌化疗期尿路感染疗效观察[J].浙江中医杂志,2013,48(3):183.
[2]陈梅.芍药甘草汤入血成分的研究[D].南京:南京中医药大学,2010.
[3]周建良,齐炼文,李萍.色谱指纹图谱在中药质量控制中的应用[J].色谱,2008,26(2):153-159.
2016-07-24
国家自然科学基金项目微小RNAs和长链非编码RNA对胃溃疡肝郁脾虚证线粒体低氧调控机制的研究,编号:81473596
# 通讯作者:郑小伟,E-mail:zhxw2103@163.com

