阿苯达唑致重度肝损伤病例分析及文献复习
苏风华,何登明
阿苯达唑致重度肝损伤病例分析及文献复习
苏风华,何登明*
药物性肝损伤;阿苯达唑;病例分析
阿苯达唑(Albendazole),商品名肠虫清,是高效广谱驱肠虫药物,其不良反应主要累及消化系统、皮肤及其附件、神经系统、血液系统等,常见严重不良反应主要包括:脑炎/脱髓鞘脑病、肝损害、贫血、白细胞减少[1]。笔者报道1例青年女性,不到2年的时间内先后发生2次阿苯达唑药物性重度肝损伤,结合2015版的《药物性肝损伤诊治指南》,报告如下。
1 病例报告
1.1 第一次发病情况女,24岁,因上腹部不适伴恶心9 d,皮肤、巩膜黄染4 d入院。无病毒性肝炎、脂肪肝等慢性肝病史,无饮酒史,家族中无类似患者。查体:未见肝掌、蜘蛛痣等慢性肝病体征,皮肤、巩膜重度黄染,肝脾未触及。肝功能:总胆红素238 μmol/L、直接胆红素129.7 μmol/L、白蛋白39 g/ L、球蛋白25 g/L、谷丙转氨酶1177 U/L、谷草转氨酶490 U/L、γ-谷氨酰转肽酶67 U/L、碱性磷酸酶92 U/ L;凝血酶原时间国际标准化比率1.25;乙型五项、甲肝IgM抗体、丙肝抗体,戊肝IgM抗体、弓形虫IgM抗体、风疹病毒IgM抗体、巨细胞病毒IgM抗体、单纯疱疹病毒IgM抗体、EB病毒IgM抗体等病毒标志物均阴性;自身免疫性肝病阴性;甲功五项及铜蓝蛋白正常。发病前1月曾自服阿苯达唑400 mg(2片),同时还服用几日的某种瘦身保健品(具体不详),无服用其他可疑药物、食物史。入院诊断:药物性肝损伤(阿苯达唑或保健品)。鉴于阿苯达唑的肝损伤发生率较低及损伤发生在服用阿苯达唑1个月后,肝损伤的来源更倾向于保健品。给予异甘草酸镁、还原型谷胱甘肽等常规保肝治疗,肝功能逐渐好转,45 d后恢复正常,随诊6个月无复发。
1.2 第二次发病情况该患者1年后,再次因上腹部不适伴恶心、皮肤、巩膜黄染7 d入院。发病前1个月再次自服阿苯达唑400 mg,无服用其他药物史。肝功能:总胆红素201 μmol/L、直接胆红素126.8 μmol/L、白蛋白40 g/L、球蛋白34.2 g/L、谷丙转氨酶941 U/L、谷草转氨酶490 U/L、γ-谷氨酰转肽酶81 U/L、碱性磷酸酶98 U/L;凝血酶原时间国际标准化比率1.20;各项肝炎标志物、自身免疫性肝病抗体均阴性;铜蓝蛋白及α-1抗胰蛋白酶正常;肝平扫及强化CT检查提示:肝右叶钙化灶,脾大,胆囊结石并胆囊炎;电子胃镜未见异常。给予常规保肝治疗后,肝功能逐渐恢复。
该患者两次发病的起病、发展、转归过程完全一致(图1)。结合既往病史,考虑第二次发病属于典型的药物再激发反应。因此,该例患者明确诊断为:药物性肝损伤,肝细胞损伤型,急性,RUCAM 10分(极可能,阿苯达唑),严重程度3级。
2 讨论
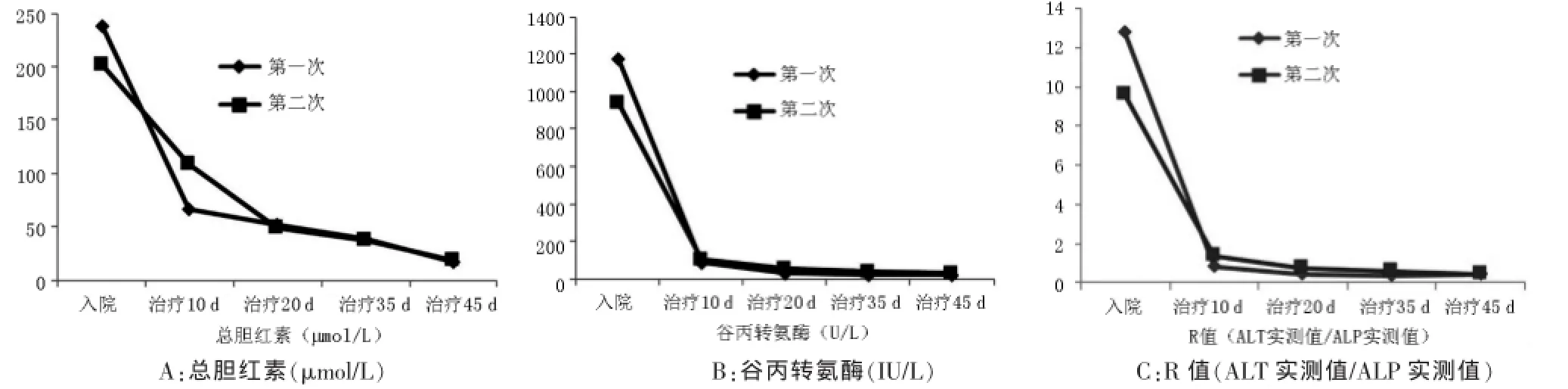
图1 两次发病肝功能主要指标变化情况
药物性肝损伤(drug-induced liver injury,DILI)是指由各类处方或非处方的化学药物、生物制剂、传统中药(TCM)、天然药(NM)、保健品(HP)、膳食补充剂(DS)及其代谢产物乃至辅料等所诱发的肝损伤[2]。已知全球有1100多种上市药物具有潜在肝毒性,我国急性DILI约占急性肝损伤住院比例的20%[2]。随着乙肝疫苗的广泛接种,HBV感染发生率将逐渐下降,DILI必然受到更多的关注。比如,近年土三七引起的肝小静脉闭塞病就受到了广泛关注[3]。
阿苯达唑为高效广谱驱虫药,药代动力学显示其口服后95%不吸收,在肠道内直接作用于成虫和虫卵,24 h内由粪便排出;其余5%由肝吸收,在肝微粒体酶和NADPH的作用下转化成丙硫咪唑亚砜和丙硫咪唑砜,前者可杀组织内幼虫和肠道内成虫,48 h内由肾排出。阿苯达唑的不良反应以神经系统不良反应[4-8]和过敏性反应的报道较多[9-12],引起严重肝损伤的报道较为少见。本例患者第一次发病前除口服阿苯达唑外,还同时服用保健品,近年来,保健品导致药物性肝损伤的报道越来越多,所以第一次发病不排除保健品因素所致肝损伤。第二次发病时,患者只服用过阿苯达唑,RUCAM因果关系评分达到10分,根据药物性肝损伤药物再激发反应的理论,确定为阿苯达唑导致的药物性肝损伤。
阿苯达唑不良反应的发生有一定的潜伏期,短的如过敏性休克、过敏性药疹等速发型过敏反应多在用药后30 min内发生,神经系统不良反应多在用药后3 d至数月发生,最长的如血液系统损害多在用药半年内发生[1]。本例阿苯达唑肝损伤的潜伏期较长,两次发病都是在服药后1个月左右开始出现自觉症状。文献报道阿苯达唑肝损害潜伏期多在服药后数小时至几日,1个月或数月后发病罕见报道[13-16]。不同病例潜伏期的长短可能在发病机制上存在差异。
药物性肝损伤发生机制有直接肝不良反应和特异质性肝不良反应两种。直接肝不良反应是指摄入体内的药物和(或)其代谢产物对肝产生的直接损伤,具可预测性,与药物剂量密切相关,潜伏期短,个体差异不显著[2]。特异性肝不良反应作用是由于药物代谢酶系、跨膜转运蛋白及溶质转运蛋白的基因多态性导致酶或转运蛋白功能异常,增加了宿主对DILI的易感性,具不可预测性,临床较为常见,个体差异显著,与药物剂量常无相关性,动物实验难以复制,临床表现多样,又可分为免疫特异质性DILI和遗传特异质性DILI[2]。从发病机制上看,本例阿苯达唑肝损害考虑为特异质性肝不良反应,遗传特异质性DILI可能性较大,药物代谢相关基因多态性可能是导致其发生严重肝损伤的主要原因。刘毅[13]报道1例口服史克肠虫清后3 d即出现明显症状,首次立即出现畏寒、发热等过敏反应,第二次服药后乏力、食欲缺乏、尿黄,皮肤、巩膜黄染等表现,考虑为免疫变态反应介导的药物性肝炎。因药物代谢涉及多种酶类及蛋白质,具体何种基因多态性决定了阿苯达唑对本例患者产生肝不良反应,有待深入研究。
该例肝损伤较重,严重程度达到3级,属于重度肝损伤,虽然凝血机制并未受损,但总胆红素和谷丙转氨酶升高幅度均超过10倍正常上限。根据受损靶细胞类型,本例阿苯达唑肝损伤临床分型为典型的肝细胞损伤型,主要以谷丙转氨酶及胆红素升高为主,碱性磷酸酶升高及白蛋白下降不明显,无明显瘀胆情况。虽然本例肝损伤较重,但对常规保肝药物治疗比较敏感,40 d内肝功能完全恢复正常,这也符合其肝细胞损伤性的病理特点。王婧等[16]报道,41例接受阿苯达唑治疗的广州管圆线虫病患者,发生肝功能异常者26例,主要表现为转氨酶轻中度升高,仅1例出现总胆红素升高。可见阿苯达唑引起重度肝损伤者并不常见。国外亦有阿苯达唑引起肝损伤的报道,但不如国内报道多[17-21]。
尽管阿苯达唑耐受性良好、价格经济、疗效肯定,且用于“蛔虫病、蛲虫病”适应证是作为非处方药管理的。赵世丹等[1]对58例个案报道进行分析时,未明确诊断或自行服用的达30例,占个案报道总数的51.72%,其中不乏严重不良反应的病例。该例患者服用阿苯达唑就是典型的自发行为,未在任何医师指导下进行,亦未进行大便虫卵等相关检查,仅在自觉“食欲不佳”的情况下,凭儿时祖母的“定期打虫”观念和“肠虫清”广告的影响而自行决定服用阿苯达唑。
总之,阿苯达唑可在特定人群中发生重度肝损伤,应严格把握适应证,尽可能在医师指导下应用,避免在诊断不明确的情况下自行服用等不合理使用现象,以最大限度减少其不良反应的发生。
[1]赵世丹,王慧,刘翠丽.阿苯达唑不良反应的文献分析[J].中国药物警戒,2013,10(5):299-302.
[2]中华医学会肝病学分会药物性肝病学组.药物性肝损伤诊治指南[J].临床肝胆病杂志,2015,31(11):1752-1769.
[3]从明,何芳.土三七致肝小静脉闭塞病3例[J].当代医学,2014,20(20):132-133.
[4]刘琦,田淑芬,吴珊.肠虫清所致的变态反应性脑病1例[J].实用医学杂志,2011,27(14):2618.
[5]王苹莉,倪渝鲲.阿苯达唑致脱髓鞘脑病1例[J].药物流行病学杂志,2011,20(7):381.
[6]袁春云,陈瑶,尹炜凡.丙硫咪唑致脑干及高颈段脊髓脱髓鞘病1例报告[J].临床神经病学杂志,2010,23(5):388.
[7]王夏红,李蜀渝,穆俊林.咪唑类驱虫药致迟发性脑病45例分析[J].中国误诊学杂志,2004,4(3):443-444.
[8]唐干烈.肠虫清治疗囊虫病致迟发性脑水肿1例[J].蛇志,2000,12(3):79-80.
[9]周永红.肠虫清引起结肠过敏性紫癜1例报告[J].浙江临床医学,2004,6(10):834.
[10]张金才,隋志芳.肠虫清致过敏性紫癜1例[J].潍坊医学院学报,2004,26(2):150.
[11]刘思同.服用史克肠虫清引起过敏性紫癜1例报道[J].井冈山医专学报,2001,8(1):88.
[12]刘福文,谢淑荣,杨万荣.肠虫清致严重荨麻疹一例[J].小儿急救医学,2001,8(2):84.
[13]刘毅.史克肠虫清致急性肝损伤一例[J].临床肝胆病杂志,2001,17(3):155.
[14]张琪.阿苯达唑致发热肝脏损害1例[J].药物流行病学杂志,2009,18(5):385-386.
[15]李国进.肠虫清致肝脏损害1例[J].人民军医,1991(10):59.
[16]王婧,郑晓燕,阴赪宏,等.阿苯达唑致广州管圆线虫病患者肝损害的临床分析[J].中国病原生物学杂志,2008,3(3):209-211.
[17]Bagheri H,Simiand E,Montastruc JL,et al.Adverse drugs relation to anthelmintics[J].The Annals of Pharmacotherapy,2004,38(3):383-388.
[18]El-Mufti M,Kamag A,Ibrahim H,et al.Albendazole therapy of hydatid disease:2-year follow-up of 40 cases[J].Ann Trop Med Parasitol,1993,87(3):241-246.
[19]Ríos David,Restrepo Juan C.Albendazole-induced liver injury:a case report[J].Colomb Med,2013,44(2):119-120.
[20]Choi GY,Yang HW,Cho SH,et al.Acute drug-induced hepatitis caused by albendazole[J].J Korean Med Sci Korea South,2008,23(5):903-905.
[21]Amoruso C,Fuoti M,Miceli V,et al.Acute hepatitis as a side effect of albendazole:a pediatric case[J].Pediatr Med Chir,2009,31(6):262-264.
[2016-08-20收稿,2016-09-18修回][本文编辑:董冰媛]
R657.3
B
10.14172/j.issn1671-4008.2017.03.014
271000山东泰安,解放军88医院全军肝病诊治中心(苏风华,何登明)
何登明,Email:hedengming@sina.com

