脂肪双胺稀土金属配合物的合成及催化性能的研究*
周 琳,冯乙巳,朱 强
(1.桐城师范高等专科学校;2.合肥工业大学)
*安徽省高等学校自然科学研究重点项目(KJ2016A701)
0 引言
Henry反应是基于羰基和含α-活泼氢的硝基烷烃化合物发生亲核取代的反应.它是形成C-C键的常用方法,生成的产物β-硝基醇的双官能团化合物则是有应用前景广阔的中间体,可以合成硝基烯,硝基酮,2-氨基醇等多种化合物[1].特别是通过在不对称Henry反应中进一步还原可以得到的手性β-硝基醇类化合物,其用途更为广泛,很多具有生物活性的药物都可以用它合成[2].为了避免在反应中过多使用有机试剂而造成的环境污染问题,通过水相或无溶剂Henry 反应就成为人们研究的方向.Ballini等人分别用新型相转移催化剂水溶液中进行Henry反应和用化学当量的KOH粉末在无溶剂条件下来进行Henry反应,存在后期提纯中仍需要有机试剂,操作繁冗,产率不是很高等问题[3].
将脂肪双胺配体稀土金属配合物应用于催化Henry反应,合成在很多领域具有广泛应用的β-硝基醇及其衍生物,解决工业生产和日常生活所需要的防腐杀菌剂、杀菌灭藻剂和工业水处理剂等需求,同时β-硝基醇及其衍生物是很多天然产物和医药的中间体,因此选择性地催化不对称Henry反应具有很高的研究价值[4].尽管目前文献已经报道了一些具有催化活性的稀土金属配合物,但即具有高催化活性又具有一定经济实用性的稀土金属配合物却不多.
该研究的主要内容是:通过相应的合成手段,组装出多个脂肪双胺配体稀土金属配合物;通过现代的科学表征手段对所组装的配合物进行构架表征,然后进一步研究其催化Henry反应活性.为Henry反应制备β-硝基醇及其衍生物提供合理的反应途径.
1 实验部分
1.1 实验所需仪器和试剂
实验过程中所用的主要仪器和原料见表1.

表1 主要试剂仪器
1.2 脂肪双胺化合物制备
(1)N,N-二甲基乙二胺为基体(简称L1H2)
在250 mL的圆底烧瓶内加入约150 mL的无水甲醇,开启搅拌,依次加入N,N-二甲基乙二胺(84.7mL, 772 mmol)和37%乙二醛水溶液(25 mL, 336 mmol),水浴温度在75℃,反应24 h左右,反应体系逐渐出现白色悬浊物,TLC定时监测(薄层硅胶点板)至反应物不显现为反应终点.冷却至室温后,分批加入NaBH4对其进行还原,TLC监测至原料基本消失,加水淬灭,有固体析出,用CH2Cl2萃取两次,减压抽滤,得到白色固体,用冷甲醇洗涤数次,真空干燥,得白色粉末,产率约67.2%.主要反应为:

13C-NMR解谱

1H-NMR解谱

(2)苯甲胺为基体制备 (简写为L2H2)
在圆底烧瓶内加入约100 mL无水甲醇,磁开启搅拌,依次加入乙二醛水溶液(7.0 mL,84 mmol)和苯甲胺(18.5 mL, 168 mmol),控制油浴温度65℃,反应约24 h.后续处理与1.3(1)相同,最终产率:61.1%.主要反应为:

13C-NMR解谱
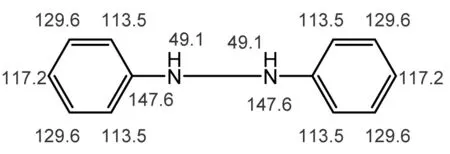
1H-NMR解谱

(3)环己胺为基体制备(简写为L3H2)
在圆底烧瓶内加入约150 mL无水甲醇,磁开启搅拌,依次加入乙二醛水溶液(10.0 mL, 120 mmol)和环己胺(27.7 mL, 240 mmol),控制油浴温度70 ℃,反应约24 h.后续处理与1.3(1)相同,最终产率:72.7%.反应为:

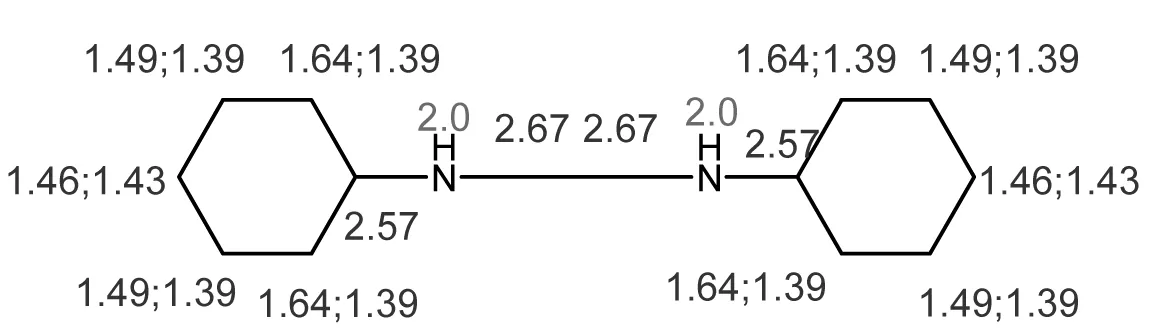
13C-NMR解谱

1H-NMR解谱
1.3 稀土金属配体制备
1.3.1无水三氯化镧的制备
称取10 g的La2O3,用20 mL浓HCl溶解,振荡使固体溶解并澄清,再加入15 g分析纯NH4Cl,用加热套加热,待溶液澄清后趁热用布氏漏斗减压抽滤,置于烘箱蒸干溶液,把所得固体装入升华管,减压状态下逐步升温以此除水.然后将温度逐渐升至450 ℃,让余下的NH4Cl慢慢升华,直至没有NH4Cl升华,得到无水三氯化镧,在氮气保护下冷却后,标定稀土含量备用[5].
1.3.2环戊二烯基钠制备
将两口瓶经过脱水脱氧处理过后,加入100 mL四氢呋喃和固体NaOH(过量),启动搅拌,通过注射器加入一定量新蒸馏的环戊二烯,反应中有气泡产生,当气泡结束后,在40 ℃的温度下反应 8~10 h.定期取样检测溶液浓度,至产物的浓度不再变化后停止反应,过滤过量的NaOH,得到浅红色环戊二烯基钠/四氢呋喃溶液,标定浓度后封管备用[6].
1.3.3(C5H5)3La(THF) 的合成
在室温下称取无水LaCl39.38 g (41.2 mmol),加入反应瓶中,搅拌同时缓缓加入适量THF溶液,将反应瓶密封,升温至50℃左右,持续活化至无块状LaCl3.冷却至室温后,在搅拌下向活化后的LaCl3的THF悬浊液中注射加入3.0当量的C5H5Na(123.6 mmol) 的THF溶液,将反应瓶密封,室温反应12 h.持续加热,然后用THF进行多次萃取,趁热通过离心机除去NaCl,在室温下澄清溶液析出大量无色块状晶体,标定含量后封存备用.
1.4 脂肪双胺稀土金属配合物的合成
由于稀土金属配合物对H2O和O2均极为敏感,因此在操作中需要采用标准的Schlenk技术,整个实验在无水无氧和Ar保护的条件下进行.实验过程中以循环泵制冷的方法降温,用水浴加热的方法升温.对易爆、易燃、有毒和有刺激性等物质的操作和处理,按照相关的操作规定进行[7].
(1)L1H2-稀土金属配合物制备
在室温下称取(C5H5)3La(THF) (0.96 g, 2.70 mmol),加入三口烧瓶中,缓慢加入THF溶液, 称取L1H2配体(8.10 mmol),加入离心瓶中并使用四氢呋喃充分溶解,再将该配体溶液缓慢加入到(C5H5)3La(THF)液的三口烧瓶中,室温反应24 h后,溶液混浊且有固体物质析出,通过离心机使固液分离.得到的固体用过量四氢呋喃溶解,持续加热,通过二次结晶提高产品纯度, 产率约73%,反应后生成的稀土金属配合物为LaR3型[8].
(2)L2H2-稀土金属配合物制备
称取(C5H5)3La(THF) (0.96g, 2.70 mmol),加入三口烧瓶中,加入THF溶液, 在离心瓶中称取L2H2配体(8.10 mmol),后续操作与(1)相同,产率63.3%.
(3)L3H2-稀土金属配合物制备
称取(C5H5)3La(THF) (0.96 g, 2.70 mmol),加入三口烧瓶中,加入THF溶液, 在离心瓶中称取L3H2配体(8.10mmol),后续操作与(1)相同,产率51.7%.

1.5 稀土金属配合物催化Henry反应
在硝基甲烷(CH3NO2)和苯甲醛(Ar-CHO)的Henry反应中存在副反应,在设计催化剂时需要尽量避开这些副反应,常见的副反应有:脱水、醛的自身缩合和Nef型反应的发生[9].

图5
在研究中发现L1H2-稀土金属配合物、L2H2-稀土金属配合物、L3H2-稀土金属配合物均可以有效地催化 Henry 反应,选用产率较高的L1H2-稀土金属配合物作为催化剂,从催化剂用量、温度、反应时间对反应条件进行评价优化.
2 结果与讨论
2.1 催化剂用量
由表2可以看出,增加催化剂的用量有助于提高反应的产率,当催化剂用量过少(0.5 mol%),Henry反应产率偏低,产率仅为51%,将催化剂用量增加到1 mol%时,反应产率迅速提高至75%,将催化剂用量增加到2 mol%时,产率可达83%.当催化剂用量继续提高时,产率趋于平缓.综合考虑,催化剂用量为2 mol%时,便可以达到较好的催化反应效果.

表2 LaR3催化Henry反应
2.2 反应温度
为了避免2 mol%以上的催化剂用量对产率影响过大,实验数据不能明显看出温度对反应的影响,我们选用1 mol%的催化剂用量. 由表3数据可知, 0~40℃时升高温度有利于反应进行,产率明显提高,但是40℃以上继续升温反而会使产率不断降低.当反应温度达到80℃时,反应体系的颜色明显变化有红棕色出现,可能存在副反应.在反应温度为40℃时,反应产率可达82%,所以认为最佳温度为40℃.

表3 LaR3催化Henry反应
2.3 反应时间
由表4可以发现,Henry在催化剂作用下反应速率得很快,反应在进行0.5 h后产率提升速度较快,如果要得到更高产率应当延长反应时间,反应在进行2 h后,产率即达到68%,反应在进行3 h后,随着时间的延长反应产率继续缓慢地提升,当反应在进行5.5 h后,产率达到85%,继续延长反应时间,产率提高趋于平缓.所以,选择5.5 h为最佳反应时间.

表4 LaR3催化Henry反应
3 结论
该研究通过以N,N-二甲基乙二胺、苯甲胺和环己胺为基体,组装成三种LaR3稀土金属配合物.通过从催化反应时间、反应温度、催化剂用量和催化剂本身的合成产率四个方面来综合评价三种LaR3稀土金属配合物作为催化剂的性能和优势,最终选用L1H2-稀土金属配合物作为硝基甲烷(CH3NO2)和苯甲醛(Ar-CHO)反应的催化剂.当催化剂用量为2 mol%、反应温度为40℃、反应时间为5.5 h时,硝基甲烷(CH3NO2)和苯甲醛(Ar-CHO)的Henry反应在催化剂作用下,副反应少,反应速率很快,最高产率可达85%.
[1]王亚军,李敬芬.超声催化α-酮酰胺的Henry反应研究[J].化学研究与应用,2012,24(08):1263-1265.
[2]刘腾,刘建军,贺池先,等.多共轭硝基二烯炔/硝基烯炔的合成以及应用研究进展[J].有机化学,2017,37(10):2609-2618.
[3]Nuno M R Martins,Kamran T, Mahmudov, Ftima M C, et al. 1D Zn(Ⅱ) coordination polymer of arylhydrazone of 5,5-dimethylcyclohexane-1,3-dione as a pre-catalyst for the Henry reaction[J]. Catalysis Communications,2016,87.
[4]张淑君,石莉娜,陈璐璐,等.Salen手性配体在不对称催化反应中的应用研究[J].化学工程与装备,2017(7):222-225.
[5]Wang Zhonghang,Devin Rappleye,Michael F Simpson. Voltammetric Analysis of Mixtures of Molten Eutectic LiCl-KCl Containing LaCl3and ThCl4for Concentration and Diffusion Coefficient Measurement[J]. Electrochimica Acta,2016:191.
[6]Ga⊇lle Malik,Angélique Ferry, Xavier Guinchard,et al. NO Bond as a Glycosidic‐Bond Surrogate: Synthetic Studies Toward Polyhydroxylated N ‐Alkoxypiperidines[J]. Chemistry - A European Journal,2013,19(6).
[7]薛科创,闫晓前.金属有机化合物的制备技术[J].山东化工,2014,43(1):98-100.
[8]刘博,顾佳,苏占华. 由Si_2W_(18)多酸构筑的过渡金属铜-有机配合物的合成及晶体结构[J]. 哈尔滨师范大学自然科学学报,2011,27(4):67-70.
[9]车阳,王锐,杜正银.聚乙二醇作为溶剂和催化剂载体在有机合成中的应用[J].化学世界,2017,58(8):490-503.

