氧化亚铜微粒的改性及其光催化性能研究
邵城,罗啸,马亚楠,张传坤,代银宝,范杰灿,杜明哲,史兆辉
(湖北汽车工业学院 理学院,湖北 十堰 442002)
氧化亚铜微粒的改性及其光催化性能研究
邵城,罗啸,马亚楠,张传坤,代银宝,范杰灿,杜明哲,史兆辉
(湖北汽车工业学院 理学院,湖北 十堰 442002)
采用液相还原法首先合成立方Cu2O微粒,进而以NaBH4对其进行改性。利用X射线衍射仪、扫描电子显微镜对产物的物相及表面形貌进行表征,并开展了产物对甲基橙溶液光催化降解性能的初步研究。结果表明:改性后的微粒形貌为立方体,随着NaBH4剂量的增大,其光催化性能呈现先增强后减弱的趋势,当NaBH4与Cu2O摩尔比为1:10时,所制备的微粒具有最优的光催化性能。
氧化亚铜;改性;光催化
微纳米材料由于具有独特的物理化学性质引起了人们的广泛关注[1],其性能由一系列因素决定,比如材料的组成、尺寸、形貌和结构等[2]。通过微米、亚微米和纳米尺度上多层次微观结构的精细调控,以实现材料在微观结构参数上可控制备,对于获得高性能的微纳米材料具有重要意义,是科研工作者不断探索的一个重要研究领域[3]。
光催化降解技术可以利用太阳能降解环境中的有机污染物,和其它污染物治理方法相比,具有能耗低、反应条件温和、操作简便、无二次污染、可直接利用太阳能等优势,是解决当前环境污染的重要途径之一[4]。因此研制高性能光催化材料具有深远的战略意义。
目前,在众多光催化剂中,金属氧化物半导体具有良好的活性和优越的光电稳定性[5]。其中,二氧化钛(TiO2)材料具有光催化性能好、化学稳定性好、价格便宜、无毒、原料易得、可分解大部分有机污染物的特点,是一种研究的最广泛的半导体光催化剂[6]。然而,锐钛矿相的二氧化钛禁带宽度为3.2 eV,只能吸收波长小于387.5 nm的紫外光用于光催化反应[7]。而太阳光中紫外光所占的能量只有太阳辐射的7%。因此二氧化钛光催化剂对于太阳能的利用效率较低。
氧化亚铜(Cu2O)作为一种重要的p型半导体材料,在太阳能电池[8]、催化降解有机污染物[9]、葡萄糖传感器[10]、气体传感器[11]、锂离子电池[12]、微纳米粒子制备的模板材料[13]、催化制氢[14]等领域具有广泛的应用价值,引起了科研工作者的关注。Cu2O禁带宽度约为2.1 eV,可吸收波长小于590 nm的太阳光用于光催化反应。相比于TiO2,Cu2O最大的优点是可以充分利用太阳光中的可见光部分,具有较高的太阳能利用效率。
文中利用液相还原法制备了一种立方氧化亚铜微粒,并利用不同量NaBH4溶液对其进行改性,研究了NaBH4与Cu2O的摩尔比对产物光催化性能的影响。
1 实验
1.1 试剂
一水合乙酸铜(Cu(CH3COO)2·H2O)、氢氧化钠(NaOH)、葡萄糖(C6H12O6)、硼氢化钠(NaBH4)。所有药品均为分析纯。
1.2 立方Cu2O微粒的制备
烧杯中加入200mL去离子水,水浴加热到70℃,继续加入2.00 g一水合乙酸铜,磁力搅拌10min,使其充分溶解,获得蓝色澄清溶液。称量2.40 g氢氧化钠,加入到10mL去离子水中,充分溶解后,将氢氧化钠溶液缓慢滴入乙酸铜溶液中,烧杯内的蓝色澄清溶液逐渐变为黑色悬浊液。等待10min后,再向悬浊液中缓慢滴入0.1 g·mL-1的葡萄糖溶液4mL,在70℃的条件下搅拌45min,悬浊液的颜色由黑色逐渐转变成为砖红色。将所得的沉淀用离心的方法取出,用水和酒精分别洗若干遍并干燥,得到立方Cu2O微粒。
1.3 Cu2O微粒的改性
取3个烧杯,每个烧杯中加入0.71 g立方Cu2O微粒,再加入50mL去离子水,通过反复超声和搅拌使Cu2O微粒充分分散。接着向每个烧杯中注入1.25mol·L-1的NaBH4溶液0.4mL、1mL和2mL,即反应过程中NaBH4与Cu2O摩尔比分别为1∶10、1∶4和1∶2。加入NaBH4溶液后,悬浊液的颜色迅速由砖红色变为黑色。离心取出沉淀,将所得样品用水和酒精清洗若干次并干燥,得到改性产物。
1.4 样品的表征方法
采用FEINova NanoSEM 450扫描电子显微镜对制备的样品进行形貌观测。利用SHIMADZU XRD-7000对样品进行X射线衍射表征。
1.5 光催化性能的测试方法
光催化反应在南京胥江XPA-7光化学反应仪内进行。取质量浓度为10mg·L-1的甲基橙(MO)溶液50mL,加入到石英试管中,并加入50mg待测粉末,搅拌使其充分分散。在350W氙灯照射条件下进行光催化反应。每隔15min进行一次取样,对取出的液体离心分离,取其上层清液,在日立UH5300紫外可见分光光度计上测定其吸光曲线。利用吸光曲线上464 nm的峰高,分析甲基橙的浓度。根据降解过程中甲基橙的浓度变化评价催化剂的性能。
2 结果及分析
2.1 立方Cu2O的形貌和结构分析
利用液相还原法,以乙酸铜作为铜盐提供铜离子,葡萄糖作为还原剂,制备了分散性较好的立方Cu2O微粒。制备过程中,Cu2+首先与OH-离子发生反应,生成Cu(OH)2沉淀。当OH-的浓度较高时,Cu(OH)2与OH-反应得到四羟基合铜络离子[Cu(OH)4]2-,之后[Cu(OH)4]2-被葡萄糖还原,生成Cu2O沉淀。整个过程中发生的化学反应为
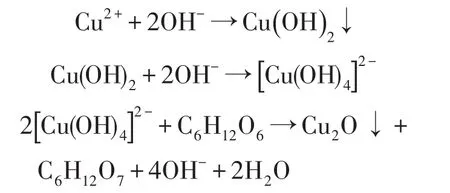
图1 为不同放大倍数下的立方Cu2O微粒的SEM图像及粒径统计图,可见在70℃水浴条件下可以得到分散性良好的Cu2O晶体,产物形状为立方体,平均尺寸为3.48μm,晶体表面暴露6个{100}晶面。
图2 为立方Cu2O微粒的XRD图谱。样品的衍射峰出现在2θ为29.7°,36.6°,42.4°,61.6°,73.9°和77.7°的位置,与立方相结构的Cu2O的标准谱(JCPDSNo.05-0667)吻合,分别对应于Cu2O的(110),(111),(200),(220),(311),(222)晶面。同时立方Cu2O微粒的主要XRD衍射峰强而窄,反映出其结晶性非常好。
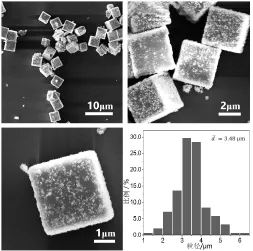
图1 立方Cu2O微粒的SEM图像和粒径统计图
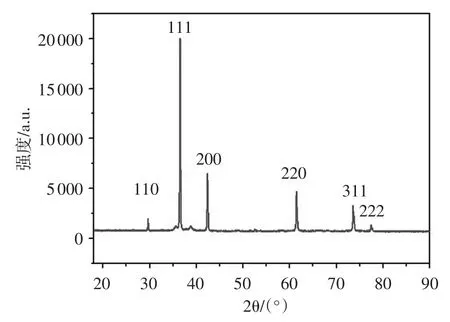
图2 立方Cu2O微粒的XRD图谱
2.2 Cu2O微粒的改性
用强还原剂NaBH4对立方Cu2O微粒进行改性。当Cu2O微粒与NaBH4溶液混合后会发生反应:

实验结果表明NaBH4的用量会影响产物的形貌、尺寸和性能。图3 a为NaBH4与Cu2O的摩尔比为1∶10时所得产物的SEM图像和粒径统计图。产物保留了Cu2O微粒的立方形貌,同时表面略显粗糙,其平均尺寸为3.39μm,比模板略有缩小。当NaBH4与Cu2O的摩尔比为1∶4时,产物表面粗糙度增大,平均尺寸缩小到3.26μm,如图3 b所示。当NaBH4与Cu2O的摩尔比为1∶2时,此时产物的平均尺寸减小到3.10μm,表面粗糙度进一步增大,如图3 c所示。由此可见,随着NaBH4用量的增加,产物的粒径逐渐减小。
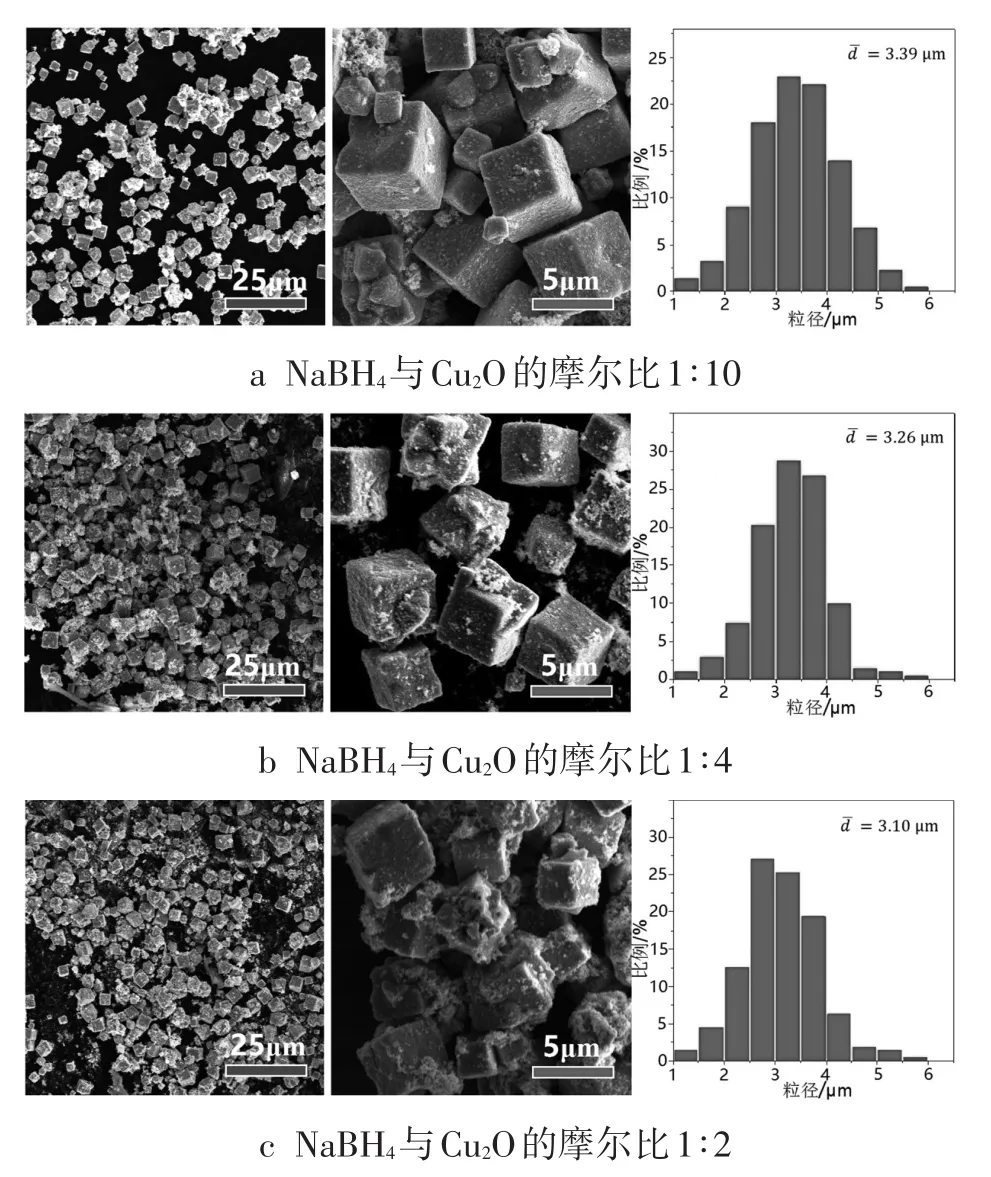
图3 Cu2O改性产物的SEM图像和粒径统计图
2.3 产物光催化性能的测试
作为一种半导体,Cu2O在受到光激发时可以产生电子-空穴对。空穴(h+)具有氧化性,电子(e-)具有还原性。电子和空穴将引起水溶液中发生一系列反应。电子可以与水中溶解的O2反应生成超氧离子O2-和H2O2。O2-和H2O2会进一步反应生成羟基自由基·OH。·OH氧化能力极强,可以与大多数有机污染物发生反应,无选择性地把有害物质氧化成CO2、H2O或矿物盐等降解产物[15]。
为了检测产物的光催化性能,将50mg待测样品加入到50mL浓度为10mg·L-1的MO溶液中,在350W氙灯照射条件下模拟太阳光进行光催化反应。每隔15min取样,离心分离出溶液,用紫外可见分光光度计对溶液中MO浓度进行测试,得到降解曲线,并与纳米二氧化钛P25的光催化性能进行对比。实验结果如图4所示,立方Cu2O微粒的光催化性能优于纳米二氧化钛P25。其原因是TiO2只能利用紫外光进行光催化反应,而Cu2O的禁带宽度较窄,可以充分利用光源中的可见光部分进行光催化反应。故Cu2O微粒对光源的利用效率高于P25,表现出良好的光催化活性。
从改性产物的光催化降解曲线可知,随着NaBH4用量的增加,产物的光催化性能呈现先增强后减弱的趋势。当NaBH4与Cu2O摩尔比为1∶10时,产物的性能最好,可能是由于少量NaBH4可将Cu2O微粒表面部分还原,使金属铜粒子点缀在微粒表面上。而铜具有良好的导电性能,有利于光生电子的传导,促进电子和空穴的分离,降低电子空穴对的复合几率,提高了光催化反应的量子效率。
另外,当加入高剂量的NaBH4时,产物的光催化性能呈现出减弱的趋势。推测,大量NaBH4不仅消耗了Cu2O的量,而且生成的铜会对Cu2O表面进行覆盖,隔绝了Cu2O光催化剂与溶液的接触。故其光催化性能呈现出减弱的趋势。
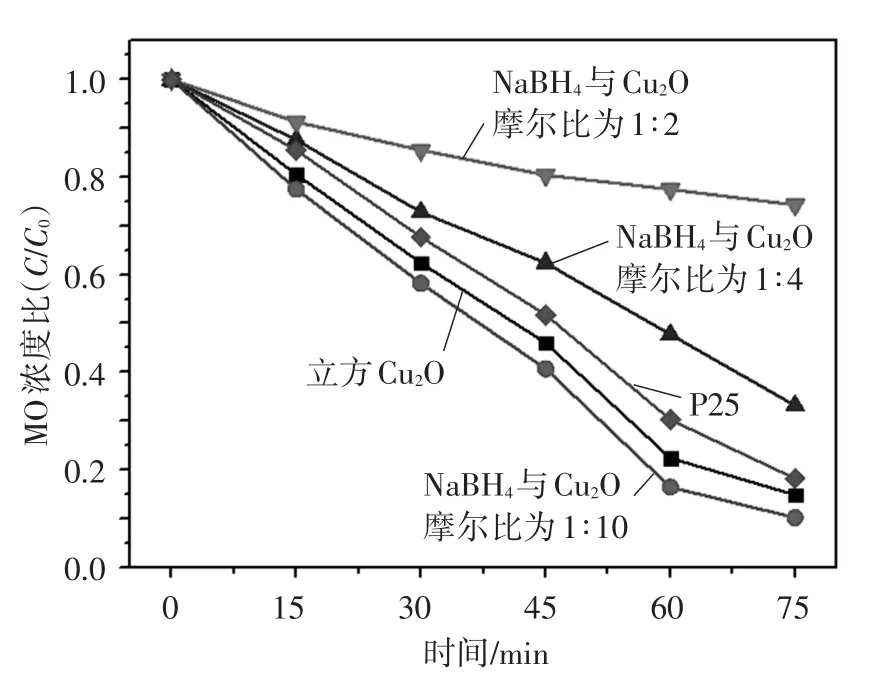
图4 Cu2O及其改性产物、纳米二氧化钛P25的光催化性能
3 结论
1)制备出形貌均匀、分散性良好的立方Cu2O微粒。其可见光催化性能优于纳米二氧化钛P25。
2)利用NaBH4溶液对立方Cu2O微粒进行改性时,随着NaBH4剂量的增大,产物的光催化性能呈现先增强后减弱的趋势。
3)当NaBH4与Cu2O摩尔比为1∶10时,所得产物表现出最优的光催化性能。
[1]Cheng L,Wang C,Feng L,et al.Functional Nanomaterials for Phototherapies of Cancer[J].Chemical Reviews, 2014,114(21):10869-10939.
[2]Sun S,Yang Z.Cu2O-templated Strategy for Synthesis of Definable Hollow Architectures[J].Chemical Communications,2014,50(56):7403-7415.
[3]Yang S,Luo X.Mesoporous Nano/micro Noble Metal Particles:Synthesisand Applications[J].Nanoscale,2014,6(9):4438-4457.
[4]Chong M N,Jin B,Chow CW K,et al.Recent Developments in Photocatalytic Water Treatment Technology:a Review[J].Water Research,2010,44(10):2997-3027.
[5]Tong H,Ouyang S,BiY,etal.Nano-photocatalytic Materials:Possibilities and Challenges[J].Advanced Materials,2012,24(2):229-251.
[6]McCullagh C,Robertson JM C,Bahnemann DW,et al. The Application of TiO2Photocatalysis for Disinfection of Water Contaminated with Pathogenic Micro-organisms:a Review[J].Research on Chemical Intermediates,2007, 33(3-5):359-375.
[7]Yu J,Jimmy CY,Zhao X.The Effectof SiO2Addition on the Grain Size and Photocatalytic Activity of TiO2Thin Films[J].Journal of Sol-Gel Science and Technology, 2002,24(2):95-103.
[8]Musa A O,Akomolafe T,Carter M J.Production of Cuprous Oxide,a Solar Cell Material,by Thermal Oxidation and a Study of its Physical and Electrical Properties[J]. Solar Energy Materials and Solar Cells,1998,51(3): 305-316.
[9]HuangW C,Lyu LM,Yang Y C,etal.Synthesis of Cu2O Nanocrystals from Cubic to Rhombic Dodecahedral Structures and Their Comparative Photocatalytic Activity[J]. Journalof the American Chemical Society,2011,134(2): 1261-1267.
[10]Gao Z,Liu J,Chang J,et al.Mesocrystalline Cu2O Hollow Nanocubes:Synthesisand Application in Non-enzymatic Amperometric Detection of Hydrogen Peroxide and Glucose[J].CrystEngComm,2012,14(20):6639-6646.
[11]Zhang J,Liu J,Peng Q,etal.Nearly Monodisperse Cu2O and CuO Nanospheres:Preparation and Applications for Sensitive Gas Sensors[J].Chemistry ofMaterials,2006, 18(4):867-871.
[12]Park JC,Kim J,Kwon H,et al.Gram-scale Synthesis of Cu2O Nanocubes and Subsequent Oxidation to CuO Hollow Nanostructures for Lithium-ion Battery Anode Materials[J].Advanced Materials,2009,21(7):803-807.
[13]Hong F,Sun S,You H,etal.Cu2OTemplate Strategy forthe Synthesis of Structure-definable Noble Metal Alloy Mesocages[J].Crystal Growth&Design,2011,11(9): 3694-3697.
[14]Zhang L,Jing D,Guo L,etal.In Situ Photochemical Synthesis of Zn-doped Cu2OHollow Microcubes for High Efficient Photocatalytic H2Production[J].ACSSustainable Chemistry&Engineering,2014,2(6):1446-1452.
[15]Tang L,Lv J,Sun S,etal.Facile Hydroxyl-assisted Synthesis of Morphological Cu2O Architectures and Their Shape-dependent Photocatalytic Performances[J].New JournalofChemistry,2014,38(10):4656-4660.
Study on Modification of CuprousOxide Microparticle and Its Photocatalytic Performance
Shao Cheng,Luo Xiao,Ma Yanan,Zhang Chuankun,DaiYinbao,Fan Jiecan,Du Mingzhe,ShiZhaohui
(Schoolof Science,HubeiUniversity ofAutomotive Technology,Shiyan 442002,China)
Cubic Cu2Omicroparticleswere synthesized by the liquid reductionmethod and NaBH4was used for themodification.The phase structure andmorphology of the reaction productwere characterized by X-ray diffraction(XRD)and scanning electronmicroscope(SEM).Studies on photocatalytic propertieswere also performed for the degradation ofmethylorange.The results show themorphology of the reaction product is cubic and its photocatalytic ability is improved firstly and then dropped as the amount of NaBH4increases.The products obtained show the best photocatalytic performancewhen the mole ratioofNaBH4to Cu2O is1:10.
cuprousoxide;modification;photocatalysis
TQ426
:A
:1008-5483(2017)01-0073-04
2016-10-28
湖北汽车工业学院大学生创新训练计划项目(SJ201572);湖北省自然科学基金项目(2014CFB631);
湖北省教育厅科研计划(Q20141802);湖北汽车工业学院博士科研启动基金(BK201301)
邵城(1995-),男,湖北十堰人,从事催化材料的制备和性能研究。E-mail:shaocheng95@yeah.net
罗啸(1986-),男,湖北十堰人,硕士,从事微纳米材料的合成和应用研究。E-mail:luox@huat.edu.cn
10.3969/j.issn.1008-5483.2017.01.017

