甲醛-硫酸亚铁协同还原浸出低品位氧化锰矿
马华菊,卢友志,陈东莲,明宪权,李维健,袁爱群,韦冬萍,周泽广,杜景龙(.桂林理工大学南宁分校, 南宁5000;.广西民族大学化学化工学院,南宁50006;.中信大锰矿业有限责任公司,南宁500)
甲醛-硫酸亚铁协同还原浸出低品位氧化锰矿
马华菊1,卢友志2,陈东莲1,明宪权3,李维健3,袁爱群2,韦冬萍2,周泽广2,杜景龙2
(1.桂林理工大学南宁分校, 南宁530001;2.广西民族大学化学化工学院,南宁530006;3.中信大锰矿业有限责任公司,南宁530022)
在硫酸介质中以甲醛-硫酸亚铁为还原剂协同还原软锰矿,考察了甲醛-硫酸亚铁摩尔比、温度、反应时间、转速、硫酸浓度等因素对锰、铝的浸出率及溶液中铁和有机残留甲酸的影响.采用单因素实验获得较佳的还原工艺条件,采用HPLC测定溶液中的甲酸.结果表明,在固定转速为200 r/min、液固比为 8 ml/g 时,最佳反应条件为:甲醛-硫酸亚铁摩尔比1∶3(甲醛1.5 mol)、浸出时间3 h、硫酸浓度 3 mol/L、温度90 ℃.在该条件下重复实验,锰的平均浸出率为93.51%,铝的平均浸出率为33.08%,铁的浓度为23.07 mol/L,甲酸浓度为0.001 g/L.
甲醛; 硫酸亚铁; 氧化锰矿;协同还原;浸出
我国的软锰矿大多为低品位软锰矿,含锰量低,回收利用的成本高而且容易带来环境污染等问题[1],随着锰资源的日渐贫乏,开发低品位软锰矿还原的新工艺对实现锰资源的合理利用有着重要的意义.目前,火法和湿法是还原软锰矿常用的两种方法,其中湿法工艺使用无机有机、生物质等作为还原剂,避免了火法工艺能耗高等弊病,简化了工艺,越来越受到人们的重视[2].常见的无机还原剂有硫酸亚铁、铁屑、双氧水等[3-5],硫酸亚铁工艺存在浸出过程中其浆料固液分离困难,后续处理工艺复杂的缺点;SO2酸耗大,存在烟气排放的问题,且SO2对人体危害较大;而双氧水价格昂贵,工艺热耗大.使用有机还原剂[6-10]则反应条件温和、锰的浸出率高且无机杂质少,常用的有机还原剂有葡萄糖、甲酸、草酸、苯胺、醇类等物质,但这些物质大多价格昂贵,而且由于产生大量的有机物残留造成极板腐蚀从而影响电流效率[11-12],难以实现产业化.
为了降低溶液中的有机物含量,采用最简单的有机物甲酸、甲醛[13-14]作为还原剂还原软锰矿,发现两者无法完全反应,溶液中仍然残留有机物.而采用甲醛-铁粉[15]作为复合还原剂可以明显降低浸出液中的甲酸残留.本文利用最简单的有机物甲醛作为还原剂,加入无机还原剂硫酸亚铁,利用二者的协同效应,改善反应条件,既能够避免因硫酸亚铁导致浆料分离困难的问题,又能够充分利用有机还原剂的高效还原效果,同时更为有效地降低了浸出液中残留的有机物,并通过工艺条件的控制,使甲醛及其氧化产物甲酸充分反应,使有机残留物接近0,避免了原料的浪费及因此带来的设备腐蚀和环境污染问题.
1 实验部分
1.1 原料
实验所用软锰矿来自广西大新某锰矿,其化学成分如表1所示,其中二氧化锰仅为25.25%,属于低品位氧化锰矿.矿石磨细后过筛(孔径0.16 mm)以备用.甲醛、硫酸亚铁、浓硫酸等均为分析纯试剂,水为去离子水.

表1 软锰矿的主要化学成分(质量分数)
1.2 实验方法
取20 g矿石粉和硫酸加入到250 mL的三口烧瓶内,将烧瓶置于恒温水浴中,三口烧瓶一侧的开口用于取样和安装温度计,中间的开口安装可用于变频无极调速的机械搅拌器,另一侧的开口安装冷凝器避免水分蒸发.当溶液达到所需温度后,再加入甲醛、硫酸亚铁溶液.
反应停止后,反应混合溶液过滤,滤液定容至250 ml,取样分析.Al, Fe浓度用电感耦合等离子体发射光谱分析(ICP, Optima 5300DV, Perkin Elmer, USA),浸出液中锰的含量按照硫酸亚铁铵滴定法分析.甲酸含量采用Agilent1260型高效液相色谱法测定,测试条件:0.03 mol/L NaH2PO4和0.02 mol/L H3PO4流动相,流速1 ml/min,波长210 nm,色谱柱为C18(5 μm,4.6 mm×250 mm),柱温30 ℃,G1314B可变波长紫外检测器定量检测.
浸出过程中甲醛和硫酸亚铁可能发生的化学反应有:
HCHO+2MnO2+2H2SO4=2MnSO4+3H2O+CO2↑
(1)
HCHO+MnO2+H2SO4=HCOOH+MnSO4+H2O
(2)
2FeSO4+MnO2+2H2SO4=Fe2(SO4)3+MnSO4+2H2O
(3)
HCOOH+MnO2+H2SO4=MnSO4+2H2O+CO2↑
(4)
2Fe3++2HCOOH=3Fe2++CO2+2H2O
(5)
3Fe2++MnO2+2H2SO4=2Fe3++MnSO4+FeSO4+ 2H2O
(6)
从中可以看出,浸出液中可能存在铁的二价和三价离子,有机物除还原剂甲醛外,只有甲酸.
2 结果与讨论
2.1 甲醛-硫酸亚铁摩尔比对浸出率的影响
当反应条件为:液固比8 ml/g,硫酸浓度为 3 mol/L,浸出温度90 ℃,总反应时间3 h,搅拌速率200 r/min时,甲醛1.95 mL为理论用量的90%(理论用量指甲醛与二氧化锰分别按方程(1)恰好完全反应时所需质量),甲醛用量及甲醛-硫酸亚铁摩尔比对浸出过程锰和铝的浸出率(ηMn和ηAl)的影响及溶液中甲酸的质量浓度(ρ(HCOOH))和铁的质量浓度(ρ(Fe))如表2所示.
从表2看到,如只添加硫酸亚铁一种还原剂时,锰的浸出率ηMn只有31.8%,浸出液中无有机物.如只添加甲醛,锰的浸出率ηMn为81.35%,浸出液中有机物残留为甲酸,说明体系中不仅发生如式(1)的反应,同时还发生如式(2)的反应.如果同时添加两种还原剂,随着甲醛-硫酸亚铁摩尔比的增加,锰的浸出率逐渐增加,当这一比值增加到1∶3.5时,锰的浸出率可到97.3%,而铝的浸出率变化不大,溶液中甲酸的质量浓度ρ(HCOOH) 先增加后降低,说明甲醛的还原效果优于硫酸亚铁.可见,增加甲醛的加入量,锰的浸出率提高,但有机物残留增加;而增加硫酸亚铁加入量,会使溶液中铁的含量逐渐增加,影响后序过滤.综合考虑,选择摩尔比为1∶3作为还原剂比例.
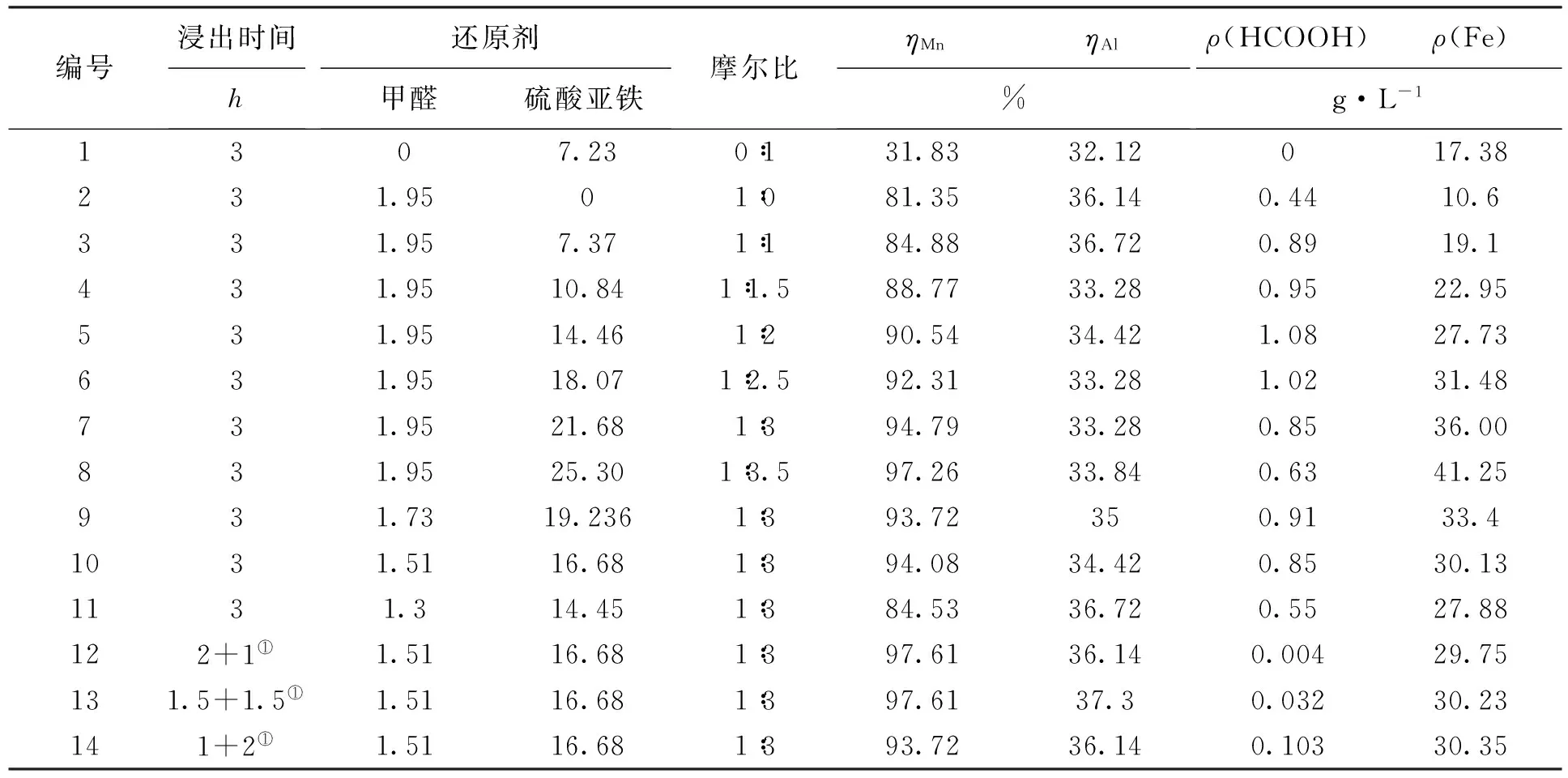
表2 还原剂摩尔比对浸出效果的影响
注:①表示“先加入甲醛反应时间+再加入硫酸亚铁反应时间”;. 浸出时间中不特别注明的,表示甲醛先反应一段时间再加入铁粉继续反应.
在改变两种还原剂的加入顺序时,发现先加入甲醛及延长甲醛反应时间有利于降低浸出液中甲酸和铁的含量,锰浸出率较高而铝的含量变化不大,说明两者的加入顺序对浸出过程有影响.当加入甲醛反应2 h后,再加入硫酸亚铁反应1 h,锰浸出率达到97.61%,而溶液中甲酸的含量达到最低值,这可能是甲醛氧化产物甲酸是一种弱还原剂,还原体系除了发生式(1)至(3)反应外,还可能发生式(4)至(5)的反应,促进了锰浸出率的提高和降低甲酸的含量.
2.2 总浸出时间对浸出率的影响
当硫酸浓度为3 mol/L,浸出温度为90 ℃,液固比为8 ml/g,搅拌速率为200 r/min,摩尔比为 1∶3 时,总浸出时间对浸出效果的影响见图1.由图1可知,随着浸出时间的增加,锰浸出率先增加后略降低,在反应3 h时达到最大,为97.6%,甲酸的浓度逐渐降低,反应进行到3.5 h时,甲酸的浓度接近0.铁的质量浓度在28.15~29.98 g·L-1之间变化, 铝的浸出率ηAl在33.84%~37.86%之间,甲酸的质量浓度0.004 g/L,因此选择总浸出反应时间为3 h.
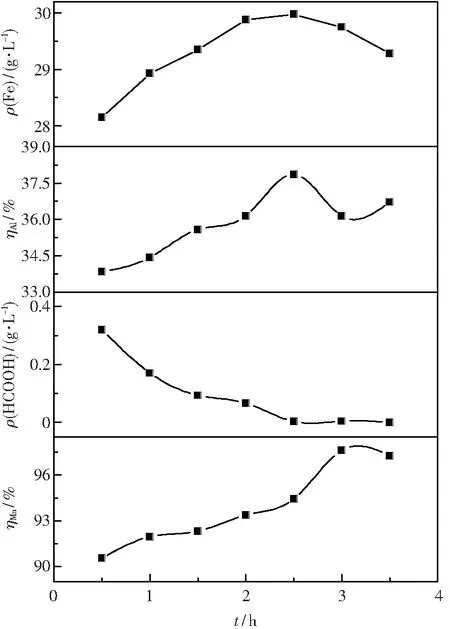
图1 总浸出时间对浸出效果的影响Fig.1 Effect of the total reaction time on the leaching result
2.3 反应温度对浸出率的影响
当硫酸浓度为3 mol/L,总浸出时间为3 h, 液固比为8 ml/g,搅拌速率为200 r/min时,浸出温度对浸出效果的影响见图2.由图2可知,随着反应温度的增高,锰的浸出率先增加后降低,当温度为90 ℃时达到最大,为97.6%,甲酸浓度先降低后不变,当温度从90 ℃增加到95 ℃时,甲酸的质量浓度为0.004 g/L不变,而铁的浓度逐渐增加但变化范围不大,铝的浸出率略有提高.为减少能量的消耗,减少铝的浸出,选择最适宜温度为90 ℃.
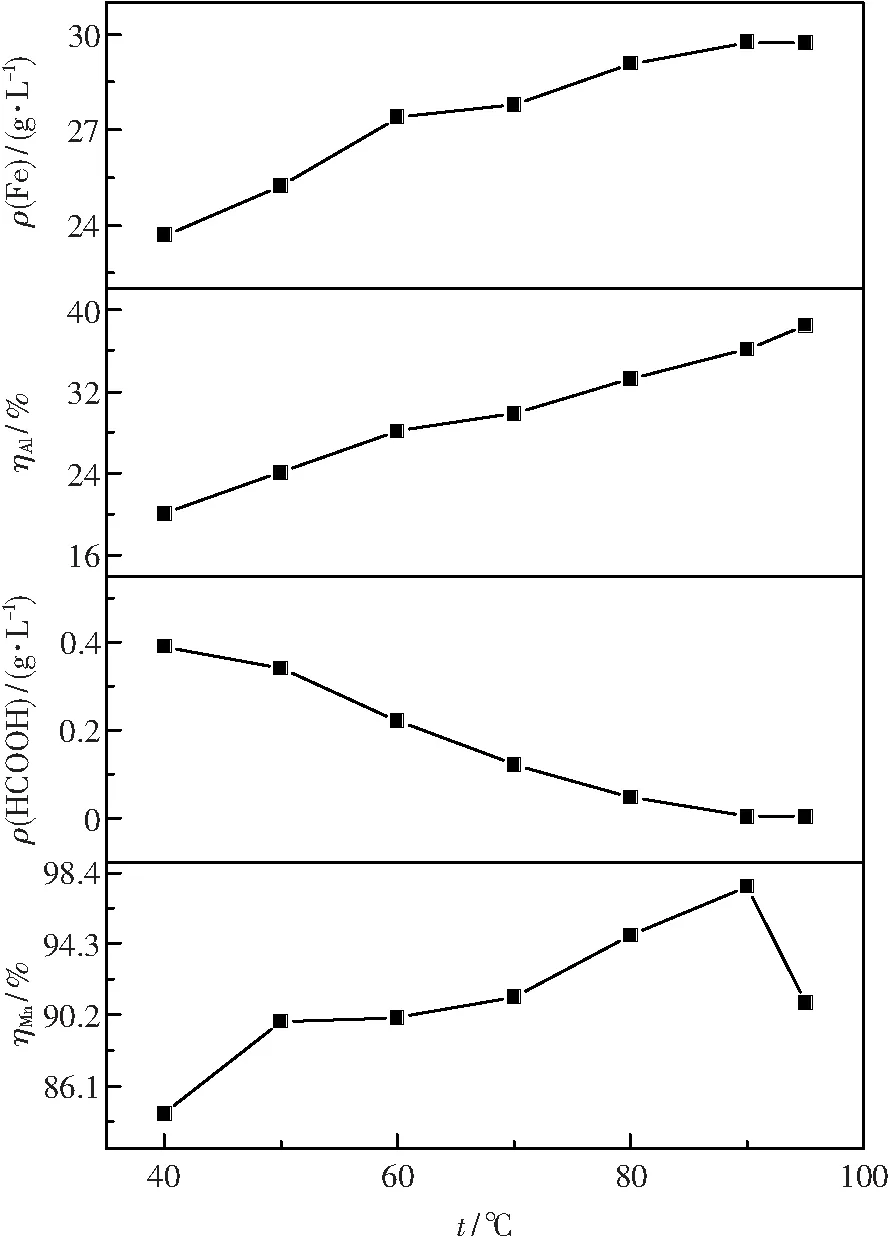
图2 浸出温度对浸出效果的影响Fig.2 Effect of reaction temperature on the leaching result
2.4 硫酸浓度对浸出效果的影响
当浸出温度为90 ℃,总浸出时间3 h,液固比为8 ml/g,搅拌速率为200 r/min时,硫酸浓度对浸出效果的影响见图3.由图3可知,随着硫酸浓度的增加,锰的浸出率逐渐增加,当硫酸浓度增加到3 mol/L时,锰的浸出率为97.6%,铝的浸出率不再提高,甲酸的含量逐渐降低,铁的浓度变化不大.
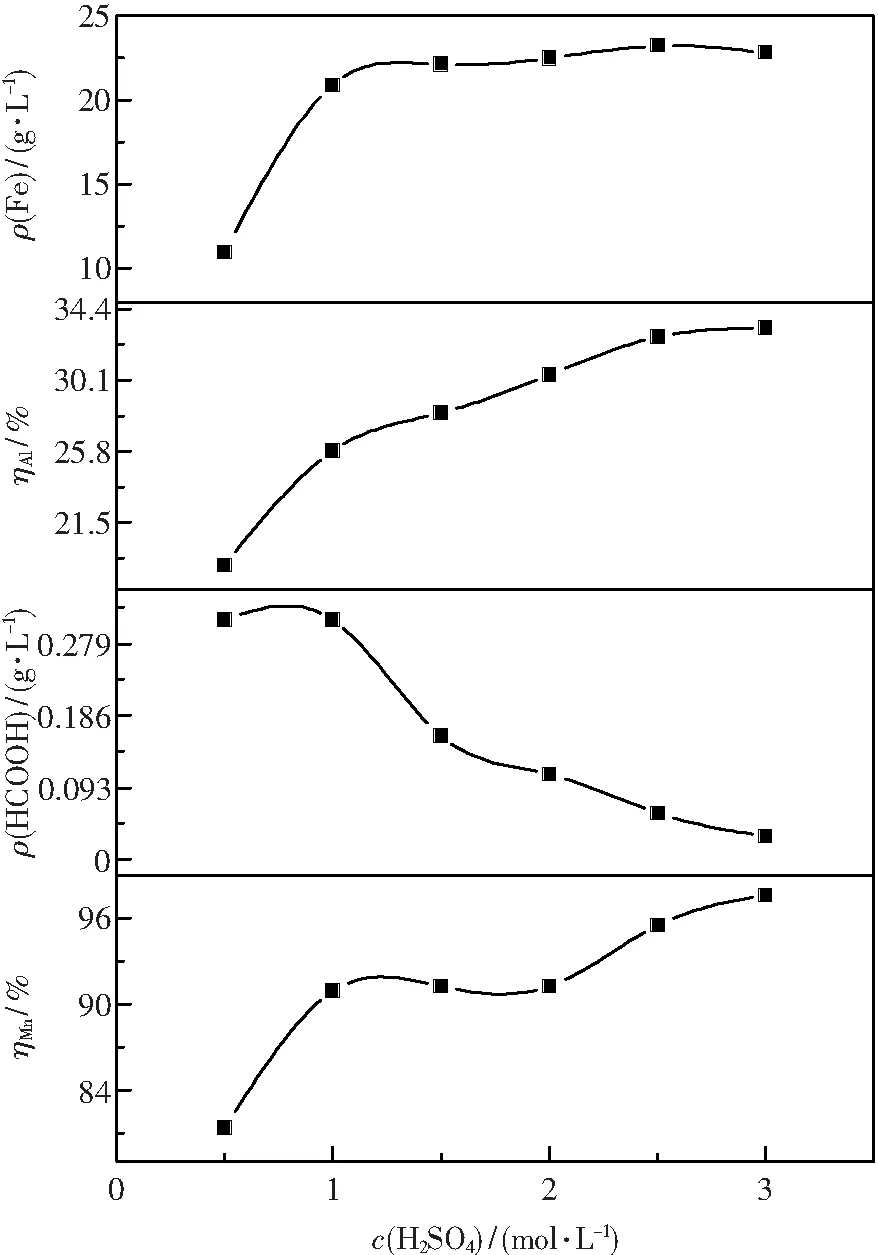
图3 硫酸浓度对浸出效果的影响Fig.3 Effect of concentration of sulfuric acid on the leaching result
2.5 转速的影响
当硫酸浓度为3 mol/L,总浸出时间为3 h, 液固比为8 ml/g,浸出温度为90 ℃时,搅拌速率对浸出效果的影响见图4.从图4可以看出,转速为200 r/min后时锰的浸出率增加不明显,甲酸的质量浓度明显降低,铁的质量浓度不再大幅增加.转速为200 r/min较为合适.
2.6 液固比对浸出率的影响
当浸出温度为90 ℃,总浸出时间为3 h,硫酸浓度为3 mol/L,搅拌速率为200 r/min时,液固比对浸出率的影响见图5.由图5可知,液固比对锰的浸出率、铁的质量浓度影响不大.甲酸的质量浓度在液固比为8 ml/g后增加较快,浸出液中甲酸的质量浓度越大对电解的负面影响越大,因此,综合考虑,液固比取8 ml/g.
由上述条件实验可以得到甲醛-硫酸亚铁浸出锰的最佳实验条件为:甲醛-硫酸亚铁摩尔比1∶3、浸出时间3 h、硫酸浓度3 mol/L、温度90 ℃.
2.7 验证实验
为了进一步验证上述数据的可重复性和稳定性,在上述最佳的浸出条件下进行三组重复实验进行验证,其结果如表3所示.结果表明,数据具有可重复性,锰的浸出率平均值为93.51%,铝的平均浸出率为33.08%,甲酸浓度接近0,铁的浓度为23.07 g·L-1,表明利用硫酸亚铁-甲醛作为还原剂,取得了较高的锰的浸出率,且甲酸的残留少.
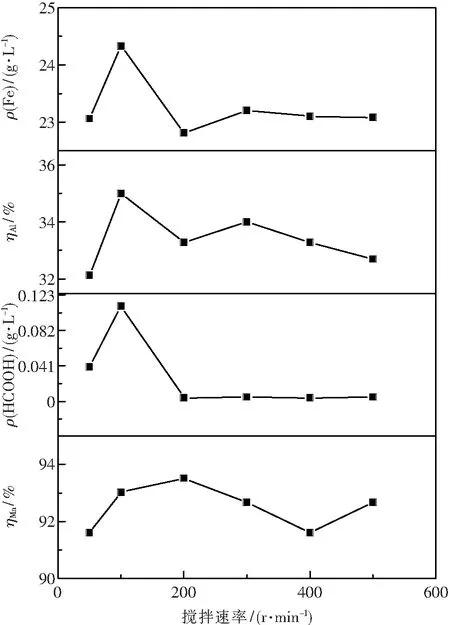
图4 搅拌速率对浸出效果的影响Fig.4 Effect of stirring rate on the leaching result
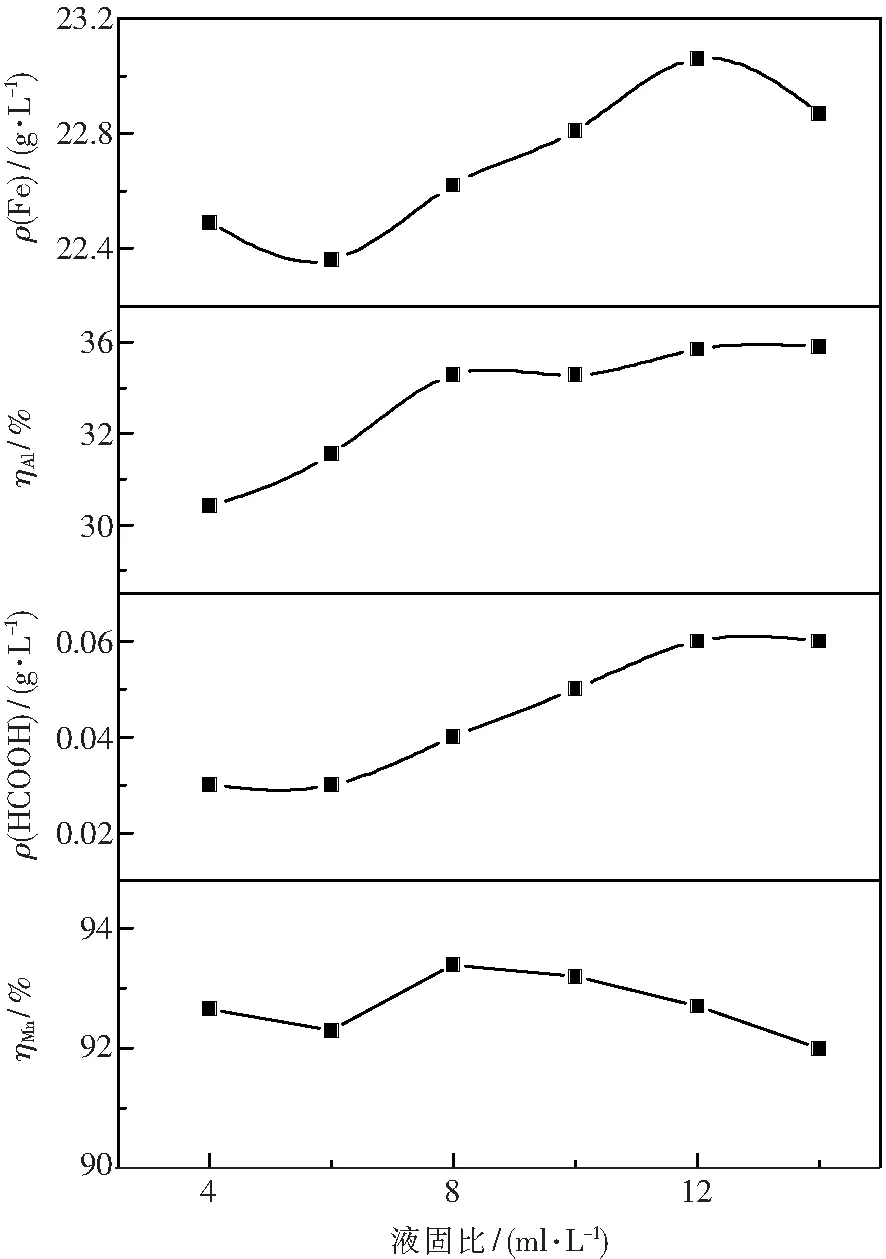
图5 液固比对浸出效果的影响Fig.5 Effect of liquid-solid ratio on the leaching result

表3 验证实验结果
3 结 论
采用甲醛和硫酸亚铁协同还原浸出低品位氧化锰矿,当液固比取8 ml/g、搅拌转速为200 r/min时,各因素对锰的浸出率影响的大小依次为:甲醛-硫酸亚铁摩尔比>反应时间>硫酸浓度>温度.该工艺最佳反应条件为:甲醛-硫酸亚铁摩尔比为1∶3、甲醛浓度为1.5 mol.、浸出时间为3 h、硫酸浓度为3 mol/L、温度为90 ℃.在该条件下重复实验,锰的平均浸出率为93.51%,浸出液中铝的质量浓度为1.15 g·L-1,铁的浓度为23.07 g·L-1,甲酸质量浓度为0.001 g·L-1,接近0.由此可见,与其他的有机物还原软锰矿技术相比,使用甲醛和硫酸亚铁协同还原浸出低品位氧化锰矿具有锰浸出率高、有机物残留少的优点,是一种高效、经济的湿法还原软锰矿新技术.
[1]李同庆. 低品位软锰矿还原工艺技术与研究进展[J]. 中国锰业, 2008, 26(2): 4-14. (LI Tongqing. Technology of low grade pyrolusite ore reduction process and recent advances [J]. China’s Manganese Industry, 2008, 26(2): 4-14.)
[2]卢友志, 卢国贤, 明宪权, 等. 有机物还原氧化锰工艺研究进展[J]. 湿法冶金, 2015, 34(1) : 1-5. (Lu Youzhil, Lu Guoxian, Ming Xianquan,etal. Research advances of reduction of manganese oxide ore by organic matter [J]. Hydrometallurgy of China, 2015, 34(1) : 1-5.)
[3]粟海锋, 冯国忠.两矿干法制取工业硫酸锰的实验研究[J].广西大学学报(自然科学版), 1995 (1): 37-40. (Su Haifeng, Feng Guozhong. Study on production of manganese sulfate by dry processes method with pyrolusite and iron pyrites [J].Journal of Guangxi University(Natural Science Edition), 1995 (1): 37-40.)
[4]Mohammad Sh B, Alireza Z , Zahra G,etal. Reductive dissolution of manganese ore in sulfuric acid in the presence of iron metal[J]. Hydrometallurgy, 2008, 90(2-4): 207-212.
[5]El-Hazek M N, Lasheen T A, Helal A S. Reductive leaching of manganese from low grade Sinai ore in HC1 using H2O2as reductant[J]. Hydrometallurgy, 2006, 84(12): 187-191.
[6]Tang Q, Zhong H, Wang S,etal. Reductive leaching of manganese oxide ores using waste tea as reductant in sulfuric acid solution[J]. Transactions of Nonferrous Metals Society of China, 2014, 24(3): 861-867.
[7]金生龙, 王雨红, 粟海锋, 等. 响应面法优化葡萄糖还原浸出半氧化锰矿的研究 [J]. 广西大学学报(自然科学版), 2014, 39(6): 1403-1408. (Jin Shenglong, Wang Yuhong, Su Haifeng. Response surface optimization of process parameters for reduction leaching of semi-oxidized manganese ore by glucose [J]. Journal of Guangxi University (Natural Science Edition), 2014, 39(6): 1403-1408.)
[8]粟海锋, 崔嵬, 文衍宣, 等.还原浸出低品位软锰矿的研究[J].广西大学学报(自然科学版), 2010, 35(3): 373-377. (Su Haifeng, Cui Wei, Wen Yanxuan,etal. Leaching of low-grade pyrolusite using rutin as reductant [J]. Journal of Guangxi University (Natural Science Edition), 2010, 35(3): 373-377.)
[9]Lasheen T A, El-Hazek M N, Helal A S,etal. Recovery of manganese using molasses as reductant in nitric acid solution[J]. International Journal of Mineral Processing, 2009, 92(3): 109-114.
[10]高玉洋,粟海锋,文衍宣. 半氧化锰矿的直接还原浸出工艺研究[J]. 广西大学学报(自然科学版), 2013, 38(3): 632-637. (Gao Yuyang, Su Haifeng, Wen Yanxuan. Direct reductive leaching of manganese from semi-oxidized manganese ore [J]. Journal of Guangxi University (Natural Science Edition), 2013, 38(3): 632-637.)
[11]卢国贤, 明宪权, 陈南雄, 等. 电解锰阴极板材料在不同溶液介质中的腐蚀研究[J].广东化工, 2014, 41(20): 42-43. (Lu Guoxian, Ming Xianquan, Chen Nanxiong,etal. Corrosion research of electrolytic manganese stainless steel plate for cathode in the different solution medium[J]. Guangdong Chemical Industry, 2014, 41(20): 42-43.)
[12]明宪权, 卢国贤, 陈南雄, 等. 电解金属锰铅阳极板在小分子有机酸中的腐蚀性研究[J]. 中国锰业, 2014, 32(4): 37-40. (Ming Xianquan, Lu Guoxian, Chen Nanxiong,etal. Corrosion research of electrolytic manganese lead plate for anode in small molecular organic acid[J]. China’s Manganese Industry, 2014, 32(4): 37-40.)
[13]Lu Y Z, Ma H J, Huang R J,etal. Reductive leaching of low-grade pyrolusite with formic acid[J]. Metallurgical and Materials Transactions B, 2015, 26(4): 1709-1715.
[14]卢友志, 韦冬萍, 马华菊, 等. 甲醛还原浸出低品位软锰矿[J]. 现代化工, 2015, 35(7): 62-65. (Lu Youzhi, Wei Dongping, Ma Huaju,etal. Reductive leaching of manganese from low-grade pyrolusite ore using methyl aldehyde as reductant[J]. Modern Chemical Industry, 2015, 35(7): 62-65.)
[15]卢友志, 马华菊, 陈东莲, 等. 甲醛和铁粉协同还原浸出低品位氧化锰矿[J]. 有色金属-冶炼部分, 2015(10): 26-30. (Lu Youzhi, Ma Huaju, Chen Donglian,etal. Synergic reductive leaching of manganese from low-grade oxide manganese ore with formaldehyde and iron powder[J]. Nonferrous Metals (Extractive Metallurgy ), 2015(10): 26-30.)
[16]Tian X, Wen X X, Yang C,etal. Reductive leaching of manganese from low-grade manganese dioxide ores using corncob as reductant in sulfuric acid solution[J]. Hydrometallurgy, 2010, 100( 3 /4) : 157-160.
Synergistic reductive leaching of manganese from low-grade oxide manganese ore with formaldehyde and ferrous sulfate
Ma Huaju1, Lu Youzhi2, Chen donglian1, Ming Xianquan3, Li Weijian3, Yuan Aiqun2,Wei Dongping2, Zhou Zeguang2,Du Jinglong2
(1.Guilin University of Technology at Nanning, Nanning 530001, China;2.School of Chemistry and Chemical Engineering, Guangxi University for Nationalities, Nanning 530006, China;3.CITIC Dameng Mining Industries Limited, Nanning 530022, China)
Effects of concentration of sulfuric acid, mole ratio of reducing agent, reaction time, leaching temperature and liquid-solid ratio as well as stirring rate on the extraction ratio of manganese and aluminum, concentrations of iron and organic residue in the leaching solution were studied by using formaldehyde and ferrous sulfate as reductants in sulfuric acid medium. Technological parameters were obtained from a single factor experiment. Organic residue of leaching solution was analyzed by HPLC. The results showed that the optimum conditions are as follows: H2SO4is 3mol/L, CH2O / FeSO4mole ratio is 3 (formaldehyde1 is 5mol), reaction time is 3 h, temperature is 90 ℃ fixed liquid-solid ratio is 8 ml/g and stirring rate is 200 r/min. The average leaching ratio is 93.51% for Mn, 33.08% for aluminum, concentration of iron is 23.07 mg/mL, concentration of formic acid is 0.001 g/L from the repeated experiments under the optimum conditions.
formaldehyde; ferrous sulfate; oxide manganese ore; synergistic reductive leaching; leach
10.14186/j.cnki.1671-6620.2017.01.009
TF 803.2
A
1671-6620(2017)01-0047-06

