微创经皮神经电刺激治疗神经痛的临床研究
李峰,千超,肖学谦
微创经皮神经电刺激治疗神经痛的临床研究
李峰,千超,肖学谦
目的:探讨微创经皮神经电刺激治疗神经痛的短期和长期临床疗效。方法:选取药物难治性严重周围神经性疼痛持续超过3月的患者87例,对疼痛触发点或痛觉过敏区定位后,采用英国Algotec Research and Development微创神经电刺激系统对定位区域行经皮电刺激治疗,以数字评价量表(NRS)法和神经病理性疼痛量表(NPS)对患者治疗前及治疗后1 h、1周、1月、3月、6月进行评估,同时采用欧洲五维度健康量表(EQ-5D)对患者治疗前和治疗后6月的健康指数进行评估。记录不良事件和满意度。结果:治疗后患者NRS和NPS在1 h时显著低于治疗前,在结束治疗周期后,患者1、3、6月NRS和NPS评分均显著低于治疗前(P<0.001),EQ-5D评分则显著高于治疗前(P<0.001)。除2例患者出现严重对侧感觉迟钝和治疗部位血肿外,其余患者均未出现不良反应,患者满意度为97.7%。结论:微创经皮电刺激治疗神经痛能显著改善难治性严重周围神经性疼痛患者的临床症状,提高患者的生活质量。
微创;经皮神经电刺激;神经痛
慢性神经病理性疼痛是一种独立性疼痛或与躯体伤害相关联的疼痛[1]。单纯的经常性药物治疗对于长期缓解症状不够,需寻找药物以外更好的治疗方法。微创侵入治疗使用电刺激使脊髓神经出现反应,进而对神经进行调节,缓解疼痛[2]。电刺激止痛的机理是通过抑制脊髓背角的疼痛信号传递,同时激活下行的抑制信号通路[3]。然而对中枢神经系统进行调节需要侵入性操作,因此越来越多的治疗选择对外周神经进行调节,其中包括微创经皮神经电刺激(percutaneous electrical nerve stimulation,PENS)[4-6]。本课题即对此进行研究。
1 资料与方法
1.1 一般资料
选取2014年5月至2015年12月我院收治的药物难治性严重周围神经性疼痛持续超过3月的患者87例,男48例,女39例;平均年龄(37±8.2)岁;带状疱疹感染治疗后33例,灼痛26例(糖尿病6例),术后疼痛28例(腹股沟疝修补术9例,腰椎手术7例,乳房切除3例,上肢手术4例,髋关节手术3例,开胸手术2例。78例(89.65%)表现出疼痛触发点和明确的神经通路,其中枕神经痛30例,三叉神经带状疱疹15例,下肢神经痛17例,肋间神经痛7例,上肢神经痛4例,胸神经痛5例;剩下的9例患者中均未发现特定的疼痛触发点,但疼痛敏感区域能明确感知。纳入标准:年龄18~80岁;周围神经疼痛的诊断符合2008年国际疼痛学会(International Association for the Study of Pain)制定的相关疼痛术语[7];疼痛持续时间超过3月;疼痛程度的数字评分法(numerical rating scale,NRS)≥7级;疼痛能定位,且适合单探头治疗;药物治疗难以缓解疼痛;能随访26周。排除标准:全身严重感染;有凝血障碍或口服抗凝药物治疗;有精神疾病或服用作用于中枢神经系统药物;心脏安装起搏装置的患者。所有纳入研究的患者均在治疗前告知本研究的目的和方法,并签署知情同意书。本研究获得医院伦理委员会批准。
1.2 方法
1.2.1 治疗方法所有受试者在治疗前1 d均在门诊行常规检查,包括血压、血氧饱和度、心电图。治疗时,首先对患者的外周神经疼痛区进行定位,确定疼痛触发点。然后将21Gauge的神经刺激器沿外周神经疼痛区域的长轴或相应的神经通路引入相应的皮下隧道,深度在皮下组织0.5~3 cm,然后将探头与神经电刺激装置相连。程序设定:程序A:刺激频率为100 Hz,强度为0.2 V,开始刺激;当刺激后患者疼痛神经通路出现感觉异常或疼痛区域出现感觉异常,随即将程序调整为主治疗程序C:刺激脉冲频率为2~100 Hz,每间隔3 s切换一次,刺激强度为0.5 V,治疗时间设定为25 min。治疗过程中,根据不同患者对刺激强度的感知,对刺激强度做出一定的调整。在电刺激结束后,轻轻拔掉探针,患者观察2 h后即可出院,3 d后进行下一次治疗。治疗频率为2次/周,所有患者治疗持续2周。
1.2.2 评价指标所有患者在治疗期间均记录其与电刺激治疗相关的不良反应事件。在治疗前(T0)、治疗后60 min(T1)、治疗后1周(T2)、治疗后1月(T3)、3月(T4)、6月(T5)对患者的疼痛采用NRS行评估,在T0-T2-T3-T4-T5时间点对病理性神经疼痛强度进行神经病理性疼痛量表(neuropathic pain scale,NPS)评估。在T0和T5时间点对患者的健康结果采用欧洲五维度健康量表(EuroQol five dimensions questionnaire,EQ-5D)进行评估,评估内容主要包括5个方面:移动性、自理能力、日常活动能力、疼痛或不适,焦虑或抑郁。治疗后满意度评价为:无效,患者诉治疗后1月其疼痛未缓解,NRS评分未见降低,需进一步治疗;有效,患者诉治疗能明显缓解其疼痛,NRS评分在6月内降低≤50%;非常好,患者诉治疗能完全缓解其疼痛,NRS评分在6月内降低>50%。
1.3 统计学处理
所有数据均采用SPSS20.0统计学软件进行分析,计量资料以(均数±标准差)表示,重复测量的方差分析,时间点两两比较采用Bonferroni检验,计数资料采用例或率表示。P<0.05为差异有统计学意义。
2 结果
2.1 患者疼痛强度评估结果
治疗后的每个时间点,患者NRS评分均显著低于治疗前(T0),有显著性差异(P<0.001);在T0时,NRS下降明显,T2时NRS则显著回升,在T3-T4-T5时间点NRS则又显著降低,与T2相比,差异有统计学意义(P<0.05),见图1、表1。
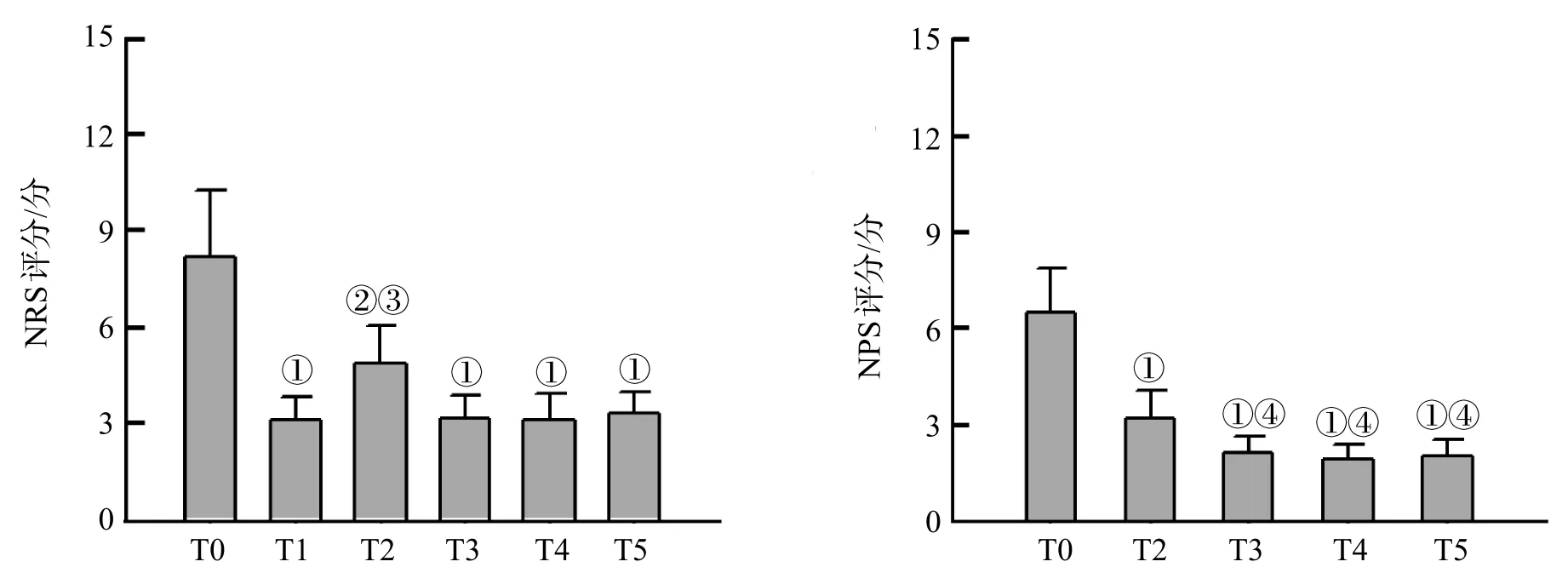
图1 治疗前后患者NRS及NPS比较

表1 治疗前后患者NRS及NPS评分比较(分,x±s)
2.2 患者神经疼痛评估结果
治疗后T2-T3-T4-T5时间点患者的NPS评分较治疗前(T0)降低,差异有统计学意义(P<0.05)。NPS评分在远期(T3-T4-T5)效果上,明显优于短期(T0-T2),差异有统计学意义(P<0.05)。
2.3 患者健康指数结果
治疗前,患者的EQ-5D评分为(0.37±0.09)分;治疗后6月,患者的EQ-5D评分为(0.88±0.21)分,明显较治疗前升高,有显著性差异(P<0.0001)。
2.5 治疗期间不良反应事件及满意度
87例患者在PENS治疗期间,仅2例出现不良反应事件,1例出现严重对侧感觉迟钝,1例出现治疗部位血肿,其余85例均诉治疗有效,患者满意度为97.7%。
3 讨论
研究表明,周围神经痛主要是由于神经周围局部水肿、血液回流受阻、缺氧导致神经营养供给障碍,神经内环境发生紊乱,出现疼痛[8]。周围神经的微循环受神经体液的调控,其主要原理是肾上腺通过α受体参与调控神经周围的血管紧张,使神经肽与各自的特异性受体作用发挥调节微循环的作用[9]。PENS是一种低频脉冲电流刺激,能够激活中枢神经系统内的阿片神经元,使内源性的吗啡样多肽释放,这一调节作用促使肾上腺皮质激素释放和皮质醇的分泌,改善血液循环[10]。此外,有研究表明,电场的刺激能起到局部营养神经的作用,其作用原理主要是局部组织蛋白在电场环境下分解,释放血管活性肽,这些活性肽能增加神经周围毛细血管渗透性,引起局部血管扩张,这一调节作用能显著改善受损神经的血供,促进受损神经的恢复[11]。PENS与外周神经刺激(peripheral nerve stimulation,PNS)和周围神经区域刺激(peripheral nerve field stimulation,PNFS)治疗不一样,它不需要一个可植入的设备,也不需要手术准备[12]。PENS治疗时采用双极针状电极刺入皮下组织,创口微小,患者易接受,治疗后可迅速拔除,且操作简单易行[13]。所有这些因素都使该方法在治疗慢性周围神经性疼痛患者时成为药物治疗方法之外的最佳选择。
本研究纳入的87例患者均为周围神经疼痛具有明确触发点或痛觉敏感区域患者,这使得PENS的使用成为可能,因为PENS的治疗主要是对外周神经进行调节[12]。本研究的结果也证实,微创PENS在短期和长期上都能明显的降低患者的疼痛强度——患者NRS评分显著降低。而神经性疼痛的治疗具有较高的难度和复杂性,为此,本研究在评估患者周围神经性疼痛时,采用NPS对患者进行评估,主要包括以下几个方面:疼痛锐钝程度、冷或热感、神经疼痛强度、整体愉悦程度、疼痛的深浅[15]。结果显示,治疗后患者NPS评分显著降低,在随访的6月中,未出现疼痛缓解后增强现象。6月后的随访显示,患者健康指数EQ-5D评分较治疗前明显升高,说明患者在治疗后因疼痛强度的减轻,焦虑和抑郁情绪明显改善,体力活动明显增多,生活质量明显提高。患者治疗后的满意度达97.7%。同时,安全性评估显示,仅2例患者出现不良反应事件,其余85例患者则均未出现任何不适症状,这表明PENS治疗安全可行。尽管如此,本研究仍然存在一定的局限性,为小样本的随机观察研究,带状疱疹后神经痛患者比率较高,下一步深入研究需扩大样本量的同时,对纳入疾病种类比例进行筛选。
[1]Vranken JH.Elucidation of pathophysiology and treatment of neuropathic pain[J].Cent Nerv Syst Agents Med Chem,2012,12:304-314.
[2]张力.经皮电刺激治疗外伤性外周神经损伤40例的效果分析[J].中国组织化学与细胞化学杂志,2012,21:157-161.
[3]Ossipov MH,Dussor GO,Porreca F.Central modulation of pain[J].J Clin Invest,2010,120:3779-3787.
[4]李小梅.经皮穴位电刺激的临床镇痛进展[J].中国疼痛医学杂志, 2014,20:826-829.
[5]凌至培,崔志强.神经病理性疼痛外科治疗[J].中国现代神经疾病杂志,2013,13:838-814.
[6]Chaudhari M,McKeown A.Implantable technologies for pain management[J].Anaesth Intens Care Med,2010,12:58-62.
[7]Haanpää M,Attal N,Backonja M,et al.NeuPSIG guidelines on neuropathic pain assessment[J].Pain,2011,152:14-27.
[8]van Hecke O,冯刚.一般人群的神经病理性疼痛:流行病学研究系统回顾[J].中国疼痛医学杂志,2015,21:327-328.
[9]涂雪松.神经干细胞移植治疗神经疾病机制的基础研究[J].神经损伤与功能重建,2014,9:507-511.
[10]Bergeron-Vézina K1,Corriveau H,Martel M,et al.High-and low-frequency transcutaneous electrical nerve stimulation does not reduce experimental pain in elderly individuals[J].Pain,2015,156:2093-2099.
[11]Rozand V,Grosprêtre S,Stapley PJ,et al.Assessment of Neuromuscular Function Using Percutaneous Electrical Nerve Stimulation[J].J Vis Exp,2015,13:298-305.
[12]Gavronsky S,Koeniger-Donohue R,Steller J,et al.Postoperative pain:Acupuncture versus percutaneous electrical nerve stimulation[J].Pain Manag Nurs,2012,13:150-156.
[13]Deer TR,Levy RM,Rosenfeld EL.Prospective clinical study of a new implantable peripheral nerve stimulation device to treat chronic pain [J].Clin J Pain,2010,26:359-372.
[14]Shaladi A,Crestani F,Saltari R,et al.Percutaneous electrical nerve stimulation of peripheral nerve for the intractable occipital neuralgia[J].Recenti Prog Med,2008,99:295-301.
[15]宋承伟,陶维元,严明敏.带状疱疹后遗神经痛的临床分析[J].神经损伤与功能重建,2014,9:537-538.
(本文编辑:王晶)
R741;R741.05
ADOI10.16780/j.cnki.sjssgncj.2017.02.029
陕西省核工业二一五医院神经外科陕西咸阳712000
2016-05-03
李峰lifeng197509@126. com

