白术中内酯类成分的TLC鉴别与UPLC含量测定
赵玉娇+徐文慧+沈小丽+田俊生+秦雪梅
[摘要]建立白术的薄层鉴别与其中3种内酯类成分含量同时测定方法。使用硅胶GF254薄层板对白术进行定性鉴别;利用UPLC-PDA梯度洗脱法同时测定白术内酯Ⅰ,Ⅱ,Ⅲ,选用Waters BEH C18色谱柱(2.1 mm×100 mm,1.7 μm),流动相为乙腈-水,检测波长235 nm。薄层鉴别特征明显,专属性强;含量测定的方法学考察结果符合规定,白术内酯Ⅰ, Ⅱ,Ⅲ线性关系良好(r>0.999 9),平均回收率分别为93.48%(RSD 1.4%), 94.97%(RSD 1.6%), 92.71%(RSD 1.2%)。所建立的白术薄层鉴别方法专属性强、重复性好,3种内酯类成分同时测定方法操作简单、灵敏度高,两者结合可以更好的用于白术的质量评价。
[关键词]白术; 白术内酯; 薄层鉴别; 超高效液相色谱; 质量评价
[Abstract]This research is to establish TLC and UPLC methods for simultaneous determination of 3 atractylenolides in Atractylodes macrocephala. Silica gel GF254 plate was used for identification of A. macrocephala, and UPLC-PDA gradient elution method was used to simultaneously determine atractylenolide Ⅰ, Ⅱ and Ⅲ. The Waters BEH C18 column(2.1 mm×100 mm,1.7 μm)with acetonitrile-water as mobile phase and the wavelength of UV detector of 235 nm were performed. The quality control study showed that the characteristic for identification by TLC was distinct and highly specific. The method of content determination was in accordance with the regulations. The quantitative evaluation of atractylenolide Ⅰ,Ⅱ and Ⅲ was in good linear range(r>0.999 9), and the average recovery was 93.48%(RSD 1.4%),94.97%(RSD 1.6%),92.71%(RSD 1.2%),respectively. TLC identification was in good specificity and repeatability, and the UPLC-PDA method for the simultaneous determination of 3 atractylenolides was simple and reliable for the quality control of A.macrocephala.
[Key words]Atractylodes macrocephala; atractylenolide; TLC; UPLC; quality control
白術为菊科植物白术Atractylodes macrocephala Koidz.的根茎,具健脾益气、燥湿利水、止汗安胎之功,用于脾虚食少、腹胀泄泻、痰饮、眩悸、水肿、自汗、胎动不安等症[1]。主要化学成分为挥发油,如
苍术酮、苍术醇等;内酯类成分,如白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ、双白术内酯等[2-4]。2015年版《中国药典》(一部)白术的质量标准[5]中,TLC鉴别仅以苍术酮为指标成分,尚无含量测定项。而苍术酮是我国传统中药白术及苍术(Rhizoma Atractylodis)等苍术属药用植物挥发油的主要活性成分[6],仅用苍术酮作为白术的鉴别指标不具有专属性。此外,白术中白术内酯Ⅰ,Ⅱ,Ⅲ也为白术的主要活性成分[7],但相对苍术酮来说含量较低,药典中只用含量较高的苍术酮作为质量控制指标,不能全面反映白术的质量,因此增加除苍术酮以外的白术内酯类成分的TLC鉴别及建立相应的含量测定方法,对于提升白术及含白术的成方制剂的质量控制具有重要意义和价值。
关于白术的薄层鉴别,除苍术酮之外未见有其他成分的研究,本实验参考其他有关内酯类成分的鉴别研究[8-9],根据该类成分的理化性质,增加了以白术内酯Ⅰ,Ⅱ,Ⅲ为指标成分并结合苍术酮的薄层鉴别方法,该方法专属性强,效果较好。关于白术的含量测定方面,以白术内酯Ⅰ,Ⅱ,Ⅲ以及苍术酮多见,研究多采用GC测定苍术酮、苍术醇等挥发性成分的含量[10-11],以HPLC测定白术中内酯类成分[12],未见有用UPLC在同波长下同时测定白术中白术内酯Ⅰ、白术内酯Ⅱ和白术内酯Ⅲ含量的分析方法[13-14]。本文基于UPLC-PDA建立了同时测定白术中白术内酯Ⅰ,Ⅱ,Ⅲ含量的分析方法,相对于HPLC具有检测灵敏度较好,分析周期短、进样量少和成本节约等特点,为建立全面可控的白术质量评价方法奠定基础。
1 材料
1.1 仪器
Waters Acquity UPLC超高效液相色谱仪(美国Waters公司,配备Acquity UPLC QSM、Acquity UPLC Sample Manager FTN、Acquity UPLC PDA Detector以及Empower工作站);CPA 225D型1/10万电子天平(德国Sartorius公司);BSA 124S型1/1万电子天平(德国Sartorius公司);Milli-Q纯水机(Direct 8/16 系统,美国Millipore公司);KQ5200E型超声波清洗器(昆山市超声仪器有限公司)。
1.2 材料
白术内酯Ⅰ对照品(纯度98%,批号YJ-A3-1160519 ),白术内酯Ⅱ对照品(纯度98%,批号YJ-A3-1160519 ),白术内酯Ⅲ对照品(纯度98.5%,批号YJ-C1-WG1160520 ),苍术酮对照品(纯度99%,批号YJ-C1-WG1160520),均购自上海永恒生物科技有限公司,硅胶GF254薄层板购自青岛海洋化工厂。甲醇、磷酸、甲酸、环己烷、二氯甲烷、乙酸乙酯均为分析纯,乙腈为色谱纯,水为超纯水。
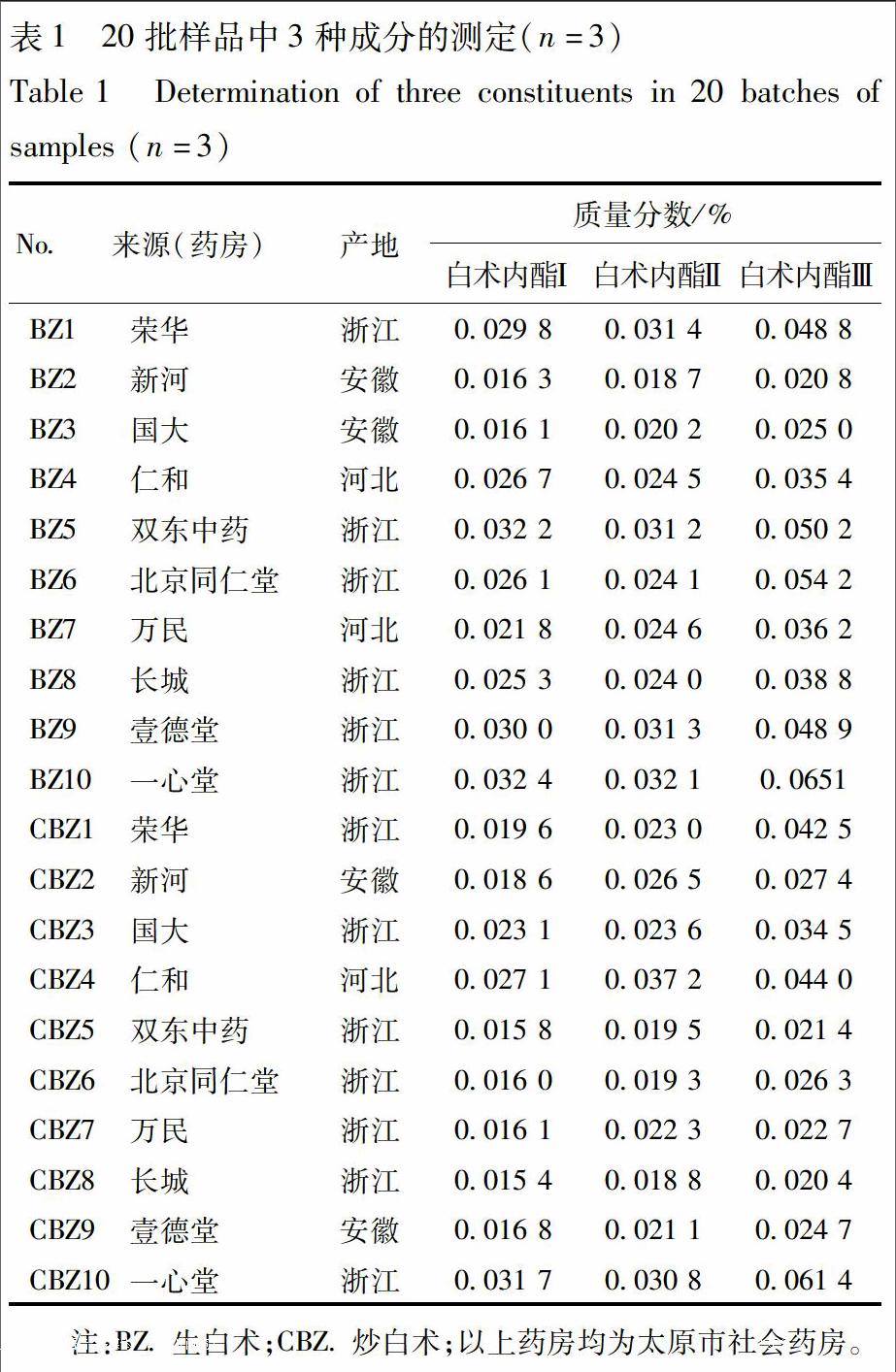
白术样本随机购自10家不同的药房,包括10批生白术和10批炒白术(样本来源见表1),经山西大学中医药现代研究中心秦雪梅教授鉴定为正品,留样于本中心。
2 方法与结果
2.1 薄层鉴别实验方法与结果
2.1.1 对照品溶液的制备
分别取白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ对照品约10 mg,精密称定,加甲醇溶解,制成质量浓度为1.186,1.270,1.161 g·L-1的对照品溶液,作为母液;分别精密吸取各母液0.5,0.5,1 mL各定容至10 mL,得59.3,63.5,116.1 mg·L-1的对照品溶液,备用。取苍术酮对照品约5 mg,精密称定,加甲醇溶解,配制成0.577 g·L-1的对照品溶液,备用。
2.1.2 供试品溶液的制备
取过3号筛(80目)的白术粉末0.5 g,加甲醇定容至5 mL量瓶中,称重,超声提取50 min,冷却至室温,加甲醇补足失重,过滤,取续滤液,作为供试品溶液。
2.1.3 薄层鉴别
照薄层色谱法(2015年版《中国药典》四部,通则0502)试验,分别吸取供试品溶液,白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ、苍术酮对照品溶液各10 μL,分别点于同一硅胶GF254薄层板上,以环己烷-二氯甲烷-乙酸乙酯-甲酸(4∶1∶1∶0.1)为展开剂,展开,取出,晾干,再喷以10%硫酸香草醛硫酸溶液,于100 ℃下加热至斑点清晰,在254 nm紫外灯下检视,供试品色谱中,在与白术内酯Ⅰ、白术内酯Ⅱ和白术内酯Ⅲ对照品色谱相应的位置上显相同颜色荧光斑点,在与苍术酮对照品色谱相应的位置上显相同暗红色斑点。
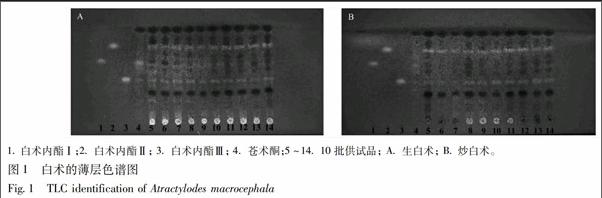
按照以上鉴别方法,对10批生白术和10批炒白术样品进行了薄层鉴别试验,其结果见图1。
2.2 含量测定实验方法与结果
2.2.1 对照品溶液的制备
分别精密吸取2.1.1项下各对照品母液0.5,0.5,1 mL定容至10 mL,得59.3,63.5,116.1 mg·L-1的混合储备液,备用。
2.2.2 供试品溶液的制备
取过3号筛(80目)的白术(BZ6)粉末约0.5 g,置10 mL量瓶中,精密称定,加入甲醇定容,称重,超声50 min,冷却至室温,加甲醇补足失重,过0.22 μm微孔滤膜,取续滤液作为供试品溶液。
2.2.3 色谱条件及系统适应性试验
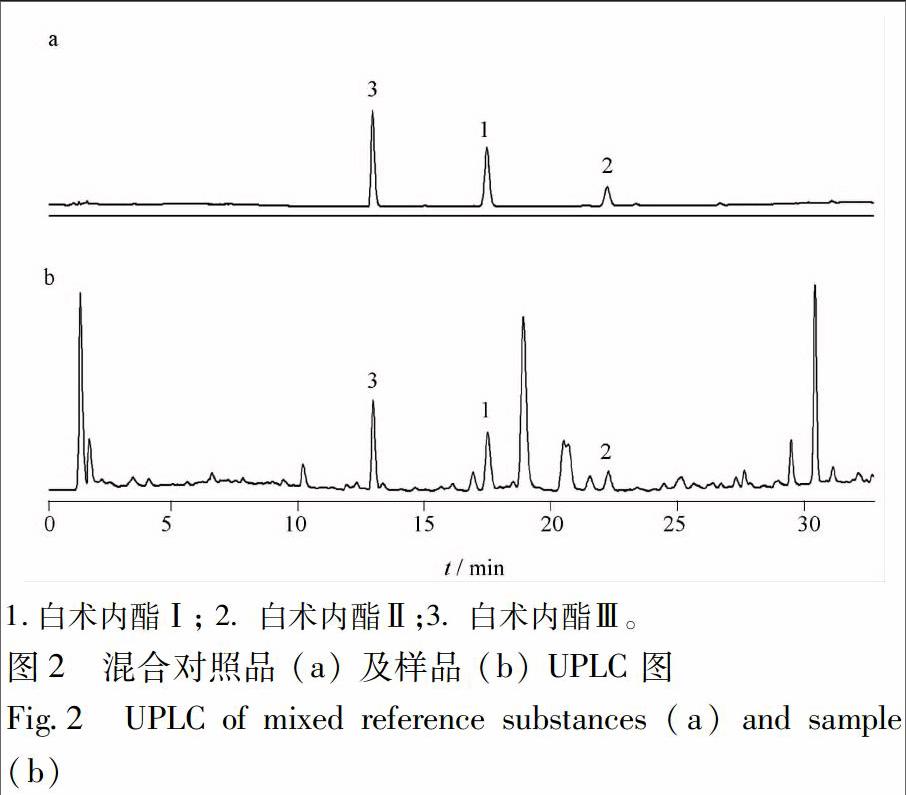
色谱柱:Waters BEH C18柱(2.1 mm×100 mm,1.7 μm);流动相:乙腈(A)-水(B)梯度洗脱,0~3 min,10%~20% A,3~7 min,20%~45% A,7~10 min,45%~46% A,10~14 min,46%~48% A,14~17 min,48%~48% A,17~18 min,48%~50% A,18~20 min,50%~53% A,20~22 min,53%~53% A,22~27 min,53%~80%A,27~30 min,80%~88% A,30~33 min,88%~10% A;检测波长:235 nm;进样量:2 μL;流速:0.2 mL·min-1;柱温:30 ℃。对照品及样品色谱图,见图2,各成分均达到基线分析,白术内酯Ⅰ、白术内酯Ⅱ和白术内酯Ⅲ的理论塔板数均大于1万,分离度均大于1.5。
2.2.4 方法学考察
2.2.4.1 线性关系 将2.2.1项下混合储备液逐级稀释成系列浓度 (分别为原浓度的1,1/2,1/4,1/6,1/8),分别进样。以峰面积为纵坐标(Y),浓度为横坐标(X),进行线性回归,回归方程见表2。
2.2.4.2 精密度试验 精密吸取2.2.2项下白术供试品溶液,连续进样6次,计算得白术内酯Ⅰ,Ⅱ,Ⅲ 峰面积的 RSD 分别为 0.60%, 0.40%, 1.4%,表明仪器的精密度良好。
2.2.4.3 稳定性试验 精密吸取2.2.2项下白术供试品溶液,在 0~24 h内,分别在0, 2, 4, 6, 8, 10, 12, 24 h进样1次,计算得白术内酯Ⅰ, Ⅱ, Ⅲ 峰面积的RSD分别为 1.6%, 1.8%, 1.6%,表明供试品溶液中3种成分在24 h内稳定。
2.2.4.4 重复性试验 取同批白术,按2.2.2项下方法制備供试品溶液,平行6份,进样测定。计算得白术内酯Ⅰ,Ⅱ,Ⅲ 峰面积的RSD分别为0.90%, 1.2%, 1.3%,表明该方法重复性良好。
2.2.4.5 回收率试验 精密称取已知白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ含量的同批白术样品0.5 g,平行9份,各置10 mL量瓶中,平均分为3组,每组分别按白术中白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ含量的50%, 100%, 150% 精密加入质量浓度为1.186, 1.270, 1.161 g·L-1白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ的母液,按2.2.2项下方法制备供试品溶液,进样测定。计算得白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ的加样回收率分别在90.48%~94.88%, 93.18%~96.79%, 90.96%~95.30%,平均回收率分别为 93.48%, 94.97%, 92.71%,RSD 分别为 1.4%, 1.6%, 1.2%,表明该方法准确度良好。
2.2.4.6 含量测定 取购置的10批生白术和10批炒白术,按2.2.2项下方法制备供试品溶液,分别进样测定,结果见表1。
3 讨论
3.1 样品提取方法考察
薄层鉴别实验中考察了不同提取溶剂,包括正己烷和甲醇,发现甲醇提取效果最佳。含量测定考察了甲醇、乙醇2种提取溶剂,结果发现甲醇提取3种白术内酯的含量最高,故选定甲醇为提取溶剂。同时考察了超声提取时间,最终确定提取方法为超声提取50 min效果较好。因此薄层鉴别实验和含量测定采用相同备样方法,即甲醇超声提取50 min。
3.2 薄层鉴别条件优化
本实验对比了石油醚(60~90 ℃)、环己烷、二氯甲烷和乙酸乙酯等多种展开剂,分别考察了二相、三相和四相展开系统以及不同展开比例对白术中指标成分的分离效果,结果以环己烷-二氯甲烷-乙酸乙酯-甲酸(4∶1∶1∶0.1)为展开剂进行薄层鉴别,各指标成分斑点清晰、分离效果最佳。分别考察了薄层板展开过程中温度和相对湿度对结果的影响,结果表明:温度为4,15,25,30 ℃时,各指标成分斑点的Rf在较小范围内波动,但对分离效果几无影响;相对湿度为32%,52%,75%,83%时,各指标成分斑点的Rf变化极小,不影响分离效果。
3.3 色谱条件优化
实验中尝试采用甲醇-水、乙腈-水、乙腈-甲酸-水、乙腈-磷酸-水等流动相系统,结果发现使用酸时白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ对照品均发生分解,而采用乙腈-水系统时无分解现象,且白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ的分离度及对称性均良好,保留时间适中。本实验中检测波长的选择是通过紫外200~400 nm 全扫描,在235 nm 处白术内酯Ⅰ、白术内酯Ⅱ和白术内酯Ⅲ 3种物质吸收较好,峰型适中,基线平稳,故确定检测波长为235 nm。
3.4 小结
文献报道白术挥发油中苍术酮不稳定,影响其不稳定的主要条件为光照和温度[15-16]。苍术酮在空气中会氧化产生白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ、表白术内酯I 和双白术内酯等几种物质[17-18]。本实验过程中也发现了这一现象,苍术酮对照品溶液在放置一段时间后发生分解,在薄层色谱图中可看到苍术酮对照品分解为白术内酯Ⅰ和白术内酯Ⅲ这2种物质见图1,而关于其转化的机制有待进一步深入研究。
本实验在国家药典的基础上增加了白术内酯Ⅰ,Ⅱ,Ⅲ的薄层鉴别方法,使鉴别内容更加全面也更有专属性;所建立的3种内酯类成分同时测定的UPLC-PDA 方法,经方法学验证和20批样品的测定,证明该法操作简便、灵敏准确,更能客观、准确的反映白术的质量,有了较为明显的改进。但本文所用样本量相对较少,且所选2种不同炮制方法的白术不是同一批次,本实验只是说明了所建方法的可行性,如果要对比不同炮制品之间的质量差异,还应增加样本量并使用同批生白术样本,经过炮制后再比较。
[参考文献]
[1]李伟,文红梅,崔小兵,等.白术的化学成分研究[J].中草药,2007,38(10):1460.
[2]陈建明,陈彬,陈建真,等.不同产地白术的化学成分研究进展[J].中医药学报,2010,38(5):144.
[3]梁志远,冉晓燕,周进康.白术内酯Ⅰ、Ⅱ、Ⅲ的化学研究进展[J].贵州师范学院学报,2013,29(9):29.
[4]池玉梅,李伟,文红梅,等.白术多糖的分离纯化和化学结构研究[J].中药材,2001,24(9):647.
[5]中国药典.一部[S].2015:103.
[6]韩邦兴,彭华胜,张玲.苍术属药用植物挥发油成分的组分分析[J].食品与机械,2015,31(4):5.
[7]何结炜,何明珍,胡子帆,等.白术区别苍术的特征性成分的研究[J].江西中医学院学报,2007,19(4):50.
[8]邵艳华,王建刚,赖小平,等.穿心莲二萜内酯类成分的高效薄层色谱指纹图谱研究[J].中药材,2014,37(2):219.
[9]徐韧柳.复方苦木消炎片薄层鉴别与脱水穿心莲内酯含量测定研究[J].中成药,2004,26(12):1003.
[10]李滢,陶海燕,杨秀伟.生白术和炒白术挥发油成分的GC-MS分析[J].药物分析,2013, 33(7):1210.
[11]邱琴,崔兆杰,刘廷礼,等.白术挥发油化学成分GC-MS研究[J].中草药,2002,33(11):980.
[12]段启,许冬谨,谢晨. HPLC法测定白术不同炮制品中白术内酯[J].中草药, 2008, 39(9):1343.
[13]王知青,尹华,王玲,等.白术的质量评价研究[J].中华中医药学刊,2011,29(4):823.
[14]张程荣,曹岗,丛晓东,等.白术化学成分和质量控制研究进展[J].中华中医药杂志,2011,26(10):2328.
[15]郝延军,桑育黎,李宝林,等.苍术酮的常温稳定性研究中成药[J].中成药,2007,29(6):895.
[16]李玲辉,窦德强.白术挥发油中苍术酮的稳定性研究[J].世界科学技术——中医药现代化,2014,16(1):193.
[17]李伟,文红梅,崔小兵,等.白术的炮制机理及其倍半萜成分转化的研究[J].中国中药杂志,2006,31(19):1600.
[18]王小芳,王芳,張亚环,等.白术挥发油中苍术酮氧化反应的动力学[J].应用化学,2007,24(3):301.
[责任编辑 丁广治]

