基于多层氧化层结构的硼颗粒点火模型研究
徐义华, 胡旭, 邹昊, 李雨林, 曾卓雄
(南昌航空大学 飞行器工程学院, 江西 南昌 330063)
基于多层氧化层结构的硼颗粒点火模型研究
徐义华, 胡旭, 邹昊, 李雨林, 曾卓雄
(南昌航空大学 飞行器工程学院, 江西 南昌 330063)
为了研究相关因素对硼颗粒点火过程的影响规律,基于多层氧化层结构,改进了硼颗粒的点火模型。该模型考虑了颗粒氧化层表面物质成分的变化、表面火焰面形成的物理过程,模型计算结果与实验数据具有较高的吻合度。应用该模型研究了环境压强、颗粒直径、气相氧化剂浓度以及环境温度对硼颗粒点火过程的影响规律。结果表明,环境压力越大,颗粒点火时间越短;颗粒粒径越大,颗粒表面氧化层越厚,从而延长了颗粒的点火时间;在较大颗粒直径(>5 μm)下增加环境内氧气浓度有利于颗粒点火,对小颗粒直径(≤5 μm)则无明显影响;水蒸气浓度越大,颗粒点火时间越短;环境温度越高,越有利于颗粒点火。
航空、航天推进系统; 固体火箭冲压发动机; 硼颗粒; 氧化层结构; 点火模型
0 引言
硼颗粒具有高质量、高体积热值的特点,是理想的固体火箭冲压发动机推进剂燃料添加剂。然而硼的高熔点、高沸点以及表面覆盖着一层氧化物,使得硼颗粒的点火燃烧不同于轻金属的气相燃烧。研究表明:硼颗粒的燃烧过程包括两个阶段:第一阶段为氧化层包覆下的燃烧阶段,在此阶段主要为颗粒氧化层的消耗与颗粒的增温,当氧化层被完全消耗时,第一阶段结束,这一阶段又称为点火过程;第二阶段则是“洁净”硼颗粒燃烧,即颗粒表面无氧化层包覆条件下的燃烧,在这一阶段,硼颗粒与环境中的氧化性气体直接反应,直到硼颗粒燃尽,这一阶段又称为燃烧过程[1-7]。
对点火过程的认识,目前存在两种典型的思想,即King[8-9]的内扩散理论及Li等[10-11]和Yeh等[12]的外扩散理论。图1为两种点火模型的对比示意图。由图1可知,King[8-9]认为在硼颗粒点火过程中,环境中的氧气通过液态氧化层B2O3(l)向颗粒表面扩散与颗粒发生反应,生成液态氧化层B2O3(l)而增厚氧化层,同时外层B2O3(l)在高温下蒸发且与环境中的水蒸气进行反应生成HBO2(g)而消耗氧化层。Li等[10-11]和Yeh等[12]则认为硼颗粒在与氧化层交界面上与B2O3(l)发生溶解反应生成(BO)n(l),并向外扩散而增厚氧化层,同时氧化层外表面的B2O3(l)和(BO)n(l)在高温下蒸发,以及液态氧化物与环境中的水蒸气进行反应生成HBO2(g)而消耗氧化层。

图1 King[8-9]、Li等[10-11]和Yeh等[12]硼颗粒点火机理对比Fig.1 Comparison of boron particles ignition mechanisms in Ref.[8-9],[10-11] and [12]
Yeh等[12]采用环境扫描电镜和X射线衍射技术,研究了硼颗粒点火过程中各个组分的扩散机理,研究结果表明,硼颗粒的温度达到1 213 K开始与B2O3(l)发生溶解反应生成了聚合物(BO)n(l)。通过对颗粒表面气体的分子量进行检测发现,颗粒周围分子量为55±3,与二氧化二硼的53.64相近,由此判断氧化层的主要蒸发产物为B2O2(g)。
Ao等[13-14]通过对773 K氧气环境中的氧化层进行扫描电镜(TEM)观测,发现氧化层分为3层结构(见图2),最外层为薄层B2O3(l),中间层为(BO)n(l),内层为B2O3(l),据此分析,提出在硼颗粒点火过程中,同时存在内扩散和外扩散。图3为Yeh等[12]和Ao等[13-14]提出的硼颗粒点火机理对比示意图,图3中xp为氧化层厚度,rp为颗粒半径。Ao等[13-14]通过实验检测氧化层微观特性,认为环境中的氧气通过液态氧化层(B2O3(l)和(BO)n(l))向颗粒表面扩散与硼颗粒发生反应,生成液态氧化层B2O3(l),以及硼颗粒在氧化层内表面与B2O3(l)反应生成(BO)n(l)向外扩散,由于氧化层最外层为B2O3(l),认为蒸发产物为B2O3(g)。通过TEM图观测可知,(BO)n(l)厚度x1与内层B2O3(l)厚度x2之比约为0.6,引入了向内与向外扩散的比例系数λ=0.6.

图2 晶体硼在773 K氧气中氧化层形态Fig.2 Configuration of crystal boron oxide in 773 K oxygen

图3 Yeh等[12]和Ao等[13-14]提出的硼颗粒点火反应机理示意图Fig.3 Schematic diagram of ignition reaction mechanisms of boron particles in Ref.[12] and [13-14]
然而,在点火过程中,根据Macek等[6]的实验现象可知,当颗粒被加温至1 800 K以上时发出光亮、形成火焰,在点火阶段存在短暂的气相燃烧。火焰面上的气相化学反应将影响颗粒的温升,从而影响到颗粒氧化层的消除速率。随着粒子温度的升高,氧化层外层B2O3(l)的蒸发速率将大于生成速率,在点火过程中,氧化层外层成分将变成(BO)n(l),则其蒸发产物将变成B2O2(g)。蒸发产物的不同导致蒸发所需的热值发生改变,从而影响硼颗粒的点火过程。蒸发产物B2O2(g)在粒子附近与氧气反应形成的火焰直接影响颗粒的温升速率,也将影响硼颗粒的点火过程。
因此,本文基于硼颗粒点火过程中出现的多层氧化层结构,考虑点火过程中形成的火焰面及表面氧化物蒸发产物的不同,在前人研究的基础上,改进硼颗粒点火模型,为含硼固体冲压发动机燃烧流动数值计算提供理论参考。
1 硼颗粒点火模型
由图2可知,硼颗粒点火过程中,温度达到723 K时,硼颗粒氧化层产物分为3层结构,引入xp代表氧化层总厚度,x0代表最外层B2O3(l)厚度。当x0>0时,即氧化层外表面存在B2O3(l)时,颗粒点火模型遵循Ao等[14]提出的模型;当xo≤0时,即氧化层外表面B2O3(l)完全消耗,在氧化层外部为(BO)n(l)时,硼颗粒的点火模型是Yeh等[12]与Ao等[14]提出的模型的综合,即考虑双向扩散机制的基础上,氧化层蒸发产物为B2O2(g)。图4为硼颗粒点火过程的反应机制。
由图4可知,当x0>0时,最外侧的B2O3(l)是由在氧化层与硼交界面上的硼溶解于B2O3(l)生成的(BO)n(l)与向内扩散的氧气反应所产生的,其反应过程如图5所示,反应方程式如下:

图4 硼颗粒点火过程反应机理Fig.4 Reaction mechanism of boron particle ignition process
B(s)+B2O3(l)→3/n(BO)n(l),
(1)
1/n(BO)n(l)+O2(g)→BO2(a)+O(a),
(2)
BO2(a)+1/n(BO)n(l)→B2O3(l),
(3)
O(a)+1/n(BO)n(l)→BO2(g).
(4)
由此可见,外层B2O3(l)是由内层B2O3(l)通过以上系列反应迁移而成,将反应(1)式~(4)式写成总包反应可得
B(s)+O2(g)→BO2(g)+Q1,
(5)
式中:Q1为反应放热,取-284 kJ/mol.
除此之外,氧气向内扩散,在氧化层与硼交界面上与硼反应:
B(s)+3/4O2(g)→1/2B2O3(l)+Q2,
(6)
式中:Q2为反应放热,取-610 kJ/mol.
在氧化层最外层表面上存在B2O3(l)蒸发,以及B2O3(l)与水蒸气反应:
B2O3(l)+H2O(g)→2HBO2(l)+Q3,
(7)
B2O3(l)→B2O3(g)+Q4,
(8)

图5 表面B2O3(l)生成的反应机制Fig.5 Reaction mechanism of surface B2O3 (L) generation
式中:Q3与Q4分别为反应放热和吸热,取值分别为-356.5 kJ/mol和366.5 kJ/mol.
当x0≤0时,在氧化层与硼交界面上,与x0>0时一样,同时存在扩散反应式(6)式、氧化层内总包反应式(5)式和溶解反应过程,硼溶解于B2O3(l)生成(BO)n(l),如反应式(1)式,(BO)n(l)蒸发得到B2O2(g),即
(BO)n(l)→B2O2,
(9)
则将(1)式与(9)式合并,得到氧化层的蒸发总反应式为
2/3B(s)+2/3B2O3(l)→B2O2(g)+Q5,
(10)
式中:Q5为反应吸热,取301.4 kJ/mol.
氧化层除了蒸发反应外,还与环境中的氧气与水蒸气发生反应,其化学反应式为
4/3B(s)+4/3B2O3(l)+2H2O(g)+O2(g)→
4HBO2(g)+Q6,
(11)
式中:Q6为反应放热,取-88 kJ/mol.
当x0>0时,氧化层表面主要为B2O3(l),蒸发产物为B2O3(g),此时蒸发过程( (8) 式)速率为
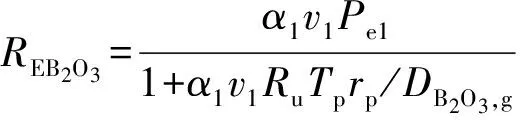
(12)

气体扩散系数利用赫兹- 克努增方程求解双分子扩散系数DAB,再利用Wilke[15]理论求解扩散系数Di,g,其计算公式分别为
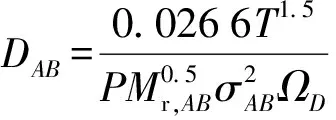
(13)

(14)
具体物质属性参考文献[15]。
在氧化层内,存在总包反应式(5)式,由于此时外层被液态B2O3所覆盖,因此在反应过程中存(BO)n(l)向B2O3(l)扩散,其反应速率为

(15)
DBO=5.11×10-5exp (-7 500/Tp) (cm2/s).
(16)


(17)
氧化层最外侧B2O3(l)与水蒸气反应( (7) 式)速率为
RH2O(x0>0)=

(18)
式中:Nu为颗粒努赛尔数;p为环境压力;pH2O为水蒸气的分压。
当x0≤0时,氧化层外表面为(BO)n(l),蒸发化学反应为 (10) 式,其速率为
(19)

在氧化层内的总包反应((5)式)及在氧化层表面反应((11)式)的产物直接进入气相环境中,产物扩散系数取值为反应最终产物在环境中的扩散系数。此时的反应速率分别为

(20)

(21)

无论x0>0或x0<0,都存在氧气向内扩散,在氧化层与颗粒交结处硼与氧气发生( (6) 式)反应,反应速率为

(22)
式中:XO2为氧气的摩尔组分含量;MB为硼的分子量,其数值为10.82;i为(6)式的化学反应当量比。考虑到(BO)n(l)和B2O3(l)物质属性基本类似,假设B2O3(l)在(BO)n(l)中的扩散系数与(BO)n(l)在B2O3(l)的扩散系数相同,即DB2O3=DBO.
在点火过程中所产生的产物中B2O2(g)化学形态最不稳定,与环境中的氧气发生化学反应,在第一阶段燃烧过程中的火焰主要由B2O2(g)与氧气的化学反应所形成。火焰面上的化学反应式为
B2O2(g)+1/2O2(g)→B2O3(l)+Q7.
(23)
由于最低火焰形成温度小于B2O3(l)的沸点(2 316 K),因此产物主要为液雾状三氧化二硼。由文献[14]计算得反应放热Q7的值为-753.3 kJ/mol. 假设在充足的氧气环境中,气相间反应速率迅速,则反应放热值由B2O2(g)的生成速率决定。
2 控制方程
硼颗粒点火过程的控制方程包括颗粒的半径rp、氧化层厚度xp和外层B2O3(l)厚度x0、以及颗粒的温度控制方程,其控制方程为
牛前胃疾病是牛养殖中的多发病,主要包括前胃弛缓、瘤胃积食、瘤胃鼓气、瘤胃酸中毒等几种。在日常养殖中如果饲养管理不当,很容易诱发各种疾病的发生,对牛养殖产业造成的危害很大。通常牛前胃疾病发生具有典型的季节性,牛前胃弛缓多发生在冬春季节,牛瘤胃积食和酸中毒主要发生在谷物成熟季节。日常养殖中,饲料缺乏维生素、矿物质、饲料粗糙、营养价值单一等,都会诱发牛前胃疾病发生。通常牛前胃疾病发病原因较为复杂,不但受到饲养管理和饲料种类的影响,也会受到机体所处生理状态等诸多因素的影响,机体出现临床症状通常是多种因素共同作用的结果。
(24)
(25)
(26)
式中:变量θ为氧气向颗粒表面扩散的程度,具体取值参考文献[16-17];ρB为颗粒密度。
根据文献[12,18]中对毕渥数的求解,得出毕渥数Bi≪1,因此假设颗粒内部温度均匀分布。在预热阶段和燃烧阶段的能量平衡方程为
(27)
式中:hc为对流换热系数;σ为斯蒂芬玻尔兹曼常数;εB为颗粒发射率;T∞为环境温度;cpB为硼颗粒比热;cpB2O3为比热,具体取值见参考文献[19];Tf为颗粒点火过程中火焰形成的临界温度。本文根据文献[3,6,12]的分析结果,对Tf取值如下:
当颗粒直径较小 (≤10 μm)时,在没有水蒸气的条件下Tf为1 800 K,在水蒸气环境下Tf为1 665 K;当颗粒直径较大时(>10 μm),在没有水蒸气的条件下Tf为1 992 K,在水蒸气环境下Tf为1 860 K.
3 硼颗粒点火模型验证与分析
根据文献[20]中的理论计算得到硼颗粒初始氧化层厚度xp为颗粒半径的1.3%,颗粒初始最外层B2O3(l)厚度x0为氧化层厚度xp的10%. 采用4阶龙格库塔法求解微分方程。
3.1 模型验证
以文献[6]中粒径为34.5 μm和44.2 μm的点火时间实验结果来验证本文模型的精度,表1列出了各实验工况条件。
由于实验中形成火焰时颗粒表层的氧化层厚度不明确,因此在此计算时从颗粒初始进入流场开始计算,颗粒初温为298 K,当颗粒温度达到火焰形成温度时开始统计点火时间[6]。表2为颗粒直径34.5 μm和44.2 μm的点火时间实验结果和数值计算结果的对比。由表2可知:当颗粒直径为34.5 μm时,最大相对误差为23.47%,最小相对误差为7.06%,平均相对误差为12.9%;当颗粒直径为44.2 μm时,最大相对误差为17.76%,最小相对误差为0.98%,平均相对误差为10.8%;计算结果与实验结果基本一致,点火模型具有较高的精度。

表1 Maeck等[6]实验工况Tab.1 Experimental conditions in Ref.[6]
文献[13]对2.3 μm的硼粒子在1~10 atm空气环境中进行了点火燃烧实验,对点火时间实验结果进行线性拟合可知,随着环境压力的上升,颗粒点火时间减小,这主要是由于随着压力的升高,氧化层与环境中氧化剂反应速率上升,增加了氧化层的消耗速率。虽然氧化层增厚速率也随着环境压力的增加而增加,但由于该反应为放热反应,提高其反应速率增加了颗粒的温升速率,使氧化层的蒸发速率增大。为了进一步验证本文模型对小粒径的硼颗粒点火计算的精度,分别选取1 atm、5 atm、10 atm空气环境下的颗粒直径2.3 μm硼粒子进行了点火计算。图6为计算结果与实验数据的对比,计算结果与实验数据基本一致。

图6 计算结果与文献[13]中实验数据的对比Fig.6 Comparison of calculated and experimental data in Ref.[13]
3.3 颗粒半径对点火的影响
为了对比颗粒尺寸对点火的影响,在环境压力为1 atm,温度为2 000 K,氧气摩尔分数为0.2的情况下,对颗粒直径分别为3 μm和5 μm的颗粒点火过程进行数值计算。颗粒初始温度为300 K. 图7和图8分别为颗粒温度与颗粒最外层氧化层厚度以及氧化层厚度随时间变化曲线。由图7可知,当颗粒温度小于1 800 K时,最外层氧化层的生成速率大于消耗速率,随着温度的持续上升,B2O3(l)的蒸发速率大幅上升,最外层氧化层被迅速剥离。由图8可知,颗粒温度小于1 920 K时,氧化层厚度基本不变,氧化层的蒸发速率与生成速率相当,随着温度的上升,氧化层蒸发速率逐渐上升,氧化层加速剥离。随着颗粒粒径越大,颗粒温升速率逐渐降低,氧化层与环境反应速率以及蒸发速率上升缓慢,从而增加了颗粒的点火时间。

图7 颗粒温度与最外层氧化层厚度随时间变化曲线Fig.7 Changes of particle temperature and thickness of the outermost layer of oxide with time

图8 颗粒温度与氧化层厚度随时间变化曲线Fig.8 Charges of particle temperature and thickness of oxide layer with time
3.4 氧化剂浓度对颗粒点火的影响
环境中的氧气和水蒸气的含量是硼颗粒点火过程中主要的影响因素。在环境压力为1 atm,温度为2 000 K的情况下,对初始温度为300 K的硼颗粒在不同氧气浓度的条件下进行点火数值计算。颗粒直径分别取值为1 μm、3 μm、5 μm和10 μm. 图9为颗粒点火时间与氧气摩尔分数之间的关系。由图9可知:在较大的颗粒直径(>5 μm)条件下,颗粒的点火时间随着氧气浓度的增加而降低;而在小颗粒直径(≤5 μm)条件下,颗粒点火时间几乎不受氧气浓度的影响。这是因为氧气摩尔分数的增加,使得点火过程中总包反应(5)式和(6)式的反应速率增大,虽然总包反应(6)式会增加颗粒表面氧化层厚度,但是由于反应(5)式与(6)式均为放热反应,随着反应速率的提高,颗粒温升速率显著上升。由 (12) 式和(19)式可以得出颗粒温度越高、表面氧化层蒸发速率越快,使得颗粒的点火时间减少。另外,由 (22) 式可知,粒径越大,氧气向内扩散速率增加趋势减缓,因此粒径越大,颗粒点火时间受氧气浓度影响越大。
在氧气摩尔分数为0.2,对不同的水蒸气浓度下颗粒直径为3 μm和5 μm的硼颗粒点火进行数值计算。图10为颗粒点火时间与水蒸气摩尔分数的关系。由图10可知,随着环境中水蒸气含量的增加,颗粒点火时间逐渐减短。这主要是由于水蒸气加速了氧化层的消耗,促进颗粒的点火。由总包反应(7)式和(11)式可知,初始阶段主要是水蒸气与氧化层最外侧B2O3(l)反应,当最外侧B2O3(l)完全消耗,水蒸气再与(BO)n(l)反应而消耗氧化层。

图9 颗粒点火时间随氧气摩尔分数变化Fig.9 Particles ignition time vs. mole fraction of oxygen

图10 颗粒点火时间随水蒸气摩尔分数变化Fig.10 Particles ignition time vs. mole fraction of H2O
3.5 环境温度对颗粒点火的影响
环境压力为1 atm、氧气摩尔分数为0.2的情况下,颗粒初始温度为300 K. 在此条件对颗粒直径分别为3 μm和5 μm的颗粒在不同环境温度的点火过程进行数值计算。图11为颗粒点火时间与环境温度的关系。由图11可知,随着环境温度的上升,颗粒点火时间明显减小,当环境温度超过2 000 K时,环境温度对颗粒点火时间的影响逐渐减小。随着环境温度的上升,颗粒的温升速率提高,由(12)式~(21)式可知,随着颗粒温度的逐渐上升,氧化层的消耗速率呈上升趋势。由 (22) 式可知,虽然氧化层增厚速率随环境与颗粒温度的增高而增高,但是该反应为放热反应,能增加颗粒的温升速率,从而使颗粒的蒸发速率增大。

图11 颗粒点火时间与环境温度关系Fig.11 Particles ignition time vs. ambient temperature
4 结论
基于多层氧化层结构,在Yeh等[12]和Ao等[14]提出的硼颗粒点火模型基础上,改进了硼颗粒点火模型,模型计算结果与实验结果基本一致。应用该模型对硼颗粒点火过程的影响因素进行了研究,得到主要结论如下:
1)随着环境压力增大,颗粒点火时间逐渐减短。
2)随着颗粒直径越大,颗粒温升速率逐渐降低,氧化层与环境反应速率以及蒸发速率上升缓慢,从而增加了颗粒的点火时间。
3)随着氧气浓度的增加,在较大的颗粒直径条件下(≥5 μm),颗粒的点火时间随着氧气浓度的增加而降低;而在小颗粒直径条件下,颗粒点火时间几乎不受氧气浓度增加的影响;水蒸气浓度越高,颗粒点火时间越小。
4)随着环境温度的上升,颗粒点火时间明显减小,当环境温度超过2 000 K时,环境温度对颗粒点火时间的影响逐渐减弱。
References)
[1] 敖文, 杨卫娟, 韩志江, 等. 硼颗粒点火燃烧模型进展研究[J]. 固体火箭技术, 2012, 35(3): 361-366, 371. AO Wen, YANG Wei-juan, HAN Zhi-jiang, et al. Research on boron particles ignition and combustion model [J]. Journal of Solid Rocket Technology, 2012, 35(3): 361-366, 371. (in Chinese)
[2] Hussmann B, Pfitzner M. Extended combustion model for single boron particles-part I: theory[J]. Combustion and Flame, 2010, 157(4): 803-821.
[3] Hussmann B, Pfitzner M. Extended combustion model for single boron particles-part II: validation[J]. Combustion and Flame, 2010, 157(4): 822-833.
[4] 胡建新, 夏智勋, 罗振兵, 等. 固体火箭冲压发动机补燃室内硼颗粒点火计算研究[J]. 含能材料, 2004, 12(6): 342-345. HU Jian-xin, XIA Zhi-xun, LOU Zhen-bing, et al. Calculation on ignition of boron particle of ducted rocket secondary chamber [J]. Energetic Materials, 2004, 12(6): 342-345. (in Chinese)
[5] 方传波, 夏智勋, 肖云雷, 等. 考虑Stefan影响的单颗粒硼着火过程研究[J]. 物理学报, 2013, 62(16): 164702-1-164702-8. FANG Chuan-bo, XIA Zhi-xun, XIAO Yun-lei, et al. Study of ignition process of boron particle with considering Stefan flow effects [J]. Acta Physica Sinica, 2013, 62(16): 164702-1-164702-8. (in Chinese)
[6] Macek A, Semple J M. Combustion of boron particles at atmospheric pressure[J]. Combustion Science and Technology, 1969, 1(3): 181-191.
[7] 王洪远, 徐义华, 胡旭, 等. 空气旋转进气对含硼固体冲压发动机二次燃烧性能影响的研究[J]. 兵工学报,2015, 36(4): 619-625. WANG Hong-yuan, XU Yi-hua, HU Xu, et al. Research on the characteristics of secondary combustion of boron-based ducted rocket with swirling air injection [J]. Acta Armamentarii, 2015, 36(4): 619-625. (in Chinese)
[8] King M K. Boron particle ignition in hot gas streams[J]. Combustion Science and Technology, 1973, 8 (5/6): 255-273.
[9] King M K. Ignition and combustion of boron particles and clouds[J]. Journal of Spacecraft and Rocket, 1982, 19(4): 294-306.
[10] Li S C, Williams F A. Ignition and combustion of boron in wet and dry atmospheres[J]. Symposium (International) on Combustion, 1991, 23(1): 1147-1154.
[11] Li S C, Williams F A. Ignition and combustion of boron particles combustion of boron-based solid propellants and solid fuels[M]. Boca Raton, FL: CRC Press Inc, 1993: 248-271.
[12] Yeh C L, Kuo K K. Ignition and combustion of boron particles[J]. Progress in Energy and Combustion Science, 1996, 22(6): 511-541.
[13] Ao W, Yang W J, Wang Y, et al. Ignition and combustion of boron particles at one to ten standard atmosphere[J]. Journal of Propulsion and Power, 2014, 30 (3): 760-764.
[14] Ao W, Zhou J H, Liu J Z, et al. Kinetic model of single boron particle ignition based upon both oxygen and (BO)ndiffusion mechanism[J]. Combustion, Explosion, and Shock Waves, 2014, 50(3): 262-271.
[15] Wilke C R. Diffusion properties of multicomponent gases[J]. Chemical Engineering Process, 1950, 46(2): 95-104.
[16] Povitsky A, Goldman Y. Boron particle ignition in high-speed flow[C]∥AIAA/SAE/ASME/ASEE 29th Joint Propulsion Conference and Exhibit. Monterey, CA: AIAA, 1993.
[17] Glassman I, Williams F A, Antaki P. A physical and chemical interpretation of boron particle combustion[C]∥Twentieth Symposium( International) on Combustion. Ann Arbor, MI: The Combustion Institute, 1984.
[18] Ulas A, Kuo K K, Gotzmer C. Ignition and combustion of boron particles in fluorine-containing environments[J]. Combustion and Flame, 2001, 127 (1/2): 1935-1957.
[19] 胡建新. 含硼推进剂固体火箭冲压发动机补燃室工作过程研究[D]. 长沙:国防科学技术大学, 2006. HU Jian-xin. Research on the secondary combustion chamber operation process of boron-based propellant ducted roeket [D]. Changsha: National Defense Science and Technology University, 2006. (in Chinese)
[20] Zhou W. Numerical study of multi-phase combustion: ignition and combustion of an isolated boron particle in fluorinated environments[D]. Princton: Princeton University, 1998.
Research on Model of Ignition of Boron Particle Based on Multiple Oxide Layer Structure
XU Yi-hua, HU Xu, ZOU Hao, LI Yu-lin, ZENG Zhuo-xiong
(School of Aircraft Engineering, Nanchang Hangkong University, Nanchang 330063, Jiangxi, China)
In order to study the influence of the related factors on the ignition process of boron particle by using numerical calculation method, an improved ignition model of boron particle is developed under the consideration of the multilayer oxide structure. The physical process of the change of species at the surface of the oxide layer and the formation of surface flame is considered in the model. The simulation results are in good agreement with published experimental data. The influences of ambient pressure, particle diameter, kinds of oxidant and their concentration, ambient temperature on the ignition process of boron particle are studied by using the improved ignition model. The simulation results show that the ignition time is shortened at higher ambient pressure. The larger the particle diameter is, the thicker the oxide layer is, thus delaying the ignition time. The higher oxygen concentration has a good effect on the ignition of boron particle on the larger particle diameter(>5 μm), but has little significant influence on smaller particle diameter(≤5 μm). The ignition of boron particle is promoted with water vapor available. The higher concentration of water vapor makes the ignition time reduced. The higher ambient temperature is useful for the ignition of boron particle.
aerospace propulsion system; solid fuel ramjet; boron particle; oxide structure; ignition model
2016-04-19
国家自然科学基金项目(51266013、51066006)
徐义华(1971—),男, 副教授,硕士生导师。 E-mail: xuyihua2003@163.com
V512
A
1000-1093(2016)12-2242-09
10.3969/j.issn.1000-1093.2016.12.009

