个体化精准抗癌光动力疗法综述
胡继辉,王倩倩,张勇,李炳南
合肥工业大学 生物医学工程系, 安徽 合肥 230009
个体化精准抗癌光动力疗法综述
胡继辉,王倩倩,张勇,李炳南
合肥工业大学 生物医学工程系, 安徽 合肥 230009
现有的癌症治疗手段主要包括外科手术、放疗和化疗3种,但都面临着不同的问题和挑战。化疗会导致严重的毒副作用,放疗需避免射线辐射,外科手术很难多次操作,各种副作用也严重影响患者的有效存活率。而光动力疗法通过注射光敏药物,直接光照病灶,能够有针对性地杀死癌细胞,整个过程几乎无损,可以反复运用、长期治疗,是一种精准抗癌疗法。传统光动力疗法由可见光激发,很难穿透皮肤并深入组织。在已有的各类成功案例中,病灶通常是数毫米厚的扁平组织,而上转换光动力复合功能材料能够由长波段红外光激发诱导光动力治疗,从而将其适用范围提高到了厘米级别。因此,上转换光动力疗法能够作用于更多种类的组织器官,更重要的是能够治疗相对大型的肿瘤病灶。然而,对于红外窗口范围之外的深层组织和大型病灶,上转换光动力疗法仍有其劣势。随着纳米技术、低功耗集成电路和无线传能技术的发展,有望发展出长效可控的植入体技术:通过微创医学植入病灶区域并在体外遥控植入体进行深层光动力治疗;利用无线传能技术,可以反复激活该微型植入体,支持长期抗癌治疗直至康复,从而能够将个体化精准光动力抗癌疗法提升到一个全新的高度。
精准治疗;光动力疗法;上转换;植入体;无线传能技术
0 引言
无论国内还是国外,癌症都是一个非常严重的医疗和社会问题。据世界卫生组织(World Health Organization,WHO)统计,癌症在致命性疾病中排名第二,仅2012年全世界死于癌症的患者就超过8200万(约占非传染性疾病死者的22%)。而在中国,据《2013中国卫生统计年鉴》,2012年恶性肿瘤所造成的死亡率排名第一(超过26%)。所以,抗癌治癌在国生民计方面占有至关重要的地位。
传统的癌症治疗方案主要有手术、放疗和化疗3种。然而,肿瘤的手术切除伴随着高复发率,放射治疗受到辐射剂量的限制,而化疗常常伴随着全身性的毒副作用。19世纪初,科学家首次观察到光动力反应,首次提出“光动力作用”这一概念。1975年,由多尔蒂等人以光敏剂应用于动物移植肿瘤的治疗,并获得了成功,从而建立了光动力疗法(Photodynamic Therapy,PDT)[1]。至今,有关PDT已做了大量的研究,并且在临床上得到了广泛应用[2]。在此基础上,进一步发展出了上转换光动力疗法(Upconversional Photodynamic Therapy,UPDT)[3],拓展了其适用症范围。随着纳米技术、低功耗集成电路和无线传能技术的发展,本文重点探讨长效可控的植入体技术[4]:通过微创手术将其植入病灶区域,并在体外遥控植入体进行深层光动力治疗;利用无线传能技术,可以反复激活该微型植入体,支持长期抗癌治疗直至康复,从而能够将光动力抗癌疗法提升到一个全新的高度。
1 光动力疗法
1.1 光动力反应
光动力反应过程,见图1。光敏剂吸收光能,从基态经历一个短暂的单重激发态后转变为存在期相对较长的三重激发态。处于激发态的光敏剂可以发生两种类型的光动力反应:① 三重激发态的光敏剂可以直接与细胞膜或一些生物大分子等底物发生反应,转移一个氢原子(电子)而形成自由基,自由基与组织氧相互作用生成可以杀伤目标细胞的氧化物(Ⅰ型反应);② 三重激发态的光敏剂把能量直接转移到氧分子上,形成一种高效的活性氧——单态氧来杀伤目标细胞(Ⅱ型反应)[5]。通常情况下,Ⅰ型反应和Ⅱ型反应会同时发生,但两者之间的发生比例取决于所使用的光敏剂类型、底物和组织氧的浓度、光敏剂与底物结合的紧密性[6]。能产生活性氧的光敏剂和能激发光敏剂的光动力是光动力疗法的两个基本要素。
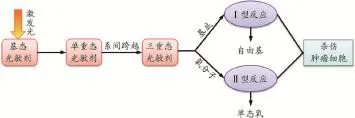
图1 光动力反应过程
1.2 光动力对肿瘤组织的破坏机制
光动力疗法对癌细胞的破坏主要有3种作用机制[2,7]:首先,光动力疗法生成的活性氧成分能够直接诱导细胞凋亡或坏死;其次,光动力能够损伤肿瘤组织的血管系统,使得癌细胞缺血性死亡;最后,光动力疗法能够激活机体的炎性反应和免疫反应。所有这些机制都有利于癌细胞的长期控制和治疗,而对癌细胞的杀伤范围和控制程度由多方面因素决定,包括使用的光敏剂类型、光敏剂在细胞内外的定位和积累、光活性、光照剂量、组织氧浓度等。所有这些因素相互作用、相互依赖[8]。
1.3 光动力疗法的优缺点
化疗药物容易诱发全身毒性,而放射疗法的电离光同样会损害正常组织。与其不同,光动力疗法对生物系统没有显著的毒副作用。与常规治疗方法相比,光动力疗法有一系列独特的优势,如微创性、可重复性,可降低长期发病率,提高患者的生活质量。在过去的40多年里,光动力疗法已经被证明对浅表性膀胱癌[9]、早期肺癌[10-11]、巴雷特食管癌[12]、头颈部癌[13]、皮肤癌[14]有显著的疗效。并且,可借助光纤技术对巨大型肿瘤、弥散性肿瘤、多发性肿瘤进行治疗。同时也被用作肿瘤切除术后的辅助治疗,以减少残留的癌细胞复发几率[15-18]。
光动力疗法与其他治疗方法相比,虽然有着明显的优势,但仍然存在着不少问题有待解决。首先,光动力疗法无法避免皮肤光过敏。病人在接受治疗期间必需避光,很不方便。其次,常用的光敏剂对肿瘤组织缺乏靶向性,难以有效富集达到病灶区域,影响治疗效果。再次,光敏剂多为疏水性分子,易团聚,在体内不易递送至癌细胞部位。最后,光动力疗法所采用的可见光穿透力较弱,有效作用范围只有数毫米左右[19]。因此,光动力疗法主要用于皮肤浅表部位病变以及空腔脏器内表面病变[20]。并且,病变范围不能超过激光的最大穿透距离。
1.4 光动力疗法的发展
上述缺点限制着光动力疗法的临床应用。近年来,国内外学者充分利用新型给药系统,在改善光敏剂对细胞、组织的靶向能力,降低治疗后的光毒性等方面已经取得一定成果。利用新型靶向给药系统作为光敏剂载体具有以下优势:①由于实体癌细胞的高通透性和滞留效应,载体可在肿瘤部位富集,且可对载体表面修饰靶向分子,从被动靶向和主动靶向两个角度来克服传统光敏剂靶向性不强的问题;② 经过表面修饰,可获得亲水性药物递送系统,解决负载疏水性光敏剂易团聚及难以输运等问题;③ 采用近红外光(波长通常在700~1000 nm)作为光动力源。由于近红外光穿透深度比可见光大一个数量级,且对正常组织和细胞具有比较低的光毒性。所以,构建新型光敏剂递送系统,其被近红外光激发,然后转换为可见光,再由可见光激发其负载的光敏剂,可克服光动力难以深入组织内部的难题[21-22]。
新型光敏剂递送系统主要有以下几类[23]:① 设计新型纳米颗粒为光敏剂的递送载体[3],包括磁性纳米颗粒、热敏性纳米颗粒、上转换纳米颗粒等;② 以脂质体为光敏剂递送载体,包括被动靶向脂质体、主动靶向脂质体等;③以聚合物胶束为光敏剂递送载体,包括递送卟啉类光敏剂的胶束、递送酞菁类光敏剂的胶束、递送稠环醌类光敏剂的胶束等;④ 以仿生型纳米系统为光敏剂递送载体。
2 上转换光动力疗法
近年来,上转换发光纳米材料(UpConversional Nano Particles,UCNPs)在光动力诊断和治疗领域脱颖而出[24-25]。其在980 nm或者800 nm波段的近红外光激发下,可发射出红、绿、蓝波段的可见光甚至是紫外波段的高能光。通过能量共振转移,能够激活其装载的光敏剂,产生单线态氧,达到诊疗一体化的目的,从而克服传统光动力疗法中光敏剂难输运、难靶向和难以治疗深层组织的缺点[3]。
2.1 上转换发光机制
上转换发光材料具有特殊性质,其受激发所发射的光子能量比激发光子的能量要高,所以称之为上转换发光。上转换发光材料通常得益于稀土元素电子间的跃迁,每种稀土离子都有特定的能级分布,而不同的稀土离子的上转换过程不同。一般而言,稀土离子的发光过程可以分为3步[26]:① 基质晶格吸收特定波段的激发能量;② 基质晶格将吸收的激发能量转移给激发离子;③ 被激发的稀土离子发出荧光,返回基态。上转换发光的过程主要有激发吸收、能量转移和光子雪崩等形式。
2.2 上转换光动力疗法
上转换发光材料的激发光在近红外波段,这是人体组织中相对透明的一个窗口,其组织穿透能力要远远好于可见光[21-22]。上转换发光材料的受激发射光在可见光波段,与许多光动力疗法中所使用的光敏剂的激发范围重叠。因此,可以设计并制备装载光敏剂的上转换发光复合功能纳米材料,其被980 nm或者800 nm波段的近红外光激发后,发射出的高能可见光进一步激活共体的光敏剂,从而诱发深部组织的光动力学治疗[27]。
2.3 上转换光动力疗法的优缺点
采用上转换发光纳米材料作为光敏剂的载体进行光动力治疗,具有独特的优势:① 通过改变掺杂不同的稀土离子及其浓度,受激发的光可实现从紫外到红外波段可调,从而有效匹配不同的光敏剂,充分利用现有成熟的光动力治疗技术;② 近红外激光器技术已经成熟,体积小巧紧凑,为上转换光动力疗法的应用转化提供了良好的条件。由此可见,将上转换发光技术引入光动力疗法,可以设计装载光敏剂的一体化复合功能材料,克服制约光动力疗法的不能应用于深层组织的难题[28]。但是,值得注意的是,上转换光动力疗法尚存在着一些根本性的问题和挑战,主要有:① 上转换发光的转换效率不高,目前的发光纳米材料及稀土掺杂机制还不能满足真正的临床应用需求;② 即便是980 nm或者800 nm的近红外光,其组织穿透窗口也只有1 cm左右的深度。但是,通常情况下,肿瘤不但位于深层组织内部,其尺寸也可能超过1 cm。
3 植入体技术
在现有的光动力疗法中,对于位处深层组织的癌细胞,需要将激发光动力的光纤植入体内,并在治疗过程中保持与体外的激光器连接,很大程度上限制了光动力疗法的有效性和适用性。一个很自然的想法便是将激发光源微型化,并装载光敏剂,一体化植入癌细胞或者肿瘤病灶附件,从而实现可遥控定制的个性化光动力疗法。
3.1 可植入设备
将医疗设备微型化并植入体内,在体实时监控生理状态和健康状况,是实现精准医疗和个性化医疗的一个长久梦想。早在50年前,便有研究者尝试将电子设备植入人体,通过记录心电、血压和体温的变化来了解生理状态,并用于医学诊断[29-32]。但是,只有在现代微机电系统和超低功耗电路技术得到充分发展之后,植入式微纳测控系统才真正走向现实。目前,在临床实践中,已经有不少商业化的植入式医疗装备,例如心脏起搏器、脑起搏器、无线内窥镜、人工耳蜗和视网膜等。但在实际应用中,各类医用植入体仍然面临着尺寸、功耗、可控性和生物相容性等一系列问题,需要发展新的系统集成、无线测控、功耗控制以及能源供给机制[33]。
3.2 可植入设备的发展
3.2.1 可植入设备的尺寸
随着纳米技术和低功耗集成电路技术的发展,可植入设备的尺寸越来越小。目前已经可以做到毫米级别,直接通过微创手术植入体内。目前应用最为成熟的有心脏起搏器、无线内窥镜等植入式系统。以色列Given Imaging公司推出的无线内窥镜已经得到美国FDA认证,包括图像传感器、无线通讯芯片、照明电路、氧化银电池等一系列模块在内,系统直径只有11 mm、长26 mm,重3.7 g,视野140°,放大倍率1:8,最小分辨率<0.1 mm。近来Xiao等[34]提出了一种无线供电的植入式传感器标签,其尺寸为直径5 mm、长17 mm,可连续监测血糖,范围为0~30 mmol。而Mortellaro等[35]则进一步设计了一个包含葡萄糖传感器、无线传能和穿戴式发射器的血糖监测植入式系统。其传感器是一个生物相容性良好的聚合物胶囊,内含微型荧光计,直径只有3.3 mm,长15 mm,尤其是内置了能够接收外源能量的微型天线,通过无线传能实现长期监测。
3.2.2 无线传能技术
任何电子装备需要电能才能运行,所以能量的供给是限制植入式电子器件使用寿命的关键。受人体生理解剖结构和有创手术的限制,医生和患者一方面希望植入电子器件的体积尽可能小;而另一方面,又希望植入电子器件的工作寿命能够尽量长。因此,目前不管是哪种植入式电子器件,几乎一半是被内部能源供给模块所占用。换而言之,医学植入电子器件的能量供给技术是保证其长期可靠运行的重要保障,也是影响器件微型化的关键因素之一[36]。
迄今为止,在医学植入电子器件中,采用率最高的供能方式主要有电池技术和磁感应技术[37]。其他方案或者是结构复杂、体积过大,或者是难以驱动植入器件完成工作。采用电池供电方式最大的问题是使用寿命。当系统电能耗尽后,必须通过外科手术对电池进行更换。使用磁感应技术供能,最大的障碍来自于较低的能量传递效率。此外,由于受内部植入环境的限制,线圈体积很小,导致系统耦合系数低,必须增大外置驱动电流,并且提高感应频率。不但会对周围的医疗设备产生射频干扰,而且外部设备携带起来也极不方便。值得注意的是,目前还没有证实此类电磁系统与人体细胞的相容性,以及细胞在这样的电磁环境下是否会发生变异等[38]。同时考虑到磁路泄漏,到底有多少能量真正能通过表皮进入人体内部,至今还没有完善的理论分析。
另一种体导电能量传递技术是通过紧贴皮肤的电极对,利用生物组织的离子型体液作为传导电流的载体,从而将体外激励能量传递到体内电极对上,进而为体内医学植入电子器件供能或者对电池进行充电[39]。值得注意的是,迄今为止,体导电能量传递技术依然处于基础理论研究,尚未形成一套有效机制来提高医学植入电子器件的能量传递效率。
斯坦福大学开发了一种专门为植入体内的医疗器械进行无线充电的新技术[4],能够为仅有米粒大小的电子设备进行无线充电,从而让这类设备彻底摆脱电池的束缚。其采用了一种新的无线传能方法[40],将近场(Near-feld)和远场(Far-feld)电磁波融为一体,从而能够通过皮肤向深层组织传播,提高了无线传能的效率,并且不会被人体组织吸收、反射和破坏。
4 个体化光动力疗法
围绕光动力疗法和上转换光动力疗法的可遥控植入体技术,本课题组已进行了一些初步研究,包括无线可控胶囊激光器以及无线传能植入线圈的技术研究。
4.1 胶囊激光器
新设计的胶囊激光器,见图2。此胶囊激光器由激光驱动模块、控制模块、通信模块、电源模块和纽扣电池组成。工作时,该胶囊激光器中的无线模块接收外部信号,传送给控制模块,触发激光驱动模块,点亮激光模块,从而进行光动力或者上转换光动力治疗。系统可根据不同的控制信号对激光驱动模块的亮度进行调节。目前系统样机模块的直径是11 mm,全长30 mm。下一步的工作目标是进一步优化集成系统,整体缩小系统尺寸到一半左右,然后装载光敏剂进行光动力疗法实验。
4.2 无线传能线圈
利用磁共振原理给无线传能提出一个新的解决方案,可以通过体外与体内两个线圈之间的电磁耦合输送电能。需要无线传能的时候,可以将体外初级射频感应线圈贴在皮肤表面,与植入体内埋在皮肤之下的小型次级感应线圈实现电磁耦合,从而获得感应电能驱动植入电子器件工作。目前课题组通过改变初级线圈形状、次级线圈匝数、线圈铜线直径等基本参数,实现了在低场条件下高效驱动10 mW的LED光源模块(图3)。下一步将优化主次线圈设计,调节谐振频率,延长主次线圈距离,尽快实现<10 mm的可植入次级线圈器件。

图2 胶囊激光器

图3 马鞍形和蝶形传能线圈实验
5 总结和展望
本文综述了个体化精准抗癌所涉及的光动力疗法、上转换光动力疗法、可植入设备和无线传能技术的基本原理、优缺点和发展状况。总体而言,随着纳米技术、低功耗集成电路和无线传能技术的发展,可遥控光动力治疗的长效植入体技术已经成为可能。在现有工作的基础上,本课题组将致力于研发高效的无线传能技术,并结合高效发光和能量转化技术,真正实现可遥控光动力治疗的长效植入体技术,增强光动力疗法在治疗深层组织大型病灶方面的能力,有效推动个体化精准抗癌光动力疗法的发展。
致谢
本项目由国家自然科学基金(61271123、31328009、61571176、61511140099),安徽省杰出青年基金(1608085J04),安徽省国际科技合作计划(1503062015)支持。
[1] Dougherty TJ,Grindey GB,Fiel R,et al.Photoradiation therapy.II. Cure of animal tumors with hematoporphyrin and light[J].J Natl Cancer Inst,1975,55(1):115-121.
[2] Abdel-Kadel MH.Photodynamic Therapy[M].Berlin Heidelberg:Springer-Verlag,2014.
[3] Lucky SS,Soo KC,Zhang Y.Nanoparticles in photodynamic therapy[J].Chem Rev,2015,115(4):1990-2042.
[4] Ho JS,Yeh AJ,Neofytou E,et al.Wireless power transfer to deep-tissue microimplants[J].Proc Natl Acad Sci U S A,2014,111(22):7974-7979.
[5] Sharman WM,Allen CM,van Lier JE.Role of activated oxygen species in photodynamic therapy[J].Methods Enzymol,2000,319:376-400.
[6] Castano AP,Demidova TN,Hamblin MR.Mechanisms in photodynamic therapy: part one-photosensitizers, photochemistry and cellular localization[J].Photodiagnosis Photodyn Ther,2004,1(4):279-293.
[7] Dolmans DE,Fukumura D,Jain RK.Photodynamic therapy for cancer[J].Nat Rev Cancer,2003,3(5):380-387.
[8] Oleinick NL,Morris RL,Belichenko I.The role of apoptosis in response to photodynamic therapy: what, where, why, and how[J].Photochem Photobiol Sci,2002,1(1):1-21.
[9] Yavari N,Andersson-Engels S,Segersten U,et al.An overview on preclinical and clinical experiences with photodynamic therapy for bladder cancer[J].Can J Urol,2011,18(4):5778-5786.
[10] Allison R,Moghissi K,Downie G,et al.Photodynamic therapy (PDT) for lung cancer[J].Photodiagnosis Photodyn Ther,2011,8(3):231-239.
[11] Moghissi K,Dixon K.Update on the current indications, practice and results of photodynamic therapy (PDT) in early central lung cancer (ECLC)[J].Photodiagnosis Photodyn Ther,2008,5(1):10-18.
[12] Hur C,Nishioka NS,Gazelle GS.Cost-effectiveness of photodynamic therapy for treatment of Barrett’s esophagus with high grade dysplasia[J].Dig Dis Sci,2003,48(7):1273-1283.
[13] Green B,Cobb AR,Hopper C.Photodynamic therapy in the management of lesions of the head and neck[J].Br J Oral Maxillofac Surg,2013,51(4):283-287.
[14] Kostović K,Pastar Z,Ceović R,et al.Photodynamic therapy in dermatology: current treatments and implications[J].Coll Antropol,2012,36(4):1477-1481.
[15] Muragaki Y,Akimoto J,Maruyama T,et al.Phase II clinical study on intraoperative photodynamic therapy with talaporfn sodium and semiconductor laser in patients with malignant brain tumors[J].J Neurosurg,2013,119(4):845-852.
[16] Rigual N,Loree T,Frustino J,et al.Sentinel node biopsy in lieu of neck dissection for staging oral cancer[J].JAMA Otolaryngol Head Neck Surg,2013,139(8):779-782.
[17] Friedberg JS,Mick R,Stevenson JP,et al.Phase II trial of pleural photodynamic therapy and surgery for patients with non-small-cell lung cancer with pleural spread[J].J Clin Oncol,2004,22(11):2192-2201.
[18] Akimoto J,Haraoka J,Aizawa K.Preliminary clinical report on safety and efficacy of photodynamic therapy using talaporfin sodium for malignant gliomas[J].Photodiagnosis Photodyn Ther,2012,9(2):91-99.
[19] 刘慧龙,刘凡光,顾瑛.影响光动力疗法的几个主要因素[J].中国激光医学杂志,2002,11:121-124.
[20] Bown SG,Rogowska AZ,Whitelaw DE,et al.Photodynamic therapy for cancer of the pancreas[J].Gut,2002,50(4):549-557.
[21] Jayakumar MK,Bansal A,Huang K,et al.Near-infrared-lightbased nano-platform boosts endosomal escape and controls gene knockdown in vivo[J].ACS Nano,2014,8(5):4848-4858.
[22] Jayakumar MK,Bansal A,Li BN,et al.Mesoporous silica-coated upconversion nanocrystals for near infrared light-triggered control of gene expression in zebrafish[J].Nanomedicine (Lond),2015,10(7):1051-1061.
[23] 王若宁,丁杨,周建平.基于光动力学疗法的光敏剂抗肿瘤靶向递送系统研究进展[J].中国新药杂志,2014,23(16):1897-1903.
[24] Mei Q,Li Y,Li BN,et al.Oxidative cleavage-based upconversional nanosensor for visual evaluation of antioxidant activity of drugs[J].Biosens Bioelectron,2015,64:88-93.
[25] Mei Q,Deng W,Yisibashaer W,et al.Zinc-Dithizone Complex Engineered Upconverting Nanosensors for the Detection of Hypochlorite in Living Cells[J].Small,2015,11(35):4568-4575.
[26] Idris NM,Jayakumar MK,Bansal A,et al.Upconversion nanoparticles as versatile light nanotransducers for photoactivation applications[J].Chem Soc Rev,2015,44(6):1449-1478.
[27] Zhang P,Steelant W,Kumar M,et al.Versatile photosensitizers for photodynamic therapy at infrared excitation[J].J Am Chem Soc,2007,129(15):4526-4527.
[28] 郑晓鹏,田甘,谷战军.荧光上转换纳米材料在光动力学治疗癌症中的应用[J].中国肿瘤临床,2014,41(1):27-31.
[29] Farrar JT,Zworykin VK,Baum J.Pressure-sensitive telemetering capsule for study of gastrointestinal motility[J].Science,1957,126(3280):975-976.
[30] SINES JO.Permanent implants for heart rate and body temperature recording in the rat[J].AMA Arch Gen Psychiatry,1960,2:182-183.
[31] Mackay RS.Radio Telemetering from within the Body:Inside information is revealed by tiny transmitters that can be swallowed or implanted in man or animal[J].Science, 1961,134(3486):1196-1202.
[32] Nagumo J,Uchiyama A,Kimoto S,et al.Echo Capsule for Medical Use (A Batteryless Endoradiosonde)[J].IRE Transactions on Bio-Medical Electronics,1962,9(3):195-199.
[33] Ratner BD.Healing with medical implants: The body battles back[J].Sci Transl Med,2015,7(272):272fs4.
[34] Xiao Z,Tan X,Chen X,et al.An Implantable RFID Sensor Tag toward Continuous Glucose Monitoring[J].IEEE J Biomed Health Inform,2015,19(3):910-919.
[35] Mortellaro M,DeHennis A.Performance characterization of an abiotic and fluorescent-based continuous glucose monitoring system in patients with type 1 diabetes[J].Biosens Bioelectron,2014,61:227-231.
[36] 唐治德.植入电子器件的体导电能量传递原理及方法研究[D].重庆:重庆大学,2007.
[37] Kim A,Ochoa M,Rahimi R,et al.New and Emerging Energy Sources for Implantable Wireless Microdevices[J].IEEE Access,2015,3:89-98.
[38] 贾智伟,颜国正,石煜,等.基于生物安全性的无线能量传输系统发射线圈优化设计[J].高技术通讯,2012,22(8):857-862.
[39] Liu H,Zhao T,Jiang W,et al.Flexible battery-less bioelectronic implants:Wireless powering and manipulation by near-infrared light[J].Small,2015,25:7071-7091.
[40] Kim S,Ho JS,Poon AS.Midfield wireless powering of subwavelength autonomous devices[J].Phys Rev Lett,2013,110 (20):203905.
Overview of Personalized Precise Photodynamic Therapy
HU Ji-hui, WANG Qian-qian, ZHANG Yong, LI Bing-nan
Department of Biomedical Engineering, Hefei University of Technology, Hefei Anhui 230009, China
The conventional techniques for cancer treatment include chemotherapy, radiotherapy, and surgery. However, chemotherapy often brings systemic side-effects, radiation therapy is limited by the cumulative radiation dose, and surgical resection of tumors is not suitable for repeated therapy. Photodynamic therapy (PDT) is an emerging precise intervention for cancer treatment, but it is yet limited to superficial lesions because of low penetration of visible light. Recently, upconversion technology was proposed as a transferring agent for PDT. It is excited by near infrared (NIR) and able to emit visible light. Without toxicity, NIR is good at tissue penetration. Therefore, upconversional PDT (UPDT) is very useful for treating solid and large tumors. One of the remaining issues is that most cancerous lesions lie inside human body and beneath deep tissues. In other words, they are still out of NIR penetration. The development of micro/nano circuits and systems for wireless power implants is studied in this paper, which are possibly employed for long-term PDT of deeply situated tumors. Furthermore, it is possible to remote control these implants that are directly placed nearby cancerous lesions. Once integrated with UPDT, such wireless power implants are capable of treating deeply situated large tumors. In conclusion, this new technology is promising to advance UPDT for precise tumor treatment.
precise treatment; photodynamic therapy; upconversion; implant; wireless powering
R454.2
A
10.3969/j.issn.1674-1633.2016.06.004
1674-1633(2016)06-0019-05
2016-02-02
国家自然科学基金(61271123、31328009、61571176、61511140099),安徽省杰出青年科学基金(1608085J04),安徽省国际科技合作计划(1503062015)。
李炳南,教授。
通讯作者邮箱:bingoon@ieee.org

