食品中蜡样芽孢杆菌平板计数的不确定度评定
吴卫玲,胡同静,钟君杰,徐振东
(1.江苏省苏州出入境检验检疫局,江苏 苏州 215104;2.江苏省苏州世标检测技术有限公司,江苏 苏州 215104)
食品中蜡样芽孢杆菌平板计数的不确定度评定
吴卫玲1,2,胡同静1,2,钟君杰1,2,徐振东1
(1.江苏省苏州出入境检验检疫局,江苏 苏州 215104;2.江苏省苏州世标检测技术有限公司,江苏 苏州 215104)
目的:为确保食品中蜡样芽孢杆菌检测结果的精确度。方法:依据GB 4789.14-2014中平板计数法对食品中蜡样芽孢杆菌的检测结果进行不确定度的评定。结果:蜡样芽孢杆菌检测结果的扩展不确定度为0.28,当样品中蜡样芽孢杆菌平板计数法的检测结果以平行样对数值的平均值表示时,其取值区间为3.17±0.28。 结论:建立的方法评定的不确定度可适用于食品的合格性判断。
食品;蜡样芽孢杆菌;平板计数法;不确定度
蜡样芽孢杆菌(Bacilluscereus)广泛分布于自然界,近年来在各类食品中的检出率较高。蜡样芽孢杆菌可产生不同毒素,引发食物中毒:一种是致吐型,是由于食品在食用前保存温度不当,放置时间过长使污染在食品中的蜡样芽孢杆菌或残存的芽孢得以生长繁殖,并产生毒素而引发呕吐;另一种是致腹泻型,是由于食入较多蜡样芽孢杆菌而产生的热稳定毒素,导致食物中毒[1]。根据香港《食品微生物含量指引》:一般即食食品含超过105cfu/g蜡样芽孢杆菌,可能危害食用者的健康或不宜供人食用[2]。目前已从多种食品中分离出该菌,包括肉、乳制品、蔬菜、鱼、土豆、糊、酱油、布丁、炒米饭以及各种甜点等。在美国,炒米饭是引发蜡样芽孢杆菌呕吐型食物中毒的主要原因;在欧洲,大多由甜点、肉饼、色拉和奶、肉类食品引起;在我国,则主要与受污染的米饭或淀粉类制品有关。食品中蜡样芽孢杆菌检测采用平板计数法时,实验过程包含诸多不确定因素。本实验对在同一相对恒定实验条件下,在同一时间段内,同一位检测人员应用同一批次的培养基和试剂,对同一批样品进行10次蜡样芽孢杆菌检测,对检测结果进行不确定度评定。
1 原理与方法
1.1 原理
依据GB 4789.14-2014食品安全国家标准《食品微生物学检验 蜡样芽孢杆菌检验》[3]第一法蜡样芽孢杆菌平板计数法进行检验,程序见图1。在同一相对恒定实验条件下,同一位实验人员对同一批次食品样品进行检测,对检测结果进行不确定度评定。本次样品为均匀并含可计算得出数目蜡样芽孢杆菌的固体食品。

图1 蜡样芽孢杆菌平板计数法检验程序Fig.1 The testing program of Bacillus cereusby plate count method
1.2 检测方法
1.2.1 样品制备
取1 kg不含蜡样芽孢杆菌的米饭于无菌取样袋中,加入100 mL无菌生理盐水,同时加入制备好的蜡样芽孢杆菌标准菌株(ATCC11778),用拍击式均质器拍击2 min,制成待测样品。
1.2.2 样品检测
称取25 g米饭置于盛有225 mL生理盐水的无菌均质袋中,用拍击式均质器拍打2 min,制成1∶10的样品稀释液。用1 mL灭菌微量移液器取1∶10样品稀释液1 mL,沿管壁缓缓注入含有9 mL灭菌生理盐水的试管内。振摇试管使其混匀,制成1∶100的样品稀释液,根据对样品污染状况的估计,按上述操作,依次制成10倍递增系列稀释样品稀释液。每递增稀释1次,换用1支1 mL无菌吸头。选择3个适宜的连续稀释度的样品稀释液,每个稀释度以0.3,0.3,0.4 mL接种量,分别接种在3块选择性培养基——甘露醇卵黄多粘菌素(MYP)琼脂平板上,用 L形棒涂布于整个表面,注意不要触及平板边缘。在通常情况下,涂布后,将平板静置10 min。如样液不易吸收,可将平板放在培养箱(30±1) ℃培养1 h,等样品匀液吸收后翻转平皿,倒置于培养箱中,(30±1) ℃培养(24±2) h。如果菌落不典型,可继续培养(24±2) h再观察。在MYP琼脂平板上,典型菌落为微粉红色(表示不发酵甘露醇),周围有白色至淡粉红色沉淀环(表示产卵磷脂酶)。选取适当菌落数平板计数,从每个平板中挑取5个典型菌落,分别划线接种于营养琼脂平板做纯培养,(30±1) ℃培养(24±2) h,进行确证实验。
1.3 数学模型的建立
选择1∶10和1∶100两个稀释度中只有一个稀释度的平板菌落数在20~200 cfu之间且有典型菌落,计数该稀释度平板上的典型菌落的条件下,建立数学模型:T = Cd/AB 。
式中: T为样品中蜡样芽孢杆菌菌落数; A为某一稀释度蜡样芽孢杆菌典型菌落的总数(本实验为1∶10稀释度); B为鉴定结果为蜡样芽孢杆菌的菌落数;C为用于蜡样芽孢杆菌鉴定的菌落数;d 为稀释因子(本实验d=10)。由于本实验采用添加阳性标准菌株,故B/C为1。
2 结果
2.1 不确定度来源
微生物检验中,一般仅对由样液制备、样液稀释、加样体积引起的不确定度进行分析,对来源于培养基、培养条件、操作人员操作技能等不便计算的不确定度忽略不计。
2.2 样液制备产生的相对标准不确定度(Um)
2.2.1 天平引入的相对标准不确定度(Um1)

2.2.2 量筒引入的相对标准不确定度(Um2)
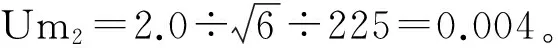
2.2.3 样液制备产生的相对标准不确定度(Um)
Um1和Um2是两个相对独立的分量,则Um2=Um12+Um22=0.0122+0.0042=0.01262。
2.3 样液稀释产生的不确定度(Uv)
2.3.1 移液器和分度吸量管(移液管)产生的不确定度分量 (Uv1,Uv2)

2.3.2 稀释产生的不确定度(Uv)
在蜡样芽孢杆菌检测过程中,采用100倍稀释,故稀释不确定度包括开始的10倍稀释和后续的10倍系列稀释。每步稀释所产生的不确定度Uvx2=(Ux12+Ux22)×bx2/(ax+bx)2。本次由连续稀释所产生的相对标准不确度Uv2=(Um12+Um22)×2252/(25+225)2+K×(Uv12+Uv22)×92/(1+9)2=(0.0122+0.0042)×0.81+K×(0.0042+0.0022)×0.81=0.01212,Uv=0.0121。K 为≥0的整数,当样品仅稀释10倍时,K=0;当样品稀释 100倍时,K=1;当样品稀释1000倍时,K=2,依次类推。稀释倍数越多,K值越大,稀释所产生的不确定度越大。
本次实验在20 ℃温度条件下进行,因此可忽略移液器、移液管等温度与校准时温度不同而引起的不确定度。若溶液温度不为20 ℃时,必须考虑温度对体积的影响。
2.4 加样体积产生的不确定度(Uj)

2.5 合成不确定度(Uy)
则u(T)=T×Uy =1.43×103×0.0384=2.69。
2.6 检测结果
本实验10次检测结果T分别为1.80×103,1.60×103,1.40×103,1.30×103,1.20×103,1.40×103,1.20×103,1.80×103,1.70×103,1.50×103cfu/g,平均值T为1.49×103cfu/g,则 log T=3.17。
2.7 扩展不确定度
取置信概率p=95%,自由度γ=10-1=9,由t分布表可得k=2.26。故Urel=k×Uy=2.26×0.0384=0.086784≈0.087,则U=Urel×log T≈0.087×3.17≈0.28。
2.8 不确定度报告
当样品中蜡样芽孢杆菌平板计数法的检测结果以平行样对数值的平均值表示时,其取值区间为3.17±0.28;当检测结果以平行样的平均值表示时,相对于对数值的取值再取反对数得其取值区间分布。
3 讨论
食品中蜡样芽孢杆菌的平板计数法实验步骤复杂,实验过程中的不确定因素较多,不确定度的来源包括样液制备、样液稀释、加样体积等,其中对来源于培养基、培养条件、操作人员操作技能等不便计算的不确定度可忽略不计。除了来源于以上介绍的几种不确定度外,还有来源于样品的种类、性状和稳定性、检测操作的环境、微生物培养条件、菌落计数、培养基、菌落的相互重叠等产生的不确定度,但均可以通过严格控制实验环境、培养条件、提高检测人员的操作技能,来降低其不确定度来源。
在 CNAS-CL07:2011《测量不确定度评估和报告通用要求》[7]中8.2规定:检测实验室应有能力对每一项有数值要求的测量结果进行测量不确定度评估。测量结果不确定度的评定是检测实验室质量体系的重要组成部分,而且测量结果不确定度的评定可以使实验室提供的数据更具有效性、科学性、公正性、可靠性。本文采用的评定方法适用于日常工作中,食品中蜡样芽孢杆菌平板法计数结果的不确定度评定,其不确定度主要来源于样品稀释、加样和重复检测等方面。
[1]齐哲,张伟,刘卫华,等.FTA滤膜与环介导等温扩增技术结合快速检测消毒乳中的蜡样芽孢杆菌[J].中国食品学报,2009(3):156-161.
[2]香港食品环境卫生署食品安全中心.食品微生物含量指引[Z].2014:13.
[3]GB 4789.14-2014,食品微生物学检验 蜡样芽孢杆菌检验[S].
[4]JJC 1036-2008,电子天平[S].
[5]JJG 196-2006,常用玻璃量器[S].
[6]JJG 646-2006,移液器检定规程[S].
[7]CNAS-GL07:2011,测量不确定度评估和报告通用要求[S].
The Uncertainty Evaluation of Plate Count Method for Bacillus cereus in Food
WU Wei-ling1,2, HU Tong-jing1,2, ZHONG Jun-jie1,2, XU Zhen-dong1
(1.Suzhou Entry-Exit Inspection and Quarantine Bureau, Suzhou 215104, China;2.Suzhou World Standard Testing Technology Co., Ltd., Suzhou 215104, China)
Objective:To ensure the accuracy of testing results ofBacilluscereusin food. Methods: According to GB 4789.14-2014, the uncertainty of plate count method for detection ofBacilluscereusin food is evaluated. Results: The expanded uncertainty of detection results is 0.28, when the testing result ofBacilluscereusin food by using the plate count method is in parallel to the sample for average value, the value range is 3.17±0.28. Conclusion: The uncertainty evaluation can accurately evaluate the eligibility of food and ensure the safety of food.
food;Bacilluscereus; plate count method; uncertainty
2016-06-22
吴卫玲(1987-),女,工程师,硕士,研究方向:食品化妆品微生物学。
TS201.3
A
10.3969/j.issn.1000-9973.2016.12.027
1000-9973(2016)12-0118-04

