钠离子电池用膨胀石墨的电化学法制备及性能探究*
李 欢,曹晓燕,韩晓琪,王 玮
(1. 中国海洋大学 化学化工学院,山东 青岛 266000;2. 中国海洋大学 材料科学与工程研究院,山东 青岛 266000)
钠离子电池用膨胀石墨的电化学法制备及性能探究*
李 欢1,曹晓燕1,韩晓琪1,王 玮2
(1. 中国海洋大学 化学化工学院,山东 青岛 266000;2. 中国海洋大学 材料科学与工程研究院,山东 青岛 266000)
为了探究膨胀石墨的储钠性能,利用电化学法制备了膨胀石墨,采用XRD对其结构进行了表征,并利用恒电流充放电、循环伏安(CV)、电化学阻抗谱(EIS)对其储钠性能进行了分析。结果表明,鳞片石墨经过电化学氧化再经过高温瞬时膨胀之后,层间距略微增大,但依然保持着石墨的层状结构。以二乙二醇二甲醚(DEGDME)为电解液,膨胀石墨对钠离子表现出较好的嵌/脱钠容量、倍率性能和循环性能:当电流密度为700 mA/g时,其可逆比容量为110.9 mAh/g,是10 mA/g时容量的66.8%。在100 mA/g电流密度下循环100次时,其第100次循环时的放电比容量为154.8 mAh/g,第一次循环时的放电比容量为134.8 mAh/g,容量保持率为114.8%。通过PITT测试,得出钠离子在膨胀石墨中的化学扩散系数为DNa+=7.7×10-8cm2/s。
膨胀石墨;负极;二乙二醇二甲醚;PITT;钠离子电池
0 引 言
在现有电池储能体系中,锂离子电池具有高电压、高能量密度以及更长久的循环寿命等特点[1-3],是近年来移动储能体系的首选。但是,锂资源相对稀缺,在一定程度上限制了锂离子电池的可持续发展。钠和锂属于同一主族元素,具有相似的物理化学性质,钠离子电池和锂离子电池具有类似的工作原理,而且钠资源丰富,价格低廉,因此,钠离子电池的研究近年来引起人们的广泛关注。
就钠离子电池负极而言,软碳[4-5]与硬碳[6-7]是目前研究较多的活性材料。硬碳一般由高分子聚合物热解而来[8],石墨化程度低、层状构造不发达,但具有丰富的微孔结构,微孔宽度一般在0.4 nm左右[9-11];而软碳则呈易石墨化性,一般用石油焦、沥青焦、煤焦等热处理获得[12]。无论是硬碳还是软碳,其制造成本相对较高,工艺相对繁琐,需要消耗较高的能量,而且,由于这些碳材料的本身结构原因,它们的电导率较低,且充放电过程中的电荷转移电阻较高,导致钠离子电池的性能不佳。
石墨是锂离子电池中常用的负极材料,但钠离子因半径比锂离子大而难以在石墨层中进行可逆的脱嵌,因此石墨曾被认为不能用作钠离子电池的负极[13-14]。但也有研究表明[15-17],醚类电解液如THF、Me-THF、DME、DEE等对钠离子具有较强的稳定性,而且具有二齿配体结构的线性DME分子对钠离子的稳定性要优于单齿配体结构的THF。DME与钠离子螯合后,形成的Na-DME复合物的大小主要由DME分子决定,且复合物具有刚性,该复合物与碳材料负极的相互作用较纯粹的钠离子要有所增强,可以克服插层阻力而共嵌进石墨层中,形成三元石墨插层化合物[18],进而实现了钠离子在石墨碳层间的可逆脱嵌。线性结构的二乙二醇二甲醚(DEGDME)具有三齿配体结构,其对钠离子的稳定性要强于DME[19],因此,与钠离子形成的Na-DEGDME复合物在共嵌进石墨层中时可以更容易地克服相邻碳层膨胀时的阻力,实现溶剂化钠的共嵌,从而解决了因钠离子与石墨层间距不匹配而无法储钠的问题[18]。
Kim H等[20]对天然石墨在DEGDME电解液中的储钠行为进行了深入研究。研究发现,钠离子在DEGDME电解液中以溶剂化钠的形式共嵌进天然石墨碳层之后,石墨碳层在高分辨率透射电子显微镜(HR-TEM)下呈现出褶皱状,原先有序的碳层结构变得无序,且相邻碳层间的距离增加到0.42~0.53 nm,明显大于天然石墨的相邻碳层距离0.33 nm。经过脱钠之后,无序的碳层结构恢复为有序状,但相邻碳层距离却变为0.34 nm。虽然由于天然石墨具有标准层状结构使得石墨碳层在插层物的作用下可以沿着c轴方向很容易膨胀开,从而在一定程度上缓解了插层物所带来的应力[17],但插层化合物在反复的共嵌与脱嵌过程中,天然石墨较小的层间距会使得插层阻力[18]较大,从而影响其储钠的可逆性。
对此,人们就膨胀石墨用于钠离子电池负极展开了研究。石墨的碳层间距增加并且仍依旧保持着层状结构的话,可使插层阻力有所减小,而且插层物产生的应力对石墨碳层结构的破坏作用也可能会在一定程度上得到减弱,经过电化学或化学氧化之后引入的一些功能基团也可能会对储钠性能具有一定的改善作用。目前,膨胀石墨造价相对较低,可大规模工业化生产,并且其电导率相对较高[21-22],具有丰富的网络状孔隙结构,比表面积较大[23-24],如果膨胀石墨可应用于钠离子电池负极的话,对钠离子电池而言,无论是性能上,还是价格上,比目前所用的碳材料都会具有很大的优势。
膨胀石墨的制备方法主要有化学法和电化学法。化学法一般是采用H2SO4-HNO3体系[25],此法虽工艺简单,但酸用量大,制备过程中由于某些化学因素难以控制,使得插入物在层间分布不均匀,导致产品的稳定性较差,而且环境污染严重。同化学法相比,用电化学法制备可膨胀石墨,其氧化剂用量和酸的浓度可大大降低,而且电化学插层反应时,插入物在层间分布均匀,产品的可膨胀性能稳定[24]。
本文以电化学方法制备的膨胀石墨用作钠离子电池负极材料,以二乙二醇二甲醚(DEGDME)为电解液,通过恒电流充放电、循环伏安(CV)、电化学阻抗谱(EIS)技术一系列电化学测试,探究了所制备的膨胀石墨的储钠性能,并利用恒电位间歇滴定法(PITT)测定了钠离子在膨胀石墨中的化学扩散系数。
1 实 验
1.1 膨胀石墨的制备
以一定固液比称取一定质量的天然鳞片石墨,以尼龙布袋包裹后,浸入到硫酸、过氧化氢混合液中,并在0.8 A电流下(电极表面积为5.3 cm2)电解 2 h,然后水洗至pH值为6~7,80 ℃下真空干燥8 h,并于800 ℃下膨化60 s。
1.2 样品的物理性能分析
使用多晶 X 射线衍射仪(Bruker D8 Advance,德国) 分析材料的晶体结构,扫描范围 10~40°,扫描速率 3°/min,管电压40 kV,管电流40 mA。
1.3 样品的电化学性能测试
将膨胀石墨和LA水性粘结剂,Super P导电剂,在质量比为8∶1∶1下混合,加入适量的蒸馏水进行调浆,涂覆于铜箔上。80 ℃下真空干燥,制备成负极极片。
以钠片作为对电极,1 mol/L 的 NaPF6/(DEGDME) 为电解液,组装成电池后,采用新威电池测试系统(CT-3008W)测定电池倍率性能和循环性能,倍率性能分别在10~700 mA/g的电流密度下进行恒电流充放电测试,循环性能测试是在电流密度为100 mA/g的条件下循环100次。循环伏安(0.005~2.5 V,0.1 mV/s)和交流阻抗(100 kHz~10 MHz)测试采用的分别是瑞士万通的Autolab PGSTAT204电化学工作站和德国ZAHNER公司的IM6型电化学工作站。
2 结果与讨论
2.1 材料的XRD分析
图1为鳞片石墨和膨胀石墨的XRD图谱,由图1可知,膨胀石墨在26°附近也出现了典型的石墨(002)面衍射峰,且衍射峰的峰强度显著降低,表明经过电化学氧化插层再经高温瞬时膨化处理之后所得的膨胀石墨,仍旧保持着石墨的层状晶体结构。
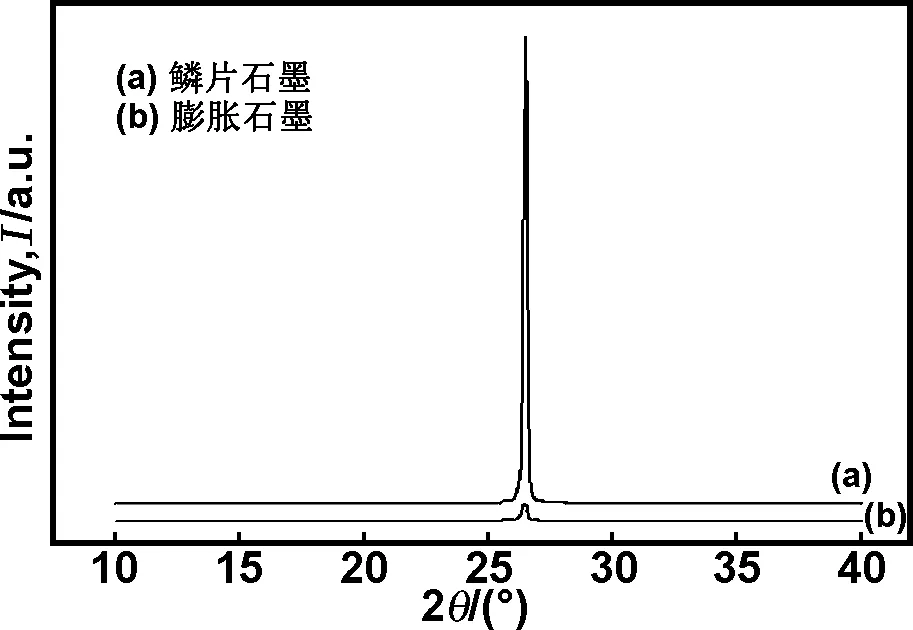
图1 鳞片石墨和膨胀石墨的XRD图谱
Fig 1 XRD patterns of flake graphite and expanded graphite
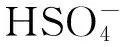
2.2 充放电曲线分析
图2为鳞片石墨和膨胀石墨在10mA/g的电流密度下的充放电曲线。由充放电曲线可以看出,鳞片石墨的充放电曲线中,在0.55 V(vs Na+/Na)左右出现一个非常明显的电压平台,在0.8 V(vs Na+/Na)附近出现一个相对较小的电压平台。平台现象揭示的是两相共存区,即两种不同阶的溶剂化钠-石墨层间化合物(Na-DEGDME-GICs)的共存区[26-27]。与鳞片石墨不同的是,膨胀石墨的充放电曲线没有出现非常明显的电压平台,而是表现为0~1.1 V(vs Na+/Na)之间倾斜的直线,原因可能是:膨胀石墨的碳层结构不像鳞片石墨那样标准,其内部存在的纳米碳层的无序堆积结构导致储钠活性位点变得复杂而导致[28]。
鳞片石墨的首次嵌、脱钠比容量分别为276.5和126.3 mAh/g,首次不可逆容量为150.2 mAh/g;而膨胀石墨的首次嵌、脱钠比容量分别为267.9和161.2 mAh/g,首次不可逆容量为106.7 mAh/g。可见,膨胀石墨的首次脱钠比容量较鳞片石墨有明显升高,且不可逆容量有较大幅度的降低。这表明与鳞片石墨相比,膨胀石墨与电解液的相容性提高,由于电化学氧化处理时一些功能基团的引入,以及孔隙结构的增多使得储钠的活性位点增多。
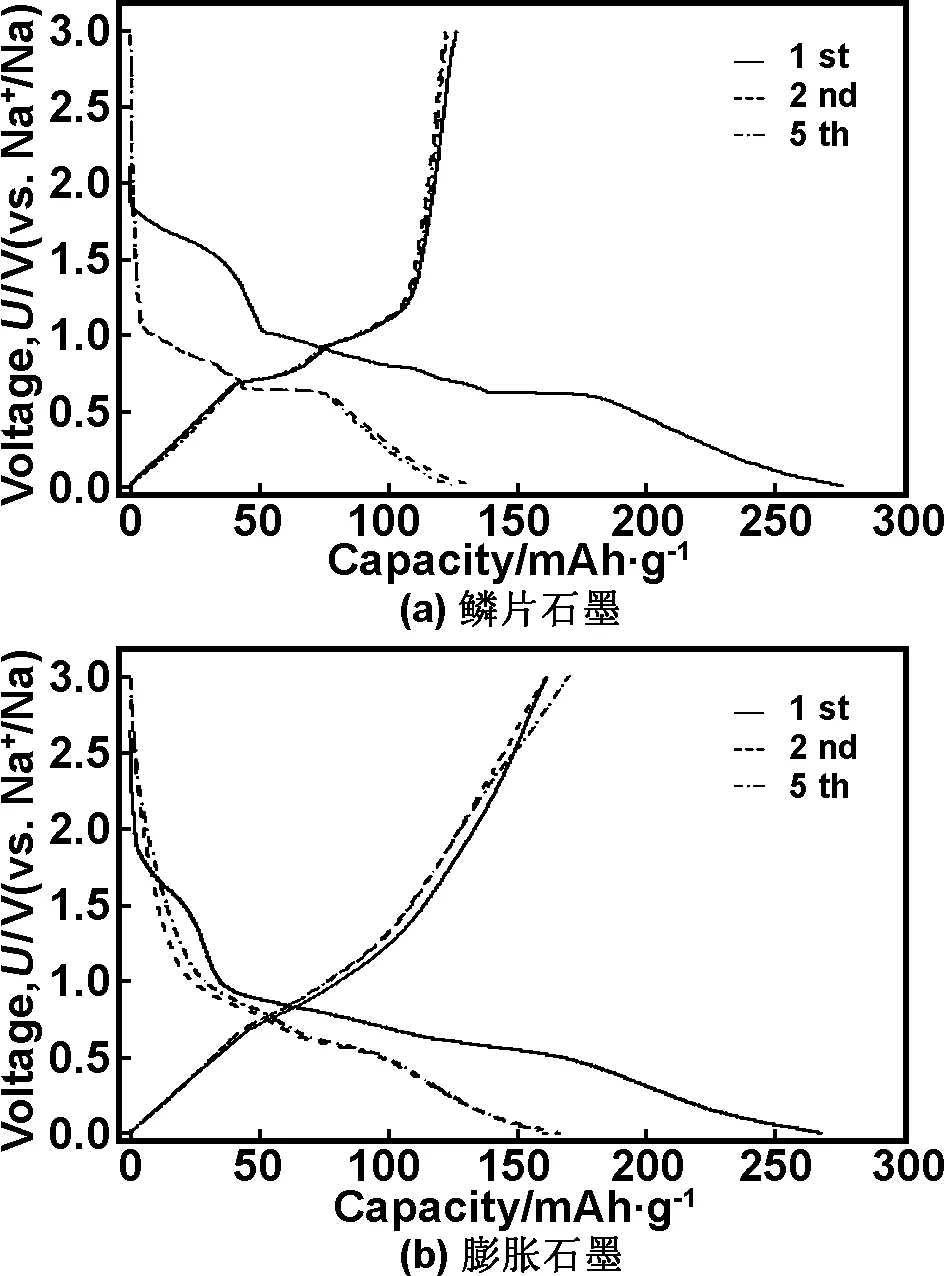
图2 鳞片石墨和膨胀石墨在10 mA/g电流密度下的充放电曲线
Fig 2 Galvanostatic charge/discharge profiles of flake graphite and expanded graphite at 10 mA/g
首次不可逆容量的存在,主要是与首次嵌钠过程中伴随着电解液的分解,并在石墨表面形成固体电解质膜(SEI膜)或钠离子与膨胀石墨中所含的残余含氧基团发生不可逆反应有关[29]。鳞片石墨的第5次嵌、脱钠比容量分别为125.7和123.3 mAh/g;而膨胀石墨的第5次嵌、脱钠比容量分别为161.2和169.7 mAh/g。可见,膨胀石墨的储钠性能较鳞片石墨有较为明显的改善。
2.3 循环伏安测试与分析
图3(a)为鳞片石墨和膨胀石墨在0.1 mV/s扫速下的循环伏安曲线。图3(b),(c)为膨胀石墨的首圈及第2、3圈的循环伏安曲线。由图可以看出,膨胀石墨的首次循环伏安曲线在0.3 V(vs Na+/Na)和1.5 V(vs Na+/Na)附近出现不可逆的还原峰,其对应的是在首次嵌钠过程中电解液的分解并在石墨材料表面形成SEI膜的过程或者钠离子与石墨材料表面存在的基团发生不可逆反应的过程。这也与充放电曲线中,首次不可逆容量较大相符合,如图3(d)所示。在随后的循环扫描中,这些还原峰均不在出现,这表明SEI膜在首次循环扫描中就已经开始形成,并在之后的循环扫描中能够持续存在。
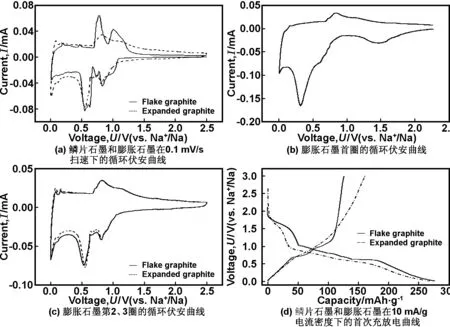
图3 (a) 鳞片石墨和膨胀石墨在0.1 mV/s扫速下的循环伏安曲线;膨胀石墨首圈(b)和第2、3圈(c)的循环伏安曲线;(d)鳞片石墨和膨胀石墨在10 mA/g电流密度下的首次充放电曲线
Fig 3 (a) Cyclic voltammograms of flake graphite and expanded graphite at 0.1 mV/s;the first (b) and the second and third cycles of CVs (c) of the expanded graphite; (d) the first cycle of galvanostatic charge/discharge profiles of flake graphite and expanded graphite at 10 mA/g
由鳞片石墨的循环伏安曲线可以看出,主要在0.12,0.55,0.73和0.82 V附近出现嵌钠的还原峰,其对应的是Na-DEGDME复合物嵌入石墨层间生成不同阶的石墨层间化合物的过程,其中,0.82 V附近的峰显示的是1阶和4阶的共存;0.73 V附近显示的是4阶和3阶的共存;0.55 V附近显示的是3阶和2阶的共存;0.12 V显示的是2阶和1阶的共存[19,30-31]。膨胀石墨的循环伏安曲线中也在相同的电位附近出现了嵌钠峰,但与鳞片石墨不同的是膨胀石墨的峰强度均有所降低,而在0.01 V附近的还原峰变强。由于经过电化学氧化处理之后所得的膨胀石墨可能会引入一定的功能基团,同时又因为其具有丰富的孔隙结构,增加了储钠活性位点,钠离子可吸附在碳纳米片层两侧或存储在纳米孔道或纳米空穴之中[4],对应于0.01 V附近的还原峰,因此,储钠性能有所提高。这也与充放电曲线中膨胀石墨的容量增大相一致。
2.4 倍率性能测试与分析
图4为膨胀石墨在不同电流密度下的倍率性能和100 mA/g电流密度下循环100次的循环性能曲线。
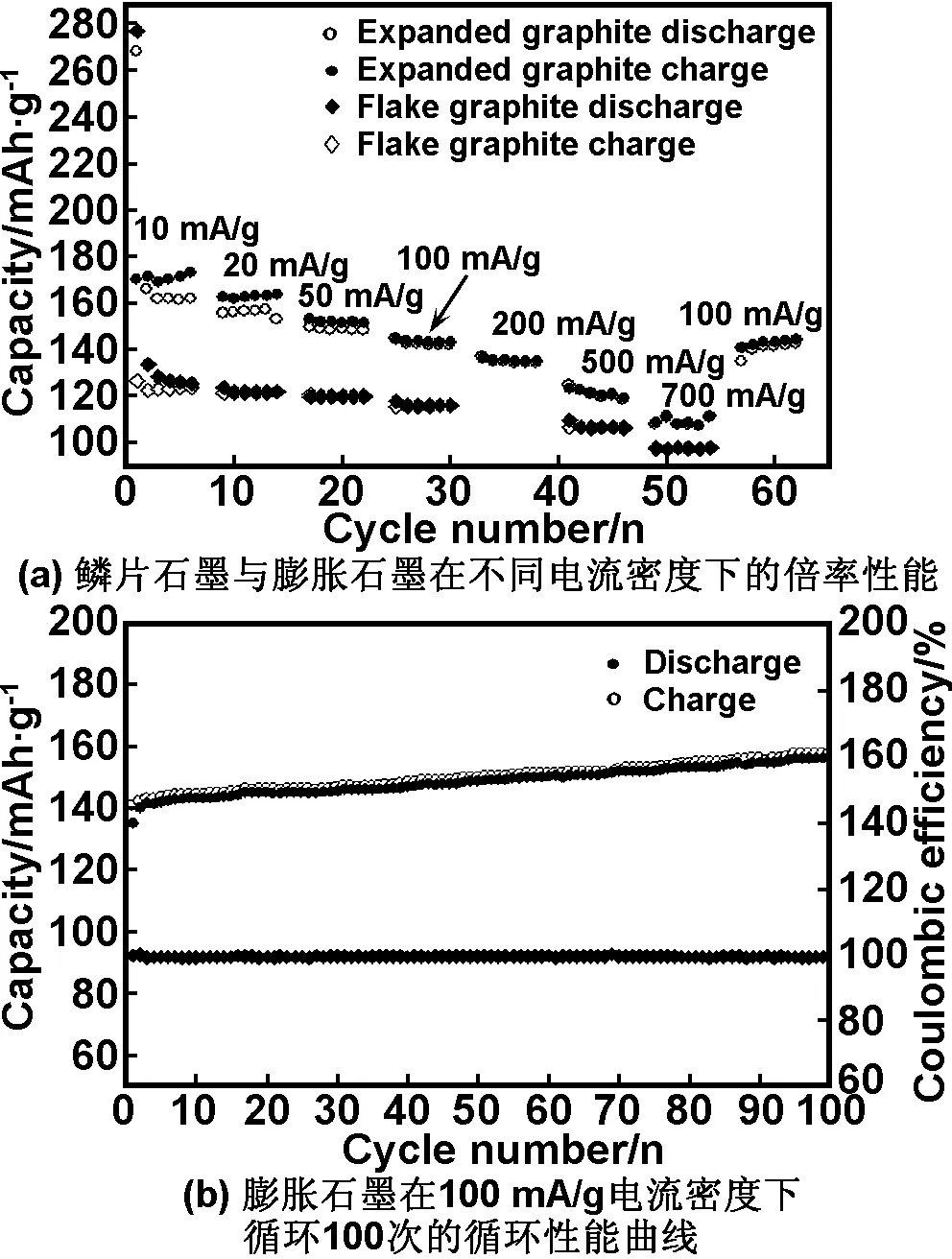
图4 鳞片石墨与膨胀石墨在不同电流密度下的倍率性能和膨胀石墨在100 mA/g电流密度下循环100次的循环性能曲线
Fig 4 Rate capability of flake graphite and expanded graphite at variant current and cycle stability of expanded graphite at 100 mA/g for 100 cycles
如前所述,虽然DEGDME对钠离子具有较好的稳定性,而且具有刚性性质的Na-DEGDME复合物能够克服插层阻力,即可以克服使相邻碳层膨胀开的阻力实现共嵌[18-19]。但,由于鳞片石墨层间距较膨胀石墨小,插层阻力较大,在溶剂化钠反复的共嵌与脱嵌过程中,鳞片石墨碳层受到的应力较大并可能会使鳞片石墨碳层剥落[17],导致鳞片石墨循环性能变差。而对膨胀石墨而言,由于其依然保持着石墨的层状结构,且层间距增大,使得插层阻力及因插层物的存在所产生的应力都相对减弱,从而具有较优异的循环性能,100 mA/g电流密度下循环100次时,其第100次循环时的嵌钠比容量为154.8 mAh/g,第一次循环时的嵌钠比容量为134.8 mAh/g,容量保持率为114.8%。对于锂离子电池碳负极材料而言,其在首次充放电之后可逆容量逐渐增大,有多种模型对这种现象进行解释,如,在碳原子层表面形成多层锂离子,形成共价分子Li2,Li—C—H键,锂离子在微腔结构中形成原子簇等[32],由于钠和锂在元素周期表的同一主族, 具有相似的物理化学性质,因此可以推测以上模型对于解释钠离子电池中碳负极材料的可逆容量随着循环次数逐渐增高这种现象具有一定的合理性。图4(a)为鳞片石墨和膨胀石墨在不同电流密度下的倍率性能,由图可知,膨胀石墨在不同电流密度下的充放电容量较鳞片石墨均有较为明显地提升。其中,当电流密度为10,50,100,500和700 mA/g时,膨胀石墨的放电比容量分别为为166.0,148.3,141.5,120.1和110.9 mAh/g。从10~700 mA/g电流密度的充放电过程中,膨胀石墨的放电可逆比容量从166.0 mAh/g下降到110.9 mAh/g,容量保持率为66.8%,当电流密度降回到100 mA/g时,放电可逆比容量上升为143.0 mAh/g。表明,在经过溶剂化钠的快速嵌入与脱出过程后,膨胀石墨的结构没有受到明显破坏,有较好的稳定性。图5为以鳞片石墨和膨胀石墨作为电极活性物质时,在不同电流密度下得到的Ragone图,可以看出,与鳞片石墨相比,膨胀石墨表现出较高的能量密度和功率密度,即使在700 mA/g的电流密度下,膨胀石墨的能量密度(132 Wh/kg)和功率密度(825 W/kg)依然优于鳞片石墨(85 Wh/kg,425 W/kg)。
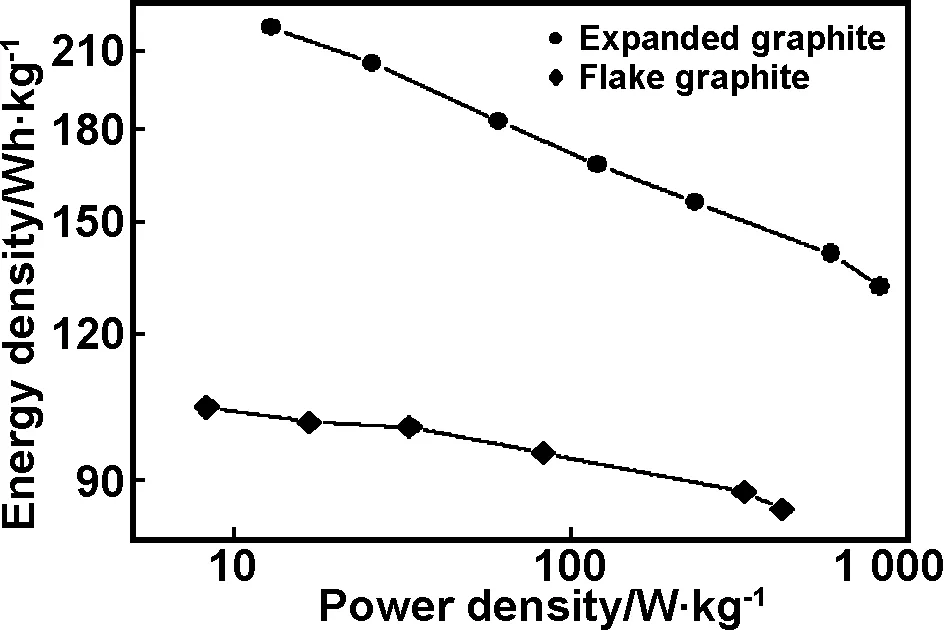
图5 鳞片石墨和膨胀石墨的Ragone图
Fig 5 Ragone plots for the flake graphite and expanded graphite based cells with Na metal as the counter/reference electrodes
从20~200 mA/g电流密度的充放电过程中,膨胀石墨的放电可逆比容量从156.9 mAh/g下降到134.9 mAh/g,容量保持率为86%,而Wen Y等[33]用改进的Hummer法制备的膨胀石墨以PC为电解液,从20~200 mA/g电流密度的充放电过程中,可逆比容量从284 mAh/g下降到91 mAh/g,容量保持率仅为32%;从200~500 mA/g电流密度的充放电过程中,膨胀石墨的放电可逆比容量从134.9 mAh/g下降到120.1 mAh/g,容量保持率为89%,而Zhou X等[34]通过热解氧化石墨烯掺杂的聚合物电解质前驱体得到的用于储钠的电极材料,以EC/PC(1∶1)为电解液,其从200~500 mA/g电流密度的充放电过程中,可逆比容量从192 mAh/g下降到150 mAh/g,容量保持率仅为78%。由此可见,以DEGDME为电解液,膨胀石墨具有较高的容量保持率,表现出较好的储钠性能,因此,当用作钠离子电池时其优异性能是不言而喻的。
2.5 交流阻抗测试与分析
图6为鳞片石墨和膨胀石墨电极在10 mA/g电流密度下充放电5次后的阻抗图和阻抗拟合图,测试电压均为2.3 V;插图表示横坐标0~160 Ω的放大图与等效电路。其中,R1表征的是溶液电阻;EIS高频区的半圆(R2Q3)归属于溶剂化钠从固体电解质膜(SEI膜) 迁移进入膨胀石墨的过程;EIS中频区的半圆(R5Q4)归属于电极反应的电荷转移过程(中高频区的半圆如插图所示);Q6,表征的是钠离子在电极中的扩散特性,对应于EIS低频区的倾斜直线。通过Z-view软件对阻抗图谱进行等效模拟电路分析发现,鳞片石墨的R2、R5分别为78.2和432.3 Ω;而膨胀石墨的R2、R5分别为26.7和18.0 Ω,即,膨胀石墨的R2、R5较鳞片石墨有明显降低。这可能由于膨胀石墨层间距较鳞片石墨有所增大,且具有特殊的孔隙结构,其与电解液的相容性较鳞片石墨也有所提高,因此,当其用作钠离子电池负极时的电荷转移电阻Rct(即,R5)与表面固体电解质膜(SEI膜) 的电阻RSEI(即,R2)较鳞片石墨要小很多,这一结果也与充放电分析相一致。
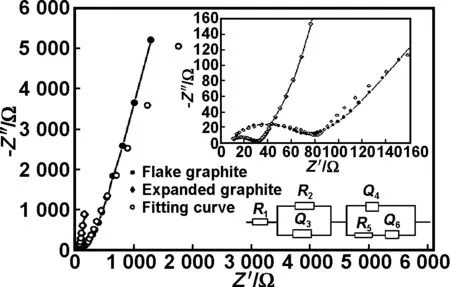
图6 鳞片石墨和膨胀石墨电极在10 mA/g电流密度下充放电5次后的阻抗图和阻抗拟合图
Fig 6 Nyquist plots of flake graphite and expanded graphite at 2.3 V after 5 cycles at 10 mA/g
2.6 恒电位间歇滴定(PITT)测试与分析
恒电位间歇滴定法(PITT)是通过瞬间改变电极材料在电极/电解液边界附近的反应粒子浓度,测定电流-时间曲线,通过该曲线可以确定反应粒子的扩散系数。PITT法测定钠离子扩散系数的方法有两种,一种是对球状电极求解扩散方程,另一种是对平面电极求解扩散方程,本文采用的是后一种方法。经过推导及合理的近似[35],可得钠离子在活性材料中的扩散系数DNa+如下
(1)
式中,DNa+为钠离子的扩散系数;t为扩散时间;L为电极上活性物质的扩散厚度。
在进行PITT测试前,首先对实验电池以10 mA/g的电流密度进行数次充放电,使电极活性材料得到电化学活化。将电池放电至0.07 V,然后静置8 h以上,当电池的开路电压在30 min内的变化不超过0.1 mV,即可以认为电极达到稳态,然后在LK9805Z恒电位仪上对电极进行PITT测试。在进行PITT测试时,对工作电极施加比开路电压大50 mV的一个阶跃电位,即,从0.07 V阶跃到0.12 V,得到电流对时间的曲线(I-t曲线),如图7(a)所示。
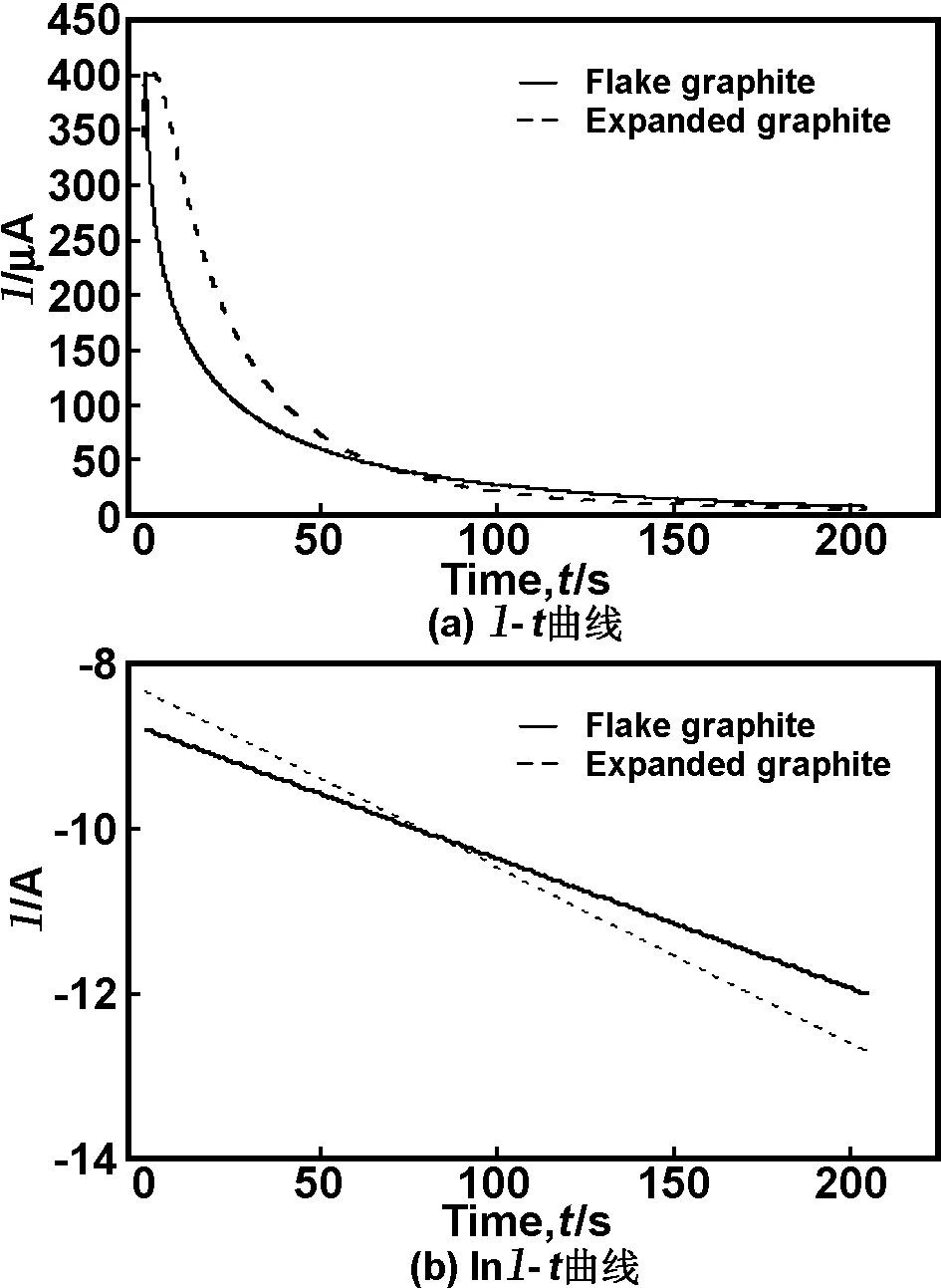
图7 鳞片石墨与膨胀石墨电极恒电位阶跃测试的I-t曲线和lnI-t曲线(从0.07 V阶跃至0.12 V)
Fig 7I-tand lnI-tcurves of a potential step from 0.07 to 0.12 V for the flake graphite and expanded graphite electrodes
通过I-t曲线变换得到lnI-t的线性关系曲线,经线性拟合之后得到如图7(b) 所示斜线,求出lnI-t的斜率分别为-0.0157,-0.0210 s-1,由于鳞片石墨的粒径多在20~100 μm之间,而电极厚度为30 μm,因此L以30 μm计,代入式(1)进行计算,得出钠离子在鳞片石墨和膨胀石墨中的扩散系数分别为DNa+=5.7×10-8cm2/s、DNa+=7.7×10-8cm2/s。由此可以看出,钠离子在膨胀石墨中的化学扩散系数要大于鳞片石墨,表明鳞片石墨经过膨胀之后层间距增大,使得溶剂化的钠离子在石墨碳层间的脱嵌变得容易,这也与钠离子在膨胀石墨中的插层阻力要小于鳞片石墨这一论断相符合。
3 结 论
以电化学方法制备的膨胀石墨用作钠离子电池负极,在DEGDME电解液中探究了其倍率性能及循环稳定性,结果表明,膨胀石墨由于依旧保持着较好的层状结构,同时其层间距较鳞片石墨有所增大且具有特殊的孔隙结构,并且电化学氧化处理时可能会引入一定的功能基团,使得其用作钠离子电池负极材料时,表现出较优的电化学性能。当电流密度为10,50,100,500和700 mA/g时,其放电比容量分别为166.0,148.3,141.5,120.1和110.9 mAh/g,电流密度为700 mA/g时的容量为10 mA/g时的66.8%。膨胀石墨在不同电流密度下的能量密度和功率密度均较鳞片石墨有较大幅度提升。在100 mA/g电流密度下循环100次,容量保持率为114.8%,通过PITT测试,得出钠离子在膨胀石墨中的化学扩散系数为DNa+=7.7×10-8cm2/s,与在鳞片石墨中的扩散系数DNa+=5.7×10-8cm2/s相比有所提升,显示出膨胀石墨优异的嵌脱钠性能。
致谢:感谢中国科学院青岛生物能源与过程研究所崔光磊研究员对本文实验提供的帮助;感谢新威尔电子有限公司免费提供的电池测试系统。
[1] Kraytsberg A, Ein-Eli Y. Higher, stronger, better… a review of 5 volt cathode materials for advanced lithium-ion batteries [J]. Advanced Energy Materials, 2012, 2(8): 922-939.
[2] Hwang Y H, Bae E G, Sohn K S, et al. SnO2nanoparticles confined in a graphene framework for advanced anode materials [J]. Journal of Power Sources, 2013, 240: 683-690.
[3] Prabakar S J R, Hwang Y H, Bae E G, et al.Graphene oxide as a corrosion inhibitor for the aluminum current collector in lithium ion batteries[J]. Carbon, 2013, 52: 128-136.
[4] Winter M, Besenhard J O, Spahr M E, et al. Insertion electrode materials for rechargeable lithium batteries [J]. Advanced Materials, 1998, 10(10): 725-763.
[5] Alcantara R, Madrigal F J F, Lavela P, et al. Characterisation of mesocarbon microbeads (MCMB) as active electrode material in lithium and sodium cells [J]. Carbon, 2000, 38(7): 1031-1041.
[6] Johnson B A, White R E. Characterization of commercially available lithium-ion batteries [J]. Journal of Power Sources, 1998, 70(1): 48-54.
[7] Bommier C, Luo W, Gao W Y, et al. Predicting capacity of hard carbon anodes in sodium-ion batteries using porosity measurements [J]. Carbon, 2014, 76: 165-174.
[8] Thomas P,Billaud D. Electrochemical insertion of sodium into hard carbons [J]. Electrochimica Acta, 2002, 47(20): 3303-3307.
[9] Dahn J R, Xing W, Gao Y. The “falling cards model” for the structure of microporous carbons [J]. Carbon, 1997, 35(6): 825-830.
[10] Ravikovitch P I, Vishnyakov A, Russo R, et al. Unified approach to pore size characterization of microporous carbonaceous materials from N2, Ar, and CO2adsorption isotherms [J]. Langmuir, 2000, 16(5): 2311-2320.
[11] Bommier C, Luo W, Gao W Y, et al. Predicting capacity of hard carbon anodes in sodium-ion batteries using porosity measurements [J]. Carbon, 2014, 76: 165-174.
[12] Wang Y G, Chang Y C, Ishida S, et al.Stabilization and carbonization properties of mesocarbon microbeads (MCMB) prepared from a synthetic naphthalene isotropic pitch [J]. Carbon, 1999, 37(6): 969-976.
[13] Ge P, Fouletier M. Electrochemical intercalation of sodium in graphite [J]. Solid State Ionics, 1988, 28: 1172-1175.
[14] Nobuhara K, Nakayama H, Nose M, et al. First-principles study of alkali metal-graphite intercalation compounds [J]. Journal of Power Sources, 2013, 243: 585-587.
[15] Alcántara R, Lavela P, Ortiz G F, et al. Carbon microspheres obtained from resorcinol-formaldehyde as high-capacity electrodes for sodium-ion batteries [J]. Electrochemical and Solid-State Letters, 2005, 8(4): A222-A225.
[16] Inagaki M,Tanaike O. Host effect on the formation of sodium-tetrahydrofuran-graphite intercalation compounds [J]. Synthetic Metals, 1995, 73(1): 77-81.
[17] Inagaki M, Tanaike O. Determining factors for the intercalation into carbon materials from organic solutions [J]. Carbon, 2001, 39(7): 1083-1090.
[18] Tanaike O, Inagaki M. Ternary intercalation compounds of carbon materials having a low graphitization degree with alkali metals [J]. Carbon, 1997, 35(6): 831-836.
[19] Kim H, Hong J, Yoon G, et al. Sodium intercalation chemistry in graphite [J]. Energy & Environmental Science, 2015, 8(10): 2963-2969.
[20] Kim H, Hong J, Park Y U, et al. Sodium storage behavior in natural graphite using ether-based electrolyte systems [J]. Advanced Functional Materials, 2015, 25(4): 534-541.
[21] Zheng G, Wu J, Wang W, et al. Characterizations of expanded graphite/polymer composites prepared by in situ polymerization [J]. Carbon, 2004, 42(14): 2839-2847.
[23] Celzard A, Schneider S, Marêché J F. Densification of expanded graphite [J]. Carbon, 2002, 40(12): 2185-2191.
[24] Kang F,Zheng Y P, Wang H N, et al. Effect of preparation conditions on the characteristics of exfoliated graphite [J]. Carbon, 2002, 40(9): 1575-1581.
[25] Inagaki M, Tashiro R, Washino Y, et al. Exfoliation process of graphite via intercalation compounds with sulfuric acid [J]. Journal of Physics and Chemistry of Solids, 2004, 65(2): 133-137.
[26] Dahn J R. Phase diagram of LixC6[J]. Physical Review B, 1991,44(17):9170.
[27] Winter M, Besenhard J O, Spahr M E, et al.Insertion electrode materials for rechargeable lithium batteries [J]. Advanced Materials, 1998, 10(10): 725-763.
[28] Yoo E J, Kim J, Hosono E, et al. Large reversible Li storage of graphene nanosheet families for use in rechargeable lithium ion batteries [J]. Nano Letters, 2008, 8(8): 2277-2282.
[29] Wenzel S, Hara T, Janek J, et al. Room-temperature sodium-ion batteries: Improving the rate capability of carbon anode materials by templating strategies [J]. Energy & Environmental Science, 2011, 4(9): 3342-3345.
[30] Kim J S, Park Y T. Characteristics of surface films formed at a mesocarbon microbead electrode in a Li-ion battery[J]. Journal of Power Sources, 2000,91(2):172-176.
[31] Takami N, Satoh A, Hara M, et al. Rechargeable lithium-ion cells using graphitized mesophase-pitch-based carbon fiber anodes [J]. Journal of the Electrochemical Society, 1995, 142(8): 2564-2571.
[32] Zhou H, Zhu S, Hibino M, et al. Lithium storage in ordered mesoporous carbon (CMK-3) with high reversible specific energy capacity and good cycling performance [J]. Advanced Materials, 2003, 15(24): 2107-2111.
[33] Wen Y, He K, Zhu Y, et al.Expanded graphite as superior anode for sodium-ion batteries [J]. Nature Communications, 2014, (5):4033-4035.
[34] Zhou X, Zhu X, Liu X, et al.Ultralong cycle life sodium-ion battery anodes using a graphene-templated carbon hybrid [J]. The Journal of Physical Chemistry C, 2014, 118(39): 22426-22431.
[35] Wen C J, Boukamp B A, Huggins R A, et al. Thermodynamic and mass transport properties of “LiAl” [J]. Journal of the Electrochemical Society, 1979, 126(12): 2258-2266.
Electrochemical properties of expanded graphite prepared by electrochemical method for Na-ion batteries
LI Huan1, CAO Xiaoyan1,HAN Xiaoqi1, WANG Wei2
(1. College of Chemistry and Chemical Engineering,Ocean University of China,Qingdao 266000,China;2. Institute of Materials Science and Engineering,Ocean University of China,Qingdao 266000,China)
In order to investigate the properties for sodium-ion storage of expanded graphite, an expanded graphite was prepared by electrochemical method. The structure of the samples were characterized by X-ray diffraction (XRD) and the electrochemical behaviors were studied using galvanostatic charge/discharge test, cyclic voltammogram, and electrochemical impedance spectra. The results indicated that the modified flake graphite still kept the layer structure after electrochemical oxidation and expansion, while the average interlayer distance expanded slightly. Using diethylene glycol dimethyl ether (DEGDME) as the solvent, the capacity of sodium-ion insertion and extraction of the expanded graphite as well as the the rate performance and cycling behavior were improved significantly. A high reversible capacity of 110.9 mAh/g could be obtained at 700 mA/g, which was 66.8% of the capacity at 10 mA/g. After cycling over 100 charge/discharge cycles at 100 mA/g, the expanded graphite still maintained the high capacity of 154.8 mAh/g, with a capacity retention ration ratio of 114.8%. A study of potentiostatic intermittent titration technique(PITT) yield that the mean Na-ion diffusion coefficient, was 7.7×10-8cm2/s.
expanded graphite; anode; DEGDME; PITT; sodium ion battery
1001-9731(2016)12-12162-07
国家高技术研究发展计划(863计划)资助项目(2014AA052303);国家自然科学基金资助项目(51572247);山东省科技攻关计划资助项目(2011GGX10201)
2016-02-01
2016-06-16 通讯作者:曹晓燕,E-mail: caoxy@ouc.edu.cn, 王 玮
李 欢 (1991-),男,安徽亳州人,硕士,师承曹晓燕教授,从事新能源材料研究。
TM912
A
10.3969/j.issn.1001-9731.2016.12.027

