不同生长调节物质对水稻生长及镉积累的影响
何 冰,陈小勤,辛子兵,陆覃昱,石 桥,顾明华,王学礼
广西大学农学院,南宁 530005
不同生长调节物质对水稻生长及镉积累的影响
何 冰,陈小勤,辛子兵,陆覃昱,石 桥,顾明华*,王学礼
广西大学农学院,南宁 530005
比较脱落酸(ABA)、乙烯利(ETH)、水杨酸(SA)和茉莉酸甲酯(MeJA)4种植物生长调节物质(PGR)对水稻生长及籽粒镉(Cd)积累的影响差异。试验采用重金属污染土种植水稻,于分蘖期、灌浆期各进行1次PGR叶面喷施处理,分析灌浆期叶片光合指标,丙二醛(MDA)含量以及收获期各部位生物量和Cd含量。结果表明:(1) 低浓度ABA(5mg/L)可维持水稻正常产量;高浓度ABA(15mg/L)则导致产量下降。ETH对水稻地上部生长和单株产量有显著抑制作用,SA和MeJA(0.56mg/L)均可保证地上部正常生长,维持正常产量。(2) 外施4种PGR均抑制灌浆期叶片气孔开放,降低蒸腾速率和光合速率,抑制效果最明显的是高浓度MeJA(0.56mg/L)。(3) 在供试浓度范围内SA、低浓度ABA(5mg/L)以及高浓度MeJA均可降低灌浆期叶片MDA含量,减少质膜过氧化水平。(4) 4种PGR均可降低水稻籽粒Cd含量,其中低浓度ABA(5mg/L)抑制籽粒Cd积累的效应最佳。相关性分析结果表明,PGR抑制籽粒积累Cd的效应与地上部向籽粒转运Cd的调控机制有关,与蒸腾速率无显著相关关系。(5) 综上所述,低浓度ABA(5mg/L)处理对水稻产量无影响,且籽粒Cd含量降低程度最大。适当浓度的PGR可降低水稻籽粒Cd含量,在中低度重金属污染农田生态修复实践中具有一定的应用前景,但必须精确控制PGR的处理时间和处理浓度,避免出现抑制生长和降低产量的负效应。
水稻;镉(Cd);生长调节物质(PGR)
镉(Cd)是生物毒性最强的重金属之一[1]。工业“三废”大量排放,矿业的过度开采以及不合理的农业措施,导致土壤Cd污染日趋严重,大量农田存在Cd污染问题[2]。作为非必需元素,Cd在作物体内过量积累将导致作物产量和质量下降,更为严重的是Cd通过食物链进入人体,对身体健康造成严重的危害[1, 3]。因此,减少作物对Cd的吸收和积累,保障农产品的安全生产迫在眉睫。
植物生长调节物质(PGR)是一类对植物的生长发育有调节作用的化学物质,包括植物内源激素和人工合成的生长调节剂。其中脱落酸(ABA)、水杨酸类(SAs)、茉莉酸类(JAs)以及油菜素甾醇类(BRs)等被认为在植物抵御干旱、盐碱、低温、高温、重金属等逆境方面起重要作用[4- 10]。PGR参与植物对重金属污染的反应[11-13]。有研究表明,PGR可能通过提高抗氧化剂的活性调节氧化还原水平,或者直接作为一种抗氧化剂淬灭活性氧,对研究植物的重金属抗性有重要意义[14- 16]。Hsu[17]认为在Cd胁迫下水稻通过增加内源ABA,降低了蒸腾效率,使Cd由根系向地上部的转运下降。
本文通过比较脱落酸(ABA)、乙烯利(ETH)、水杨酸(SA)以及茉莉酸甲酯(MeJA)处理后水稻生长及籽粒积累Cd的差异,初步分析不同PGR影响水稻籽粒Cd积累的效应机制。
1 材料与方法
1.1 试验设计
试验供试土壤采自广西壮族自治区某重金属污染地区农田。土壤基本理化性质和重金属含量为:全氮,1.411 g/kg;全磷,0.3084 g/kg;全钾,9.861 g/kg;有机质,23.30 g/kg;碱解氮,62.48 mg/kg;速效磷,33.50 mg/kg;速效钾,88.00 mg/kg;土壤pH,6.16;总Cd含量,7.67 mg/kg;有效态Cd含量,4.00 mg/kg。
将采集的污染土自然风干,过筛(孔径5 mm),装入不透光塑料桶(高24 cm,直径25.5 cm)中,每桶装土7.5 kg,并施入0.675 g K2O和0.75 g P2O5做基肥,混匀,完全淹水平衡两周。供试水稻品种为宜香9303。将培育好的水稻秧苗(4叶1心期)移入装有污染土的塑料盆中,每盆5株。移苗时每盆追施0.45 g 氮,分蘖期追施0.3375 g 氮(均为尿素提供)。试验共设9组处理(表1),每组4个重复。分别于分蘖期、灌浆期各进行1次PGR叶面喷施,平均用量为每盆30 mL,以叶面均匀覆有水珠、叶尖滴水为限。
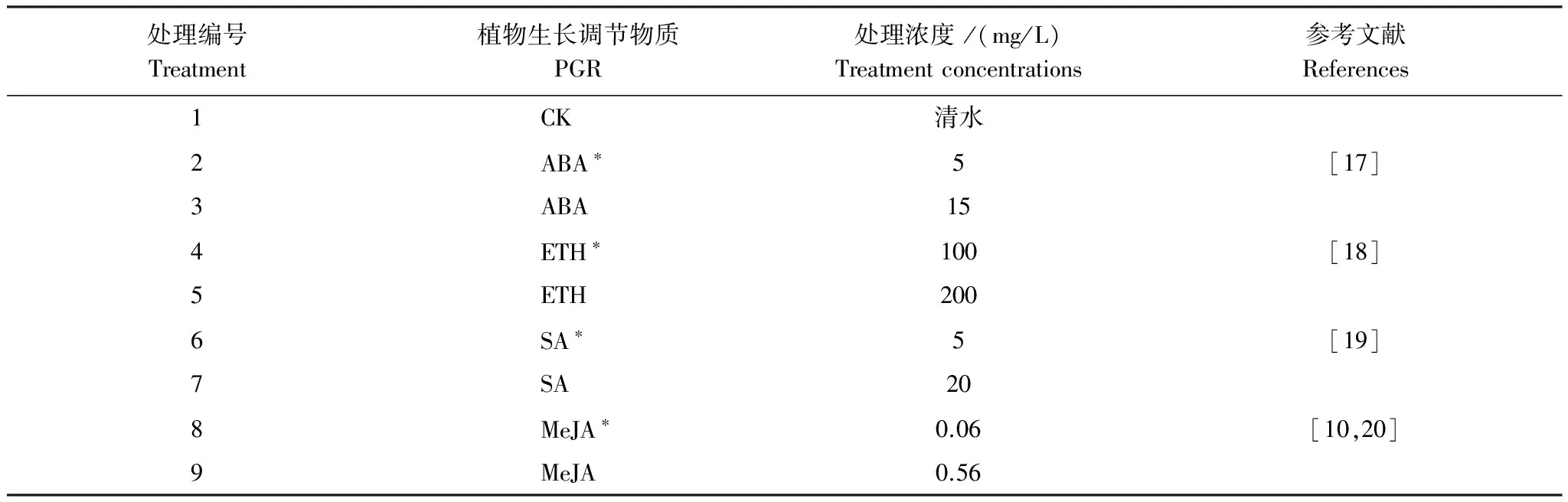
表1 PGR处理浓度
ABA: 脱落酸; ETH: 乙烯利; SA: 水杨酸; MeJA: 茉莉酸甲酯. ABA, ETH, SA, MeJA means Abscisic acid, Ethylene, Salicylic acid and Methyl Jasmonate,respectively
1.2 测定项目及方法
1.2.1 植株株高和干重
植株收获前,用卷尺测定株高,以茎基部到所有叶片向上伸展最高点的长度表示株高。植株收获后分为根、地上部(茎和叶)和籽粒,分别用自来水冲洗干净,然后用20 mmol/L EDTA-Na2浸泡20 min,最后用去离子水反复冲洗,吸水纸擦干表面水分。籽粒置于烘箱中35 ℃恒温烘干,称干重,脱壳,留糙米。根、地上部分别置于烘箱中105 ℃杀青30 min,65 ℃恒温烘干至恒重,称重。
1.2.2 叶片光合指标
试验进行于水稻灌浆期喷施PGR处理后第2天,用光合作用测定仪(LI-6400xt,美国LI-COR公司)测定水稻完全展开叶的净光合速率、蒸腾速率、胞间CO2浓度和气孔导度。测定时间为9: 00—12: 00。
1.2.3 植物Cd含量
将根部、地上部(茎和叶)和籽粒样品分别粉碎,过100目筛,称取0.300g植物样品装入微波消解管中,加入8 mL优级纯HNO3,于微波消解仪(MARS 6,美国CEM公司)中消解,采用石墨原子吸收法(PinAAcle 900T,美国铂金公司)测定消解液中的Cd含量。
1.2.4 叶片MDA含量
在灌浆期PGR处理后第2天取水稻第一片完全展开叶,每盆的样品分别剪碎混匀,各称取0.5g新鲜叶片,液氮研磨,加入5 mL 0.05 mol/L磷酸缓冲液(pH 7.8),于10000r/min(0—4℃)离心10 min,取上清液按陈建勋等[17]方法测定MDA含量。
1.2.5 数据分析
文中所有数据均为4次重复的平均值,数据的处理采用Excel 2010进行统计,使用SPSS进行方差分析(ANVON)和多重比较(Duncan)。
2 结果分析
2.1 供试PGRs对Cd胁迫下水稻生物量、株高、根冠比的影响
土壤中过量的Cd抑制作物生长[21],降低作物产量[22]。不同PGR对Cd胁迫下水稻生长的影响并不相同(表2)。ABA与ETH均进一步降低了水稻株高和地上部干重,提高了根系干重和根冠比。说明在供试浓度范围内,ABA和ETH均表现出促进根系生长,抑制地上部生长的效应。SA处理后水稻根系和地上部干重增加,根冠比略有提高,但株高随着处理浓度增加呈下降趋势。说明在供试浓度范围内,SA可促进根系和地上部生长,促进水稻植株矮壮。MeJA处理后水稻根系和地上部干重变化不大,根冠比略有增加,但株高随着处理浓度增加呈下降趋势,说明在供试浓度范围内,MeJA对根系生长无影响,但可促使水稻植株变矮。
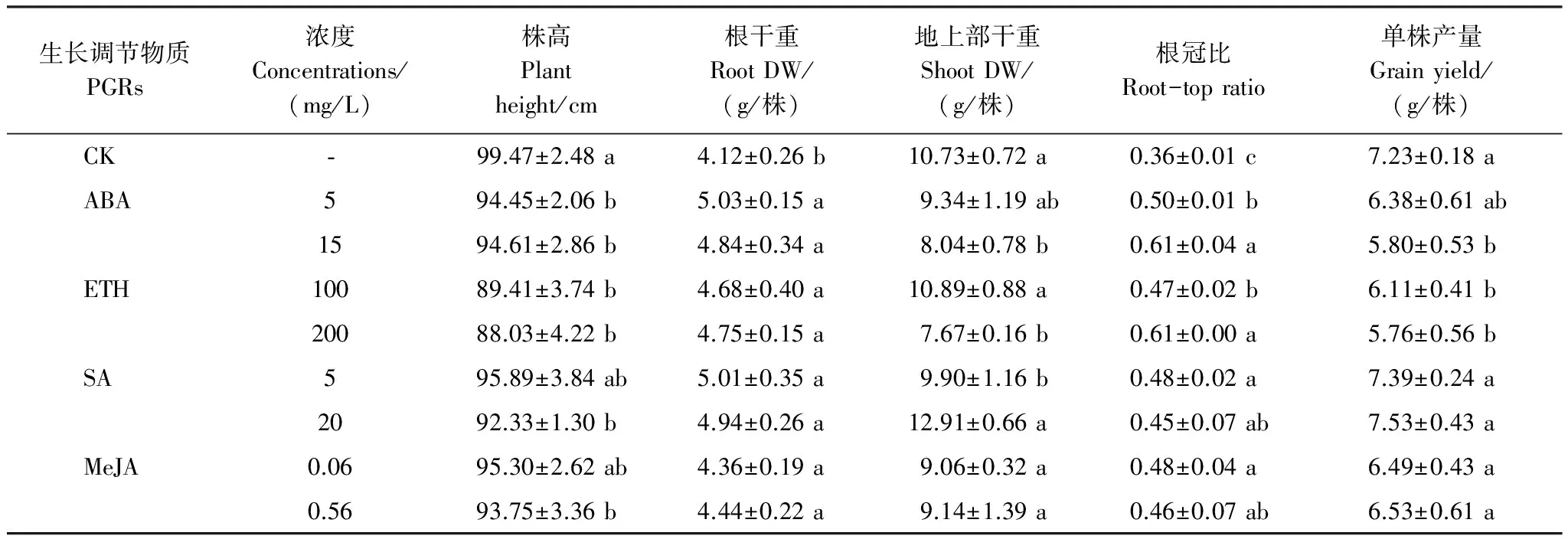
表 2 PGR对Cd胁迫下水稻生长的影响
不同字母表示同一激素不同浓度处理组与对照组相比差异显著(P<0.05);DW: 干重dry weight
2.2 供试PGRs对Cd胁迫下水稻单株产量的影响
产量是评估水稻生长的重要指标。低浓度(5 mg/L)ABA对水稻单株产量无影响,而高浓度(15 mg/L)ABA处理的水稻单株产量比对照下降了19.78%;高浓度(200 mg/L)ETH和低浓度(100 mg/L)ETH均显著抑制了水稻单株产量,分别比对照下降了15.49%和20.33%;供试浓度范围内的SA和MeJA处理对水稻单株产量无影响(表2)。从相关性分析上看(表3),水稻产量与地上部干重呈显著正相关,与根冠比呈显著负相关,与根系干重和株高无显著相关关系。由此推测,抑制地上部生长是ABA和ETH导致水稻产量降低的主要原因。而SA和MeJA对地上部生长无影响,在单株产量上也未表现出抑制效应。
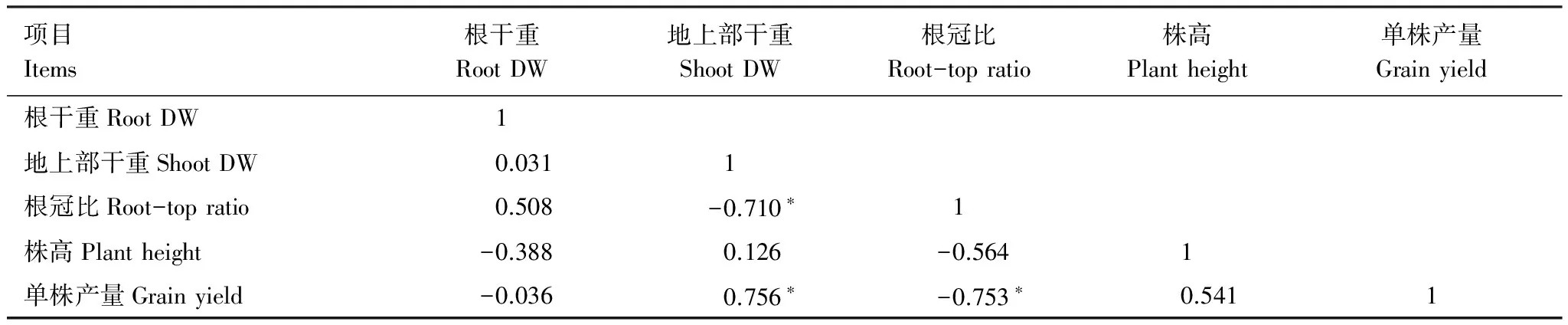
表3 Cd胁迫下水稻生长及产量性状相关性分析
*,**分别表示在0.05、0.01水平(双侧)上显著相关
2.3 供试PGRs对Cd胁迫下叶片光合速率、蒸腾速率、气孔导度和胞间CO2浓度的影响
4种PGR均有降低气孔导度和蒸腾速率的作用(表4),其中MeJA降低气孔导度和蒸腾速率的幅度最大。高浓度(0.56 mg/L)MeJA处理后水稻叶片气孔导度和蒸腾速率分别下降了75.8%和66.9%;高浓度(15 mg/L)ABA处理后水稻叶片气孔导度和蒸腾速率分别下降了44.8%和32.2%。从净光合速率上看,MeJA处理后光合速率的下降幅度最大,其次为ETH,而ABA和SA对光合作用的影响最小。除MeJA处理后的胞间CO2浓度低于对照外,其它3种PGR处理并不影响胞间CO2浓度。MeJA处理组的叶片气孔导度和蒸腾速率下降的同时伴随着胞间CO2浓度的下降,暗示MeJA处理导致气孔导度降低是引起净光合速率下降的主要因素;ABA、SA和ETH处理后水稻气孔导度和蒸腾速率下降的同时并未伴随着胞间CO2浓度的下降,暗示3种PGR引起的净光合速率下降并不仅仅是由于气孔关闭,还可能存在对光合作用暗反应的抑制。
相关分析表明,水稻籽粒Cd含量与光合速率呈极显著正相关(P<0.01),与蒸腾速率无显著相关关系(表5)。
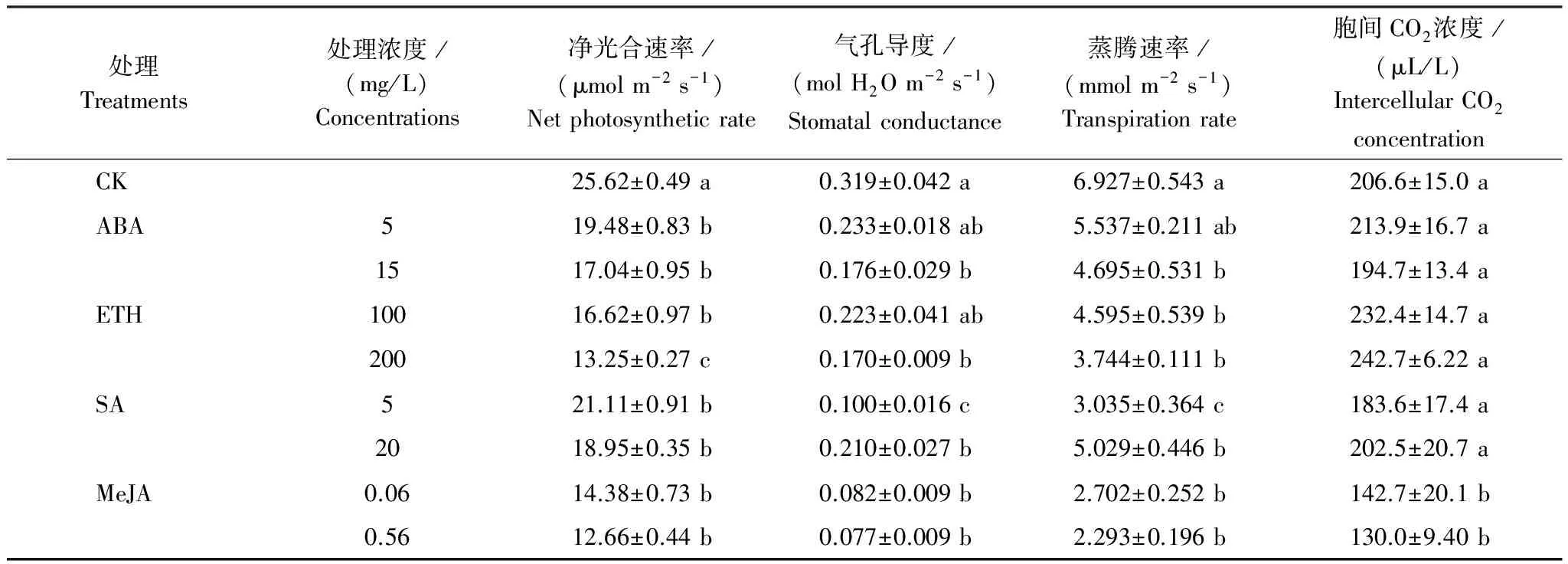
表4 PGR处理对水稻叶片光合作用的影响

表5 Cd胁迫下水稻籽粒Cd含量与叶片光合速率和蒸腾速率相关性分析
2.4 供试PGRs对Cd胁迫下叶片MDA含量的影响
MDA是植物体内膜脂过氧化产物,其含量反映植物遭受逆境伤害的程度[23-24]。从图1可知,低浓度ABA(5 mg/L)处理后MDA含量低于对照,但高浓度ABA(15 mg/L)处理无此效应;高浓度和低浓度的ETH处理后水稻叶片MDA含量均与对照持平;SA和MeJA处理后MDA含量均低于对照。说明供试浓度范围内的SA和MeJA以及低浓度ABA可一定程度地减缓植株受到的Cd伤害;而供试浓度范围内的ETH以及高浓度ABA并未能减少Cd胁迫造成的膜质过氧化损伤。
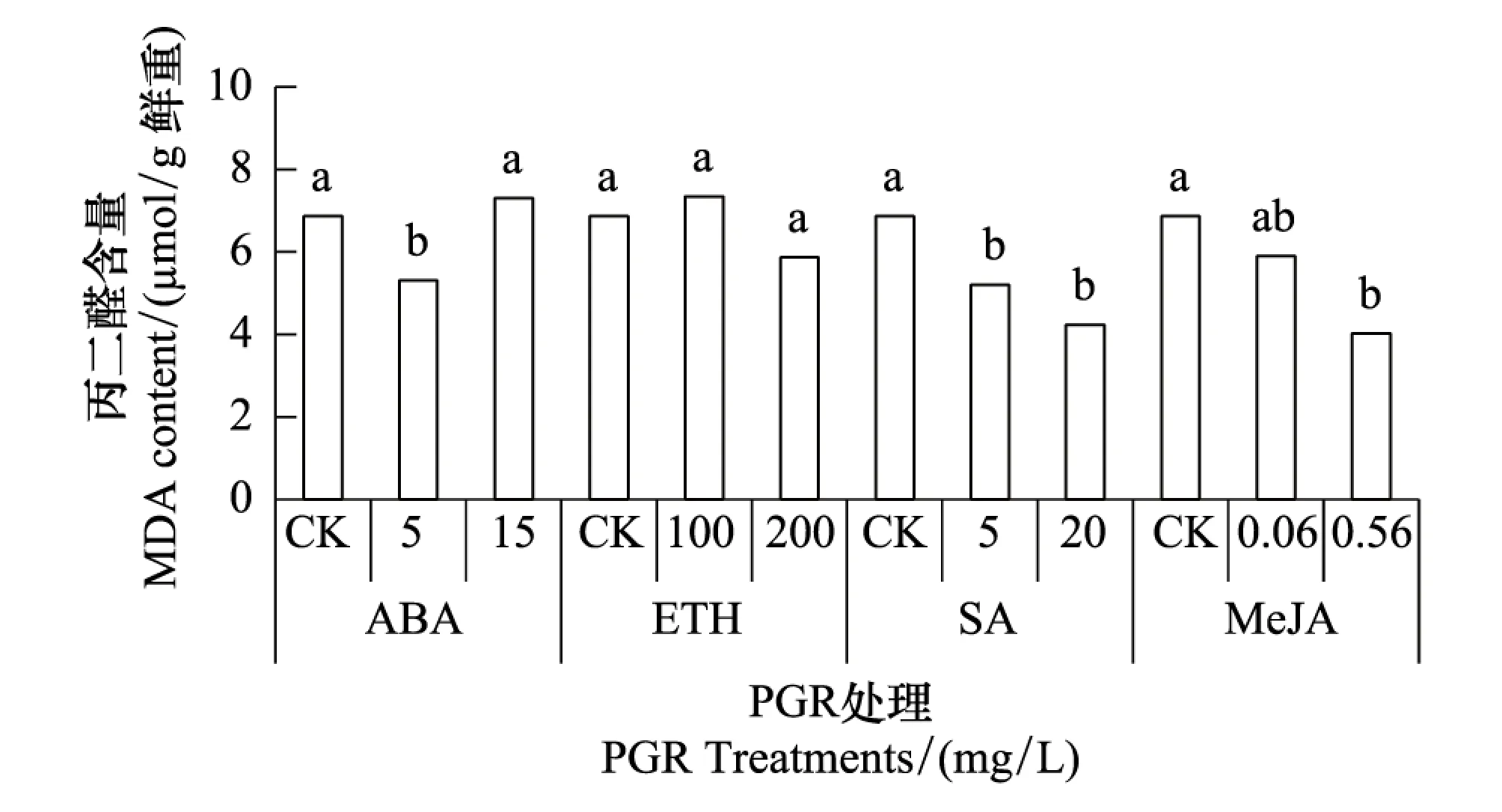
图1 不同PGR处理对Cd胁迫下叶片MDA含量的影响 Fig.1 The effect of different PGRs on MDA concentration in leaves of rice under Cd stress
2.5 供试PGRs对Cd胁迫下水稻籽粒Cd含量以及Cd转运系数的影响
在4种PGR中,仅高浓度(15 mg/L)ABA和高浓度(200 mg/L)ETH处理降低水稻根部Cd含量。与对照相比,ABA对水稻地上部Cd含量无影响,高浓度ETH使水稻地上部Cd含量降低11%,而低浓度SA和MeJA则分别使水稻地上部Cd含量增加18%和23%。籽粒Cd含量是衡量稻米品质的重要指标。从表6可知,4种PGR处理均可降低水稻籽粒Cd含量,其中ABA的抑制效果最明显,5 mg/L 和15 mg/L ABA处理条件下籽粒Cd含量分别比对照降低了37%和21%。100 mg/L ETH、20 mg/L SA和0.56 mg/L MeJA处理后籽粒Cd含量的下降幅度分别为13%、11%和15%。
从表6可知,高浓度ABA、低浓度的ETH、SA以及MeJA均提高了根部向地上部的Cd转运系数,增加程度最大的是高浓度ABA,增加程度为对照的55%。除高浓度ETH外,其余各PGR处理的地上部向籽粒的Cd转运系数均比对照有所降低,其中低浓度ABA下降程度最大,与对照相比下降33%;低浓度ETH下降程度最小,与对照相比下降19%。
相关分析表明,水稻籽粒Cd含量与根部Cd含量及地上部向籽粒转运系数呈显著正相关(P<0.01),水稻籽粒Cd含量与地上部Cd含量及根部向地上部转运系数无显著相关关系。
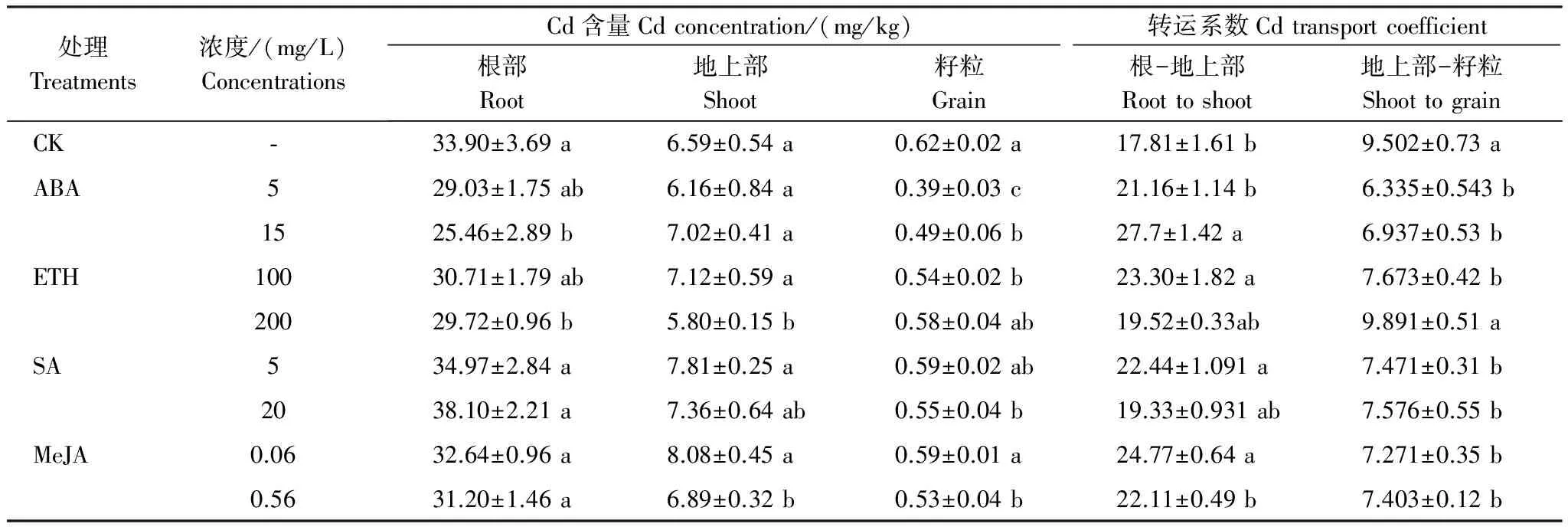
表6 PGR对水稻Cd含量及Cd转运系数的影响
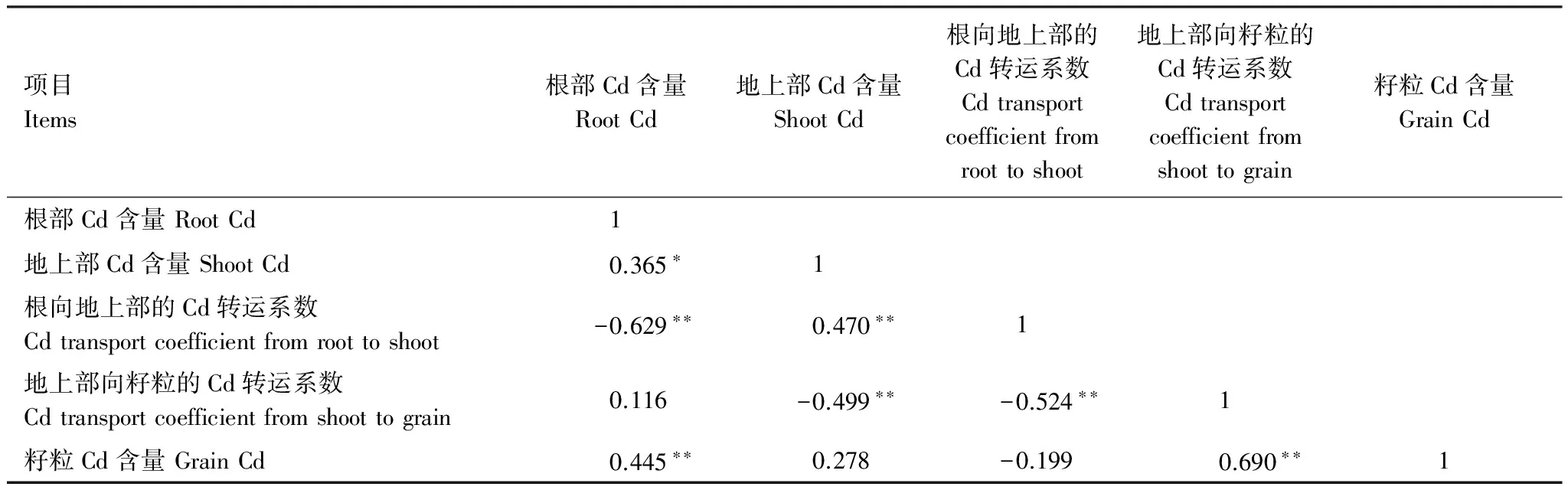
表7 水稻籽粒Cd含量与其他部位Cd含量及转移系数相关性分析
3 讨论
植物体内存在5大类激素:生长素、赤霉素、细胞分裂素、脱落酸和乙烯。此外,还有一些“新发现的植物激素类物质”,如水杨酸(SA)、茉莉酸(MJ)、油菜素内酯(BL)、独角金内酯(SLs)等[25]。脱落酸、水杨酸、茉莉酸和乙烯被认为是植物的主要“胁迫激素”,在植物处于低温胁迫、盐胁迫、渗透胁迫、干旱胁迫、重金属胁迫、病害等逆境时,这些物质在植物体内迅速积累,提高细胞抗氧化水平,保护生物膜和蛋白质,维持一定的光合作用,减少逆境对植物生长的影响[26]。近年来,研究发现外施生长调节物质可促进植物的生长,增强抗氧化能力,提高生物量或作物产量,减少重金属积累[27-29]。这些结果促进了生长调节剂在重金属污染土壤修复实践中的应用。
3.1 供试PGRs对增强水稻抗性,维持正常生长的影响
植物激素在植物应答逆境胁迫中有至关重要的作用,非生物胁迫导致内源激素增加,诱导植物产生抗性,维持正常生长。本试验结果表明,高浓度ABA和ETH导致水稻地上部生长受抑和单株产量降低;而SA和MeJA未表现出抑制效应。研究表明,Cd,Zn 和Al等重金属或有毒元素胁迫可诱导植物体内的ABA水平增加[30-31]。Stroiński[32]推测ABA 参与根细胞中Cd 胁迫信号的转导。乙烯通过调节小麦叶片脯氨酸、谷胱甘肽代谢,从而缓解Cd胁迫引起的脂质过氧化反应[33]。Monteiro[34]认为乙烯信号传导通路的改变可能与细胞内氧化应激的代谢途径有关。Chen[35]等发现外源MeJA通过增加秋茄叶片抗坏血酸含量、过氧化氢酶活性、抗坏血酸过氧化物酶活性从而降低Cd胁迫造成的脂质过氧化损伤。研究表明,外源SA可通过增加细胞膜中的不饱合脂防酸比例[36]、抑制大麦幼苗根系中活性氧的产生[37]或作为抗氧化剂直接参与活性氧的淬灭过程[38],减少Cd胁迫对植物的损伤。本试验结果表明,高浓度ABA(15mg/L)处理的水稻叶片MDA含量高于低浓度ABA(5mg/L)处理,而水稻单株产量低于低浓度ABA处理,说明低ABA处理水平有利于水稻抵御Cd的伤害,而高ABA处理水平则不利于增强水稻抗性。100—200 mg/L乙烯处理并不能缓解Cd胁迫引起的叶片膜质过氧化,最终表现为地上部生物量和产量下降。SA和高浓度MeJA处理均表现为叶片MDA含量比对照降低,说明SA和MeJA处理具有减缓质膜过氧化的作用,在Cd胁迫下维持地上部正常生长,最终表现为产量与对照持平。总之,在Cd胁迫下,15mg/L ABA和100—200 mg/L ETH未能表现出减缓质膜过氧化和维持生长的效应;而5—20 mg/L SA和0.56 mg/L MeJA处理对减少膜质过氧化,维持正常产量有积极的作用,说明4种PGR在诱导水稻对Cd的抗性方面具有不同的调控机制。必须注意的是,合适的施用浓度是PGR能否发挥调节作用、诱导植物抗性增强的重要影响因素。
3.2 供试PGRs对水稻籽粒积累Cd的影响
本试验结果表明, 4种PGR均可在一定程度上减少水稻籽粒对Cd的积累。低浓度ABA对水稻籽粒积累Cd的抑制效应最强。土壤中的Cd需要经过根系吸收、根系向茎部转运、茎部向上运输及茎部木质部向韧皮部的横向转运等过程才能进入籽粒[39]。光合作用为植物生理活动包括Cd的运输和积累直接或间接地提供能量,蒸腾作用被认为是Cd吸收和向上迁移的动力来源[40]。Salt[41]等认为ABA引起的气孔关闭和蒸腾作用下降是抑制Brassicajuncea从根向地上部转运Cd的可能机制。Hsu[17]等认为Cd 胁迫导致水稻内源ABA 增加,而增加的ABA 降低了蒸腾效率使Cd 由根系向地上部的转运下降,最终表现为ABA 降低了水稻地上部对Cd 的积累。钱海胜[42]等发现外源ABA处理降低不结球白菜地上部分Cd含量主要是通过抑制Cd向地上部的运输,这与ABA降低气孔导度、抑制蒸腾速率有着密切的关系。在本试验中,低浓度ABA处理后叶片蒸腾速率与对照持平,但籽粒Cd含量与对照相比明显下降;高浓度ABA处理后叶片蒸腾速率高于低浓度ABA处理组,但籽粒Cd含量低于低浓度ABA处理。Hossain[43]等认为MeJA与ABA均可诱导拟南芥气孔关闭,而且ABA在MeJA的信号转导过程中起重要作用。在本试验中,MeJA处理后叶片蒸腾速率下降程度比ABA处理更大,但其籽粒Cd含量高于ABA处理。相关性分析(表5)结果表明,籽粒Cd含量与叶片光合速率呈极显著正相关关系,与蒸腾作用无显著相关关系,暗示水稻叶片维持一定的光合作用有利于籽粒对Cd的积累,而蒸腾速率并不是PGR调控水稻向上运输Cd的主要影响因素。虽然试验结果无法排除蒸腾速率在ABA或MeJA抑制籽粒积累Cd等方面的积极作用,但暗示该影响效应比较小。
试验结果表明,水稻籽粒Cd含量与根系Cd含量、地上部向籽粒的Cd转运系数均表现为极显著正相关(P<0.01)(表7)。高浓度ABA与ETH处理降低水稻根部Cd含量,而SA与MeJA无此效应(表6)。从地上部向籽粒的Cd转运系数分析,ABA、SA和MeJA在供试浓度范围内均抑制Cd从地上部向籽粒的转运,而ETH仅在低浓度(100 mg/L)条件下表现出相似效应(表6)。因此,ABA处理使籽粒Cd含量下降可能是由于ABA抑制根系吸收和Cd从茎部向籽粒转运的双重影响的结果;100 mg/L ETH,20 mg/L SA和0.56 mg/L MeJA处理使籽粒Cd含量降低可能是由于Cd从地上部向籽粒转运受到抑制的结果。水稻茎节是地上部Cd积累的主要部位,控制水稻体内Cd从本质部向韧皮部转运,以及灌浆期Cd向籽粒的转运[44]。由于在水稻茎节中网络状分布的维管束并不直接相通,因此木质部导管的元素向周围韧皮部的运输不是一个连续的过程,阻碍了元素向叶片和籽粒的迁移。Yu[45]观察到水稻第一茎节中金属硫蛋白基因的转录水平比剑叶高150倍,受Cd、Pb、Al、Cu等金属离子诱导表达,这一结果暗示茎节是水稻茎部向籽粒转运重金属的主要关隘。在本试验中,水稻籽粒Cd含量与地上部向籽粒的Cd转运系数的相关系数达0.690(P<0.01)。与其他3种PGR相比,低浓度ABA处理后地上部向籽粒的Cd转运系数最低,这与“低浓度ABA处理后籽粒Cd含量最低”的结果相一致。由此推测,PGR抑制籽粒对Cd的积累主要与Cd在茎节部位从木质部向韧皮部转运的过程有关,但目前相关的报道较少。PGR如何直接或间接地调控水稻地上部向籽粒运输Cd的过程,需要进一步的研究。
综上所述,供试4种PGR均可在一定程度上减少水稻籽粒对Cd的积累。低浓度ABA对水稻籽粒积累Cd的抑制效应最强,推测其中机制与ABA减缓地上部向籽粒运输Cd有关;低浓度ABA并不降低产量,但高浓度ABA导致水稻减产。供试浓度范围内的ETH处理既减少水稻籽粒中的重金属含量同时也明显降低产量。SA和MeJA虽不影响产量但水稻籽粒中的重金属含量降低程度低于ABA。由于具有施用简单、成本低、环境友好等特点,PGR在中低度重金属污染农田的生态治理实践中应具有一席之地。PGR对时间和剂量的准确性要求较高,不同时间处理、不同剂量水平可能会导致不同的生理效应,这是PGR在实际应用中必须注意的问题。
[1] 崔玉静, 赵中秋, 刘文菊, 陈世宝, 朱永官. 镉在土壤-植物-人体系统中迁移积累及其影响因子. 生态学报, 2003, 23(10): 2133- 2143.
[2] 国家环境保护总局. 中东部地区生态环境现状调查报告. 环境保护, 2003, (8): 3- 8.
[3] He J Y, Zhu C, Ren Y F, Yan Y P, Jiang D A. Genotypic variation in grain cadmium concentration of lowland rice. Journal of Plant Nutrition and Soil Science, 2006, 169(5): 711- 716.
[4] 刘林德, 姚敦义. 植物激素的概念及其新成员. 生物学通报, 2002, 37(8): 18- 20.
[5] 吴耀荣, 谢旗. ABA与植物胁迫抗性. 植物学通报, 2006, 23(5): 511- 518.
[6] 刘红娟, 刘洋, 刘琳. 脱落酸对植物抗逆性影响的研究进展. 生物技术通报, 2008, (6): 7- 9.
[7] 丁义峰, 刘萍. 水杨酸诱导植物抗逆性研究进展. 生物学教学, 2011, 36(11): 2- 4.
[8] 陈珍, 朱诚. 水杨酸在植物抗重金属元素胁迫中的作用. 植物生理学通讯, 2009, 45(5): 497- 502.
[9] 康云艳, 郭世荣, 段九菊. 新型植物激素与蔬菜作物抗逆性关系研究进展. 中国蔬菜, 2007, (5): 39- 42.
[10] 蔡昆争, 董桃杏, 徐涛. 茉莉酸类物质(JAs)的生理特性及其在逆境胁迫中的抗性作用. 生态环境, 2006, 15(2): 397- 404.
[11] Fuhrer J. Ethylene biosynthesis and cadmium toxicity in leaf tissue of beans (PhaseolusvulgarisL.). Plant Physiology, 1982, 70(1): 162- 167.
[12] Zawoznik M S, Groppa M D, Tomaro M L, Benavides M P. Endogenous salicylic acid potentiates cadmium-induced oxidative stress inArabidopsisthaliana. Plant Science, 2007, 173(2): 190- 197.
[13] Jin X, Heng X Y, Xia L. Protective effects of proline against cadmium toxicity in micropropagated hyperaccumulator,SolanumnigrumL.. Plant Cell Reports, 2009, 28(2): 325- 333.
[14] 何俊瑜, 任艳芳, 王阳阳, 李兆君. 不同耐性水稻幼苗根系对镉胁迫的形态及生理响应. 生态学报, 2011, 31(2): 522- 528.
[15] 丁佳红, 薛正莲, 杨超英. 水杨酸对铜胁迫下水稻幼苗膜脂过氧化作用的影响. 黑龙江农业科学, 2013, (1): 14- 18.
[16] Ahmad P, Nabi G, Ashraf M. Cadmium-induced oxidative damage in mustard [Brassicajuncea(L.) Czern. & Coss. ] plants can be alleviated by salicylic acid. South African Journal of Botany, 2011, 77(1): 36- 44.
[17] Hsu Y T, Kao C H. Role of abscisic acid in cadmium tolerance of rice (OryzasativaL.) seedlings. Plant, Cell and Environment, 2003, 26(6): 867- 874.
[18] 文廷刚, 陈昱利, 杜小凤, 吴传万, 钱新民, 吴雪芬, 王伟中. 不同植物生长调节剂对小麦籽粒灌浆特性及粒重的影响. 麦类作物学报, 2014, 34(1): 84- 90.
[19] Mishra A, Choudhuri M A. Effects of salicylic acid on heavy metal-induced membrane deterioration mediated by lipoxygenase in rice. Biologia Plantarum, 1999, 42(3): 409- 415.
[20] Beltrano J, Ronco M G, Montaldi E R, Carbone A. Senescence of flag leaves and ears of wheat hastened by methyl jasmonate. Journal of Plant Growth Regulation, 1998, 17(1): 53- 57.
[21] Ci D W, Jiang D, Dai T B, Jing Q, Cao W X. Effects of cadmium on plant growth and physiological traits in contrast wheat recombinant inbred lines differing in cadmium tolerance. Chemosphere, 2009, 77(11): 1620- 1625.
[22] Wu F D, Zhang G P, Dominy P, Wu H X, Bachir D M L. Differences in yield components and kernel Cd accumulation in response to Cd toxicity in four barley genotypes. Chemosphere, 2007, 70(1): 83- 92.
[23] 吴灵琼, 成水平, 杨立华, 吴振斌. Cd2+和Cu2+对美人蕉的氧化胁迫及抗性机理研究. 农业环境科学学报, 2007, 26(4): 1365- 1369.
[24] 彭艳, 李洋, 杨广笑, 何光源. 铝胁迫对不同小麦SOD、CAT、POD活性和MDA含量的影响. 生物技术, 2006, 16(3): 38- 42.
[25] Bulak P, Walkiewicz A, Brzezińska M. Plant growth regulators-assisted phytoextraction. Biologia Plantarum, 2014, 58(1): 1- 8.
[26] de Vleesschauwer D, Gheysen G, Höfte M. Hormone defense networking in rice: tales from a different world. Trends in Plant Science, 2013, 18(10): 555- 565.
[28] Hadi F, Bano A, Fuller M P. The improved phytoextraction of lead (Pb) and the growth of maize (ZeamaysL.): the role of plant growth regulators (GA3and IAA) and EDTA alone and in combinations. Chemosphere, 2010, 80(4): 457- 462.
[29] Agami R A, Mohamed G F. Exogenous treatment with indole- 3-acetic acid and salicylic acid alleviates cadmium toxicity in wheat seedlings. Ecotoxicology and Environmental Safety, 2013, 94: 164- 171.
[30] Hollenbach B, Schreiber L, Hartung W, Dietz K J. Cadmium leads to stimulated expression of the lipid transfer protein genes in barley: implications for the involvement of lipid transfer proteins in wax assembly. Planta, 1997, 203(1): 9- 19.
[31] Fediuc E, Herman Lips S, Erdei L. O-acetylserine (thiol) lyase activity inPhragmitesandTyphaplants under cadmium and NaCl stress conditions and the involvement of ABA in the stress response. Journal of Plant Physiology, 2005, 162(8): 865- 872.
[33] Khan M I R, Nazir F, Asgher M, Per T S, Khan N A. Selenium and sulfur influence ethylene formation and alleviate cadmium-induced oxidative stress by improving proline and glutathione production in wheat. Journal of Plant Physiology, 2015, 173: 9- 18.
[34] Monteiro C C, Carvalho R F, Gratão P L, Carvalho G, Tiago T, Medici L O, Peres L E P, Azevedo R A. Biochemical responses of the ethylene-insensitive Never ripe tomato mutant subjected to cadmium and sodium stresses. Environmental and Experimental Botany, 2011, 71(2): 306- 320.
[35] Chen J, Yan Z Z, Li X Z. Effect of methyl jasmonate on cadmium uptake and antioxidative capacity inKandeliaobovataseedling under cadmium stress. Ecotoxicology and Environmental Safety, 2014, 104: 349- 356.
[36] Belkadhi A, de Haro A, Obregon S, Chaïbi W, Djebali W. Exogenous salicylic acid protects phospholipids against cadmium stress in flax (LinumusitatissimumL.). Ecotoxicology and Environmental Safety, 2015, 120: 102- 109.
[37] Tamás L, Mistrík I, Alemayehu A, Zelinová V, Bocová B, Huttová J. Salicylic acid alleviates cadmium-induced stress responses through the inhibition of Cd-induced auxin-mediated reactive oxygen species production in barley root tips. Journal of Plant Physiology, 2015, 173: 1- 8.
[38] Popova L P, Maslenkova L T, Yordanova R Y, Ivanova A P, Krantev A P, Szalai G, Janda T. Exogenous treatment with salicylic acid attenuates cadmium toxicity in pea seedlings. Plant Physiology and Biochemistry, 2009, 47(3): 224- 231.
[39] Hart J J, Welch R M, Norvell W A, Sullivan L A, Kochian L V. Characterization of cadmium binding, uptake, and translocation in intact seedlings of bread and durum wheat cultivars. Plant Physiology, 1998, 116(4): 1413- 1420.
[40] Marschner H. Marschner′s Mineral Nutrition of Higher Plants. London: Academic Press, 1986: 674- 674.
[41] Salt D E, Prince R C, Pickering J I, Raskin I. Mechanisms of cadmium mobility and accumulation in Indian mustard. Plant Physiology, 1995, 109(4): 1427- 1433.
[42] 钱海胜, 陈亚华, 王桂萍, 沈振国. 镉在不结球白菜中的积累及外源脱落酸对镉积累的影响. 南京农业大学学报, 2008, 31(4): 61- 65.
[43] Hossain M A, Munemasa S, Uraji M, Nakamura Y, Mori I C, Murata Y. Involvement of endogenous abscisic Acid in methyl jasmonate-induced stomatal closure in Arabidopsis. Plant Physiology, 2011, 156(1): 430- 438.
[44] Fujimaki S, Suzui N, Ishioka N S, Kawachi N, Ito S, Chino M, Nakamura S. Tracing cadmium from culture to spikelet: noninvasive imaging and quantitative characterization of absorption, transport, and accumulation of cadmium in an intact rice plant. Plant Physiology, 2010, 152(4): 1796- 1806.
[45] Yu L H, Umeda M, Liu J Y, Zhao N M, Uchimiya H. A novel MT gene of rice plants is strongly expressed in the node portion of the stem. Gene, 1998, 206(1): 29- 35.
Effects of four plant growth regulators on growth and cadmium accumulation in rice
HE Bing, CHEN Xiaoqin, XIN Zibing, LU Qinyu, SHI Qiao, GU Minghua*, WANG Xueli
CollegeofAgriculture,GuangxiUniversity,Nanning530005,China
Cadmium (Cd) pollution has become a serious problem following rapid industrial development. The increasing amounts of Cd in farmlands are the result of increased discharge of industrial waste, abuse of chemical fertilizers, and other man-made sources. Cd likely causes damage to crop physiology when its concentration in soil exceeds the maximum tolerable limit, resulting in growth inhibition and grain yield reduction. Continuous intake of Cd causes human health problems. Therefore, reducing Cd concentration in rice grain, a staple food for half of the world′s population, is extremely important and urgent. Plant growth regulators (PGRs) are chemicals—plant endogenous hormones and artificially synthetic growth regulators—that affect and regulate plant growth and/or development at trace levels. Some PGRs play important roles in inducing plant tolerance to drought, salt, low temperature, high temperature, and heavy metals. In this study, the roles of four PGRs, abscisic acid (ABA), ethylene (ETH), salicylic acid (SA), and methyl jasmonate (MeJA), were investigated during stress responses to Cd treatments in rice. Rice seedlings, grown in heavy metal-contaminated soil, were sprayed with the four PGRs on leaves twice, one time each during tillering and filling stages. On the second day after the PGR treatments during the filling stage, the photosynthesis indices and malondialdehyde (MDA) contents of the upper leaves were analyzed. After harvesting, the roots, shoots, and grains were collected to investigate Cd content, biomass, and yield. The results were as follows: (1) The ABA treatment at 5 mg/L maintained normal rice growth and yield, while the ABA treatment at 15 mg/L showed the opposite effects. Treatment with two different levels of ETH significantly decreased the grain yield compared to that of the control. However, SA and MeJA high-level treatments maintained normal yields. (2) The exogenous application of the four PGRs inhibited stomatal opening and reduced the transpiration and photosynthetic rates. Interestingly, the most obvious inhibitory action was observed following the treatment with 0.56 mg/L MeJA. (3) Both the SA treatments, 5 mg/L ABA and 0.56 mg/L MeJA treatments, reduced MDA production and prevented plasma membrane peroxidation of leaves at the tillering stage. (4) Decreases in the Cd concentrations were observed in rice grain treated with the four PGRs at their appropriate levels, and the ABA treatment at 5 mg/L showed the strongest inhibitory effect. The grain Cd content showed positive and highly significant (P<0.01) correlation with the Cd translocation factor from shoot to grain, but it did not show a significant correlation with the transpiration rate. PGRs may inhibit the accumulation of Cd in the grain by regulating Cd transport from shoots to grain. (5) In summary, ABA treatment at 5 mg/L had no effect on grain yield but induced the maximum decline in grain Cd content compared to the treatments with other PGRs. Proper application of PGRs can reduce the Cd content in rice grain and can be used in bioremediation of heavy metal polluted farmland. For a practical application of PGRs, appropriate timing, and accurate concentrations are the critical factors to avoid negative effects of inhibited growth and reduced rice yields.
rice; Cd; plant growth regulator
农业部专项资助项目(2014- 2016);广西土壤污染与生态修复人才小高地项目;国家自然科学基金金资助项目(31560122)
2015- 04- 27;
日期:2016- 03- 03
10.5846/stxb201504270861
*通讯作者Corresponding author.E-mail: gumh@gxu.edu.cn
何冰,陈小勤,辛子兵,陆覃昱,石桥,顾明华,王学礼.不同生长调节物质对水稻生长及镉积累的影响.生态学报,2016,36(21):6863- 6871.
He B, Chen X Q, Xin Z B, Lu Q Y, Shi Q, Gu M H, Wang X L.Effects of four plant growth regulators on growth and cadmium accumulation in rice.Acta Ecologica Sinica,2016,36(21):6863- 6871.

