伊立替康联合洛铂二线治疗广泛期小细胞肺癌46例临床观察
王儒柳,阮新建,贾 佳,王 飞,刘慧龙,刘彦芳,王 莉
(1.人民日报社门诊部,北京 100733; 2.中国人民解放军北京军区总医院肿瘤科,北京 100700)
伊立替康联合洛铂二线治疗广泛期小细胞肺癌46例临床观察
王儒柳1,阮新建2,贾 佳2,王 飞2,刘慧龙2,刘彦芳2,王 莉2
(1.人民日报社门诊部,北京 100733; 2.中国人民解放军北京军区总医院肿瘤科,北京 100700)
目的 观察伊立替康联合洛铂二线治疗广泛期小细胞肺癌(SCLC)的疗效和毒副反应。方法 选取SCLC患者46例,予伊立替康200 mg/m2加入0.9%氯化钠注射液250 mL中,稀释后静脉滴注1.5 h,第1天;洛泊30 mg/m2加入5%葡萄糖注射液500 mL中,稀释后静脉滴注2 h,第1天;每21 d为1个周期,2个周期后评价疗效和不良反应发生情况。结果 46例均可评价疗效,完全缓解1例,部分缓解15例,疾病稳定19例,疾病进展11例,客观缓解率为34.78%,疾病控制率为76.09%,中位无进展生存期为4.6个月,中位生存期为7.8个月。不良反应主要为血液学毒性和消化道反应。结论 伊立替康联合洛铂方案用于治疗广泛期SCLC疗效较好,但毒副反应较大,值得临床进一步研究。
伊立替康;洛铂;小细胞肺癌;毒副反应
肺癌是严重危害人类健康与生命的最常见的恶性肿瘤,已成为全世界肿瘤死亡的主要原因。小细胞肺癌(SCLC)是一种高度侵袭性的恶性肿瘤,生长迅速,倍增时间短,早期易出现远处广泛转移,约占肺癌总数的15% ~20%[1]。SCLC对化学治疗(简称化疗)、放射治疗(简称放疗)高度敏感,临床依托泊苷(VP-16)联合顺铂(DDP)或卡铂(CBP)的化疗方案是目前公认的一线标准化疗方案[2],有效率为60%~80%。但大部分患者会在数月内出现肿瘤复发、疾病进展,并产生耐药,目前尚无标准的二线化疗方案。为探寻有效的二线化疗方案,我院对46例一线使用VP-16联合DDP或CBP化疗方案治疗后6个月内复发进展的SCLC患者,予二线伊立替康(CPT-11)联合洛铂(LBP)方案治疗,现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:均经细胞学或病理诊断为SCLC;按照美国退伍军人肺癌协会小细胞肺癌分期分为广泛期;根据实体瘤评价标准(RESIST)至少有1个可测量的病灶;KPS评分大于60分;预计生存时间超过3个月;入组前曾接受过一线VP-16联合DDP或CBP方案化疗,化疗结束6个月内出现肿瘤复发或转移;治疗前血常规、肝功能、肾功能、心功能均正常,无重要器官病变;均无明显化疗禁忌,具有依从性和可随访性。
病例选取:选择2012年6月至2014年12月46例患者,其中男25例,女21例;平均年龄48.5岁;KPS 60分6例,70分22例,80分15例,90分3例;3个月内复发17例,3~6个月内复发29例。
1.2 方法
CPT-11200mg/m2加入0.9%氯化钠注射液250mL中,稀释后静脉滴注1.5 h,第1天给药;LBP 30 mg/m2加入5%葡萄糖注射液500 mL中稀释后静脉滴注2 h,第1天给药,每21 d为1个周期。所有患者化疗前常规应用5-羟色胺3(5-HT3)受体拮抗剂止吐;每周至少监测1次血常规及血生化,了解骨髓抑制以及肝、肾功能变化等情况,以便及时对症处理:若白细胞低于3×109/L时给予重组人粒细胞集落刺激因子(G-CSF)防止粒缺性感染发热,若血小板低于30×109/L,可考虑输注血小板防止出血倾向。严密观察消化道反应,尤其是发生迟发性腹泻时,应积极使用盐酸洛哌丁胺止泻及补液等处理,防治水电解质紊乱。
1.3 疗效判定指标
根据RESIST标准对肿瘤客观疗效进行评价,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。客观缓解率(ORR)为CR+PR患者占全组患者的百分率。疾病控制率(DCR)为CR+PR+SD患者占全组患者的百分率。无进展生存期(PFS)为自首次治疗开始至疾病进展或末次随访,总生存期(overall survival,OS)为患者首次用药到任何原因死亡的时间。患者治疗前及每化疗2个周期后行影像学CT检查评价疗效,获CR或PR应于4周后进行疗效确认。
不良反应评价标准按照美国国立癌症研究所(NCI)制订的不良反应评价标准(CTCAE第 3版)分0~4级评定,完成1个周期即可进行评价。
2 结果
2.1 临床疗效
所有患者均完成2个周期以上化疗,平均完成3.8个疗程,均可以评价近期疗效。其中CR 1例(2.17%),PR 15例(32.61%),SD19例(41.30%),PD11例(23.91%);ORR 16例(34.78%);DCR 35例(76.09%),中位PFS为4.6个月,中位OS为7.8个月。
2.2 不良反应发生情况
主要不良反应为血液学毒性和消化道反应。血液学毒性发生率高76.09%(35/46),且较严重,其中3~4级白细胞减少发生率为47.83%(22/46),3~4级血红蛋白减少发生率为32.61%(15/46),3~4级血小板减少发生率45.65%(21/46);消化道反应发生率高65.52%(30/46)但多较轻,最常见消化道反应为腹泻发生率为32.61%(15/46),其中3~4级腹泻为13.04%(6/46),3~4级恶心 4.35%(2/46);其他如口腔炎发生率15.22%(7/46),肝脏毒性发生率8.70% (4/46),均为1~2级。全组无毒性相关死亡病例。详见表1。
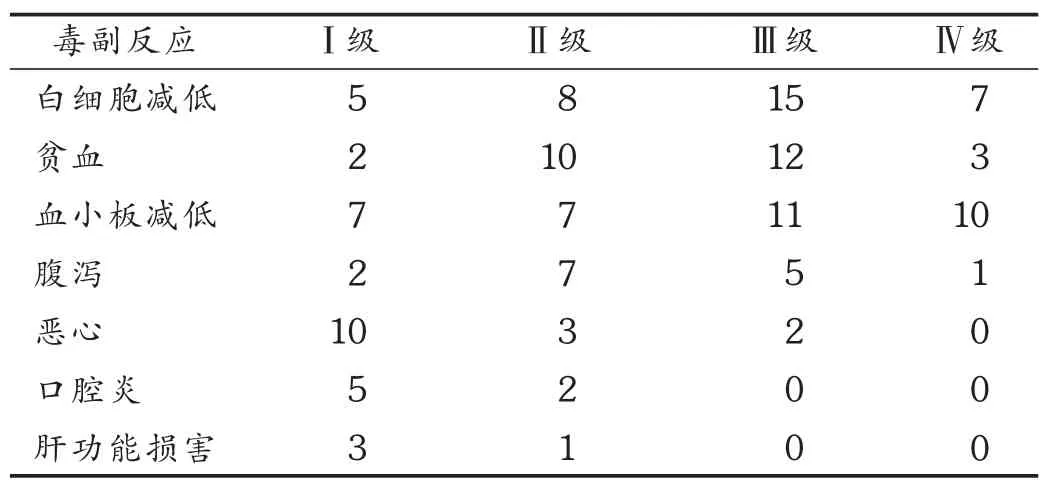
表1 CPT-11联合LBP治疗复发性SCLC的毒副反应(例)
3 讨论
SCLC恶性程度高,侵袭性强,生长迅速,转移早,预后较差[3]。尽管初治时SCLC对化疗敏感性较高,但缓解期短,多在化疗停止后3个月左右出现复发转移,且二线治疗疗效差。此时大多数患者体质弱、耐受性低,依从性差,更易出现毒副反应如骨髓抑制、感染、脏器功能损害等,二线化疗药物选择一定要谨慎并切合实际。临床上迫切需要新的有效药物来提高患者生活质量、延长无病生存期。
CPT-11是喜树碱的衍生物,为DNA拓扑异构酶Ⅰ抑制剂,其与TopoⅠ-DNA形成的复合物结合,稳定此复合物,从而使断裂的DNA单链不能重新接合,阻止DNA复制及抑制RNA合成,为细胞周期S期特异性药物[4]。CPT-11的抗瘤活性强,对SCLC有较高疗效,对初治患者单药有效率可达50%,对既往接受过化疗患者单药有效率可达41%。CPT-11的毒副反应主要为骨髓抑制和腹泻,其中腹泻又分为早期腹泻和迟发型腹泻,早期腹泻由乙酰胆碱能综合征引起,属于一过性反应,偶尔发生,可通过阿托品预防和治疗。而迟发型腹泻一般发生在用药后第5~8天,可用盐酸洛哌丁胺口服进行治疗[5]。有研究表明[6],伊立替康的迟发型腹泻反应程度可能与UGT1A1有关。
铂类药物是肺癌化疗基础用药之一。洛铂是第3代铂类抗癌药,化学结构为1,2-二氨基-环丁烷-乳酸合铂,具有抗癌活性强、毒性轻、起效快、持续时间长和肿瘤组织中浓度高而血浆中浓度低的特点。与第1代的DDP和第2代的 CBP的抑瘤作用相似,通过形成Pt-GG与Pt-AG链内交叉连接,阻碍DNA的复制与转录过程,从而干扰肿瘤细胞周期运行,对多种肿瘤均有广谱抗癌活性,对耐DDP的细胞株仍有一定的细胞毒性作用。与顺铂、卡铂之间无交叉耐药。其主要毒副作用为骨髓毒性,特别是血小板减少,为剂量限制性毒性,其他常见的不良反应为胃肠道反应、肾毒性等,但不明显,总体说来较顺铂、卡铂安全性好[7]。LBP在化学结构、理化性质、药效学和药动学等方面具有诸多鲜明特性,并由此构成高效、低毒、不交叉耐药之优势,且逐渐在临床应用中得以显现[8]。
伍志新等[9]对伊立替康联合洛铂治疗复发性广泛期SCLC的临床研究中发现:ORR为38.9%,DCR为69.4%,中位PFS为4.6个月,中位OS为7.8个月。毒副反应主要为血液学毒性和消化道毒性,3~4级白细胞减少、血红蛋白减少和血小板减少,发生率分别为41.7%,50.0%,72.2%;腹泻发生率为69.4%,其中3~4级腹泻为13.9%。蒋侃等[10]对CPT-11联合LBP治疗复发性广泛期SCLC临床观察,ORR为35%,DCR为65%,中位PFS 4.2个月,中位OS 7.9个月,主要毒副反应为血液学毒性、恶心呕吐及腹泻。其中3~4级白细胞下降为40%,3~4级血小板下降为10%;腹泻发生率为35%为1~2级,恶心发生率50%,呕吐发生率30%,无3~4级恶心、呕吐;全组无毒性相关死亡。本研究组46例晚期复发小细胞肺癌患者,经过至少2个周期的CPT-11联合LBP方案化疗,ORR为34.78%,DCR为73.91%,中位PFS为4.6个月,中位OS为7.8个月。疗效与国内学者研究相似,进一步证明CPT-11联合洛铂作为二线治疗复发性SCLC的有效性,为一线治疗失败的患者提供了新的选择。其主要毒副反应为血液学毒性和消化道反应,其中3~4级白细胞减少、血红蛋白减少、血小板减少,发生率分别为47.83%,32.61%,45.65% 。本研究组患者血液学毒性发生率高且重,可能与患者一般情况欠佳、多周期化疗及放疗后骨髓功能差等因素有关,也可能与入组样本量小有关。虽然严重的3~4级骨髓抑制经过积极对症处理后大多缓解,但因迟滞了化疗计划的有序进行,延长住院时间,增加了医疗费用。其中有3例PR患者,出现4度骨髓抑制,给予积极成分输血、使用G-CSF等药物处理,白细胞低、血小板低仍迟迟不能纠正,不能继续治疗,终因疾病进展而死亡。出于对患者安全性与耐受性的考虑,国内临床医师对伊立替康、洛铂的使用时间及剂量,目前还缺乏标准方案。本研究再次证实伊立替康联合洛铂二线治疗广泛期小细胞肺癌的临床价值,也应高度重视不良反应发生情况。
综上所述,CPT-11联合LBP作为复发的广泛期SCLC的二线治疗方案,具有较好的疗效和安全性,但还需要进一步扩大临床研究,寻找最适合我国肿瘤患者的最佳剂量及用药方式,在获得最好临床疗效的同时,最大限度减少化疗药物不良反应的发生。
[1]程 颖,柳 影.小细胞肺癌治疗的新探索[J].临床肿瘤学杂志,2011,16(1):1-8.
[2]Schmittel A.Second-line therapy for small-cell lung cancer[J]. Expert Rev Anticancer Ther,2011,11(4):631-637.
[3]刘晓晴,郭万峰.小细胞肺癌多学科综合治疗进展[M]//中国临床肿瘤学进展2014.北京:人民卫生出版社,2014:65.
[4]Hahn KK,Wolff JJ,Kolesar JM.Pharmacogenetics and irinotecan therapy[J].Am J Health Syst Pharm,2006,63(22):2 211-2 217.
[5]张容榕,林 琳,刘爱学,等.两种方案治疗广泛期小细胞肺癌的临床观察[J].肿瘤预防与治疗,2014,27(3):130-133.
[6]侯宝元,张晓虹.UGT1A1基因多态性与伊立替康不良反应的相关性[J].武汉大学学报:医学版,2014,35(6):941-944.
[7]Yu Peng,Jiangkui Liu,Qiang Lin,et al.Clinical progression of lobaplatin in combination chemotherapy for patients with recurrence or metastatic cancer[J].The Chinese-German Journal of Clinical Oncology,2014,13(8):386-391.
[8]梁宇峰,隋东虎,程 颖,等.一类抗肿瘤新药洛铂治疗小细胞肺癌临床研究进展[J].中国新药杂志,2014,23(2):184-188.
[9]伍志新,陈立军,宋文军,等.伊立替康联合洛铂治疗复发性广泛期小细胞肺癌(SCLC)的临床研究[J].现代肿瘤医学,2014,22(6):1 344-1 346.
[10]蒋 侃,黄 诚,吴 标,等.伊立替康联合洛铂治疗复发广泛期小细胞肺癌临床观察[J].中国实用医药,2011,6(18):1-2.
Second-line Treatment of Irinotecan Combined with Lobaplatin for Extensive Stage Small Cell Lung Cancer in 46 Cases
Wang Ruliu1,Ruan Xinjian2,Jia Jia2,Wang Fei2,Liu Huilong2,Liu Yanfang2,Wang Li2(1.The Out-patient Department of People′s Daily Agent,Beijing,China 100733; 2.Department of Oncology,PLA General Hospital of Beijing Military
Area Command,Beijing,China 100700)
Objective To observe the efficacy and toxicity of second-line treatment of irinotecan combined with lobaplatin for extensive small cell lung cancer(SCLC).M ethods 46 cases of SCLC patients were selected and given irinotecan 200 mg/m2into the normal saline 250 mL,diluted and then intravenous dripped for 1.5 h on the first day;lobaplatin 30 mg/m2into 5% glucose 500 mL,diluted and then intravenous dripped for 2 h on the first day.21 d was 1 cycle.After two cycles of treatment,the efficacy and adverse reactions were evaluated.Results 46 cases could be evaluated.There were 1 case of complete remission(CR),15 cases of partial remission(PR),19 cases of stable disease(SD),11 cases of progressive disease(PD);the objective response rate(ORR)was 34.78%,the disease control rate(DCR)was 76.09%;the median progression-free survival(PFS)was 4.6 months,and the median survival(OS)was7.8 months.Adverse reactionswere hematologic toxicity and gastrointestinalreactions.Conclusion Irinotecan combined with lobaplatin program for the treatment of relapsed SCLC has a good effect but also larger toxicity,which is worthy of further study.
irinotecan;lobaplatin;small cell lung cancer(SCLC);toxicity
2016-05-18;
2016-07-09)
R969.4;R979.1
A
1006-4931(2016)19-0095-03

