氢氧化钠溶液中硫化钠对Q235钢的腐蚀行为研究∗
杨夏琼,陈朝轶∗,李军旗,赵 聪,刘 龙,魏国令
(1.贵州大学材料与冶金学院,贵州贵阳550025;2.贵州省冶金工程与过程节能重点实验室,贵州贵阳550025)
氢氧化钠溶液中硫化钠对Q235钢的腐蚀行为研究∗
杨夏琼1,2,陈朝轶1,2∗,李军旗1,2,赵 聪1,2,刘 龙1,2,魏国令1,2
(1.贵州大学材料与冶金学院,贵州贵阳550025;2.贵州省冶金工程与过程节能重点实验室,贵州贵阳550025)
通过盐雾腐蚀实验和电化学腐蚀实验,借助腐蚀失重法、宏观形貌分析、SEM、EDS和EIS等分析方法,研究了Q235钢在不同S2-浓度的氢氧化钠溶液中的腐蚀行为。研究结果表明: S2-浓度的变化对Q235钢的腐蚀行为有着显著的影响,宏观及微观形貌分析均表明随着S2-浓度的升高试样的腐蚀越来越严重;EDS分析表明腐蚀产物主要由Fe、S、O三种元素组成,S2-浓度为4g/L时腐蚀程度较轻故Fe含量很高,S2-浓度为5 g/L时,Fe的氧化反应导致O含量升高,S2-浓度为6 g/L时,Fe的硫化反应为主要反应,导致S含量明显升高而O含量有所下降;当S2-浓度从3 g/L增至6 g/L时,由于S2-与Fe发生反应使得腐蚀失重从2.8732 g/m2增大至3.4451 g/ m2,腐蚀电流密度从0.931μA/cm2逐渐上升至5.092μA/cm2,而当S2-浓度为7 g/L时由于生成了较致密的FeS膜覆盖在试样表面使得腐蚀失重和腐蚀电流密度均有所下降。
氢氧化钠;硫化钠;Q235钢;腐蚀行为;极化曲线
我国高品位铝土矿资源的日渐短缺,使得氧化铝生产行业越来越广泛地使用高硫铝土矿[1-3]生产氧化铝。高硫铝土矿中的硫在拜耳溶出过程中主要以和少量的形态转入铝酸钠溶液,进而对设备材质造成严重腐蚀。目前关于硫腐蚀的研究多集中在石油化工[4-6]和纸浆及造纸工业领域[7-9]。 而近年来硫的碱性腐蚀研究多集中在硫化钠及其在纯氢氧化钠溶液中对钢材等的腐蚀。Hazlewood等[8-9]探究了Na2S及NaOH与低碳钢腐蚀速率之间的关系,研究发现在氢氧化钠浓度恒定时,升高Na2S的浓度会导致碳钢腐蚀速率变大。还有研究表明S2-对金属腐蚀具有促进作用,因为阻碍了具有保护性的钝化膜的形成而加速了腐蚀。然而曹华珍等[10]认为高活度的 OH-或S2-有利于钢表面氧化膜及硫化膜的生成,使钢的基体得到保护进而降低了其腐蚀电流。也有研究[11]表明 Na2S溶液中大量存在的 S2-会与Fe2+反应在碳钢表面生成FeS,该层致密的 FeS膜会起到抑制腐蚀的作用,且FeS膜的致密程度也会随Na2S浓度的升高而增强。郝文魁[12]认为碱性溶液中硫化物的存在会导致碳钢表面形成钝化膜进而促进碳钢的钝化并减缓其腐蚀,而该钝化膜的耐蚀性能则取决于其厚度及成分。但还有研究认为 S2-浓度较低时会对腐蚀产生抑制,而随着 S2-浓度的升高,腐蚀速率又逐渐变大。这是因为S2-与OH-会在Fe的表面发生竞相吸附,当S2-浓度较低时OH-会占据Fe的表面并生成致密的钝化膜,从而起到抑制腐蚀的作用。
Q235钢为氧化铝生产设备的主要用钢,研究氢氧化钠溶液中硫化钠对Q235钢的腐蚀行为的影响能够为进一步研究生产过程中氧化铝设备的硫腐蚀提供重要依据。因此本文借助盐雾腐蚀实验和电化学腐蚀实验研究了Q235钢在含不同浓度Na2S的NaOH溶液中的腐蚀行为。
1 实验方法
1.1 实验材料与溶液
实验用材料为氧化铝生产工艺流程中罐体材料所用的Q235钢,其宏观形貌如图1所示。其化学成分如表1所示。

图1 Q235钢的宏观形貌

表1 Q235钢的化学成分(w t%)
实验用的氢氧化钠溶液是通过分析纯NaOH试剂溶于蒸馏水配制而成,然后将分析纯Na2S· 9H2O溶于已配制的氢氧化钠溶液中获得含不同浓度硫化钠的氢氧化钠溶液。
1.2 盐雾腐蚀实验
将Q235钢材切割成尺寸为15 mm×15 mm× 2.5 mm的试样,用180、240、360、600、800目砂纸逐级打磨试样使其表面光滑平整,酒精脱脂,蒸馏水冲洗,冷风吹干后放入干燥皿内待用,实验前取出试样用游标卡尺测量其尺寸并计算出其表面积,用电子天平称量其重量,精确到小数点后四位。将试样放置于YWX/Q-250盐雾腐蚀箱中进行腐蚀失重实验,该实验模拟的是氧化铝生产中的晶种分解环节,故实验温度设定为50℃,采用试样挂片、连续喷雾的方式分5组进行。腐蚀溶液为S2-浓度分别为3 g/L、4 g/L、5 g/L、6 g/L、7 g/L的NaOH溶液,氢氧化钠的质量浓度为115 g/L,腐蚀时间均为120 h。
实验结束后,按GBT1645-1996标准对腐蚀试样进行清洗[13-14],清除完腐蚀产物后用无水乙醇清洗,吹干后称重。最后计算出其腐蚀速率,计算公式为:

式中:W0、W1分别为腐蚀前、后试样质量,A为试样表面积,t为腐蚀时间。
1.3 电化学腐蚀实验
采用VSP多通道电化学工作站进行电化学腐蚀实验,实验温度控制为50℃,采用传统的三电极体系,铂电极为辅助电极,饱和甘汞电极(SCE)为参比电极,所测试样为工作电极[15-16],工作电极由切割好的Q235钢试样制备而成,形状为柱形,工作面积为2.25 cm2,非工作部分用环氧树脂进行密封。首先对不同实验条件下的工作电极进行动电位极化曲线扫描,扫描速度2 mv/s,扫描电压范围为-1.2~-0.2 V。研究中的所有电极电位均为相对于饱和甘汞电极电位。
2 结果与讨论
2.1 宏观形貌分析
Q235钢材在含不同S2-浓度的NaOH溶液中经过120 h盐雾腐蚀后的宏观形貌如图2所示。

图2 Q235钢在不同S2-浓度的NaOH溶液中腐蚀120 h后的宏观形貌图(a)3g/L (b)4g/L (c)5g/L (d)6g/L (e)7g/L
从图中可以看出,当S2-浓度为3 g/L时,Q235钢试样表面经120 h腐蚀后仅个别位置出现轻微的点蚀,而其余位置并无明显的腐蚀迹象,试样表面较为完好;当S2-浓度为4 g/L时,试样表面点蚀坑的数量明显增多,且比较均衡地分布在基体表面,点蚀位置较为分散,出现这种现象的原因是随着S2-浓度上升,S2-外扩散加剧,S2-与基体接触机会增大,发生腐蚀反应概率增大;当S2-浓度为5 g/ L时,基体表面出现区域性黄色斑块,局部腐蚀严重,腐蚀产物堆积在基体的表面,整体腐蚀呈严重趋势;当S2-为6 g/L时,明显可见Q235钢试样表面整体呈现为黄褐色即发生了较为全面的腐蚀,大量产物堆积在基体表面,点蚀坑变多且部分坑变深,整体呈现不平整,这种现象由于S2-浓度增大,S2-不断浸入基体内核发生腐蚀反应,产生大量的腐蚀产物堆积在基体表面,该产物为硫铁化合物呈现黄色;当S2-浓度上升到7 g/L时,试样表面腐蚀产物颜色进一步加深,腐蚀坑的数量也呈现出上升趋势,且出现了腐蚀沟槽,在腐蚀沟槽的两边有腐蚀产物堆积。通过上述宏观形貌图的对比可以发现,随着S2-浓度的上升,Q235钢的腐蚀程度不断加剧。
2.2 微观形貌及能谱分析
经过120 h的盐雾腐蚀后Q235钢试样表面的微观形貌及能谱如图3所示。

图3 Q 235钢在不同S2-浓度的NaOH溶液中腐蚀120 h后的SEM和EDS图(a)4g/L (b)5g/L (c)6g/L
从图3中可以看出,腐蚀形态以点蚀为主,局部区域存在少许均匀腐蚀,随着S2-浓度逐渐增大,点蚀坑数量逐渐增多,腐蚀坑加深,均匀腐蚀区域逐渐扩大,腐蚀产物不断增多,总体上腐蚀呈现出加剧的趋势。当S2-浓度为4 g/L时,基体表面呈现出许多点蚀坑并散落在基体各部分,但是点蚀程度较轻,个别位置有白色的腐蚀沟槽,有少许腐蚀产物堆积在腐蚀沟槽两侧;当S2-浓度为5 g/L时,点蚀坑数量明显增多,点蚀坑周围腐蚀产物的量也增多,材料表面腐蚀沟槽增多,分布于腐蚀沟槽周围的腐蚀产物明显增多,试样的腐蚀程度加剧;当S2-浓度为6 g/L时,Q235钢材试样表面腐蚀产物呈颗粒状,密集分布于试样表面,腐蚀产物层变厚,点蚀坑颜色变黑,由于S2-浓度提升,S2-与Fe发生腐蚀反应,产生大量疏松的硫铁化合物附着在基体表面,导致腐蚀产物脱落,点蚀坑深度相应的加深。

表2 Q 235钢在不同S2-浓度的NaOH溶液中腐蚀120 h后点蚀区域EDS分析结果(原子个数百分比)
腐蚀区域能谱分析结果如表2所示,腐蚀产物主要含有O、S、Fe,以及少量的Na。随着S2-浓度的升高,氧元素的原子个数百分比先上升后降低,硫元素的原子个数百分比不断上升,铁元素的原子个数百分比不断下降,说明腐蚀产物主要为铁的硫化物和铁的氧化物。S2-浓度为4 g/L时,铁与硫、氧发生腐蚀反应程度低,所以腐蚀产物主要由铁元素组成,氧元素和硫元素的含量相对较低;当S2-浓度上升为5 g/L时,腐蚀产物中硫和氧的含量相应升高,但是氧上升的幅度较硫大,此时铁的氧化物含量较硫化物高,结合微观形貌图可以看出腐蚀产物较致密;当S2-浓度上升到6 g/L时,硫化物含量继续提升,氧的相对含量有所下降,S与基体接触机会增大,产生疏松的腐蚀产物附着在基体表面,与微观形貌图相吻合。Na含量随着S含量增加不断上升,是由于在含NaOH的碱性环境中钠离子不断扩散到疏松的腐蚀产物层。
2.3 腐蚀失重分析
Q235钢在不同S2-浓度下经120 h喷雾腐蚀后腐蚀失重结果如表3所示,S2-浓度与腐蚀失重变化关系如图4所示。

表3 Q235钢在不同S2-浓度下经120 h腐蚀后的腐蚀失重和腐蚀速率变化

图4 Q235钢腐蚀失重与S2-浓度变化关系图
从表3和图4可以看出随着S2-浓度的升高腐蚀失重呈现出先不断增大后稍有下降的趋势,腐蚀速率同样先增大后减小,S2-浓度的上升对Q235钢腐蚀具有明显的促进作用。S2-浓度为3 g/L时,腐蚀失重较小,为2.8732 g/m2,此时由于S2-浓度较低,主要是OH-与Fe反应生成致密的氧化膜附着在基体表面,S与Fe的反应为次要反应,故腐蚀失重相对较小;当S2-浓度上升到4g/L时,腐蚀失重较明显的增大,S2-浓度较低时腐蚀反应控制步骤为溶液外扩散,当S2-浓度上升,S2-活性增大,进入到基体内核的概率增大,故发生腐蚀概率增大,故此阶段腐蚀失重逐渐增大;当S2-由4g/L上升到5 g/L时,腐蚀失重迅速增大,达到3.3121 g/m2,由于碱性环境中S2-和OH-与Fe的腐蚀反应是处于竞争关系,S2-浓度较低时主要发生铁的氧化反应,当S2-浓度上升时,主要发生铁的硫化反应,OH-与Fe反应处于相对抑制状态,S2-大量进入基体生成疏松硫铁化合物,致使腐蚀失重迅速增大;随着S2-浓度进一步上升到6 g/L,腐蚀失重达到最大值为3.4451 g/m2,S2-浓度上升外扩散达到极值,此时基体内扩散为腐蚀反应限制条件。当S2-浓度达到7 g/L时,腐蚀失重不增反而有少许下降,这是由于高浓度的硫化物迅速与基体形成腐蚀产物覆盖在试样表面,使反应内扩散减弱,故腐蚀失重也相应减小。
2.4 最大点蚀深度分析
Q235钢在不同S2-浓度下经120 h盐雾腐蚀后的最大点蚀深度变化如表4和图5所示。

表4 Q235钢最大点蚀深度随S2-浓度变化情况

图5 Q235钢腐蚀试样最大点蚀深度与S2-浓度关系图
表4和图5所示,含硫化合物在碱性环境中对Q235钢的腐蚀反应是化学反应和电化学反应共同作用的结果。S2-浓度由3 g/L增加到7 g/L的过程中,试样的最大点蚀深度先加深后变浅,然后又不断加深,说明S2-的浓度变化对试样的腐蚀反应有显著影响。当S2-浓度由3 g/L增加到4 g/L时,随着S2-浓度增加,最大点蚀深度变深,平均腐蚀速率增大,表面腐蚀产物呈疏松的砂状,为亮黑色,同时在溶液中发现黑色块状,为试片腐蚀脱落产物,此时硫铁化合物生成使腐蚀深度增加。当S2-浓度由4 g/L上升到5 g/L时,最大点蚀深度变浅,此时由于OH-和S2-与基体反应的能力相当,基体表面为均匀腐蚀状态,此时最大点蚀深度较浅。当S2-浓度由5 g/L上升到7 g/L时,硫化反应占据主导地位,OH-与基体反应处于抑制状态,基体表面生成呈疏松状的腐蚀产物,随着S2-浓度增加,腐蚀反应趋于剧烈,故试样的最大点蚀深度逐渐加深。
2.5 极化曲线分析
Q235钢在不同S2-浓度下经120 h腐蚀后的极化曲线如图6所示。对极化曲线进行Tafel拟合,拟合结果如表5所示。
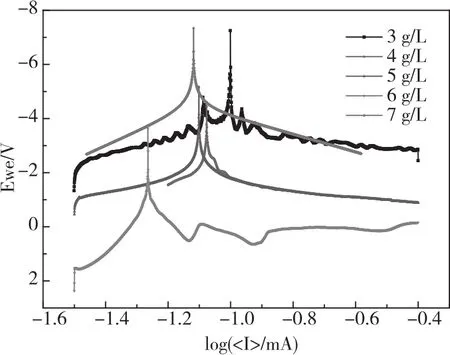
图6 Q235钢材在不同S2-浓度下极化曲线

表5 Q235钢材在不同S2-浓度下极化曲线的拟合数据表
如图6和表5所示,Q235钢在不同S2-浓度下经120 h腐蚀后,当S2-浓度由3 g/L增大到6 g/L时,腐蚀电流密度逐渐增大,由于S2-浓度增加,加速了腐蚀反应外扩散,加大S2-向基体扩散的速度,故此时腐蚀电流密度与S2-浓度变化密切相关,S2-促使腐蚀。当S2-由6 g/L增大到7 g/L时,腐蚀电流密度反而减小,腐蚀反应有所下降,由于高浓度硫化物与基体迅速发生腐蚀反应,腐蚀产物覆盖在基体表面影响腐蚀进一步进行,故此时腐蚀电流密度下降。
3 结论
(1)由宏观形貌和微观形貌分析可知,随着NaOH溶液中S2-浓度的递增,Q235钢腐蚀越来越严重,腐蚀情况也在逐渐加剧,即 S2-的存在对Q235钢的腐蚀行为具有显著影响;由腐蚀失重分析可知,当S2-浓度由3 g/L增加至6 g/L时,腐蚀失重及对应的腐蚀速率都在逐渐增大,而当S2-浓度为7 g/L时试样的腐蚀失重及腐蚀速率却出现了下降,这是由于硫铁化合物迅速覆盖在试样表面,使反应内扩散减弱所致。
(2)极化曲线分析可知,S2-浓度由3 g/L增至6 g/L时腐蚀反应的外扩散即S2-向基体扩散的速度也随之增大,故腐蚀电流密度从0.931μA/cm2迅速增至5.092μA/cm2,S2-浓度为7 g/L时腐蚀产物覆盖在基体表面导致腐蚀电流密度下降至3.273μA/cm2。
(3)EDS分析结果可知,腐蚀产物主要由Fe、S、O三种元素组成,S2-浓度为4 g/L时Fe的含量高达80.26%,当S2-浓度为5 g/L时,由于Fe的氧化反应导致O的含量明显升高,而当S2-浓度升高至6 g/L时,Fe的硫化反应为主要反应,因此S含量明显升高而O含量有所下降。
致谢:对帮助该论文顺利完成的陈朝轶老师和其他同学表示诚挚的谢意。
[1]贾永真,王家伟,李军旗,等.硫含量对铝酸钠种分母液盐蒸发结晶析出的影响[J].过程工程学报,2013,13(5):801-806.
[2]杨夏琼,陈朝轶,李军旗,等.硫对钢材碱性腐蚀的研究综述[J].表面技术,2015,44(9):89-95.
[3]吕国志.利用高硫铝土矿生产氧化铝的基础研究[D].沈阳:东北大学,2010.
[4]冯拉俊,马小菊,雷阿利.硫离子对碳钢腐蚀性的影响[J].腐蚀科学与防护技术,2006(3):180-182.
[5]胡洋,李晓刚,李明,等.16Mn(HIC)钢在D405设备环境下的腐蚀行为研究[J].石油化工腐蚀与防护,2006,23(1):13 -15.
[6]吴考民,王可中,石鑫,等.含硫原油对输油管道的腐蚀性[J].油气储运,2010(8):616-618.
[7]ABDEL S H,ANNA M B.Effect of Surface Preparation prior to Cerium Pre-treatment on the Corrosion Protection Performance of Aluminum Composites[J].Journal of Applied Electrochemistry,2005,41(2):44-47.
[8]HAZLEWOOD P E.Factors Affecting the Corrosivity of Pulping Liquors[D].Atlanta:Georgia Institute of Technology,2006.
[9]HAZLEWOOD P E,SINGH PM,HSIEH JS.Corrosion Behavior of Carbon Steels in Sulfide-containing Caustic Solutions[J].Industrial&Engineering Chemistry Research,2006,45(23):7789 -7794.
[10]曹华珍,张九渊,郑国渠,等.碳钢在含硫介质中的极化行为[J].腐蚀与防护,2002,23(10):427-429.
[11]罗哲媛,俞敦义,杨继林.渗铝钢在Na2S溶液中的腐蚀行为研究[J].材料开发与应用,2000,15(4):14-16.
[12]郝文魁,刘智勇,李晓刚,等.16Mn钢及其热影响区在碱性硫化物环境中的应力腐蚀行为与机理[J].金属学报,2013 (7):881-889.
[13]陈朝轶,李玲,王家伟,等.3003铝合金盐雾加速腐蚀行为[J].轻金属,2014,24(2):54-58.
[14]杨京,陈朝轶,张湘黔,等.温度对0359铝合金腐蚀的影响[J].热加工工艺,2015,44(4):47-51.
[15]Qiaoling Xie,Wenmi Chen.Corrosion behavior of 16Mn low alloy steel in sulfide-containing Bayer solutions[J].Corrosion Science,2014(86):252-260.
[16]吴茂永,田继强,曹立新,等.钨铝合金在不同NaCl溶液中的电化学腐蚀行为研究[J].腐蚀科学与防护技术,2015,27 (1):25-30.
(责任编辑:王先桃)
Study of Sodium Sulfide on Corrosion Behavior of Q235 Steel in Sodium Hydroxide Solution
YANG Xiaqiong1,2,CHEN Chaoyi1,2∗,LIJunqi1,2,ZHAO Cong1,2,LIU Long1,2,WEIGuoling1,2
(1.School of Material and Metallurgy,Guizhou University,Guiyang 550025,China;2.Guizhou Provincial Key Laboratory of Metallurgical Engineering and Process Energy Saving,Guiyang 550025,China)
The corrosion behavior of 16 Q235 steel in sodium hydroxide solution with different S2-concentration was studied by salt spray corrosion and electrochemical corrosion testand analyzed by corrosion weight lossmethod,SEM,EDSand EIS.The results show that corrosion behavior of Q235 steel is notably affected by the concentration changing of S2-.Macro-morphology and micro-morphology analysis demonstrated corrosion of sample get worse with the growth of S2-concentration.EDS analysis demonstrated corrosion products were consist of Fe,S and O predominantly,the content of Fe was high when S2-concentration was 4g/L as the extent of corrosion was lightly.The content of O escalated when S2-concentration was 4g/L as oxidation of Fe.The content of Smarkedly elevated while the content of O dropped as the vulcanization reaction of Fe being dominant.Weight loss increased form 2.8732 g/m2to 3.4451g/m2and corrosion current density increased from 0.931μA/cm2to 5.092μA/cm2when S2-concentration increased from 3g/L to 6g/L as the reaction of S2-and Fe.However,the weight loss and corrosion current density showed an opponent trend when the S2-concentration grow up to 7g/L.The reason is that a densemembrane of FeS covered the surface of sample with 7g/L S2-.
sodium hydroxide;sodium sulfide;Q235 steel;corrosion behavior;polarization curve
TG171
A
1000-5269(2016)04-0038-06
10.15958/j.cnki.gdxbzrb.2016.04.08
2016-02-30
国家自然科学基金(51574095,51474079);贵州省校合作项目(LH[2014]7609)
杨夏琼(1990-),男,在读硕士,研究方向:金属电化学腐蚀,Email:yangxiaqionghpu@163.com.
∗通讯作者:陈朝轶,Email:ccy197715@126.com.

