急性心肌梗死直接PCI术后脑出血再发心肌梗死1例
邱景伟,浦奎,程艳慧
· 病例报告 ·
急性心肌梗死直接PCI术后脑出血再发心肌梗死1例
邱景伟1,浦奎2,程艳慧2
1 病例
患者女性,72岁,主因“突发胸骨后疼痛2 h”入院。既往高血压病史10余年,最高血压180/90 mmHg(1 mmHg=0.133kPa),间断服用降压药物(具体用药未提及),血压维持在130~140/70~85 mmHg。入院查体:体重50 kg,血压120/62 mmHg,脉搏50 次/min,口唇无紫绀,双肺呼吸音清楚,未闻及干湿啰音,心音低钝、心率50 次/min,心律齐,各瓣膜听诊区未闻及杂音。心电图示:窦性心律,Ⅱ、Ⅲ、aVF导联ST段弓背向上抬高0.2~0.4 mV,Ⅰ、aVL,V1~V4导联ST段压低0.1~0.25 mV,三度房室传到阻滞,交界区逸博(图1)。肌酐清除率49.7 ml/min,白细胞计数10.7×109/L,中性粒细胞60.7%,血钾3.28 mmol/L,血糖、肝肾功能、电解质及凝血正常。初步诊断:①急性下壁心肌梗死、心功能KillipⅠ级;②高血压3级、极高危;③低钾血症。给予阿司匹林300 mg、硫酸氢氯吡格雷300 mg嚼服后经右股动脉行急诊冠状动脉造影,造影示左冠状动脉主干正常,前降支及左旋支弥漫性病变,前降支中段偏心性狭窄80%,远端血流TIMI 3级;右冠状动脉多处斑块,后三叉前弥漫性狭窄,次全闭塞,左室后支未显影,BMW导丝通过病变到达后降支远端,PILOT导丝到达左室后支远端,球囊扩张左室后支病变后血流恢复,在后三叉前后连续置入2.5×36 mm及2.5×14 mm EXCEL药物支架,高压球囊后扩张后无残余狭窄,远端血流TIMI 1级,给予盐酸替罗非班冠脉内推注后血流恢复TIMI 3级(图2),术中共用普通肝素10 000U。术后患者胸痛缓解,ST段回落,T波倒置(图3)。继续抗栓治疗:阿司匹林100 mg,1/d,硫酸氢氯吡格雷75 mg,1/d,低分子肝素4250 U,1/12 h(连用7 d),鉴于患者冠状动脉病变严重,术后应用盐酸替罗非班0.1μg/(kg·min)(应用36 h),患者生命体征平稳,三度房室传到阻滞消失,窦性心律恢复1:1传导,血压100~130/60~80 mmHg间,血常规未见异常。术后第1 d磷酸肌酸激酶1062.0 U/L(参考值10~200 U/L,AMI临界值>400 U/L)、磷酸肌酸激酶同工酶80.0 U/L(参考值0~250 U/L, AMI 临界值>50.0 U/L),血常规正常;第3 d磷酸肌酸激酶301.0 U/L、磷酸肌酸激酶同工酶23.0 U/L,血常规正常。第3 d凌晨4点患者突然出现恶心、呕吐、头痛等症状,查体:血压143/63 mmHg,神智清楚,查体合作,颈软,四肢运动及感觉正常,肌力及肌张力正常,病理征阴性。行头颅CT检查提示脑出血,神经外科会诊建议暂停抗栓治疗,甘露醇防颅内压升高导致脑疝,奥拉西坦静点,同时给予镇静,止痛,质子泵抑制剂预防应激性溃疡,经过上述处理,患者生命体征平稳,恶心、呕吐症状缓解,头痛症状明显缓解。第7 d复查头颅CT示左小脑大片状高密度影,最大横截面5.1×2.6 cm,出血量约10 ml,破入蛛网膜下腔,较第3 d无明显出血进展。第11 d再次复查CT示左小脑大片状高密度影,最大横截面3.7 cm×2.5 cm,较前缩小,处于吸收期。当日上午10:25患者突发胸骨后疼痛,伴大汗,恶心,呕吐,心电图提示Ⅱ、Ⅲ、aVF导联ST段弓背向上抬高0.2~0.5 mV、T波直立,三度房室传导阻滞,交界区逸博心律(图4),监测生命体征:血压76/53 mmHg,心室率35~45 次/min、血氧饱和度95%~99%,考虑再发急性下壁心肌梗死,给予多巴胺升压,经对症处理后收缩压稳定于110~130 mmHg,家属拒绝临时起搏治疗;考虑停用双联抗血小板导致支架内急性血栓可能性,但脑出血尚未稳定,如再次抗凝或抗血小板治疗则可致脑出血加重,仍给予对
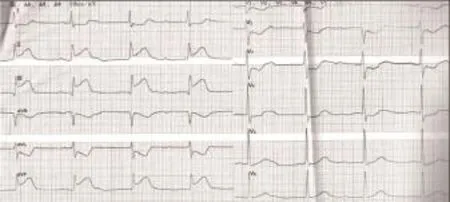
图1 入院时心电图

图2 冠状动脉造影图注:图2a:右冠状动脉多处斑块,后三叉前弥漫性狭窄,次全闭塞,左室后支未显影;图2b:后三叉前后连续置入2.5×36 mm及2.5 ×14 mm EXCEL药物支架后,左室后支病变后血流恢复,右冠状动脉血流TIMI 3级
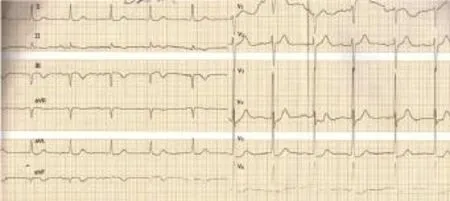
图3 急诊PCI术后心电图
症治疗,仅在血压稳定后加用小剂量硝酸脂类药物扩血管治疗,心电图提示ST段有所回落,变为二度Ⅱ型房室传导阻滞,第12 d复查心肌酶磷酸肌酸激酶830.0 U/L、磷酸肌酸激酶同工酶71.0 U/L,再次升高,支持再发急性心肌梗死诊断。第19 d患者房室传导功能进一步改善传导比例多为3:2传导,间断可见1:1传导,ST段回落,T波倒置。头痛等中枢症状完全缓解,给予出院。出院后半年复查心电图示一度房室传导阻滞,患者生命体征平稳,无不适主诉。
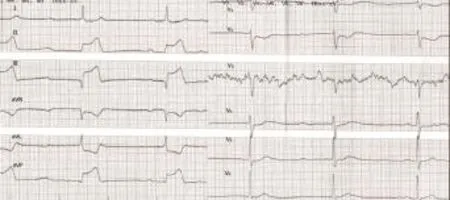
图4 脑出血后第8 d再发胸痛时心电图
2 讨论
术后出血是PCI术后常见并发症之一,包括穿刺血管局部,消化道,腹膜后,颅内出血。颅内出血是少见并发症,发生率大约0.04%(10/25086)[1],病情凶险,死亡及致残率极高,不容忽视。本例患者急性心肌梗死直接PCI术后出现脑出血,停用抗血小板药物后再发支架内急性血栓导致再次发生急性心肌梗死后存活,且未致残,是鲜有报道的病例。
PCI术后出血多与凝血功能障碍、抗凝不当或持续高血压有关;目前随着PCI治疗、及围手术期抗凝及双联甚至三联抗血小板治疗的广泛应用,PCI术后出血的病例报道增多,出血可发生在多种组织和器官,而颅内出血易压迫脑组织,导致神经功能的丧失甚至脑疝而危及生命,是PCI术后多种出血并发症中最危险及预后最差的一种。一旦脑出血,出血量少时应停用抗血小板及抗凝药物,加用脱水药物;如出血量大,存在发生脑疝危险或已发生脑疝,在积极给予脱水治疗时,应及时行脑外科紧急手术治疗,降低死亡率,但致死率及致残率极高,预后极差。本例患者在直接PCI术后第3 d出现小脑幕下出血,影像学评估出血量约10 ml,停用抗栓药物,给予甘露醇脱水后,未出现脑疝表现,考虑出血停止,病情逐渐稳定;鉴于患者此次为急性下壁心肌梗死,行急诊PCI,停用抗血小板药物后容易出现支架内急性血栓,未给予抗纤溶及止血药物治疗脑出血。
高血压病是导致患者PCI术后自发性脑出血的主要危险因素,长期高血压导致颅内小动脉壁结构发生改变,损伤小动脉壁内膜,易发生微破裂,这一过程随年龄增长而累积;如凝血系统异常(如使用抗栓药物)或血压发生突然升高时,易导致颅内小动脉破裂出血,发生脑出血[2]。本例患者为高龄女性,既往高血压病史10余年,考虑颅内小动脉存在上述改变,抗栓治疗不当导致凝血系统异常则是导致脑出血的另一主要原因。血小板糖蛋白Ⅱb/Ⅲa受体拮抗剂联合阿司匹林、氯吡咯雷三联抗血小板治疗显著增加住院期间出血危险[3]。
随着抗栓治疗强度的增加,缺血事件发生率下降的同时,出血并发症明显增加,而严重出血并发症可部分抵消抗栓治疗带来的疗效,甚至增加死亡率及致残率。如何维持减少出血并发症和治疗缺血的平衡,应结合GRACE及CRUSADE评分,结合不同的评分结果,综合考虑合适的抗栓方案,既可保缺血治疗的疗效,又能降低出血发生的几率。CRUSADE对于识别出血并发症高危患者,权衡抗栓治疗与出血并发症的获益和风险,对于指导临床治疗,处置,改善患者预后,具有重要意义[4]。
[1] Mehta SR,Bassand JP. Dose comparisons of clopidogrel and aspirin in acute coronary syndromes[J].N Engl J Med,2010,363(22):930-43.
[2] 王苏,李志忠,张京梅. PCI术后并发小脑出血成功治疗一例[J]. 中国介入心脏病学杂志,2009,17(16):229-30.
[3] Lim MJ,Eagle KA,Gore JM,et al. Treating patients with acute coronary syndromes with aggressive antiplatelet therapy(from the Global Registry of Acute Coronary Events)[J]. Am J Cardiol,2005,96 (3):917-21.
[4] Subherwal S,Bach RG,Chen AY,et al. Baseline risk of major bleeding in non-ST-segment-elevation myocardial infarction:the CRUSADE(Can Rapid risk stratification of Unstable angina patients Suppress Adverse outcomes with Early implementation of the ACC/AHA Guidelines)Bleeding Score[J]. Circulation,2009,119(11):1873-82.
本文编辑:孙竹
R541.4
A
1674-4055(2016)11-1389-02
1300142 天津,解放军第二五四医院干部病房三科;2300142 天津,解放军第二五四医院心血管内科
邱景伟,Email:qiujingwei@163.com
10.3969/j.issn.1674-4055.2016.11.30

