干扰素治疗代偿期乙肝肝硬化45例临床效果观察
王 娟, 刘先进, 羌 韧
(南通大学附属第三人民医院 传染科, 江苏 南通, 226001)
干扰素治疗代偿期乙肝肝硬化45例临床效果观察
王 娟, 刘先进, 羌 韧
(南通大学附属第三人民医院 传染科, 江苏 南通, 226001)
代偿期肝硬化; 干扰素; 疗效; 不良反应
慢性乙型肝炎可以进一步发展为肝硬化、肝细胞癌,严重者可以出现肝功能衰竭,甚至死亡[1]。抗病毒治疗可以延缓或终止病情进展,公认的抗病毒治疗药物有干扰素和核苷(酸)类似物两大类[2]。干扰素抗病毒有效率相对低,起效慢,副作用较多,但其具有疗程相对固定、不易产生病毒耐药、HBeAg和HBsAg血清学转换率高、应答持久且能减少肝癌的发生。中国《慢性乙型肝炎防治指南(2010-2015年版)》[3]建议代偿期乙肝肝硬化患者慎重应用干扰素,如果使用也应从小剂量开始,并根据患者情况逐渐增加至治疗量。作者对肝功能Child-Pugh分级为A级的HBeAg阳性代偿期乙肝肝硬化患者采用干扰素治疗,取得了较好的疗效,现报告如下。
1 资料与方法
1.1 一般资料
选取2010年1月—2015年6月南通大学附属第三人民医院传染科住院或门诊接受干扰素治疗的HBeAg阳性代偿期乙肝肝硬化(LC)患者45例, HBeAg阳性慢性乙型肝炎(CH)患者50例,年龄、性别无显著差异(P>0.05), 诊断符合《中国慢性乙型肝炎防治指南(2015年版)》[4], 符合指南抗病毒指证,并检查抗HAV-IgM、抗HCV-IgG、抗HDV- IgM、抗HEV-IgM 和IgG、抗MCVIgM和抗EBM- IgM排除重叠感染。排除干扰素治疗的禁忌证:血清胆红素大于正常值2倍;失代偿性肝硬化;自身免疫性疾病;有重要器官病变(严重心、肾疾患、糖尿病、甲状腺疾病、神经精神异常)[5]。
1.2 方法
① 治疗前根据白蛋白、总胆红素、丙氨酸氨基转移酶(ALT)、HBeAg、HBV-DNA、B超等检查将患者分为4组。Ⅰ组为LC患者: ALT≥2~<5 ULN; Ⅱ组为LC患者: ALT<2 ULN; Ⅲ组为CH患者: ALT<2 ULN; Ⅳ组为CH患者: ALT≥2~<5 ULN。② 所有患者均予聚乙二醇干扰素α-2a(PegIFNα-2a)180 μg 或聚乙二醇干扰素α-2b(PegIFNα-2b)80 μg每周1次皮下注射,肝硬化患者治疗第1个月从小剂量开始,总疗程72周。③ 治疗24、48、72周、停药1年后检查肝功能、HBsAg、HBeAg、HBV-DNA、甲状腺功能、血常规等各项指标,记录患者用药后的不良反应和副作用。④ 所有肝功能均使用本院生化检测仪(型号奥林巴斯AU2700)检测。HBV-DNA定量采用ABI7500荧光PCR仪检测,试剂购于上海科华公司, HBV-DNA<103copies/mL为阴性。HBV-M定量采用微粒酶免疫法检测(MEIA法),为Abbot公司试剂。
2 结 果
治疗48、72周,Ⅰ、Ⅱ、Ⅲ组HBeAg、HBV-DNA转阴率显著高于Ⅳ组(P< 0.05), 治疗72周与48周相比, HBeAg、HBV-DNA转阴率无显著差异(P>0.05)。见表1。停药1年后复查HBeAg、HBV-DNA持续应答情况。Ⅰ、Ⅱ、Ⅲ组HBeAg阴性率依次为55%、52%、48%, 显著高于Ⅳ组28%(P<0.05); Ⅰ、Ⅱ、Ⅲ组HBV-DNA阴性率依次为55%、52%、48%,显著高于Ⅳ组28%(P<0.05)。4组不良反应发生情况见表2。4组不良反应发生率无显著差异(P>0.05)。
3 讨 论
干扰素是机体被病毒感染后产生的一类具有抗病毒活性的可溶性糖蛋白[5]。目前中国批准用于慢性乙肝抗病毒的干扰素包括普通α干扰素(IFN-α)和聚乙二醇干扰素(PegIFN-α)。PegIFN-α是乙肝患者的一线抗病毒药物之一,具有疗程确切、乙型肝炎e抗原血清转换率高及治疗结束后持续应答率高等优点。关于乙肝肝硬化的抗病毒治疗,美国肝脏病研究协会(AASLD)2015年慢性乙肝诊疗指南[6]及中国慢性乙型肝炎防治指南(2015年版)均建议代偿期肝硬化患者中一旦HBV-DNA 水平升高就应考虑抗病毒治疗,都主张慎重使用干扰素,主要担心其诱发过度免疫反应而加重肝损伤,导致失代偿和肝衰竭,指南均推荐长期应用核苷(酸)类似物[3, 7-8]。有研究[9]发现干扰素治疗肝硬化患者, HBeAg清除率远高于非肝硬化患者。另一项研究[10]发现PEG-IFN-α-2b治疗肝硬化78周后HBV-DNA和HBeAg转阴率远高于无肝硬化组,而二组不良反应发生率相似。作者知道基线肝功能(包括血清ALT、AST、胆红素水平等)、HBsAg、HBeAg状态、HBV-DNA、B超检查。基线丙氨酸氨基转移酶(ALT)水平、HBsAg、HBeAg及HBV-DNA低滴度水平、肝脏组织病理改变是PegIFN-α治疗应答的重要预测因素。林荣芳等[11]入选了51 例接受PegIFN-α治疗的HBeAg阳性CHB患者,发现在ALT≤10 ULN且有相对禁忌证的情况下,血清ALT>7 ULN者, 48周血清学应答率明显升高,提示基线ALT水平对PegIFN-α治疗应答具有预测价值。本研究显示HBeAg阳性代偿期乙肝肝硬化患者与基线ALT同水平基线的慢性乙肝相比,有较高的应答率和持续应答率(P<0.05), 基线ALT低水平的HBeAg阳性的代偿期乙肝肝硬化患者也有较高的应答率和持续应答率(P<0.05)。
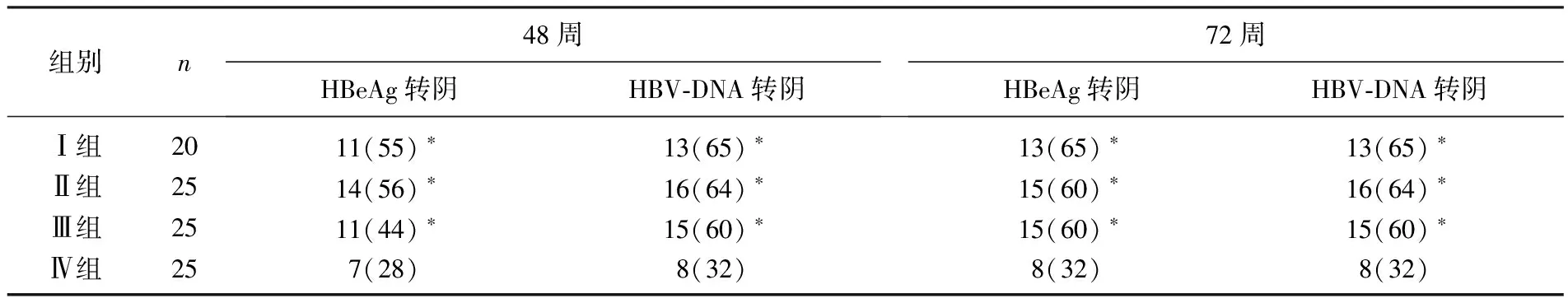
表1 干扰素治疗后4组HBeAg、HBV-DNA转阴情况比较[n(%)]
与Ⅳ组比较, *P<0.05。
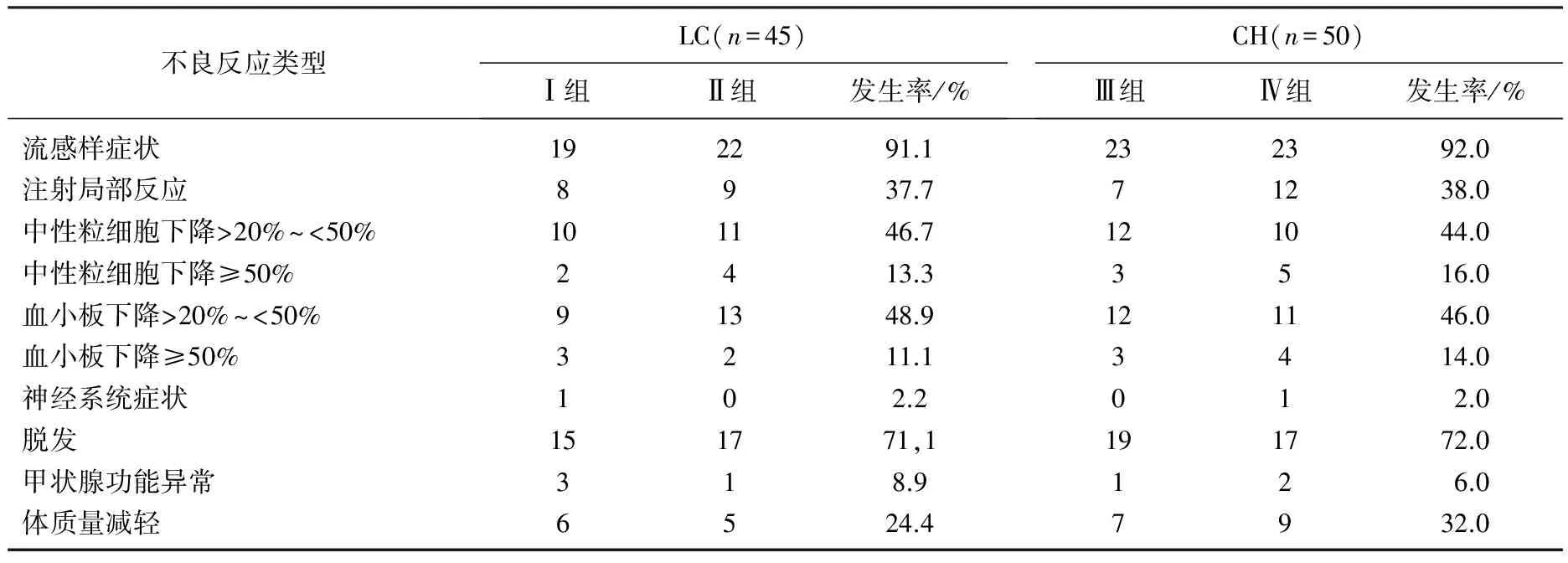
表2 干扰素不良反应发生情况
有研究显示,在乙肝干扰素抗病毒疗效的预测因素中,肝组织炎症程度是最重要因素,慢性肝炎患者ALT与肝组织的炎症程度呈正相关, ALT在一定程度上反映了肝组织的严重程度。而肝硬化患者, ALT不能完全反映肝组织的炎症程度,作者统计了15例Child-Pugh A级、ALT正常的行脾切除治疗肝硬化患者,在术中行肝活检,结果显示其肝组织的炎症程度90%为G3、G4, 因此作者认为这可以解释基线ALT较低水平代偿期乙肝肝硬化患者有较高的应答率。
干扰素常见的不良反应有流感样症状、外周血细胞下降、内分泌和代谢性疾病、消化道症状和神经精神异常等[12-15]。本研究PegIFN-α治疗HBeAg阳性代偿期乙肝肝硬化患者,为避免干扰素诱发过度免疫的风险,干扰素从小剂量开始,根据患者耐受情况及不良反应情况逐渐增加到治疗剂量,治疗期间不良反应发生率与慢性乙肝相比无显著差异。
[1] Ganem D, Prince A M. Hepatitis B virus infection-natural history and clinical consequences[J]. N Engl J Med, 2004, 350(11): 1118-1129.
[2] Hoofnagle J H, Doo E, Liang T J, et al. Management of hepatitis B: summary of a clinical research workshop[J]. Hepatology, 2007, 45(4): 1056-1075.
[3] 中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙型肝炎防治指南(2010年版)[J]. 中国肝脏病杂志: 电子版, 2011, 3(1): 40-56.
[4] 中华医学会肝病学分会. 慢性乙型肝炎防治指南(2015年版)[J]. 中国肝病学杂志, 2015, 7(3): 1-18.
[5] 宫嫚, 辛绍杰, 邹正升, 等. 复方鳖甲软肝片治疗慢性乙型肝炎患者对血清肝纤维化指标的影响[J]. 实用肝脏病杂志, 2015, 18(6): 585-589.
[6] Lin F C, Young H A. Interferons: Success in anti-viral immunotherapy[J]. Cytokine Growth Factor Rev, 2014, 25( 4): 369-376.
[7] 徐莹, 王卫彬, 李湛东, 等.《2015 年美国肝病学会指南更新版: 慢性乙型肝炎的治疗》摘译[J]. 临床肝胆病杂志, 2016, 32( 2): 223-229.
[8] Sokal E M, Paganelli M, Wirth S, et al. Management of chronic hepatitis B in childhood: ESPGHAN clinical practice guidelines: consensus of an expert panel on behalf of the European Society of Pediatric Gastroenterology, Hepatology and Nutrition[J]. Hepatology, 2013, 59(4): 814-829.
[9] WHO. Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection[EB/OL]. 2015-07-12. http: //www. who. int/hiv/pub/hepatitis/hepatitis-b-guidelines/en/.
[10] VanZonneveldM, Honkoop P, Hansen B E, et al. Long-term fol-low-up of alpha-interferon treatment of patients with chronic hepatitis B[J]. Hepatology, 2004, 39(3): 804-810.
[11] 张鸿飞, 杨晓晋, 朱世殊. α干扰素治疗小儿慢性肝炎副作用的长期观察[J]. 中华实验和临床病毒学杂志, 2000, 14 (4): 376-378.
[12] 林荣芳, 王长连, 黄品芳, 等. 聚乙二醇干扰素α-2a治疗HBeAg阳性慢性乙型肝炎的疗效预测指标[J]. 医药导报, 2014, 33(4): 449-452.
[13] Sulkowski M S, Cooper C, Hunyady B, et al. Management of adverse effects of Peg-IFN and ribavirin therapy for hepatitis C[J]. Nat Rev Gastroenterol Hepatol, 2011, 8(4): 212-223.
[14] McHutchison J G, Lawitz E J, Shiffman M L, et al. Peginterferon alfa-2b or alfa-2a with ribavirin for treatment of hepatitis C infection[J]. N Engl J Med, 2009, 361( 6): 580-593.
[15] Roomer R, Hansen B E, Janssen H L, et al. Thrombocytopenia and the risk of bleeding during treatment with peginterferon alfa and ribavirin for chronic hepatitis C[J]. J Hepatol, 2010, 53(3): 455-459.
[16] Buster E H, Hansen B E, Buti M, et al. Peginterferon alpha-2b is safe and effective in HBeAg-positive chronic hepatitis B patients with advanced fibrosis[J]. Hepatology, 2007, 46( 2): 388-394.
2016-09-29
R 657.3
A
1672-2353(2016)23-156-02
10.7619/jcmp.201623057

