HPLC-ELSD法测定琥乙红霉素片中琥乙红霉素的含量
李志得,张彩云,汪 霞(鄂州市食品药品检验检测中心,湖北鄂州 436099)
HPLC-ELSD法测定琥乙红霉素片中琥乙红霉素的含量
李志得*,张彩云,汪 霞(鄂州市食品药品检验检测中心,湖北鄂州 436099)
目的:建立高效液相色谱-蒸发光散射检测器法测定琥乙红霉素片中琥乙红霉素含量的方法。方法:色谱柱为Dikma-C18,流动相为乙腈-0.05%二乙胺(70∶30,V/V),流速为1.0 ml/min,柱温为30℃,进样量为10 μl。结果:琥乙红霉素检测进样量线性范围为1.216~7.296 μg(r=0.999 2);定量限为0.304 μg,检测限为0.076 μg;精密度、稳定性、重复性试验的RSD<2.0%;加样回收率为97.59%~104.19%(RSD=1.71%,n=6)。结论:该方法操作简便、结果准确、灵敏度高、重复性好,可用于测定琥乙红霉素片中琥乙红霉素的含量。
琥乙红霉素片;高效液相色谱法;琥乙红霉素;含量测定
琥乙红霉素属大环内酯类抗菌药物,为红霉素的琥珀酸乙酯,具有广谱抗菌作用。2015年版《中国药典》(二部)采用水解琥乙红霉素后,用微生物检定法测定其含量[1],此试验过程复杂、操作烦琐、影响因素多、重复性较差[2]。目前,现有文献多采用高效液相色谱法(HPLC)测定琥乙红霉素的含量[3-6],均采用紫外检测器,检测波长为210 nm左右;而琥乙红霉素仅在紫外末端有吸收,因此此试验灵敏度低。为尽量减小紫外末端吸收引起的基线干扰,笔者采用HPLC-蒸发光散射检测器(ELSD)法,建立了测定琥乙红霉素片中琥乙红霉素含量的方法,以期为控制该制剂的质量提供参考。
1 材料
1.1 仪器
2695型HPLC仪,包括2424蒸发光散射检测器、e2695泵、Empower 2色谱工作站(美国Waters公司);KQ-3000型数控超声波清洗器(昆山市超声仪器有限公司,功率:300 W,频率:40 kHz);BS21S型十万分之一电子天平(德国Sartorius公司)。
1.2 药品与试剂
琥乙红霉素片(西安利君制药有限责任公司,批号:1402052、1311474、1403016,规格:0.125 g/片);琥乙红霉素对照品(中国食品药品检定研究院,批号:130425-200002,纯度>98%);乙腈为色谱纯,其余试剂均为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:Dikma-C18(250 mm×4.6 mm,5 μm);流动相:乙腈-0.05%二乙胺(70∶30,V/V);流速:1.0 ml/min;柱温:30℃;进样量:10 μl。.
2.2 溶液的制备
2.2.1 对照品溶液 精密称取琥乙红霉素对照品0.030 40 g,置于25 ml量瓶中,加乙腈溶解并定容,制成每1 ml含琥乙红霉素1.216 mg的溶液,作为对照品贮备液。精密量取上述对照品贮备液4.0 ml,置于10 ml量瓶中,加乙腈溶解并定容,制成每1 ml含琥乙红霉素0.486 mg的溶液,作为对照品溶液。
2.2.2 供试品溶液 取本品10片,精密称定,研细,混匀,精密称取适量(约相当于琥乙红霉素35 mg),置于100 ml量瓶中,加乙腈溶解,超声处理10 min,放冷,加乙腈定容,摇匀,滤过,取续滤液,即得。
2.2.3 阴性对照溶液 按样品的处方工艺和配方比例,取不含琥乙红霉素的辅料制备阴性样品,再按“2.2.2”项下方法制备阴性对照溶液,即得。
2.3 系统适用性试验
精密量取“2.2”项下对照品溶液、供试品溶液和阴性对照溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,琥乙红霉素与其他杂质峰均能达到基线分离,分离度>2.0;理论板数以琥乙红霉素峰计>5 000,保留时间为10 min。结果表明,其他成分对测定无干扰。
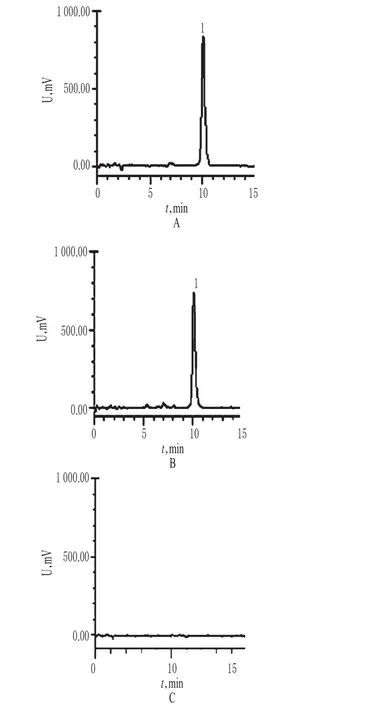
图1 高效液相色谱图A.对照品;B.供试品;C.阴性对照;1.琥乙红霉素Fig 1 HPLC chromatogramsA.reference substance;B.test sample;C.negative control;1.erythromycin ethylsuccinate
2.4 线性关系考察
精密量取“2.2.1”项下对照品贮备液1.0、2.0、3.0、4.0、5.0、6.0 ml,分别置于10 ml量瓶中,加乙腈定容,摇匀,即得系列对照品溶液。分别精密量取上述系列对照品溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。以琥乙红霉素进样量的对数值为横坐标(x)、峰面积的对数值为纵坐标(y)进行线性回归,得琥乙红霉素对数值的回归方程为y=1.100 5x+6.606 1(r=0.999 2)。结果表明,琥乙红霉素峰面积的对数值与进样量的对数值线性关系良好,琥乙红霉素检测进样量线性范围为1.216~7.296 μg。
2.5 定量限与检测限考察
取“2.2.1”项下对照品溶液适量,等倍逐步稀释,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为10∶1时,得定量限;当信噪比为3∶1时,得检测限。结果,琥乙红霉素的定量限为0.304 μg,检测限为0.076 μg。
2.6 精密度试验
精密量取“2.2.1”项下对照品溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。结果,琥乙红霉素峰面积的RSD=0.92%(n=6),表明仪器精密度良好。
2.7 稳定性试验
精密量取同一供试品溶液(批号:1402052)适量,分别于室温下放置0、4、8、12、18、24 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,琥乙红霉素峰面积的RSD=1.08%(n=6),表明供试品溶液在24 h内稳定性良好。
2.8 重复性试验
取同一批样品(批号:1402052)适量,精密称定,共6份,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积。结果,琥乙红霉素的平均含量为98.4%,RSD=0.84%(n=6),表明本方法重复性良好。
2.9 加样回收率试验
取已知含量的样品(批号:1402052)6份,研细,精密称取适量(约相当于琥乙红霉素9 mg),分别精密加入琥乙红霉素对照品9 mg,置于50 ml量瓶中,加乙腈适量,超声处理10 min,放冷,加乙腈定容,摇匀,滤过,取续滤液,按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表1。
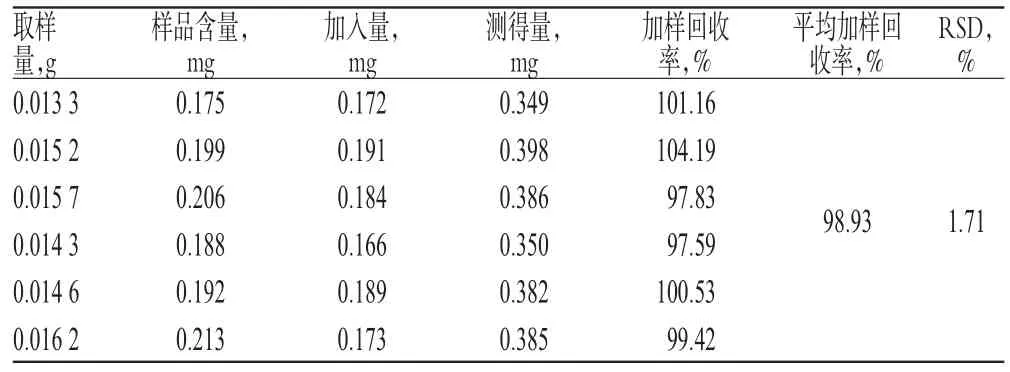
表1 加样回收率试验结果(n=6)Tab 1 Results of recovery test(n=6)
2.10 样品含量测定
取3批样品各适量,分别按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并按两点外标法计算样品含量,结果见表2。
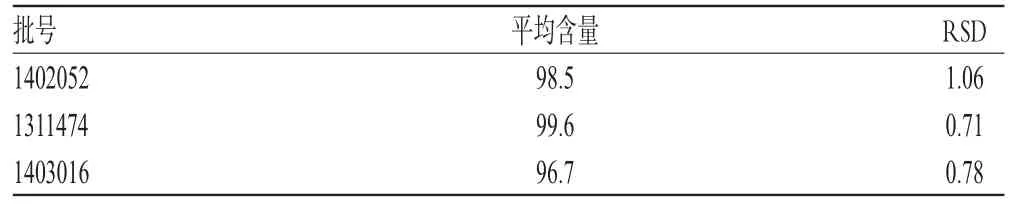
表2 样品含量测定结果(n=3,%)Tab 2 Results of content determination of samples(n=3,%)
3 讨论
3.1 检测方法的选择
目前,琥乙红霉素的测定方法主要有生物检定法[1]、HPLC法[3-6],紫外分光光度法[7-10]、电化学法[11-12]等。亦有用HPLC法测定琥乙红霉素中游离红霉素[13]、HPLC-串联质谱法测定琥乙红霉素颗粒体内活性代谢物的报道[14],但上述方法灵敏度低。因此,笔者采用ELSD,可提高检测的灵敏度。
3.2 溶剂和流动相的选择
试验中曾用流动相作为溶剂溶解对照品和样品,但稳定性较差。笔者参考相关文献[4]经过多次试验比较,发现采用乙腈作为溶剂溶解样品,在24 h内具有良好的稳定性。故本试验选择乙腈作为溶剂。关于流动相的选择,笔者曾用乙腈-水、乙腈-乙酸铵缓冲液等作为流动相,结果色谱不出峰或峰形极差,改用乙腈-0.05%二乙胺(70∶30,V/V)后,色谱峰形理想,保留时间合适,理论板数按琥乙红霉素峰计达到5 000以上。因此,本试验最终选择乙腈-0.05%二乙胺(70∶30,V/V)作为流动相。
综上所述,本方法操作简便、结果准确、灵敏度高、重复性好,可用于测定琥乙红霉素片中琥乙红霉素的含量。
[1] 国家药典委员会.中华人民共和国药典:二部[S].2015年版.北京:中国医药科技出版社,2015:1 246.
[2] 李夏林,张丽英.管碟法测定琥乙红霉素含量的不确定度分析[J].中国医药导报,2011,8(12):42.
[3] 宋金春,于龙环.HPLC法测定琥乙红霉素静脉乳剂的含量[J].中国药师,2013,16(5):675.
[4] 陈燕,刘虹,赵海鹏.高效液相色谱法测定琥乙红霉素片的含量[J].中国药品标准,2015,16(2):130.
[5] 刘雅琴,赵晓頔,王伟娜,等.琥乙红霉素片含量测定方法的改进[J].中国药师,2012,15(4):510.
[6] 简永耀,靳龙文.HPLC法测定琥乙红霉素片的含量[J].安徽医药,2008,12(8):692.
[7] 王红专,林冰,袁竹青,等.电荷转移分光光度法测定琥乙红霉素[J].河南化工,2015(6):52.
[8] 王晓玲,张萍,陈燕.甲基红褪色光度法测定琥乙红霉素[J].应用化工,2014,43(9):1 712.
[9] 胡小明,彭勤龙.琥乙红霉素与甲基红的荷移反应研究[J].分析科学学报,2015,31(5):701.
[10] 陈莲惠,谢梦,叶莉,等.甲基绿褪色光度法测定琥乙红霉素[J].分析试验室,2014(2):187.
[11] 任艳艳,金根娣,胡效亚.琥乙红霉素在碳糊电极上的电化学测定方法[J].应用化学,2011,28(6):704.
[12] 王伟峰,潘玉莹,杨梅霞,等.毛细管电泳-化学修饰电极电致化学发光法测定琥乙红霉素[J].药物分析杂志,2010,30(10):1 900.
[13] 罗慧萍,易秋艳,王灿,等.HPLC法测定琥乙红霉素中游离红霉素的含量[J].药物分析杂志,2014,34(12):2 264.
[14] 王爱华,刘天扬,杨杨,等.HPLC-MS/MS法测定琥乙红霉素颗粒体内活性代谢物[J].药物分析杂志,2011,31(3):448.
(编辑:刘 柳)
Content Determination of Erythromycin Ethylsuccinate in Erythromycin Ethylsuccinate Tablet by HPLCELSD
LI Zhide,ZHANG Caiyun,WANG Xia(Ezhou Center for Food and Drug Control,Hubei Ezhou 436099,China)
OBJECTIVE:To establish a method for the content determination of erythromycin ethylsuccinate in Erythromycin ethylsuccinate tablet.METHODS:The column of Dikma-C18with mobile phase of acetonitrile-0.05%diethylamine(70∶30,V/V)at a flow rate of 1.0 ml/min,column temperature was 30℃,and the sample size was 10 μl.RESULTS:The linear range of erythromycin ethylsuccinate was 1.216-7.296 μg(r=0.999 2);limit of quantitation was 0.304 μg,the limits of detection was 0.076 μg,respectively;the RSDs of precision,stability and reproducibility tests were no more than 2.0%,the average recoveries was 97.59%-104.19%(RSD=1.71%,n=6).CONCLUSIONS:The method is simple and accurate with high sensitivity and reproducibility,and can be used for the content determination of Erythromycin ethylsuccinate tablet.
Erythromycin ethylsuccinate tablet;HPLC;Erythromylin ethyisuccinate;Content determination
R917
A
1001-0408(2016)33-4744-03
2015-11-30
2016-05-16)
*副主任技师。研究方向:抗菌药物及中药检验。电话:0711-3863027。E-mail:Lzd-5@163.com
DOI 10.6039/j.issn.1001-0408.2016.33.46

