HPLC法同时测定藏药独一味中山栀苷甲酯、木犀草素、芹菜素的含量
乙永林,孙连先(1.连云港市疾病预防控制中心,江苏连云港 003;.连云港市第二人民医院,江苏 连云港 03)
HPLC法同时测定藏药独一味中山栀苷甲酯、木犀草素、芹菜素的含量
乙永林1*,孙连先2(1.连云港市疾病预防控制中心,江苏连云港 222003;2.连云港市第二人民医院,江苏 连云港 222023)
目的:建立同时测定独一味中山栀苷甲酯、木犀草素、芹菜素含量的方法。方法:采用高效液相色谱法。色谱柱为Diamonds C18,流动相为乙腈-0.1%磷酸溶液(梯度洗脱),流速为1.0 ml/min,检测波长为238 nm(山栀苷甲酯)、348 nm(木犀草素、芹菜素),柱温为25℃,进样量为10 μl。结果:山栀苷甲酯、木犀草素、芹菜素检测质量浓度线性范围分别3.08~308 μg/ml(r=0.999 8)、3.72~372 μg/ml(r=0.999 9)、2.92~292 μg/ml(r=0.999 9);精密度、稳定性、重复性试验的RSD<3.0%;加样回收率分别为95.38%~103.15%(RSD=1.85%,n=9)、96.05%~102.66%(RSD=2.07%,n=9)、95.49%~103.59%(RSD=2.18%,n=9)。结论:该方法操作简便,精密度、稳定性、重复性好,可用于独一味中山栀苷甲酯、木犀草素、芹菜素含量的同时测定。
独一味;山栀苷甲酯;木犀草素;芹菜素;含量;高效液相色谱法
独一味为唇形科植物独一味Lamiophlomis rotate(Benth.)Kudo的干燥地上部分[1],藏语又称“大巴”“打布巴”,在我国四川、青海、甘肃、西藏等地区广泛分布,常于9~10月采收,以根及根状茎入药,味苦,微寒,有小毒,可补髓、止血[2]。临床上主要用于急性软组织损伤、关节炎、腰椎间盘突出等症的治疗。
独一味含有多种有效成分,如黄酮类、环烯醚萜苷类、苯乙醇苷类、总环烯醚萜苷等,其中黄酮类成分和苯乙醇苷类成分具有良好的镇痛作用[3];环烯醚萜苷类具有显著的抗炎作用[4-5];总环烯醚萜苷具有吸水特性,因此对小鼠断尾出血、兔腹主动脉出血、兔耳中动脉出血和大鼠肝脏组织损伤出血有很好的止血作用[6-8]。近年来,由于对独一味的需求日益加大,其质量控制标准也日趋严格,因此笔者采用高效液相色谱法(HPLC)建立同时测定其中独一味中山栀苷甲酯、木犀草素、芹菜素含量的方法,以为独一味药材的质量标准研究提供参考。
1 材料
1.1 仪器
600型HPLC仪,包括2487双通道紫外检测器、Millennium32色谱工作站(美国Waters公司);BS224S型分析天平(德国Satorius公司)。
1.2 试剂
山栀苷甲酯对照品(批号:111873-201101,纯度>98%)、木犀草素对照品(批号:111520-201204,纯度>98%)、芹菜素对照品(批号:111901-201205,纯度>98%)均购自中国食品药品检定研究院;乙腈、磷酸为色谱纯,其余试剂均为分析纯,水为纯化水。
1.3 药材
独一味药材购自南京医科大学附属淮安第一医院中药房,由连云港市第二人民医院孙连先副主任中药师鉴定为真品。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:Diamonds C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸溶液(B,含1 mmol/L十六烷基三甲基溴化铵),梯度洗脱(0~12 min,10%A;12~20 min,10%→18.5% A);检测波长:238 nm(山栀苷甲酯)、348 nm(木犀草素、芹菜素);流速:1.0 ml/min;柱温:25℃;进样量:10 μl。记录色谱,详见图1。在上述色谱条件下,理论板数以山栀苷甲酯、木犀草素、芹菜素峰计分别为4 500、5 200、6 500;各成分基线分离良好,分离度>1.5。
2.2 溶液的制备
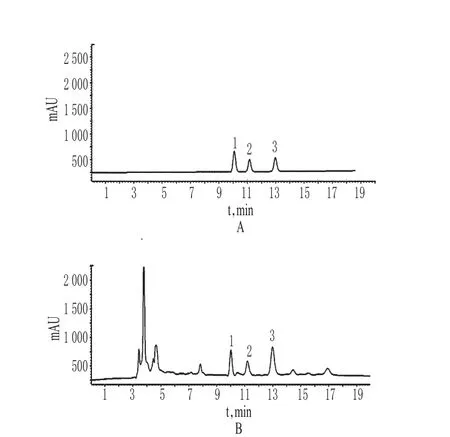
图1 高效液相色谱图A.混合对照品;B.供试品;1.山栀苷甲酯;2.木犀草素;3.芹菜素;Fig 1 HPLC chromatogramsA.mixed reference substance;B.test sample;1.dipsacoside;2.luteolin;3. apigenin
2.2.1 混合对照品溶液 称取减压干燥至恒质量的山栀苷甲酯、木犀草素、芹菜素对照品适量,加60%甲醇制成山栀苷甲酯、木犀草素、芹菜素质量浓度分别为0.308、0.372、0.292 mg/ml的混合对照品溶液。
2.2.2 供试品溶液 取样品药材粉末(过2号筛)约0.5 g,精密称定,加60%甲醇40 ml,称定质量,回流提取60 min,冷却后以60%甲醇补足减失的质量,摇匀,静置,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.3 线性关系考察
精密量取“2.2.1”项下混合对照品溶液1 ml,分别加60%甲醇稀释至100、80、60、40、20、1 ml,制成系列混合对照品溶液。精密量取上述系列混合对照品溶液各10 μl,按“2.1”项下色谱条件进样测定,记录峰面积。以山栀苷甲酯、木犀草素、芹菜素质量浓度(x,μg/ml)为横坐标、峰面积(y)为纵坐标进行线性回归,得山栀苷甲酯、木犀草素、芹菜素回归方程分别为y=16.379x+0.461 2(r=0.999 8)、y=22.435x+0.396 4(r=0.999 9)、y=38.598x+0.528 6(r=0.999 9)。结果表明,山栀苷甲酯、木犀草素、芹菜素检测质量浓度线性范围分别为3.08~308、3.72~372、2.92~292 μg/ml。
2.4 精密度试验
取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,山栀苷甲酯、木犀草素、芹菜素峰面积的RSD分别为1.52%、2.07%、2.75%(n=6),表明仪器精密度良好。
2.5 稳定性试验
取“2.2.2”项下供试品溶液适量,分别于室温下放置0、2、4、8、10、12 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,山栀苷甲酯、木犀草素、芹菜素峰面积的RSD分别为1.61%、2.07%、1.82%(n=6),表明供试品溶液在12 h内基本稳定
2.6 重复性试验
精密称取同一批样品适量,按“2.2.2”项下方法制备供试品溶液,共6份,再按“2.1”项下色谱条件进样测定,记录峰面积并计算含量。结果,山栀苷甲酯、木犀草素、芹菜素的平均含量分别为4.683、8.457、3.274 mg/g,RSD分别为1.32%、1.87%、2.43%(n=6),表明本方法重复性良好。
2.7 加样回收率试验
取已知含量样品适量,共6份,分别加入高、中、低质量的山栀苷甲酯、木犀草素、芹菜素对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表1。
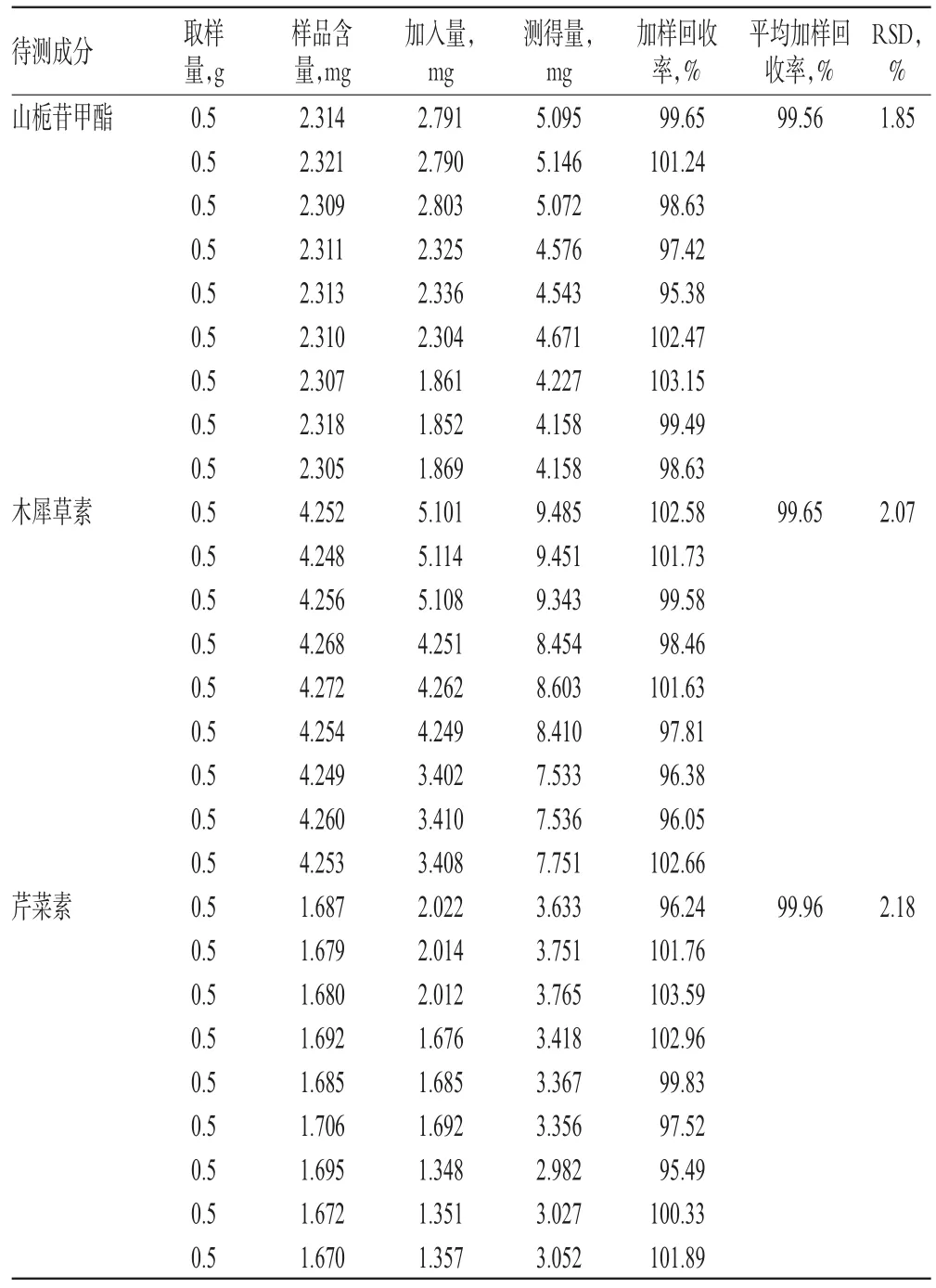
表1 加样回收率试验结果(n=9)Tab 1 Results of recovery test(n=9)
2.8 样品含量测定
取样品各适量,分别按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算样品含量,结果见表2。
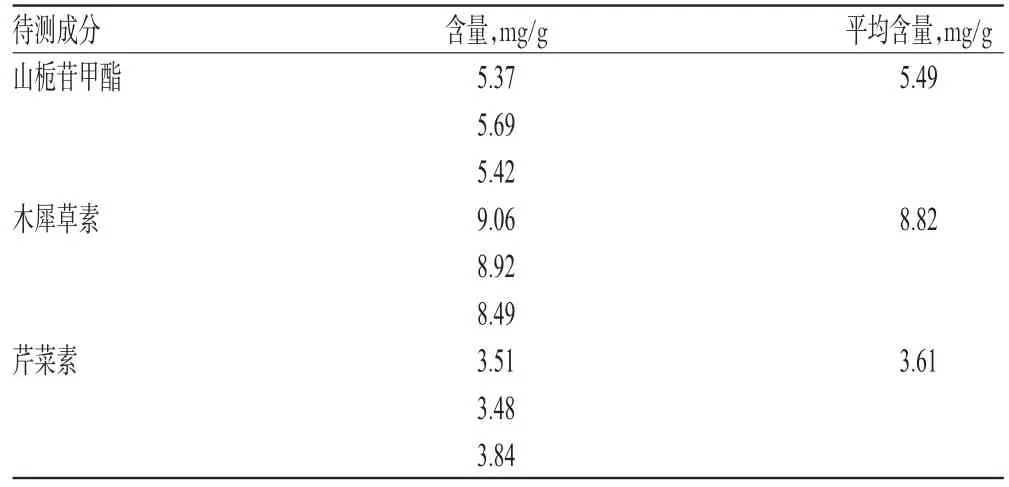
表2 样品含量测定结果(n=3)Tab 2 Results of contents determination of samples(n=3)
3 讨论
3.1 流动相的考察
黄酮类成分大多含有酚羟基,极性较大,且容易以离子形式存在,色谱峰容易拖尾且保留值太小。因此,本试验在流动相中加入了十六烷基三甲基溴化铵离子对试剂,使样品离子在流动相中与离子对试剂的反离子生成无荷电的疏水性离子对,从而改善峰形和分离度。
3.2 检测波长的考察
笔者分别对3个被测成分进行190~400 nm全波长扫描,结果表明,山栀苷甲酯最大吸收波长为238 nm,木犀草素最大吸收波长为254、354 nm,芹菜素最大吸收波长为258、342 nm,由于在238 nm波长处木犀草素和芹菜素的含量很低,而348 nm波长处可更好地测定木犀草素和芹菜素的含量,因此本试验设置两个波长来检测3个成分的含量。
3.3 供试品提取方法的考察
在预试验中,笔者分别考察了不同提取方式(水回流提取法、水提醇沉提取法)、不同体积分数甲醇(100%、80%、60%、40%)、不同料液比(1∶160、1∶80、1∶40、1∶20)和不同提取时间(30、60、90 min)。结果表明,0.5 g药材粉末中加60%甲醇40 ml,回流提取60 min时有效成分含量较高。
综上所述,本方法操作简便,精密度、稳定性、重复性好,可用于独一味中山栀苷甲酯、木犀草素、芹菜素含量的同时测定。
[1] 国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:262.
[2] 青海高原生物研究所植物室.青藏高原药物图鉴[M].西宁:青海人民出版社,1978:108.
[3] 张凤,孙连娜,陈万生.不同产地独一味中苯乙醇苷类的含量测定与品质评价[J].中国中药杂志,2008,33(11):1 346.
[4] 朱斌,龚念,彭崇胜,等.独一味镇痛作用及其有效成分研究[J].中国药理学与毒理学杂志,2012,26(3):442.
[5] Zhang F,Wu ZJ,Sun LN,et al.Iridoid glucosides and a C13-norisoprenoid from Lamiophlomis rotata and their effects on NF-κ B activation[J].Bioorg Med Chem Lett,2012,22(13):4 447.
[6] 汪茜,孙秋艳,杨婷,等.独一味巴布膏抗炎作用研究[J].中药药理与临床,2010,26(1):49.
[7] 张泉龙,邱建国,李茂星,等.独一味环烯醚萜苷外用止血作用研究[J].医药导报,2011,30(7):877.
[8] Li M,Jia Z,Hu Z,et al.Experimental study on the hemostatic hemostatic activity of the Tibetan medicinal herb Lamiophlomis rotate[J].Phytother Res,2008,22(6):759.
(编辑:张 静)
Simultaneous Determination of Dipsacoside B,Luteolin and Apigenin in Zang Medicine Lamiophlomis rotata by HPLC
YI Yonglin1,SUN Lianxian2(1.Center for Disease Control and Prevention of Lianyungang,Jiangsu Lianyungang 222003,China;2.The Second People's Hospital of Lianyungang,Jiangsu Lianyungang 222023,China)
OBJECTIVE:To establish a method for the contents determination of dipsacoside B,luteolin and apigenin in Zang medicine Lamiophlomis rotata.METHODS:HPLC was performed on the column of Diamonds C18with mobile phase of acetonitrile-0.1%phosphoric acid solution(gradient elution)at a flow rate of 1.0 ml/min,detection wavelength was 238 nm for dipsacoside B,348 nm for luteolin and apigenin,column temperature was 25℃,and injection volume was 10 μl.RESULTS:The linear range was 3.08-308 μg/ml for dipsacoside B(r=0.999 8),3.72-372 μg/ml for luteolin(r=0.999 9)and 2.92-292 μg/ml for apigenin(r=0.999 9);RSDs of precision,stability and reproducibility tests were lower than 3.0%;recoveries were 95.38%-103.15%(RSD=1.85%,n=9),96.05%-102.66%(RSD=2.07%,n=9)and 95.49%-103.59%(RSD=2.18%,n=9).CONCLUSIONS:The method is simple with good precision,stability and reproducibility,and can be used for the simultaneous determination of dipsacoside B,luteolin and apigenin in Zang medicine L.rotata.
Lamiophlomis rotata;Dipsacoside B;Luteolin;Apigenin;Content;HPLC
R927
A
1001-0408(2016)33-4733-03
2016-06-22
2016-09-13)
*副主任药师。研究方向:医院药学。E-mail:lygyyl@sina.com
DOI 10.6039/j.issn.1001-0408.2016.33.42

