石柑子药材的HPLC指纹图谱研究Δ
罗文汇,刘布鸣,彭丽诗,邱宏聪,陈 昭,江洁怡(1.广东省中医药工程技术研究院,广州 510095;2.广东省中医药研究开发重点实验室,广州 510095;.广西壮族自治区中医药研究院,南宁 50022;.广东仙乐制药有限公司,广东汕头 51501)
石柑子药材的HPLC指纹图谱研究Δ
罗文汇1,2*,刘布鸣3,彭丽诗4,邱宏聪3,陈 昭1,2,江洁怡1,2(1.广东省中医药工程技术研究院,广州 510095;2.广东省中医药研究开发重点实验室,广州 510095;3.广西壮族自治区中医药研究院,南宁 530022;4.广东仙乐制药有限公司,广东汕头 515041)
目的:建立石柑子药材的高效液相色谱(HPLC)指纹图谱。方法:采用HPLC法。色谱柱为Thermo Hypersil ODS-2,流动相为甲醇-0.4%磷酸溶液(梯度洗脱),流速为1.0 ml/min,检测波长为300 nm,柱温为30℃,进样量为10 μl。以阿魏酰酪胺色谱峰为参照峰,测定24批药材的HPLC图谱,采用《中药色谱指纹图谱相似度评价系统》(2004A版)进行共有峰鉴定和相似度评价。结果:24批石柑子药材有16个共有峰,其中21批药材的相似度>0.8。结论:该研究所建指纹图谱专属性强、结果稳定,可为石柑子药材的质量控制提供依据。
石柑子;高效液相色谱法;指纹图谱
石柑子为南方地区习用中草药,为天南星科石蒲藤Pothos chienesis(Raf.)Merr.的干燥全草,主要分布于广东、广西、台湾等省区。具有行气止痛、消积除胀、祛风除湿、散瘀解毒的功效,多用于治疗心胃气痛、疝气、小儿疳积、食积腹胀、晚期血吸虫病、肝脾肿大、风湿痹痛、脚气肿痛、跌打损伤、骨折、聤耳流脓、鼻渊等症[1-2]。现代研究发现,石柑子含有苷类、生物碱、黄酮、蒽醌、香豆素、萜类内酯、甾体、三萜类、糖类、有机酸、氨基酸、蛋白质、挥发油和油脂类等化合物[3-6]。因此,笔者采用高效液相色谱法(HPLC)建立了石柑子药材的指纹图谱[7-8]分析方法,旨在为有效控制其质量提供科学依据。
1 材料
1.1 仪器
e2695-2489型HPLC仪,包括PAD二极管阵列检测器、四元梯度泵、Empower2数据处理软件系统(美国Waters公司);Advantage A10超纯水系统(美国Millipore公司);XS205DU型电子分析天平(瑞士Mettler-Toledo公司);KQ5200DE型数控超声波清洗器(昆山市超声仪器有限公司,功率:250 W,频率:40 kHz);HH-8型数显恒温水浴锅(金坛市科析仪器有限公司)。
1.2 试剂
阿魏酰酪胺对照品(笔者自制,经H谱、C谱和质谱确定结构,经HPLC测定纯度≥99.5%);丁香酸对照品(笔者自制,经H谱、C谱和质谱确定结构,经HPLC测定纯度≥99.0%);香草酸对照品(成都瑞芬思生物科技有限公司,批号:X-030-140801,纯度>98%);甲醇为色谱纯,其余试剂均为分析纯,水为超纯水。
1.3 药材
石柑子药材均由广西壮族自治区中医药研究院提供(见表1),经该院赖茂祥研究员鉴定为真品。
2 方法与结果
2.1 色谱条件
色谱柱:Thermo Hypersil ODS-2(250 mm×4.6 mm,5 μm);流动相:甲醇(A)-0.4%磷酸溶液(B),梯度洗脱(洗脱程序见表2);流速:1.0 ml/min;检测波长:300 nm;柱温:30℃;进样量:10 μl。

表1 石柑子药材来源Tab 1 Origin of Pothos chinensi

表2 梯度洗脱程序Tab 2 Gradient elution program
2.2 溶液的制备
2.2.1 混合对照品溶液 精密称定阿魏酰酪胺、丁香酸、香草酸对照品适量,加50%甲醇制成阿魏酰酪胺、丁香酸、香草酸质量浓度分别为60.42、120.14、71.25 μg/ml的混合对照品溶液,过0.45 μm微孔滤膜,取续滤液,即得。
2.2.2 供试品溶液 取本品粉末(过4号筛)约2 g,精密称定,置于具塞锥形瓶中,精密加入50%甲醇25 ml,称定质量,超声处理30 min,放冷,再次称定质量,用50%甲醇补足减失的质量,滤过,精密量取续滤液10 ml,蒸干,残渣加50%甲醇溶解并定容至2 ml,过0.45 μm微孔滤膜,取续滤液,即得。
2.3 方法学考察
2.3.1 精密度试验 取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件连续进样测定6次,以阿魏酰酪胺峰的保留时间和峰面积为参照,记录各共有峰相对保留时间和相对峰面积。结果,各共有峰相对保留时间的RSD<1%,相对峰面积的RSD<2%(n=6),表明仪器精密度良好。
2.3.2 稳定性试验 取“2.2.2”项下供试品溶液(编号:S20)适量,分别于室温下放置0、2、4、8、16、24 h时按“2.1”项下色谱条件进样测定,以阿魏酰酪胺峰的保留时间和峰面积为参照,记录各共有峰相对保留时间和相对峰面积。结果,各共有峰相对保留时间和相对峰面积的RSD均<3%(n=6),表明供试品溶液在24 h内基本稳定。
2.3.3 重复性试验 精密称取同一批样品(编号:S20)适量,按“2.2.2”项下方法制备供试品溶液,共6份,再按“2.1”项下色谱条件进样测定,以阿魏酰酪胺峰的保留时间和峰面积为参照,记录各共有峰相对保留时间和相对峰面积。结果,各共有峰相对保留时间和相对峰面积的RSD均<3%(n=6),表明本方法重复性良好。
2.4 指纹图谱的建立及共有峰的指认
2.4.1 指纹图谱的建立 取24批石柑子药材粉末适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,得特征指纹图谱,详见图1。

图1 24批石柑子药材的高效液相色谱叠加图Fig 1 HPLC overlay chromatograms of 24 batches of P.chienesis
2.4.2 石柑子对照图谱的生成 采用国家药典委员会颁布的《中药色谱指纹图谱相似度评价系统》(2004 A版),选取时间窗宽度为0.1 min,以中位数生成对照谱图,经过多点校正后自动匹配,生成石柑子指纹图谱共有模式,并计算24批石柑子药材的指纹图谱与该共有模式的相似度。结果表明,24批石柑子药材共有特征峰16个,其中2号峰为香草酸,3号峰为丁香酸,11号峰为阿魏酰酪胺;由于阿魏酰酪胺色谱峰出峰时间居中且稳定,与相邻峰分离良好,特征明显,因此选择阿魏酰酪胺色谱峰为参照峰,详见图2。
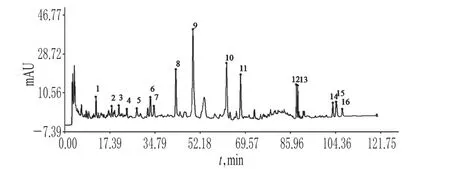
图2 24批石柑子药材的高效液相色谱共有峰Fig 2 HPLC chromatograms of the common peaks 24 batches of P.chienesis
2.4.3 相对保留时间和相对峰面积分析 采用《中药色谱指纹图谱相似度评价系统》(2004 A版)对24批石柑子药材的色谱进行比较分析。24批石柑子药材指纹图谱相对保留时间和相对峰面积见表3、表4。
2.4.4 相似度分析 采用《中药色谱指纹图谱相似度评价系统》(2004 A版)对24批石柑子药材的色谱进行比较分析。结果,24批药材中,12批样品的相似度在0.9以上,9批样品的相似度在0.8~0.9之间,其余3批样品的相似度在0.7~0.8之间(见表5)。对相似度在0.8以下的3批样品进行分析,11号样品中茎的部分较多而叶的部分较少,从而导致化学成分有所不同,共有峰较少;12号样品生长年限较短,叶片较幼嫩,叶绿素较多,成分富集不够;22号样品在贮存过程中有少量霉变,可能导致部分成分发生变化。由此表明,石柑子药材的质量受到生长年限、采收加工和贮存条件等诸多因素的影响。
3 讨论
本研究收集的24批石柑子药材均采自广西瑶族山区或购买于广西当地药材市场,具有良好的道地性和代表性。通过对流动相体系、色谱柱、检测波长、柱温和流速以及供试品提取方法、提取溶剂和提取时间进行优选,最终确定了石柑子HPLC指纹图谱方法。经方法学考察,结果符合要求。

表3 24批石柑子药材的指纹图谱共有峰相对保留时间Tab 3 Relative retention time of fingerprint common peaks of the 24 batches of P.chinensi
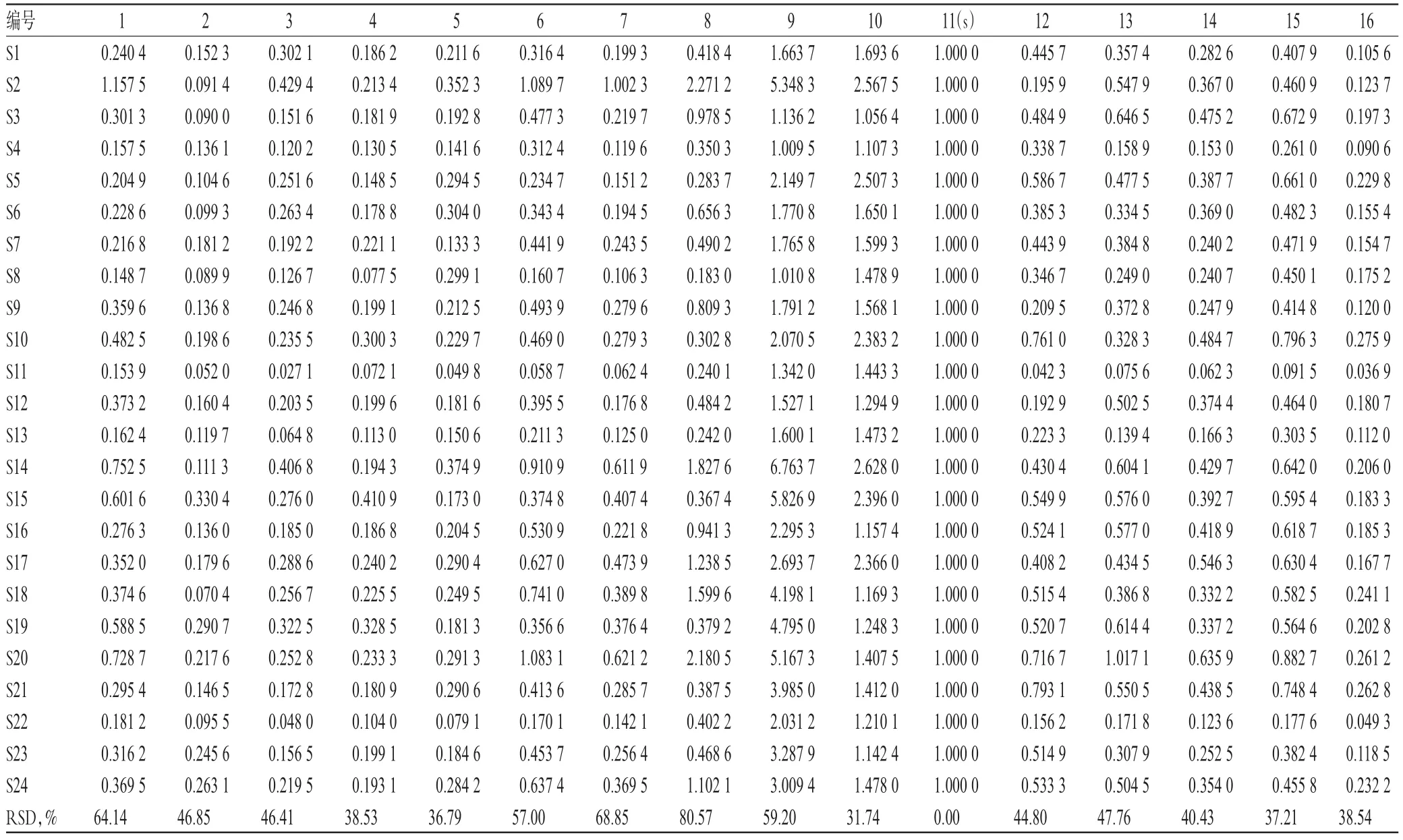
表4 24批石柑子药材的指纹图谱共有峰相对峰面积Tab 4 Relative peak areas of fingerprint common peaks of the 24 batches of P.chinensi
笔者采用上述方法,确定了石柑子药材的16个共有峰,通过与对照品图谱的比对,指认了其中2、3和11号色谱峰,分别为香草酸、丁香酸和阿魏酰酪胺。由于β-谷甾醇的最大吸收波长在200 nm附近,在300 nm波长处无紫外吸收,故β-谷甾醇的色谱峰在指纹图谱上未显示。
中药色谱指纹图谱相似度评价系统在共有模式的生成过程中有中位数和平均数两种计算方法,笔者发现对于同一种样品而言,两种计算结果有一定的区别。因为所采药材均为天然产物,受海拔、气候、生长条件等自然因素影响,各批次间差异较大。对于个别差异过大的样品应该降低其在对照图谱生成过程中所占的比例,故认为采用中位数的算法比较合理。
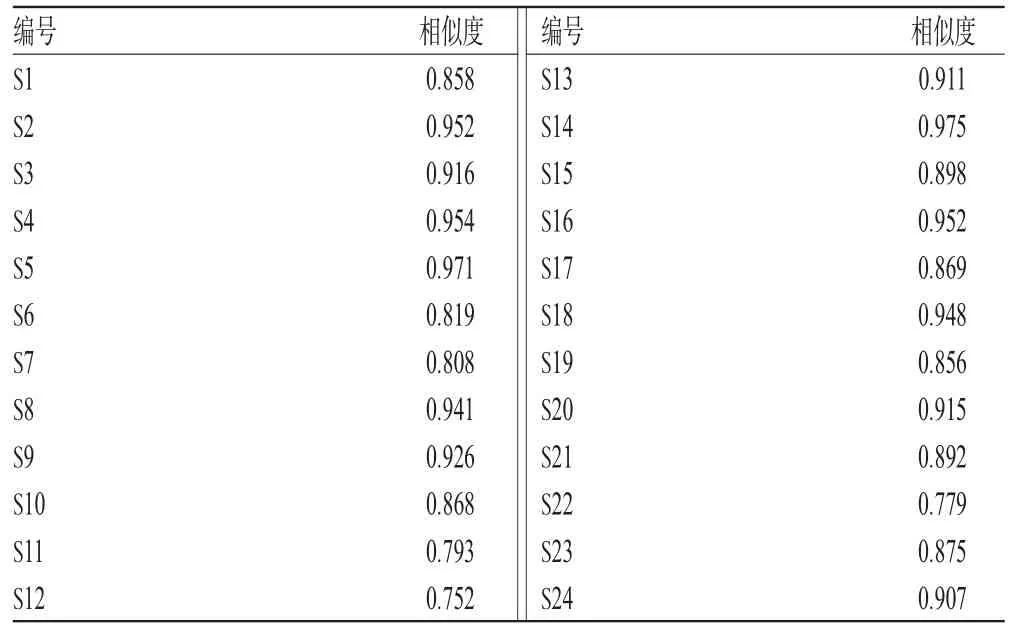
表5 24批石柑子药材相似度评价结果Tab 5 Similarity of fingerprint common peaks of the 24 batches of P.chinensi
通过中药色谱指纹图谱相似度评价软件生成24批石柑子药材HPLC指纹图谱的共有模式,可作为其特征图谱。16个共有峰在24批石柑子药材HPLC指纹图谱中均稳定存在,但各个特征峰的相对含量分布在各批次的石柑子药材之间存在差异。
综上所述,本研究所建指纹图谱专属性强、结果稳定,可为石柑子药材的质量控制提供依据。
[1] 马丽莎,黄诺嘉.石蒲藤的生药学研究[J].今日药学,2008,18(3):36.
[2] 庞声航,余胜民,黄琳芸,等.广西20种传统瑶药抗肿瘤筛选研究[J].广西中医药,2006,29(4):53.
[3] 曾立,杨林,效思,等.瑶药葫芦钻化学成分的初步研究[J].江苏农业科学,2012,40(3):287.
[4] 覃振林,韦海英,廖东燕.柚子枫挥发油化学成分研究[J].时珍国医国药,2012,23(5):1 099.
[5] 尹文清,张岩,宋鑫明,等.石柑子总有机酸的提取工艺与含量测定[J].中药材,2009,32(1):124.
[6] 纪明昌,肖世基,蒋舜媛,等.石柑子的化学成分研究[J].中草药,2015,46(1):28.
[7] 孙庆文,王悦云,徐文芬,等.道地药材黔党参的HPLC指纹图谱研究[J].中国药房,2013,24(7):628.
[8] 孙冬梅,谭志灿,毕晓黎,等.RP-HPLC法同时测定布渣叶中牡荆苷和异牡荆苷的含量[J].中国药房,2013,24(7):630.
Study on the HPLC Fingerprint of Pothos chinensis
LUO Wenhui1,2,LIU Buming3,PENG Lishi4,QIU Hongcong3,CHEN Zhao1,2,JIANG Jieyi1,2(1.Guangdong Provincial Institute of Traditional Chinese Medicine,Guangzhou 510095,China;2.Guangdong Provincial Key Laboratory of R&D in Traditional Chinese Medicine,Guangzhou,510095,China;3.Guangxi Zhuang Autonomous Region Institute of Chinese Medicine and Pharmaceutical Science,Nanning 530022,China;4.Guangdong Sirio Pharma Co.,Ltd.,Guangdong Shantou 515041,China)
OBJECTIVE:To establish the HPLC fingerprint of Pothos chinensis.METHODS:HPLC was performed on the column of Thermo Hypersil ODS-2 with mobile phase of methanol-0.4%phosphoric acid solution(gradient elution)at a flow rate of 1.0 ml/min,detection wavelength was 300 nm,column temperature was 30℃,and injection volume was 10 μl.Using ferulic acid tyramine peak as reference,HPLC spectrum of 24 batches of medicinal herbs was determined,and TCM Chromatographic Fingerprint Similarity Evaluation System(2004 edition)was adopted for common peak identification and similarity evaluation.RESULTS:There were 16 common peaks totally in the 24 batches,similarity of the 21 batches of medicinal materials were higher than 0.8. CONCLUSIONS:The established fingerprint is specific,stable,and can provide basis for quality control of P.chinensis.
Pothos chinensis;HPLC;Fingerprint
R917
A
1001-0408(2016)33-4701-04
2015-12-28
2016-02-25)
(编辑:张 静)
广西中药质量标准研究重点实验室开放课题项目(No.桂中重开201302);广西科学研究与技术开发计划项目(No.桂科重1355001-4-5)
*副主任中药师。研究方向:中药质量评价。电话:020-83482098。E-mail:acid123@126.com
DOI 10.6039/j.issn.1001-0408.2016.33.31

