人工甜味剂在不同类型土壤中的淋溶行为研究
马铃,冯碧婷,周萌,胡宏伟,孙红文,*
1. 南开大学环境科学与工程学院 环境污染过程与基准教育部重点实验室,天津 300350 2. 天津市机动车排污检控中心,天津 300391 3. 天津泰达绿化集团有限公司,天津 300457
人工甜味剂在不同类型土壤中的淋溶行为研究
马铃1,冯碧婷1,周萌2,胡宏伟3,孙红文1,*
1. 南开大学环境科学与工程学院 环境污染过程与基准教育部重点实验室,天津 300350 2. 天津市机动车排污检控中心,天津 300391 3. 天津泰达绿化集团有限公司,天津 300457
人工甜味剂(artificial sweeteners)是一类人工合成或半合成的蔗糖替代品,广泛应用于食品、药物、个人护理品和饲料中,但是大多数人工甜味剂在人和动物体内几乎不被代谢而随尿液和粪便直接进入环境。在天津污水河沿线及甜味剂厂附近不同深度土层中检测到安赛蜜、糖精、甜蜜素和三氯蔗糖。为探讨人工甜味剂在土壤中的移动性及其对地下水污染的风险,应用土柱淋溶实验研究了安赛蜜和三氯蔗糖在2种土壤中的淋溶行为,并观测了人工甜味剂淋溶对土柱淋出液的溶解性有机质(DOM)、pH以及电导率 (EC) 的影响。结果表明安赛蜜和三氯蔗糖在2种土壤中表现出较强的移动性,超过87%的甜味剂均被淋出,只有不到13%的甜味剂被土壤截留或损失,因此对地下水具有较大的风险。安赛蜜和三氯蔗糖能够促进土壤溶解性有机质的溶出,但对淋出液的pH和电导率无显著影响。
人工甜味剂;土壤;淋溶行为
Received 29 November 2015 accepted 26 February 2016
人工甜味剂是一类具有甜味而几乎不被人体代谢的人工合成或半合成的蔗糖替代品,由于其低成本、高甜度、极易溶于水等特性而被广泛应用[1-3]。但是,人工甜味剂对人体的安全性一直备受争议,各国都给出了较严格的规定[4]。大多数人工甜味剂在人和动物体内几乎不被代谢而随尿液和粪便直接进入环境介质[5],而且研究已表明一些人工甜味剂在环境中具有持久性,在环境中的浓度表现出逐渐增高的趋势[2,6]。近年来,几种典型的人工甜味剂(糖精、安赛蜜、甜蜜素和三氯蔗糖)在水体中已广泛被检出且浓度较高[7-11],本课题组也在天津的污水处理厂、地表水、饮用水、降水及地下水中检测到上述4种人工甜味剂[12]。虽然4种典型的人工甜味剂极性强、水溶性高,容易分配到水相中,但仍有研究报道人工甜味剂能够通过污水灌溉、粪肥返田、污泥施肥以及生活垃圾填埋等农业活动进入土壤[13-15]。
目前,有关土壤中人工甜味剂的环境调查研究鲜有报道,仅有少量文献研究了人工甜味剂在土壤中的迁移和降解。研究表明甜蜜素和糖精在土壤中降解较快,半衰期分别为0.8和3.3 d,安赛蜜和三氯蔗糖降解较为缓慢,表现出较强的稳定性[13]。人工甜味剂由于较强的极性而难以吸附在土壤颗粒中,因此,相对稳定的人工甜味剂很可能在土壤中发生淋溶或是在含水层中稳定存在,从而对地下水带来潜在风险。
本研究初步调查了天津市污水河沿线及工业点源附近土壤中不同深度层中甜味剂的污染状况,选取了2种典型的人工甜味剂安赛蜜和三氯蔗糖为实验对象,对其在2种不同类型土壤中的淋滤行为进行了研究,并分析了土壤理化性质对甜味剂淋溶行为的影响。
1 材料与方法(Materials and methods)
1.1 仪器与设备
Agilent 1200系列液相串联6410B三重四级杆质谱(美国Agilent Technologies公司);固相萃取装置(美国Supelco公司);SMADZU TOC-Vcph型TOC分析仪(日本岛津公司)。
1.2 试剂与材料
安赛蜜、糖精、甜蜜素和三氯蔗糖标准品购自美国Sigma-Aldrich公司;3种氘代内标(安赛蜜-d4、糖精-d4和三氯蔗糖-d6)购自加拿大Toronto Research Chemicals公司;离子对试剂Tris (三羟甲基氨基甲烷)购自美国Sigma-Aldrich公司;醋酸铵、醋酸钠、甲醇、乙腈、丙酮均为色谱纯,购自德国CNW Technologies公司,其他试剂氯化钙、石英砂等均为分析纯;Poly-Sery PWAX固相萃取柱(3 mL/60 mg)和50 mL聚丙烯离心管均购自德国CNW Technologies公司;实验全过程采用去离子水。
淋溶装置的主体采用玻璃材质的圆柱型柱子,内径5 cm,高60 cm。
2种供试土壤分别采集于天津市南开区花园和天津市东丽区农田,分别属于粘土和壤粘土,具体理化性质见表1。经风干后的土壤充分混匀,采用四分法,经研磨后过2 mm孔径筛,分别装入外层包有铝箔纸的密封袋中,于-20 ℃保存。
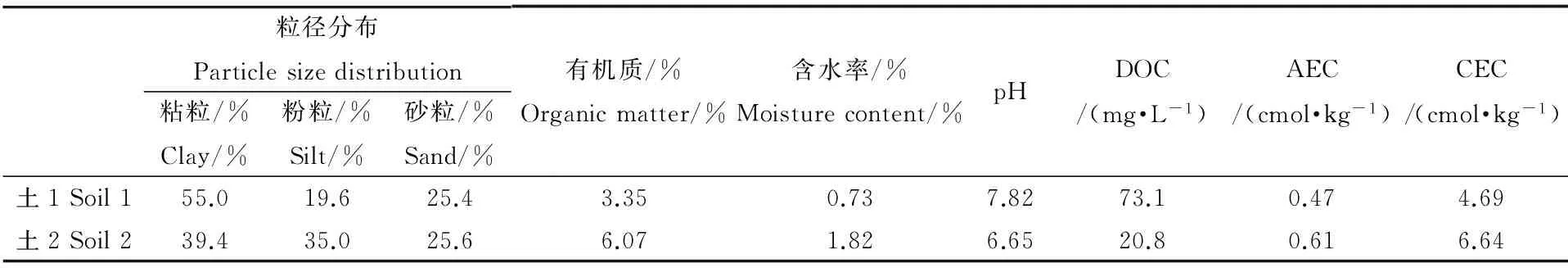
表1 土壤基本理化性质
注:DOC,溶解性有机碳;AEC,阴离子交换容量;CEC,阳离子交换容量。
Note: DOC is an acronym that stands for dissolved organic carbon; ACE is anion exchange capacity; CEC is cation exchange capacity.
1.3 环境调查
在天津污水河沿线及一个人工甜味剂工厂附近共4个采样点采集土壤表层(0~10 cm)及亚表层(10~30 cm)土壤,每个样品均在100 m2地块,按照梅花采样法采集土壤,现场混合,带回实验室。
1.4 实验方法
1.4.1 土柱淋溶实验
通过淋溶试验评价污染物在土壤中的移动性和污染地下水的可能性,具体的试验操作参考经济合作与发展组织(OECD)准则中的土柱淋溶实验方法[16]。将土壤在121 ℃下高压蒸汽灭菌30 min后装柱。土柱的高度为30 cm,下填2 cm玻璃纤维及2 cm石英砂,上面覆盖2 cm石英砂,然后在土柱表层分别加入1 mL 10 mg·L-1三氯蔗糖或安赛蜜的标准使用液,并用铝箔纸包裹避光,静置24 h后开始淋溶实验。
用0.01 mol·L-1氯化钙溶液模拟雨水对土柱进行淋溶,直到淋出液没有目标物检出,同时测定土柱的最大持水量。经测定,土1和土2的最大饱和持水量分别为:275 mL 和300 mL。每淋出25 mL滤液(1个孔体积)为1个采样点,每天可收集3批样品,每个柱子收集40个样品,共1 000 mL淋溶液。本实验淋溶液用量基于天津市近10年年平均降水量(500 mm)计算得出。淋溶速度并不均匀,平均淋溶速度为 0.05 mL·min-1。
1.4.2 吸附平衡常数(Kd)值的测定
准确称取1.5 g土壤样品于50 mL聚丙烯离心管中,加入15 mL 0.01 mol·L-1氯化钙溶液(溶液中分别含有100 μg·L-1安赛蜜/三氯蔗糖标准液),于(25±0.5) ℃下进行恒温振荡24 h (经吸附动力学预实验测得,2种人工甜味剂在6 h后均已达到吸附平衡)。在4 200 r·min-1转速下离心10 min,取1 mL上清液再于15 000 r·min-1转速下离心10 min。取200 μL上清液,并加入200 μL对应的氘带内标,用Vortex混合均匀后,测定人工甜味剂含量。吸附量由差值法获得,Kd值由土壤吸附态浓度Qe(μg·kg-1)与溶液平衡态浓度Ce(μg·L-1)的比值计算。
1.5 测定方法与实验数据分析
1.5.1 样品中人工甜味剂的分析测定
水样:取1 mL淋出液,于15 000 r·min-1转速下离心10 min。取100 μL上清液于进样瓶中,同时加入100 μL对应的氘带内标溶液(80 μg·L-1三氯蔗糖-d6、40 μg·L-1糖精-d4和40 μg·L-1安赛蜜-d4),充分混合,供HPLC-MS/MS测定。
土壤样品:土壤样品经冷冻干燥后,研磨,过0.2 mm孔径筛。准确称取5 g土壤样品,加入10 μL对应的氘带内标溶液(2 mg·L-1三氯蔗糖-d6,1 mg·L-1糖精-d4和1 mg·L-1安赛蜜-d5)。用25 mL 0.01 mol·L-1醋酸钠溶液(pH=4)进行提取,提取2次,每次振荡20 min,合并2次上清液过固相萃取小柱。将洗脱液氮吹至近干,用甲醇定容到0.5 mL,取200 μL浓缩液供HPLC-MS/MS分析测定。固相萃取方法以及液相色谱和质谱条件参考本课题组已建立的方法[17-18],加标回收率及方法检出限和定量限见表2。

表2 土壤中4种人工甜味剂(AS)的加标回收率及方法检出限和定量限
1.5.2 水样中pH、DOC和电导率的测定
水样中pH和电导率的测定方法参照《土壤分析手册》[19];土壤溶解性有机碳(DOC)的提取:用土水比为1:2的纯净水振荡提取16 h,离心,将上清液过0.45 μm的微孔滤膜,采用SMADZU TOC-Vcph型TOC分析进行测定[20]。
1.5.3 数据分析和质量控制
每1处理土柱作2个平行,同时设置空白对照组。淋出液和土壤中人工甜味剂的含量取2个平行样品的算术平均值。数据分析采用Excel处理软件。使用SPSS对数据进行统计学分析,采用Spearman法进行相关性分析。
2 结果(Results)
2.1 人工甜味剂在天津若干土壤中的污染状况
沿天津大沽排污河沿线三3个点(D1~3)及1个甜味剂工厂附近的点位(T)采样,分别采集表层土和亚表层土(图1)。在4个采样点均检测出安赛蜜、糖精和甜蜜素,浓度在0.22~15.57 μg·kg-1之间;而在D1和D2处检出三氯蔗糖,浓度在0.55 ~ 1.38 μg·kg-1之间。糖厂附近糖精和甜蜜素浓度明显高于其他点位,属于点源污染。在同一个点位的亚表层土中人工甜味剂的浓度明显低于表层土。

图1 人工甜味剂在天津大沽排污河沿线(D1-3)及某糖厂(T)附近表层土(A)和亚表层土(B)中的浓度Fig. 1 Concentrations of artificial sweeteners in the topsoil (A) and subsoil (B) at sites along Dagu Drainage Canal (D1-3) and a sugar factory (T) in Tianjin
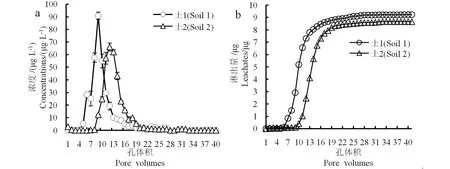
图2 安赛蜜在2种土壤中的(a)相对淋溶曲线及(b)累积淋溶曲线Fig. 2 (a) Relative leaching curves and (b) cumulative leaching curves of acesulfame in the two soils
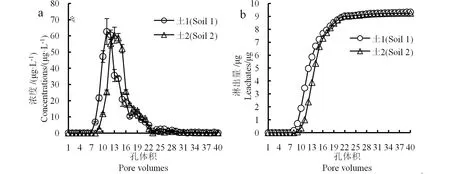
图3 三氯蔗糖在两种土壤中的(a)相对淋溶曲线及(b)累积淋溶曲线Fig. 3 (a) Relative leaching curves and (b) cumulative leaching curves of sucralose in the two soils
2.2 模拟降雨条件下2种土壤中安赛蜜的淋溶行为
由图2(a)可知,土1中,安赛蜜从第4个孔体积(淋滤第2天)开始淋出,第8 ~ 9个孔体积时(第3天)淋出浓度达到最大值(94.8 μg·L-1),到第21个孔体积时(第7天)已有90%的安赛蜜被淋出(图2(b)),并且安赛蜜从开始淋出到淋出液浓度降至1 μg·L-1以下,共经过17个孔体积的时间。土2中,安赛蜜从第9个孔体积(第3天)开始淋出,到第13 ~ 14个孔体积(第5天)淋出浓度达到最大值(66.1 μg·L-1),在第33个孔体积时(第11天)淋出液浓度降至1 μg·L-1以下,共经过24个孔体积的时间。由图2(b)可知,安赛蜜在土1中的淋出总量较大,共有9.24 μg (92.4%)被淋出,说明其在土壤中的移动性更强。
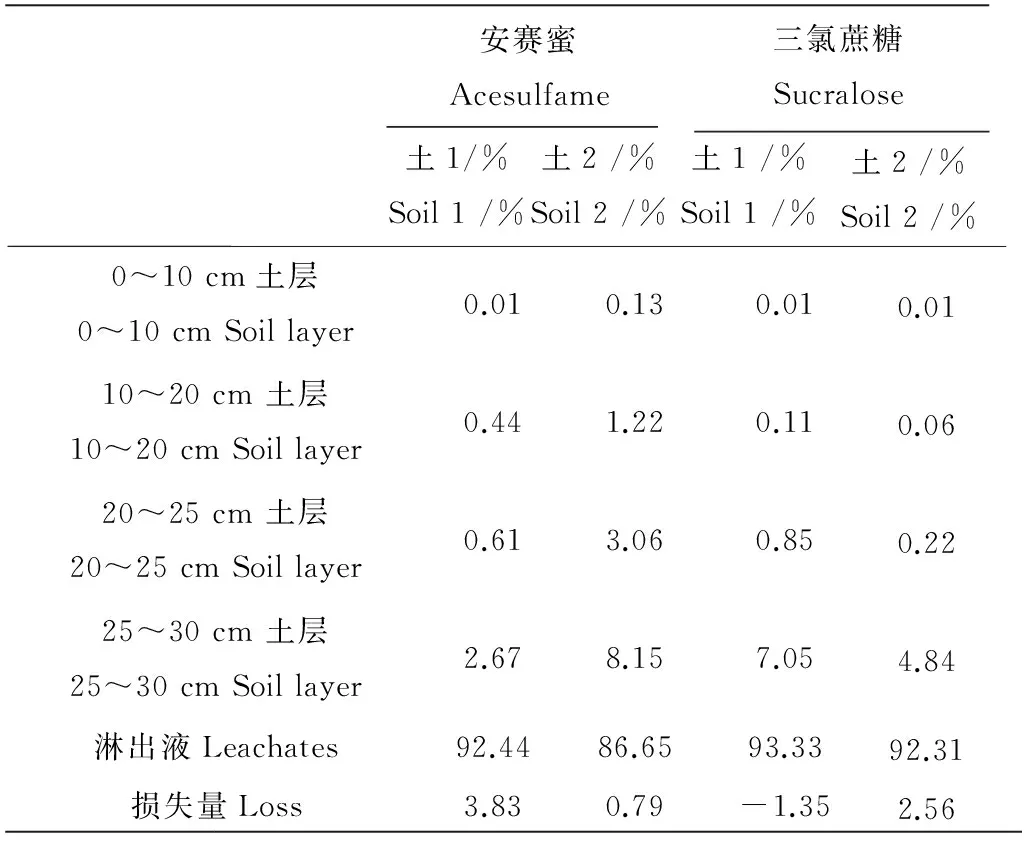
表3 实验结束时2种人工甜味剂在不同深度土壤及淋出液中的分布
此外,对淋溶体系中安赛蜜进行了质量平衡计算(表3),对于土1,高达92.44%的安赛蜜被淋出,只有3.73%的安赛蜜被土壤截留,大约有3.83%的安赛蜜损失;而土壤中残留的安赛蜜主要存在于土壤下层(25~30 cm段)。土2中,淋出液和土柱中的安赛蜜总回收率高达99.21%,损失的安赛蜜仅占加入量的0.79%。
2.3 模拟降雨条件下2种土壤中三氯蔗糖的淋溶行为
由图3(a)可知,土1中,三氯蔗糖从第7个孔体积(淋滤第3天)开始淋出,在第11 ~12个孔体积(第4天)时淋出浓度达到最大值(62.7 μg·L-1),之后到第30个孔体积(第10天)时淋出液浓度降至1 μg·L-1以下。类似地,对于土柱2,三氯蔗糖也从第7个孔体积(淋滤第3天)开始淋出,到第13 ~ 14个孔体积(第5天)时淋出浓度达到最大值(60.4 μg·L-1),并在第28个孔体积(第10天)时淋出液浓度降至1 μg·L-1以下。由图3(b)可知,三氯蔗糖在2种土壤中的总淋出量和淋溶速率相近,土2略慢于土1。
同样对淋溶体系中三氯蔗糖进行了质量平衡计算(表3),土1中93.33%的三氯蔗糖被淋出,仅6.67%的三氯蔗糖被土壤截留或损失;土2中,92.31%的三氯蔗糖被淋出,大约5.13%的三氯蔗糖被土壤截留,最终损失2.56%的三氯蔗糖。土壤中残留的三氯蔗糖同样存在于土壤下层(25~30 cm段)。
2.4 人工甜味剂的Kd值及其对土柱淋出液理化性质的影响
为解释人工甜味剂在土壤中的移动性,实验中采用单点法测定了安赛蜜和三氯蔗糖在2种土壤中的吸附常数(Kd)值。结果显示,安赛蜜在土1和土2中的Kd值分别为4.24和13.7 L·kg-1,三氯蔗糖在2种土壤中的Kd值分别为1.38和2.28 L·kg-1。
同时测定了淋出液的DOC、pH及EC值,以考察甜味剂淋出对土壤溶液理化性质的影响。对于未添加安赛蜜的土柱(图4a),淋出液中DOC随孔体积的增加呈现降低的趋势;而在添加了安赛蜜的土柱淋出液中,DOC呈现出先增大后降低的趋势,最终降到与未添加安赛蜜的土柱相似的浓度水平。经统计学分析,添加了安赛蜜的土柱淋出液的DOC随孔体积的变化与安赛蜜随孔体积的变化之间存在显著相关性(P<0.05),因此可以推测,土壤中的安赛蜜的淋溶带动了溶解性有机质的溶出。为了验证实验结果,本研究还进行了摇瓶实验,实验结果发现,对于空白对照体系,其上清液中DOC的平均浓度为10.0 mg·L-1;对于添加了安赛蜜的体系,其上清液中DOC的平均浓度为42.2 mg·L-1,约为空白组上清液中DOC浓度的4倍。该实验结果再次验证了安赛蜜能够促进土壤溶解性有机质的溶出。
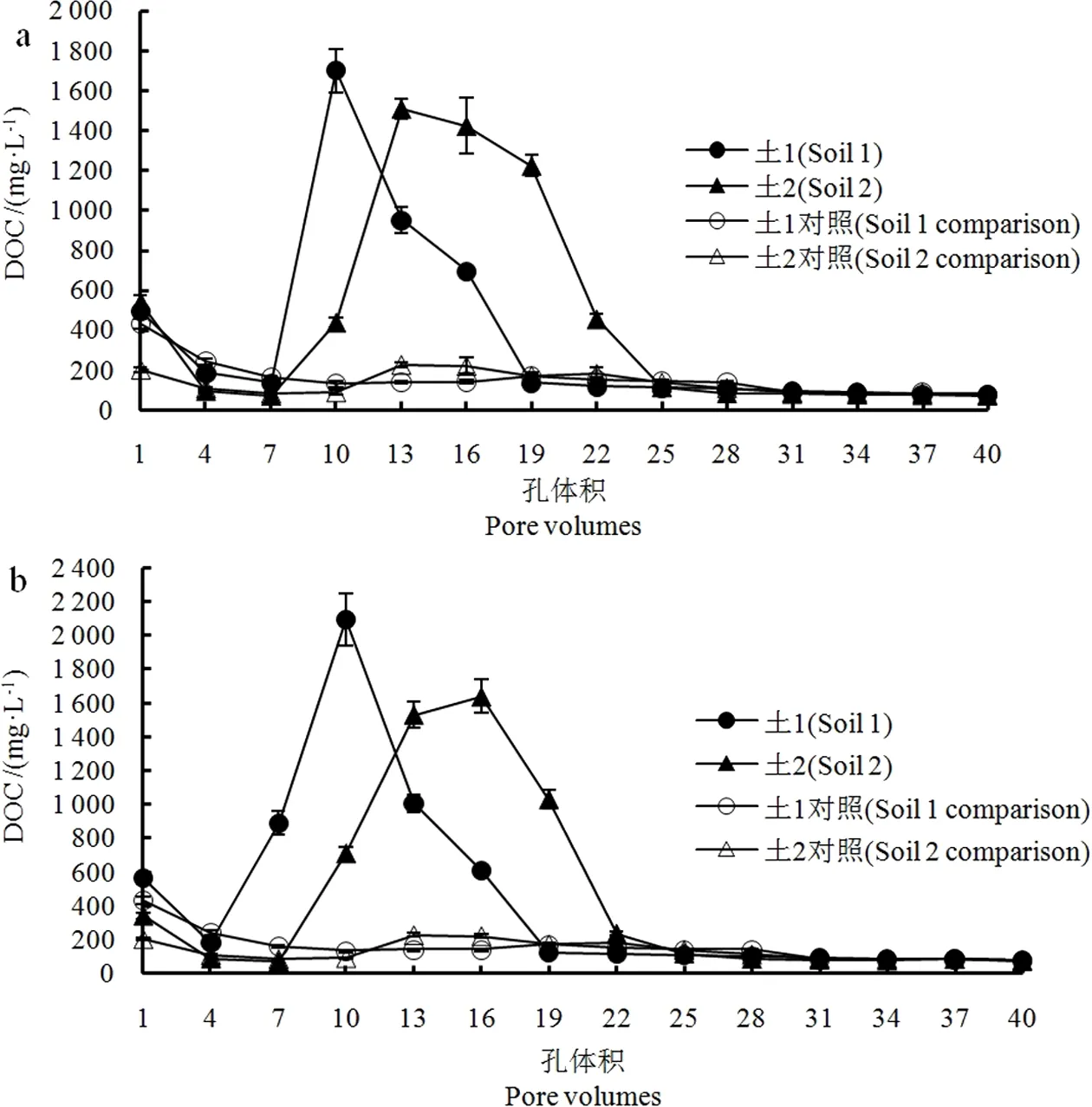
图4 在添加和未添加(a)安赛蜜或(b)三氯蔗糖的条件下,土柱淋出液中DOC的浓度变化Fig. 4 Concentrations of DOC in leachates from soil columns with and without (a) acesulfame and (b) sucralose
对三氯蔗糖而言,添加组与空白组中淋出液DOC随孔体积的变化趋势(图4b)与安赛蜜相似,且在统计学上,添加三氯蔗糖的土柱淋出液DOC随孔体积的变化曲线与三氯蔗糖的淋溶穿透曲线之间存在显著相关性(P<0.05),因此土壤中三氯蔗糖的淋溶带动了溶解性有机质的溶出。同样地,摇瓶实验也验证了这一点,对于添加了三氯蔗糖的体系,其上清液中DOC的平均浓度为38.5 mg·L-1,约为空白组上清液中DOC浓度的3.8倍。
本研究还测定了添加及未添加甜味剂,淋出液中pH及电导率(EC)的变化,由于土壤强的缓冲能力,添加甜味剂的实验组与对照组淋出液的pH及EC值没有明显差异(数据未显示)。
3 分析讨论(Analysis and discussion)
土壤调查中主要检测出安赛蜜、糖精和甜蜜素,三氯蔗糖在部分样品中也有检出。人工甜味剂在土壤中的污染水平在文献中很少报道。本文的研究结果表明,污水灌溉及工业点源污染可造成土壤中人工甜味剂的污染。Buerge等[13]研究发现,甜蜜素和糖精在土壤中的降解半衰期较短,分别为0.4~6 d和3~12 d,这可以用来解释结论中亚表层土中甜蜜素和糖精的浓度显著低于表层土。此外,化学物质在不同深度土层中的分布还与其吸附截留和淋溶有关。由于这4种人工甜味剂极性较强(logKow在-1.61~-0.91之间),水溶性较高(Sw在4~283 g·L-1之间),所以稳定性较强的人工甜味剂很有可能向下迁移至地下水。
通过土柱淋溶实验发现安赛蜜和三氯蔗糖均表现出较强的淋溶特性,对地下水具有较大的风险。对于安赛蜜(pKa=2.0,logKow= -1.33,溶解度为270 g·L-1),其分子中含有多个极性基团,而且在实验条件下主要以阴离子形式存在,土壤胶体颗粒带负电,对其具有静电斥力作用,促使其进入孔隙水进行迁移。而土壤中目标化合物的淋溶性取决于该物质在土壤颗粒上的吸附性和在土壤中的溶解性之间的平衡[21]。由此可知上述吸附作用对目标化合物移动性的影响不占主导地位,而阴离子的存在形式可能增加了化合物的溶解性,使其更易分配到水相中。对于三氯蔗糖(pKa=11.8,logKow= -1.0,溶解度为283 g·L-1),它为中性分子,但是存在多个羟基,水溶性较高,所以三氯蔗糖在土1和土2中的淋出量分别达到了93%和92%。另外,用吸附常数值可进一步解释人工甜味剂在土壤中的移动性,相比于其他传统憎水性化合物高达103~105的吸附系数,人工甜味剂的吸附系数很低,在1.38~13.7 L·kg-1之间,具有较强的流动性。而对于土2种安赛蜜的淋出速度和总量都明显低于土1,这主要是因为土2具有较高的有机质含量,较低的DOC含量,因此对于有机污染物具有较大的截留能力[22]。
安赛蜜和三氯蔗糖的淋溶曲线存在一定差异。对于同一种土壤,三氯蔗糖的淋溶曲线不同于安赛蜜。就土1而言,三氯蔗糖淋出时间略晚于安赛蜜,且淋出浓度的最大值低于安赛蜜,但是两者的总淋出量相近,分别为9.3 μg和9.2 μg。而在土壤中检测出三氯蔗糖的含量略高于安赛蜜,这不能完全用Kd值解释,主要可归结为2种化合物与溶解性有机质的交互作用不同。对于土2,三氯蔗糖与安赛蜜的淋出时间和浓度峰值均较为接近,但三氯蔗糖的总淋出量高于安赛蜜。原因是土2种人工甜味剂的Kd值相差一个数量级,因此,2种物质在水土之间的分布差异较为明显,土2截留了5%的三氯蔗糖、12%的安赛蜜。
实验中,安赛蜜和三氯蔗糖的降解损失较少(<4%),印证了文献中安赛蜜和三氯蔗糖在土壤中比较稳定的结论[13]。因此这2种人工甜味剂一旦污染地表土,污染地下水的可能性较大。相比于地表水,目前世界范围内对于地下水的监测尚十分有限。部分研究者在垃圾填埋场、养猪场化肥池(人工甜味剂是猪饲料的添加剂)以及污水管网下游地下水中主要检测出安赛蜜,其最高浓度达到了18 μg L-1,而其它人工甜味剂极易被微生物降解,浓度较低[9-11,23]。另外,本课题组在天津5处地下水中也广泛检测出4种典型的人工甜味剂[12]。针对于土壤及地下水大范围的调查,特别是污染源沿线的调查还有待进一步展开。
[1] Kroger M, Meister K, Kava R. Low-calorie sweeteners and other sugar substitutes: A review of the safety issues [J]. Comprehensive Reviews in Food Science and Food Safety, 2006, 5: 35-47
[2] Lange F, Scheurer M, Brauch H J. Artificial sweeteners - A recently recognized class of emerging environmental contaminants: A review [J]. Analytical and Bioanalytical Chemistry, 2012, 403(9): 2503-2518
[3] Tollefsen K E, Nizzetto L, Huggett D B. Presence, fate and effects of the intense sweetener sucralose in the aquatic environment [J]. Science of the Total Environment, 2012, 438: 510-516
[4] Chattopadhyay S, Raychaudhuri U, Chakraborty R. Artificial sweeteners - A review [J]. Food Science, 2011, 51(4): 611-621
[5] Weihrauch M R, Diehl V. Artificial sweeteners-Do they bear a carcinogenic risk [J]. Annals of Oncology, 2004, 15(10): 1460-1465
[6] Scheurer M, Storck F R, Brauch H J, et al. Performance of conventional multi-barrier drinking water treatment plants for the removal of four artificial sweeteners [J]. Water Research, 2010, 44(12): 3573-3584
[7] Scheurer M, Brauch H J, Lange F T. Analysis and occurrence of seven artificial sweeteners in German waste water and surface water and in soil aquifer treatment (SAT) [J]. Analytical and Bioanalytical Chemistry, 2009, 394(6): 1585-1594
[8] Loos R, Gawlik B M, Boettcher K, et al. Sucralose screening in European surface waters using a solid-phase extraction-liquid chromatography-triple quadrupole mass spectrometry method [J]. Journal of Chromatography A, 2009, 1216(7): 1126-1131
[9] Roy J W, Van Stempvoort D R, Bickerton G. Artificial sweeteners as potential tracers of municipal landfill leachate [J]. Environmental Pollution, 2014, 184(1): 89-93
[10] Robertson W D, Van Stempvoort D R, Solomon D K, et al. Persistence of artificial sweeteners in a 15-year-old septic system plume [J]. Journal of Hydrology, 2013, 477(1): 43-54
[11] Van Stempvoort D R, Robertson W D, Brown S J. Artificial sweeteners in a large septic plume [J]. Ground Water Monitoring and Remediation, 2011, 31(4): 95-102
[12] Gan Z W, Sun H W, Feng B T, et al. Occurrence of seven artificial sweeteners in the aquatic environment and precipitation of Tianjin, China [J]. Water Research, 2013, 47(14): 4928-4937
[13] Buerge I J, Keller M, Buser H R, et al. Saccharin and other artificial sweeteners in soils: Estimated inputs from agriculture and households, degradation, and leaching to groundwater [J]. Environmental Science & Technology, 2011, 45(2): 615-621
[14] Ordonez E Y, Quintana J B, Rodil R, et al. Determination of artificial sweeteners in sewage sludge samples using pressurised liquid extraction and liquid chromatography-tandem mass spectrometry [J]. Journal of Chromatography A, 2013, 1320: 10-16
[15] Oppel J, Broll G, Löffler D, et al. Leaching behaviour of pharmaceuticals in soil-testing-systems: A part of an environmental risk assessment for groundwater protection [J]. Science of the Total Environment, 2004, 328(1-3): 265-273
[16] The Organisation for Economic Co-operation and Development (OECD). Guidelines for the Testing of Chemicials: Leaching in Soil Columns [S]. Paris: OECD, 2004
[17] Gan Z W, Sun H W, Wang R N, et al. A novel solid-phase extraction for the concentration of sweeteners in water and analysis by ion-pair liquid chromatography-triple quadrupole mass spectrometry [J]. Journal of Chromatography A, 2013, 1274(1): 87-96
[18] 冯碧婷, 干志伟, 孙红文, 等. 土壤中典型人工甜味剂的前处理方法优化及高效液相色谱-串联质谱分析[J]. 色谱, 2014, 32(9): 930-935
Feng B T, Gan Z W, Sun H W, et al. Optimization of sample pretreatment method for determination of typical artificial sweeteners in soil by high performance liquid chromatography-tamdem mass spectrometry [J]. Chinese Journal of Chromatography, 2014, 32(9): 930-935 (in Chinese)
[19] 鲍士旦. 土壤农化分析[M]. 北京: 中国农业出版社, 2007: 152-200
[20] Wang T, Sun H, Zhang Y. Cadmium immobilization by bioamendment in polluted farmland in Tianjin, China [J]. Fresenius Environmental Bulletin, 2012, 17: 3507-3514
[21] Gibson R, Durán-lvarez J C, Estrada K L, et al. Accumulation and leaching potential of some pharmaceuticals and potential endocrine disruptors in soils irrigated with wastewater in the Tula Valley, Mexico [J]. Chemosphere, 2010, 81(11): 1437-1445
[22] Schwarzenbach R P, Gschwend P M, Imboden D M. Environmental Organic Chemistry [M]. New Jersey: John Wiley and Sons, 2003: 178-212
[23] Wolf L, Zwiener C, Zemann M. Tracking artificial sweeteners and pharmaceuticals introduced into urban groundwater by leaking sewer networks [J]. Science of the Total Environment, 2012, 430(1): 8-19
◆
Study on the Leaching Behavior of Typical Artificial Sweeteners in Soils
Ma Ling1, Feng Biting1, Zhou Meng2, Hu Hongwei3, Sun Hongwen1,*
1. College of Environmental Science and Engineering, Ministry of Education Key Laboratory of Pollution Processes and Environmental Criteria, Nankai University, Tianjin 300350, China 2. Tianjin Vehicle Emission Inspection and Control Center, Tianjin 300391, China 3. Tianjin TEDA Green Group Company, Tianjin 300457, China
Artificial sweeteners (ASs) are used worldwide as sugar substitutes in remarkable amounts in food, pharmaceuticals, personal care products as well as in animal feed, however, the majority of artificial sweeteners ingested by human and animals are almost not absorbed or metabolized and get into environment through the urine and feces directly. In this study, acesulfame, saccharin, cyclamate, and sucralose were detected in different soil layers along a sweage canal and around a sweetener factory in Tianjin. Soil column leaching experiments on acesulfame and sucralose were conducted to study their mobility and the possible risk to contaminate ground water. The results showed that more than 87% of the two tested sweeteners were detected in leachates and less than 13% of them existed in soil column or lost, mainly in the deep layer, indicating the strong mobility. Therefore, it may cause risk to groundwater. Furthermore, the influence of acesulfame and sucralose on dissolved organic matter (DOM), pH and electrical conductivity (EC) of the leachates were measured. The results indicated that both of the two artificial sweeteners could enhance the leaching of DOM, while they rarely had any impact on pH or EC of the leachates.
artificial sweeteners; soil; leaching behavior
10.7524/AJE.1673-5897.20151129005
国家自然科学基金(41225014);科技部“973”项目(2014CB441104)
马铃(1991-),女,硕士,研究方向为环境化学,E-mail: maling@mail.nankai.edu.cn
*通讯作者(Corresponding author), E-mail: sunhongwen@nankai.edu.cn
2015-11-29 录用日期:2016-02-26
1673-5897(2016)2-650-08
X171.5
A
简介:孙红文(1967—),女,环境化学博士,教授,主要研究方向为环境污染化学、人体健康与生态修复,发表论文260余篇。
马铃, 冯碧婷, 周萌, 等. 人工甜味剂在不同类型土壤中的淋溶行为研究[J]. 生态毒理学报,2016, 11(2): 650-657
Ma L, Feng B T, Zhou M, et al. Study on the leaching behavior of typical artificial sweeteners in soils [J]. Asian Journal of Ecotoxicology, 2016, 11(2): 650-657 (in Chinese)

