SiO2负载Ag-TiO2光降解催化剂的制备及性能研究
樊国栋, 张国贤, 冯昕钰
(陕西科技大学 化学与化工学院 教育部轻化工助剂化学与技术重点实验室, 陕西 西安 710021)
SiO2负载Ag-TiO2光降解催化剂的制备及性能研究
樊国栋, 张国贤, 冯昕钰
(陕西科技大学 化学与化工学院 教育部轻化工助剂化学与技术重点实验室, 陕西 西安 710021)
以钛酸丁酯为钛源、正硅酸乙酯为硅源、硝酸银为Ag源,采用溶胶-凝胶法制备Ag掺杂TiO2负载型催化剂x%Ag-TiO2/SiO2(x=0.5~3.0).通过X射线衍射(XRD)、场发射扫描电镜(FE-SEM)、透射电子显微镜 (TEM)、傅里叶红外光谱仪(FT-IR)、X射线光电子能谱(XPS)、紫外-可见-近红外光谱等对样品进行了表征.以罗丹明B(Rh B)为模拟污染物,在可见光照射下研究了Ag掺杂量对催化剂光催化性能的影响.研究结果表明,适量Ag的掺杂能在Ag-TiO2界面处形成肖特基势垒,起到捕获电子的作用,使得在TiO2中形成的电子空穴对有效的分离,从而提高催化剂的光催化能力.SiO2的引入有利于TiO2纳米颗粒更好的分散,有效的抑制了颗粒之间的团聚,从而增强了光催化剂的吸附能力.而且当SiO2与TiO2的质量比为1∶10一定时,Ag掺杂量为1.0%时,催化性能达到最佳,此时以Rh B为模拟污染物进行降解,经过105 min 可见光照射,降解率达到99.5%.
Ag掺杂TiO2; SiO2; 溶胶-凝胶法; 光催化降解
0 引言
随着工业、农业的大力发展, 环境问题日益严重,尤其是有机物对水和空气的污染影响着整个地球的安全.这些问题引起了广大学者的高度重视,因此制备一种能够处理水和空气中污染物的材料尤为重要.
半导体能够降解有机污染物而倍受关注,在众多的半导体中TiO2以其物理化学性质稳定、廉价易得、无毒、不产生二次污染、相对高的光催化效率等优良特点[1]已经应用到很多科学领域如光催化、太阳能电池、激光,传感器等,受到了广大科学工作者的青睐.但是较宽的带隙(锐钛矿3.2 eV,金红石3.0 eV)和高的电子空穴复合率严重的降低了它对太阳能的利用率[2].
为了进一步减少颗粒之间的团聚和电子空穴的复合,增强光催化性能,通常采用的改性方法有掺杂贵金属如Au、Ag、Pt、Pd等[3-6],过渡金属如Fe、Co、Ni、Mn、Cu等[7-9],非金属如C、N、S、F等[10-13]以及与半导体复合[14,15],金属氧化物的复合[16,17],稀土元素的掺杂等[18],这些在增强光催化性能方面取得了一定的效果.以上方法改性掺杂后的TiO2颗粒通常还是纳米级别,在废水处理后很难回收,SiO2既有大的体积又有大的比表面积,用它作为载体可以解决TiO2使用后难回收的问题,同时TiO2在SiO2表面能更好的分散,从而减少了催化剂颗粒之间的团聚.与纯TiO2相比,负载型TiO2/SiO2对污染物的降解能力有很大的提高.
金属Ag以其表面等离子共振效应能增加对光的吸收能力[19],在一定含量下可以有效的抑制电子空穴对的复合,延长电子空穴的寿命,增加催化剂对光的利用率,有效的提高其光催化效率[20].Mahesh等[21]通过在紫外光照射下将不同量的Ag颗粒沉积到TiO2/SiO2颗粒上,结果表明这种催化剂具有高的光催化效率和好的重复使用性.Pinho等[22]通过浸渍法制备了Ag-SiO2-TiO2纳米复合材料,研究表明这种材料对移除建筑物表面污染物有很好的效果.Wei Zhao等[23]以聚丙烯为模板通过水热法制备出Ag改性的孔状SiO2/TiO2,光催化剂结果表明,掺杂Ag后催化剂在可见光照射下对罗丹明B的光催化降解率有很大的提高.Xiaoyun Ye等[24]用TiO2修饰SiO2微球表面,然后将Ag沉积在其表面逐渐生长成面心立方的壳层,SiO2/TiO2核壳结构在界面处强的化学作用和贵金属Ag的高反射性能两者有效的促进了SiO2/TiO2/Ag多层微球颗粒的光学活性.
本文采用溶胶-凝胶法,以SiO2为载体,Ag掺杂TiO2负载到SiO2表面,通过固定SiO2的质量含量为TiO2的10%时,改变Ag掺杂量,研究Ag含量对光催化性能的影响.采用X射线衍射(XRD)、扫描电镜(SEM)、透射电镜(TEM)和红外光谱(FT-IR)对其晶型、结构和表面形貌等进行分析表征,X射线光电子能谱对Ag的化学价态进行鉴定,紫外-可见-近红外光谱研究了样品的最大吸收边带.以罗丹明B为模拟污染物,考察了在可见光照射下的光催化性能,并确定了最佳Ag掺杂量.
1 实验部分
1.1 主要试剂和仪器
(1)主要试剂:钛酸丁酯(Ti(OBu)4),天津福晨化学试剂厂,化学纯; 无水乙醇(C2H5OH),天津市河东区红岩试剂厂;冰乙酸(CH3COOH),天津市天力化学试剂有限公司;正硅酸乙酯(Si(OC2H5)4),国药集团化学试剂有限公司;硝酸银(AgNO3),天津市河东区红岩试剂厂,以上试剂均为分析纯.
(2)主要仪器:Rigalcu D/Max-3c型X射线衍射仪(XRD),日本理学公司;S-4800场发射扫描电子显微镜(SE-SEM),日本日立公司;Tecnai G2 F20型透射电镜(TEM),美国FIT公司;X射线光电子能谱(XPS),英国Kratos公司;Vector 22型傅立叶变换红外光谱仪(FT-IR),德国布鲁克公司;Cary 5000紫外-可见-近红外分光光度计,美国安捷伦;DR-5000型紫外可见分光光度计(UV-vis),美国哈希公司;GHX-Ⅱ型光化学反应仪,上海嘉鹏科技有限公司.
1.2 制备方法
用钛酸丁酯作为钛源,将18 mL钛酸丁酯和6 mL冰醋酸在磁力搅拌下先后逐滴加入到16 mL无水乙醇中,形成溶液A.取1.6 mol/L的硝酸溶液6 mL加到8 mL无水乙醇中,然后按照不同Ag含量要求分别加入相应质量的AgNO3(其含量以TiO2总质量计算) ,磁力搅拌30 min形成溶液B.将B液逐滴加入A 液中搅拌30 min,然后将1.5 mL的正硅酸乙酯加到上述混合溶液中,磁力搅拌直到形成透明凝胶为止,所得凝胶在室温下陈化24 h, 80 ℃条件下干燥4天后进行研磨,然后在箱式炉中600 ℃煅烧4 h后冷却至室温.
1.3 测试与表征
采用XRD测试样品的晶型并计算晶粒尺寸,以Cu靶Kα射线为X射线源,λ=1.514 8 Å,电压40 kV,测量角度2θ为20 °~80 °;FT-IR采用KBr压片,室温条件测试,波数范围400~4 000 cm-1;SEM和TEM观察样品的形貌、颗粒大小和晶格间距,SEM测试时样品经超声波分散处理,测试条件为加速电压3.0 kV,电流10μA;TEM 测试加速电压200 kV;X射线光电子能谱(XPS)测试使用单色AlKα靶,功率120 W(15 kV*8 mA),掠射角为90 °,所有谱线用单质碳的标准结合能284.6 ev进行校正;UV-Vis-NIR Spectrophotometer 测量范围200~800 nm.
1.4 催化剂光降解性能的测试
取浓度为10 mg/L的罗丹明B(Rh B)30 mL于石英反应器中,加入30 mg的催化剂, 在黑暗条件下搅拌30 min以达到吸附脱附平衡,溶液经离心分离,测定上层清液的吸光度记为(A0),然后打开光源进行光催化降解,光源为500 W 的汞灯,用黑紫色滤光片滤掉波长为420 nm 以下的光,每隔15 min 取样一次,经过离心使催化剂沉降,取上层清液测定其吸光度值记为(At),降解率η用下式计算:
η=(A0-At)/A0×100%
(1)
式(1)中:A0为吸附平衡时的吸光度,At为反应t时的吸光度.
2 结果与讨论
2.1 催化剂晶型和晶粒尺寸分析
图1中给出了溶胶-凝胶法制备的TiO2、TiO2/SiO2、以及不同量的Ag掺杂TiO2负载到SiO2上的系列催化剂x%Ag-TiO2/SiO2(x=0.5~3.0)的XRD 图.标记A和R分别为锐钛和金红石矿型TiO2的衍射峰.如图1所示,25.4 °、48.01 °、37.7 ° 、48.1 °、75.04 °是锐钛矿型的特征衍射峰,27.41 °、36.07 °、39.25 °、41.8 °、44.1 °、54.4 °、56.65 °、62.8 °、64.4 °、69.1 ° 、69.9 °是金红石型的特征衍射峰.
在600 ℃煅烧后纯TiO2出现很强的金红石衍射峰,因为当煅烧温度超过500 ℃时,TiO2由锐钛矿向金红石型转变.样品Ag-TiO2/SiO2经过600 ℃煅烧后金红石的衍射峰明显减弱,锐钛矿的峰显著增强,表明SiO2和Ag的加入有效的抑制了TiO2在高温煅烧时由锐钛矿向金红石的转变,提高了催化剂的热稳定性.
图1中没有SiO2和Ag明显的衍射峰,因为SiO2以非晶态形式存在,Ag的含量太少衍射峰强太弱,出峰的位置又与锐钛矿的位置接近容易被强峰掩盖.图1中可以清楚的看到,当SiO2加入后,最强衍射峰的半高宽增大,说明晶粒尺寸变小.晶粒尺寸通过Scherrer公式Dhkl=Kλ/(Bhkl·cosθ)[25]计算,式中D是晶粒的直径,K为谢乐常数,B为最强衍射峰的半高宽,θ为布拉格衍射角.计算结果表明,未加入SiO2和Ag改性前TiO2的晶粒直径为47 nm,加入SiO2改性后晶粒直径变为10.8 nm,可见SiO2的加入能够阻止TiO2晶粒的长大.Ag的掺杂对晶粒尺寸没有明显的影响.
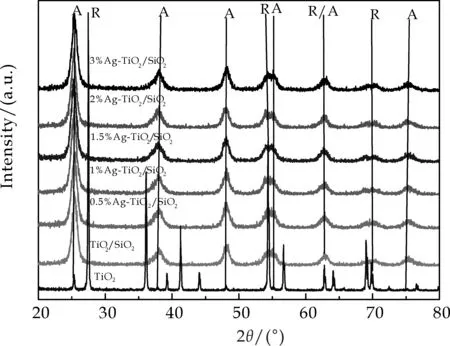
图1 w%Ag-TiO2/SiO2(w=0.5~3.0)的XRD
2.2 红外吸收光谱分析
图2是TiO2、TiO2/SiO2和x%Ag-TiO2/SiO2的FT-IR光谱图.952 cm-1左右处是Si-O-Ti的伸缩振动峰[26],从图2中可以看出当有SiO2加入时出现此峰,并且当Ag含量为1%时峰的强度最高,这说明适量掺杂Ag提高了活性组分TiO2和载体SiO2强相互作用.1 630 cm-1处的峰是样品表面吸附水所产生的[27],改性后样品峰的强度明显高于TiO2,这样有利于生成更多的·HO,提高反应活性.1 064 cm-1附近是Si-O-Si的不对称伸缩振动峰[28]. 这是因为少量Ag的加入促使TiO2与SiO2强相互作用,形成了更多的Si-O-Ti键,但是当银含量超过1%时, 过量的Ag与Ti和Si之间的作用增强,导致Si-O-Ti和Si-O-Si峰强有所减弱.

图2 w%Ag-TiO2/SiO2(w=0.5~3.0)的红外光谱图
2.3 表面形貌和结构分析
图3(a)、(b)和图3(c)、(d)分别是经600 ℃煅烧4 h后纯TiO2和1% Ag-TiO2/SiO2不同放大倍数的SEM图.从图3中可以看出,1%Ag-TiO2/SiO2表面颗粒尺寸明显小于纯TiO2,这是因为SiO2的加入使得颗粒更好的分散,有效的抑制了颗粒之间的团聚.1%Ag-TiO2/SiO2的图片上可以看到局部有发亮的小颗粒存在,说明掺杂的银富集到催化剂的表面.

(a)、(b)TiO2

(c)、(d)1%Ag-TiO2/SiO2图3 TiO2和1%Ag-TiO2/SiO2不同放大倍数的SEM照片
图4是不同放大倍数1%Ag-TiO2/SiO2的TEM图.图4(a)中颜色较深部分为结晶态的TiO2和Ag,图4(c)是图4(b)的局部放大图,从中可以看到晶格条纹的间距有0.34 nm和0.24 nm两种,它们分别对应于TiO2的(101)晶面和Ag的(111)晶面.因为SiO2为非晶态,所以图片中没有出现晶格条纹,图中有多处0.34 nm和0.24 nm的晶格条纹,表明Ag-TiO2纳米颗粒均匀的分散在SiO2表面.

(a)低倍TEM照片

(b)HRTEM照片

(c)局部HRTEM照片图4 1%Ag-TiO2/SiO2不同放大倍数的TEM图
2.4 元素价态的分析
图5是1%Ag-TiO2/SiO2的XPS全谱扫描图和Ag 3d的窄谱扫描图,Ag 3d窄谱图中373.7 eV和367.7 eV两峰分别归属于Ag-TiO2/SiO2中Ag03d3/2 和Ag03d5/2轨道的电子结合能[29],说明催化剂中银是以零价的单质Ag形式存在的,这也进一步佐证了在HTEM图中晶格间距0.24 nm 对应的应该是Ag 的(111)晶面.
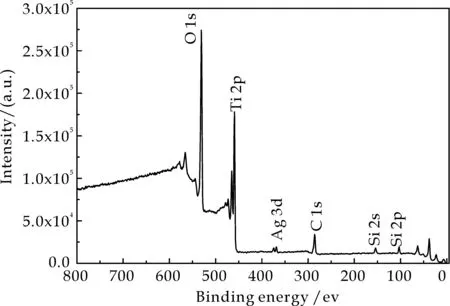
(a)全谱图

(b)Ag 3d窄谱图图5 1%Ag-TiO2/SiO2的XPS谱图
2.5 光催化性能的评价
图6为TiO2、TiO2/SiO2和x%Ag-TiO2/SiO2(x=0.5~3.0)样品对Rh B降解率的曲线图,所用光源为波长大于420 nm的可见光.从降解率曲线可以看出,经过105 min的光催化反应后,TiO2/SiO2对Rh B的降解率远大于TiO2的降解率,这是因为纯TiO2的主要晶相为金红石,而SiO2的加入抑制了在高温煅烧过程中锐钛矿相向金红石相的转变,使得TiO2/SiO2样品中金红石含量较少,其主晶相为高活性的锐钛矿,同时少量金红石和锐钛矿相的复合能够抑制光生电子和空穴的复合[30],因此TiO2/SiO2对Rh B的降解率显著提高.
将不同量Ag掺杂于TiO2/SiO2中,催化剂对Rh B的降解率会有不同程度的提高,由图6可知,Ag含量为0.5%、1.0%、1.5%、2.0%、3.0%的x%Ag-TiO2/SiO2对罗丹明B(Rh B)的降解率分别为97.6%、99.5%、98%、97%、85.6%,催化剂1%Ag-TiO2/SiO2的降解率分别是TiO2和TiO2/SiO2的11.8倍和1.1倍.1%Ag-TiO2/SiO2样品降解速率在前45 min明显高于其它Ag含量的催化剂,60 min后与含Ag量为0.5%、1.5%、2.0%的x%Ag-TiO2/SiO2样品的降解率趋于相同,而Ag含量为3%的样品降解率反而比TiO2/SiO2低,这是因为适量的加入Ag, Ag-TiO2之间形成的肖特基势垒能够捕获光生电子,有效的抑制了电子空穴的复合,因此光催化效率有较大程度的提高.但是当银含量超过1.0% 时,样品的可见光降解效率开始下降.原因是样品表面银含量过高时,大量电子集中在样品表面,会导致对空穴的吸引力增大,反而促进了电子空穴的复合,因此降低了光催化的效率.

图6 w%Ag-TiO2/SiO2(w=0.5~3.0)对Rh B 降解率曲线
以下是Ag-TiO2/SiO2的光催化机理:



2.6 催化剂响应波长范围的研究
图7是样品的紫外-可见-近红外吸收光谱,从图7中可以看出,制备的干凝胶在600 ℃煅烧后,TiO2、TiO2/SiO2和1%Ag-TiO2/SiO2样品的吸收边带分别是436 nm、447 nm、464 nm,由此可见在TiO2加入SiO2和Ag均能提高催化剂对可见光的利用率.1%Ag-TiO2/SiO2样品的吸收边带波长最长,主要原因是Ag能够吸收可见光,所以发生红移程度最大,SiO2的加入能够增加TiO2的热稳定性抑制由锐钛矿向金红石的转变,提高体系中高活性锐钛矿的含量.1%Ag-TiO2/SiO2中既有高含量的锐钛矿二氧化钛又有大的吸收边带,而且少量金红石的存在能够促进光生电子和空穴的分离,所以在可见光下的催化性能有显著的提升[31].

图7 样品的紫外-可见近红外吸收光谱
3 结论
以钛酸丁酯为钛源,正硅酸乙酯为硅源,通过溶胶-凝胶法制备了不同Ag含量的Ag-TiO2/SiO2光降解催化剂.结果表明,当SiO2与TiO2的质量比为1∶10时,适当Ag掺杂能够有效的提高催化剂在可见光下对Rh B的降解率和降解速度.Ag掺杂的TiO2颗粒均匀的分布在SiO2表面,当Ag含量为1.0%时,催化剂中TiO2纳米颗粒分散更加均匀,有利于和污染物更好的接触,从而加快反应速度提高降解效率,在可见光下照射反应105 min后对Rh B的降解率达到99.5%.该催化剂对有机物降解率高,在废水处理方面具有潜在的应用价值.
[1] Fujishima A,Rao T N, Tryk D A.Titanium dioxide photocatalysis[J].Journal of Photochemistry & Photobiology,2000(1):1-21.
[3] Zhang D.Heterogeneous photocatalytic removal and reaction kinetics of Rhodamine-B dye with Au loaded TiO2nanohybrid catalysts[J].Polish Journal of Chemical Technology,2012,14(2):42-48.
[4] Jovic V,Al Azri Z H N,Chen W T,et al.Photocatalytic H2production from ethanol-water mixtures over Pt/TiO2and Au/TiO2photocatalysts:A comparative study[J].Topics in Catalysis,2013,56(12):1 139-1 151.
[5] Chen Q,Xin Y,Zhu X.Au-Pd nanoparticles-decorated TiO2nanobelts for photocatalytic degradation of antibiotic levofloxacin in aqueous solution[J].Electrochimica Acta,2015,186:34-42.
[6] Alaoui O T,Herissan A,Quoc C L,et al.Elaboration,charge-carrier lifetimes and activity of Pd-TiO2photocatalysts obtained by gamma radiolysis[J].Journal of Photochemistry & Photobiology A Chemistry,2012,242(31):34-43.

[8] Liu J,Chen F.Plasmon enhanced photoelectrochemical activity of Ag-Cu nanoparticles on TiO2/Ti substrates[J].International Journal of Electrochemical Science,2012,7:9 560-9 572.
[10] Wu D,Wang L.Low-temperature synthesis of anatase C-N-TiO2photocatalyst with enhanced visible-light-induced photocatalytic activity[J].Applied Surface Science,2013,271:357-361.
[11] Mohamed M A,Salleh W N W,Jaafar J,et al.Incorporation of N-doped TiO2nanorods in regenerated cellulose thin films fabricated from recycled newspaper as a green portable photocatalyst[J].Carbohydrate Polymers,2015,133:429-437.
[12] Emy Marlina Samsudin,Sharifah Bee Abd Hamid,Joon Ching Juan,et al.Synergetic effects in novel hydrogenated F-doped TiO2photocatalysts[J].Applied Surface Science,2016,370:380-393.
[13] Dong Li,Jialin Jia,Tong Zheng,et al.Construction and characterization of visible light active Pd nanocrystallite decorated and C-N-S-co-doped TiO2nanosheet array photoelectrode for enhanced photocatalytic degradation of acetylsalicylic acid[J].Applied Catalysis B:Environmental,2016,188:259-271.
[14] Guo N,Liang Y,Shi L,et al.Uniform TiO2-SiO2hollow nanospheres:Synthesis,characterization and enhanced adsorption-photodegradation of azo dyes and phenol[J].Applied Surface Science,2014,305(12):562-574.
[15] Wu L,Zhou Y,Nie W,et al.Synthesis of highly monodispersed teardrop-shaped core-shell SiO2/TiO2nanoparticles and their photocatalytic activities[J].Applied Surface Science,2015,351:320-326.
[16] Li Z D,Wang H L,Wei X N,et al.Preparation and photocatalytic performance of magnetic Fe3O4@TiO2core-shell microspheres supported by silica aerogels from industrial fly ash[J].Journal of Alloys & Compounds,2016,659:240-247.
[17] Ismail A A,Abdelfattah I,Atitar M F,et al.Photocatalytic degradation of imazapyr using mesoporous Al2O3-TiO2nanocomposites[J].Separation & Purification Technology,2015,145:147-153.
[18] 樊国栋,王丽娜.热处理温度对Ce掺杂TiO2光催化剂结构与性能的影响[J].陕西科技大学学报(自然科学版),2015,33(5):46-49.
[19] Sakthivel S,Shankar M V,Palanichamy M,et al.Enhancement of photocatalytic activity by metal deposition:Characterisation and photonic efficiency of Pt,Au and Pd deposited on TiO2catalyst[J].Water Research,2004,38(13):3 001-3 008.
[20] Jakob M,Levanon H,Kamat P V.Charge distribution between UV-Irradiated TiO2and gold nanoparticles:Determination of shift in the fermi level[J].Nano Letters,2003,3(3):353-358.
[21] Mahesh K P O,Kuo D H,Huang B R.Facile synthesis of heterostructured Ag-deposited SiO2@TiO2composite spheres with enhanced catalytic activity towards the photodegradation of AB 1 dye[J].Journal of Molecular Catalysis A Chemical,2015,396:290-296.
[22] Pinho L,Rojas M,Mosquera M J.Ag-SiO2-TiO2nanocomposite coatings with enhanced photoactivity for self-cleaning application on building materials[J].Applied Catalysis B Environmental,2015,178:144-154.
[23] Wei Z,Feng L,Rong Y,et al.Synthesis,characterization,and photocatalytic properties of Ag modified hollow SiO2/TiO2hybrid microspheres[J].Applied Catalysis B Environmental,2011,103(1-2):181-189.
[24] Ye X,Cai S,Zheng C,et al.SiO2/TiO2/Ag multilayered microspheres:Preparation,characterization,and enhanced infrared radiation property[J].Applied Surface Science,2015,345:279-285.
[25] Xie C,Xu Z,Yang Q,et al.Enhanced photocatalytic activity of titania-silica mixed oxide prepared via basic hydrolyzation[J].Materials Science & Engineering B,2004,112(1):34-41.
[26] Ren C,Qiu W,Chen Y,et al.Physicochemical properties and photocatalytic activity of the TiO2/SiO2prepared by precipitation method[J].Separation & Purification Technology,2013,107(4):264-272.
[27] Zhai J,Tao X,Pu Y,et al.Core/shell structured ZnO/SiO2nanoparticles:Preparation, characterization and photocatalytic property[J].Applied Surface Science,2010,257(2):393-397.
[28] Fidalgo A,Ciriminna R,Ilharco L M,et al.Role of the alkyl-alkoxide precursor on the structure and catalytic properties of hybrid sol-gel catalysts[J].Chemistry of Materials,2005,17(26):6 686-6 694.
[29] Zhao J X,Zhang B P,Li Y,et al.Optical and photocatalytic properties of TiO2/Ag-SiO2nanocomposite thin films[J].Journal of Alloys & Compounds,2012,535(9):21-26.
[30] Li H,Shen X,Liu Y,et al.Facile phase control for hydrothermal synthesis of anatase-rutile TiO2with enhanced photocatalytic activity[J].Journal of Alloys & Compounds,2015,646:380-386.
[31] Liu J,Mccarthy D L,Cowan M J,et al.Photocatalytic activity of TiO2polycrystalline sub-micron fibers with variable rutile fraction[J].Applied Catalysis B Environmental,2016,187:154-162.
【责任编辑:陈 佳】
Study on the photodegragradation properties and preparation of silica supported Ag-TiO2
FAN Guo-dong, ZHANG Guo-xian, FENG Xin-yu
(College of Chemistry and Chemical Engineering, Key Laboratory of Auxiliary Chemistry and Technology for Chemical Industry, Ministry of Education, Shaanxi University of Science & Technology, Xi′an 710021, China)
Silica supported silver doped titanium dioxide particles were synthesized by sol-gel method using titanium tetra isopropoxide as the titanium source.Ag doping TiO2using AgNO3as the Ag source.The structure and physical properties of Ag-TiO2/SiO2particles are characterized by field-emission scanning electron microscopy(FE-SEM),fourier transform infrared spectroscopy (FT-IR),X-ray diffraction (XRD),transmission electron microscopy (TEM),X-ray photoelectron spectra (XPS),cary series UV-Vis -NIR Spectrophotometer.Photocatalytic properties of the different amount of the Ag doped has been investigated for the degradation of rhodamine B (Rh B).The result show when the quality of titanium and silicon was constant,Ag doping significantly enhanced the photodegradation activity under visible light irradiation result from the schottky barrier formed at the Ag-TiO2interface,which serve as the electron trap,facilitating the separation of electrons and holes.Compared with TiO2,introduction of SiO2effectively inhibit the aggregation of particles thus enhance the adsorption capacity of the photocatalyst.And the best catalytic performance obtained through the mass ratio of silicon and titanium was 10%,and the doping mass of Ag is 1.0%.After 105 min visible light irradiation,the degradation rate of Rh b reached 99.5%.
silver doped titania; silica dioxide; sol-gel method; photocatalytic degradation
2016-10-19
陕西省科技厅科技攻关计划项目(2014K08-12); 陕西省教育厅重点实验室科研计划项目(14JS015)
樊国栋(1964-),男,山西永济人,教授,博士,研究方向:光降解催化材料
1000-5811(2016)06-0064-07
O643.36+1
A
——以金红石为例

