镁铝尖晶石催化剂载体的制备及表征
张超武, 张利娜, 张 楠, 王夏云, 王 芬
(陕西科技大学 材料科学与工程学院, 陕西 西安 710021)
镁铝尖晶石催化剂载体的制备及表征
张超武, 张利娜, 张 楠, 王夏云, 王 芬
(陕西科技大学 材料科学与工程学院, 陕西 西安 710021)
以偏铝酸钠和氢氧化镁为原料,采用共沉淀-水热法合成镁铝尖晶石载体.利用XRD、SEM、TG-DSC和N2吸附-脱附等测试手段对样品的结构和性能进行了表征,并研究了水热时间、烧结温度等条件对镁铝尖晶石载体的结构和性能影响.所得结果表明,水热反应后得到的前驱物主要是镁铝羟基化合物,水热时间24 h能够形成镁铝尖晶石良好的片状骨架结构.在实验范围内镁铝尖晶石有良好的介孔结构,600 ℃烧结就得到了完整晶态骨架结构,随着温度的提高,样品的XRD衍射峰强度不断增加,骨架结构更完整, 温度高于900 ℃,镁铝尖晶石骨架结构塌陷,因此镁铝尖晶石催化剂载体的最佳烧结温度为800 ℃.
镁铝尖晶石; 催化剂载体; 水热法
0 引言
随着全球能源危机的加剧和全球变暖的日益严峻,环境问题越来越受到关注[1].甲烷二氧化碳重整反应制取合成气CO/H2,再以合成气为原料气制取甲醇、二甲醚等液体燃料,代替石油能源,以缓解我国液体燃料的短缺,如能实现工业化将会产生巨大的经济效益、社会效益和环境效益[2].该反应工业化的一个关键问题是开发具有高活性、高稳定性的催化剂[3].
目前,大量的研究集中于负载型非贵金属镍、钴催化剂[4].而载体的结构与性质、以及由此引起的催化剂组成、颗粒大小、金属分散度的变化等都会影响催化剂的催化性能[5].镁铝尖晶石是二元系统MgO-Al2O3中唯一的化合物[6].它是一种复合氧化物,本身具有催化活性[7].镁铝尖晶石被广泛地用作负载型金属催化剂的载体材料,它不仅兼备两种氧化物优点,并且具备两种氧化物未具备的新优点.饱和结构使其具有更好的热稳定性,晶相结构可以在很高温度下保持不变.由于晶格密度很大,水分子难以进入尖晶石内部,只能在表面上与其结合,直接提高了载体的抗水合性能[8].同时具有酸性和碱性两种活性中心,性质稳定,不易烧结,它的催化作用及其作为催化剂载体的重要作用已逐渐受到人们的广泛关注[9].
目前制备镁铝尖晶石粉体的方法有固相法[10]、共沉淀法[11]、溶胶凝胶法[12]、水热合成法[9]、燃烧合成法[13]、超临界法[14].本文采用共沉淀-水热法制备镁铝尖晶石载体.水热法制备粉体可实现形貌可控,粉体分散性较好,无团聚,水为反应介质,原料易得,降低了制备成本[15],还可加快反应速度,获得纯度高、粒径小的纳米级粒子.本文还研究了烧结温度、水热时间等条件对镁铝尖晶石载体的结构和性能影响.
1 实验部分
1.1 实验药品
偏铝酸钠(NaAlO2,CP,≥98.0%),天津市光复精细化工研究所;氢氧化镁(Mg(OH)2,AR,≥98.0%),广东省汕头市红卫化工厂;实验中所用水均为去离子水.
1.2 镁铝尖晶石的制备
以NaAlO2为铝源,以Mg(OH)2为镁源,按照摩尔比n(Mg)/n(Al)=1/2的比例分别称取原料.加入到适量去离子水中配成溶液,磁力搅拌30 min后将混合溶液转移到有聚四氟乙烯内胆的不锈钢高压釜内.在180 ℃下水热处理16~24 h,制得镁铝尖晶石前驱体,将前驱体过滤、洗涤、干燥后,在500 ℃~900 ℃电热炉中结晶化烧结5 h,最终制得纯度高、结晶状况好的MgAl2O4重整催化剂载体.
1.3 样品的分析与表征
采用日本Rigaku的D/Max-2200PC型X射线衍射仪(X-ray Diffraction, XRD)对样品晶体结构进行分析,测试条件:Cu Kα辐射,λ=0.154 18 nm,管压40 kV,管流40 mA,狭缝DS,RS和SS分别为1 °,0.3 mm和1 °.采用S-4800日立扫描电子显微镜(Scanning Electronic Microscopy & Hiroba EDX electron microscopy)对所制备的样品的形貌进行表征;采用德国耐驰STA449C型差热分析对前驱物的热处理过程进行了分析;采用美国麦克仪器生产的ASAP2460型比表面仪对样品进行N2吸附脱附测试分析.
2 结果与讨论
2.1 焙烧温度对镁铝尖晶石结构的影响
为了分析镁铝尖晶石前驱物的化学组成和结构,确定镁铝尖晶石催化剂载体的合适焙烧温度,采用TG-DSC法研究了前驱物在加热过程中的性质和状态的变化.图1为水热法制备MgAl2O4粉体的TG-DSC曲线.从TG曲线可以看出,样品在0 ℃~500 ℃有严重的失重现象.在这一区间上有三个明显的失重区.对应DSC曲线上的三个吸热峰.第一次失重在80 ℃左右,这是由于样品脱除大量自由水.第二次失重发生在210 ℃左右,这可能是由于片层结构间的结晶水脱除有关系,第三次失重发生在400 ℃左右,可能是前驱物镁铝羟基复合物脱羟基,发生了物相变化,会有部分放热,所以吸热峰较小,开始生成铝酸镁.DSC曲线显示在800℃开始曲线缓慢上升,可能由于铝酸镁形成晶态并释放结晶热,这表明铝酸镁慢慢转化为镁铝尖晶石晶相.镁铝尖晶石前驱体物质在该过程中质量损失为42.94%.结果表明镁铝尖晶石的最佳合成温度范围在800 ℃~1 000 ℃之间.
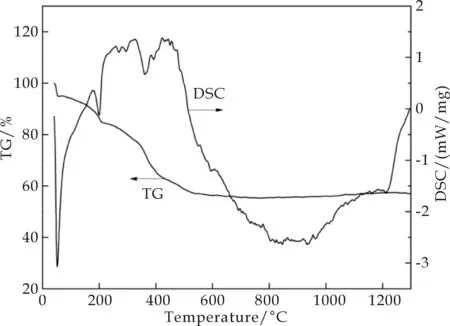
图1 镁铝尖晶石粉体的TG-DSC曲线
焙烧对前驱物制备镁铝尖晶石的形成与生长有重要的影响.图2为镁铝尖晶石粉体焙烧前后的XRD图谱.图2中a曲线是180 ℃水热反应24 h得到的前驱物XRD图谱.在2θ=11.7 °、24.0 °、35.0 °、39.5 °、46.6 °、61.8 °、62.5 °处的衍射峰为镁铝羟基化合物的特征峰.2θ=14.5 °、28.0 °、49.5 °处的衍射峰为AlO(OH)的特征峰.2θ=19.5 °、38.0 °、51.2 °、58.8 °处的衍射峰Mg(OH)2的特征峰.说明原料经水热反应后主要生成了镁铝羟基化合物和薄水铝石,还有部分Mg(OH)2没有反应,没有生成具有明显特征峰的镁铝尖晶石相.图2中b曲线是180 ℃水热反应24 h得到的前驱物经过800 ℃焙烧后所得的XRD图谱.由图2可以看出焙烧后的样品已经没有镁铝羟基化合物、薄水铝石和Mg(OH)2的特征峰,说明在800 ℃焙烧后,镁铝羟基化合物、薄水铝石和Mg(OH)2已经分解完全,在2θ=18.8 °、32.5 °、38.0 °、44.8 °、65.0 °处出现了镁铝尖晶石的特征衍射峰,对应(111)、(220)、(311)、(400)、(440)晶面,对应的JCPDS卡片号为21-1152.表明经800 ℃焙烧,镁铝尖晶石前驱物可形成镁铝尖晶石结构.
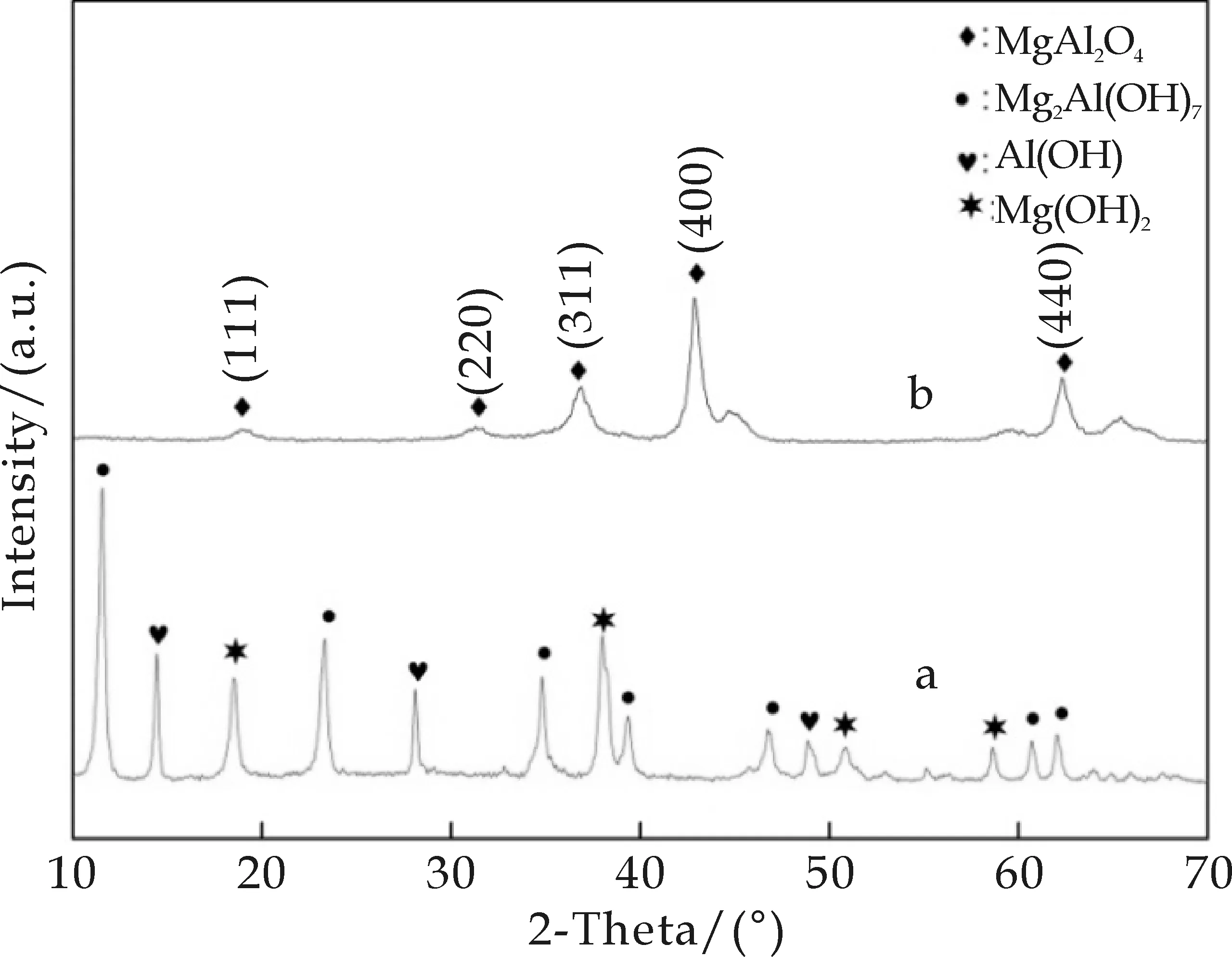
a:前驱体; b:焙烧后图2 样品的XRD图谱
烧结温度与样品的物相组成、晶体类型和微观结构有着密切的联系,为了考察烧结温度的影响,实验分别在600 ℃、700 ℃、800 ℃、900 ℃条件下对烧结的样品进行测试.图3为不同焙烧温度合成的镁铝尖晶石粉体的XRD图谱.从图3可知,合成的镁铝尖晶石前驱体经过600 ℃和700 ℃焙烧后,在2θ=38 °、44.8 °、65 °处出现的衍射峰分别对应MgAl2O4的(311)、(400)、(440)晶面,衍射峰峰形很宽且峰强较弱,其他表征镁铝尖晶石的特征峰,如(111)、(220)晶面的特征峰没出现.随着焙烧温度的增加,衍射峰强度不断提高,在800 ℃焙烧后,镁铝尖晶石的特征峰全部出现,表明此时生成完整的镁铝尖晶石相.而且衍射峰尖锐,有较好的结晶度.说明随着焙烧温度的提高,晶粒长大,试样的结晶度增强.这与图1分析结果相吻合.

a:600 ℃; b:700 ℃; c:800 ℃; d:900 ℃图3 不同焙烧温度合成的MgAl2O4粉体的XRD图谱
图4为不同焙烧温度合成的镁铝尖晶石粉体的SEM图.图4(a)是180 ℃水热反应24 h, 600 ℃焙烧得到的试样,颗粒表面是由片状结构组成,大小形状不均匀,骨架结构不明显.图4(b)是180 ℃水热反应24 h, 700 ℃焙烧得到的试样,颗粒表面是由片状结构组成,或平行生长或交叉生长,排列规则,大小较均匀.图4(c)是180 ℃水热反应24 h, 800 ℃焙烧得到的试样,颗粒表面片状结构略有长大,大小均匀,得到了完整的片状骨架结构.图4(d)是180 ℃水热反应24 h, 900 ℃焙烧得到的试样,颗粒表面片状结构略有长大,但塌陷严重.


(a)600 ℃ (b)700 ℃ (c)800 ℃ (d)900 ℃图4 不同焙烧温度合成的MgAl2O4粉体的SEM图
结果表明,随着焙烧温度的增加,镁铝尖晶石晶粒生长,骨架结构趋于完整.但温度过高,会破坏镁铝尖晶石骨架结构,因此焙烧温度800 ℃有利于镁铝尖晶石片状结构的完整生成.
图5为不同温度下烧结的样品的N2吸附脱附平衡等温线.从等温线可以看出吸附脱附有迟滞现象,等温线类型均为Ⅳ型等温线,表现为多层吸附后紧接着吸附量急剧增加的毛细管凝结.这是典型的介孔材料等温线.多孔材料的吸附过程中有由吸附曲线与脱附曲线组成的滞后环,滞后环的出现是由于毛细管凝聚作用使N2分子在低于常压下冷凝填充了介孔孔道.滞后环的特征对应于特定的孔结构信息.观察图5中N2吸附脱附平衡等温的滞后环形状可以看出,高压区吸附量大.据 IUPAC分类,为H3型滞后环.这类滞后环是片状结构的聚集体产生狭缝的介孔或大孔材料.这些孔网都是由大孔组成,并且它们没有被孔凝聚物完全填充.
图6是不同温度下烧结样品的孔径分布曲线.由图6可以看出,样品孔径分布范围较广,为0~90 nm.600 ℃、700 ℃和900 ℃焙烧的样品孔类型较多,800 ℃焙烧的样品介孔分布最多.由表1可知,600 ℃、700 ℃、800 ℃、900 ℃焙烧的样品比表面积分别为为39.84 m2·g-1、47.84 m2·g-1、82.98 m2·g-1、39.95 m2·g-1.介孔结构可以提供更多的内表面积和孔体积,有利于提高载体的活性位点的数量.因为800 ℃焙烧的样品介孔分布最集中,所以比表面积最大.
结合图4可知,镁铝尖晶石在600 ℃焙烧时开始形成骨架结构,但是骨架结构不明显,700 ℃焙烧后晶粒略有生长,但骨架结构不完整,因此在600 ℃和700 ℃焙烧时孔类型较多,且介孔分布较少,比表面积较小.在800 ℃焙烧后,镁铝尖晶石完整的片状骨架结构形成,介孔结构分布较多,孔径较小,比表面积较大.样品在900 ℃焙烧后骨架结构塌陷,温度过高使片状结构堆积形成大孔,使得比表面积降低.

(a)600 ℃
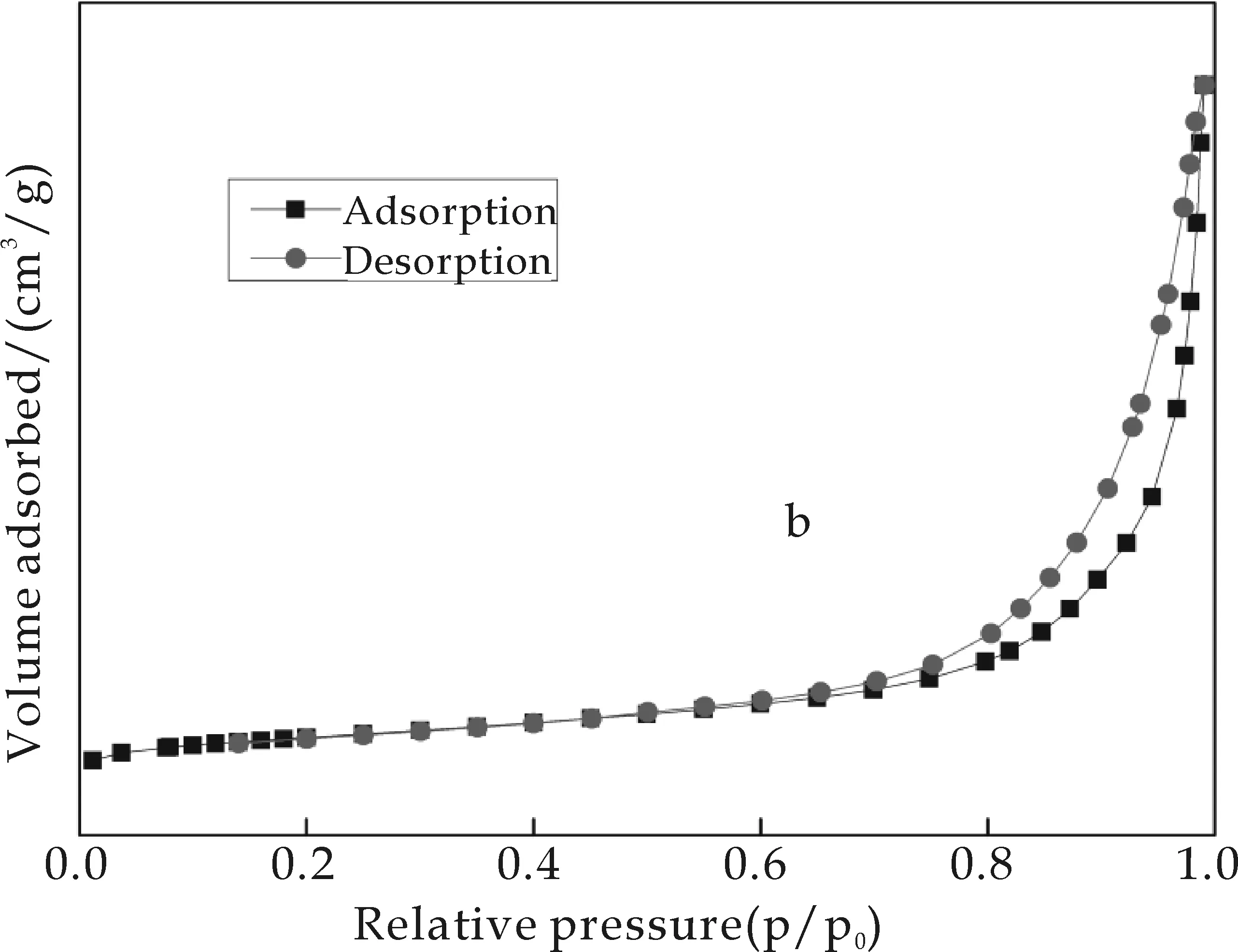
(b)700 ℃
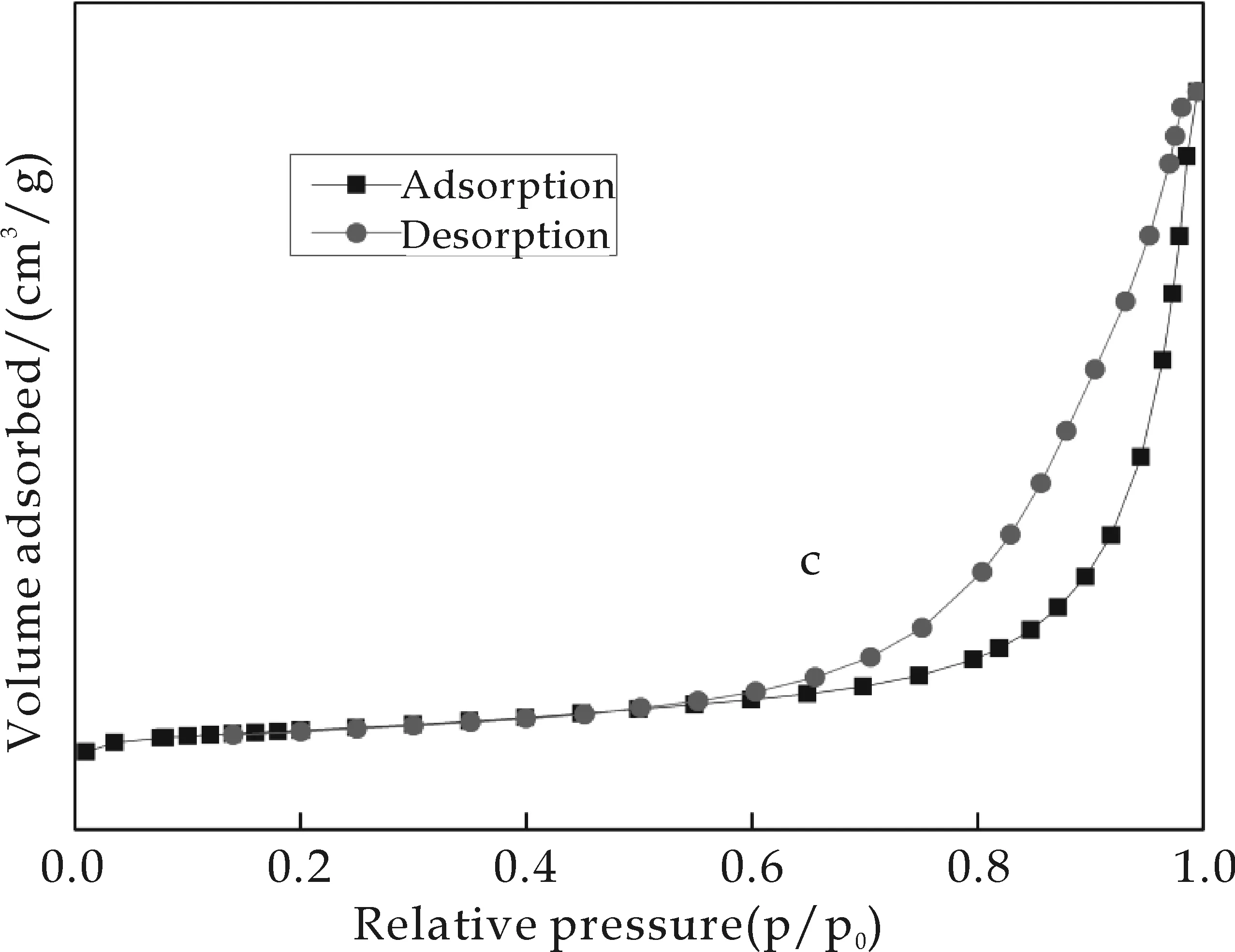
(c)800 ℃

(d)900 ℃图5 样品的N2吸附-脱附平衡等温线

a:600 ℃; b:700 ℃; c:800 ℃; d:900℃图6 样品的孔径分布

表1 不同焙烧温度下样品的比表面积
2.2 水热时间对镁铝尖晶石结构的影响
图7为在180 ℃下不同水热时间合成的镁铝尖晶石粉体的XRD图谱.从图7可知,合成的镁铝尖晶石前驱体经过焙烧后,在2θ=38 °、44.8 °、65 °处出现的衍射峰分别对应镁铝尖晶石的(311)、(400)、(440)晶面,对应的JCPDS卡片号为21-1152.其衍射峰强度高,峰宽较窄说明样品有良好的结晶度.随着水热反应时间的增加,表征镁铝尖晶石的几个弥散峰的变化明显,(111)、(220)晶面的特征峰出现,表明此时生成完整的镁铝尖晶石相.所以从X射线衍射图谱看,水热时间24 h可生成完整镁铝尖晶石相.
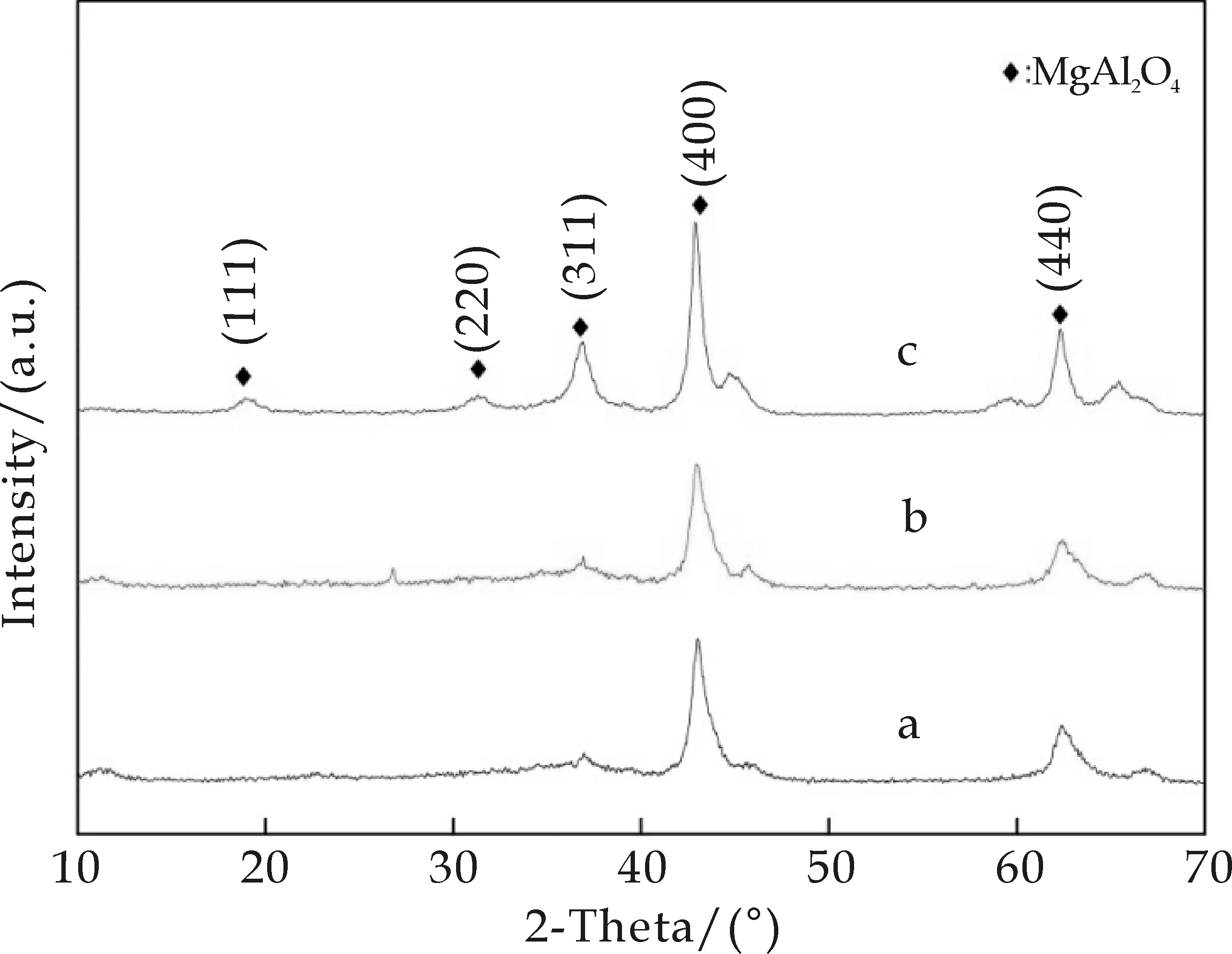
a:6 h; b:18 h; c:24 h图7 不同水热时间合成的MgAl2O4粉体的XRD谱
图8为不同水热时间合成的镁铝尖晶石粉体的SEM图.图8(a)是180 ℃水热反应6 h, 800 ℃焙烧得到的试样,颗粒表面晶粒紧密堆积,严重粘结,没有特殊的形貌,这可能是因为反应时间过短,还不足以形成完整的有序的骨架结构.图8(b)是180 ℃水热反应18 h, 800 ℃焙烧得到的试样,颗粒表面是由片状结构组成,或平行生长或交叉生长,排列规则,大小较均匀,说明水热反应18 h,颗粒在水热驱动力作用下晶粒生长按照一定的生长习性,生成了完整的结构.图8(c)是180 ℃水热反应24 h, 800 ℃焙烧得到的试样,颗粒表面片状结构长大明显.
结果表明,随着水热时间的增加,系统提供足够的时间让晶粒聚集生长,片状结构长大.因此水热反应24 h有利于镁铝尖晶石片状结构的完整生成.


(a)6 h (b)18 h (c)24 h图8 不同水热时间合成的MgAl2O4粉体的SEM图
3 结论
采用共沉淀-水热合成法制备了镁铝尖晶石催化剂载体.所得结果表明,水热反应后得到的前驱物主要是镁铝羟基化合物,180 ℃水热24 h能够形成镁铝尖晶石良好的片状骨架结构.在实验范围内镁铝尖晶石有良好的介孔结构,试样经过600 ℃焙烧得到了镁铝尖晶石片状结构,随着温度的提高,样品的衍射峰强度不断增加,晶粒生长,骨架结构更完整,但焙烧温度为900 ℃时,镁铝尖晶石骨架结构塌陷,比表面积下降,表明镁铝尖晶石最佳焙烧温度为800 ℃.高比表面积的镁铝尖晶石提供了更多的活性位点,提高活性组分在尖晶石表面的分散度,这为镁铝尖晶石作为催化剂的载体提供了更大的优势.
[1] 徐占林,毕颖丽,甄开吉,等.甲烷催化二氧化碳重整制合成气反应研究进展[J].化学进展,2000,12(2):121-129.
[2] 艾 军.CH4-CO2重整中Ni-Co/Al2O3-ZrO2催化剂的研究[D].太原:太原理工大学,2009.
[3] 郭建军.复合氧化物负载的镍基催化剂上甲烷二氧化碳重整反应及其机理的研究[D].杭州:浙江大学,2005.
[4] Bradford M C,Uannice M A.CO2reforming of CH4over supported PT catalysts[J].Journal of Catalysis,1998,173(1):157-171.
[5] Ferreira A P,Guerrero R A,Rodriguez R I,et al.Comparative study at low and mediumreaction temperatures of syngas production by methane reforming with carbondioxide over silica and alumina supported catalysts[J].Applied Catalysis A:General,1998,170(1):177-187.
[6] 姜茂发,孙丽枫,于景坤,等.镁铝尖晶石质耐火材料的开发与应用[J].工业加热,2005(2):56-69.
[7] 李春虎,赵九生,王大祥,等.纳米MgO和MgAl2O4尖晶石的制备与表征[J].无机材料学报,1996,11(3):557-560.[8] 姜瑞霞,谢在库,张成芳,等.镁铝尖晶石的制备及在催化反应中的应用[J].工业催化,2003,11(1):47-49.
[9] 李 军,周晓奇,宋志安,等.水热法制备镁铝尖晶石载体[J].工业催化,2003,10(11):44-45.
[10] Sonia A.Bocanegra,Adriana D.Ballarini,Osvaldo A. Scelza,et al.The influence of the synthesis routes of MgAl2O4on its properties and behavioral support of dehydrogenation catalysts[J].Materials Chemistry and Physics,2008,111(2):534-541.
[11] 闻 芳,杜洪兵,雷牧云,等.镁铝尖晶石超细粉末的制备[J].现代技术陶瓷,2003(3):3-4.
[12] 张 显,曾庆丰,郝富锁,等.溶胶-凝胶法制备纳米镁铝尖晶石纳米粉[J].硅酸盐通报,2009,28(S1):130-133.
[13] 吴义全,张玉峰.镁铝尖晶石超微粉的制备方法[J].材料导报,2000,14(4):41-43.
[14] C.Pommier,K.Chhor,J.F.Bocquet,et al.Reactions in supercritical fluids,a new route for oxide ceramic powder elaboration,synthesis of the spinel MgAl2O4[J].Materials Research Bulletin,1990,25(2):213-221.
[15] 曹丽云,李 雯,孔新刚,等.水热时间对K10W12O41·11H2O纳米材料光催化性能的研究[J].陕西科技大学学报(自然科学版),2016,34(2):50-53.
【责任编辑:陈 佳】
Preparation and characterization of MgAl2O4spinel as catalyst support
ZHANG Chao-wu, ZHANG Li-na, ZHANG Nan, WANG Xia-yun, WANG Fen
(School of Materials Science and Engineering, Shaanxi University of Science & Technology, Xi′an 710021, China)
The magnesium aluminate spinel catalyst carriar were synthesized by a coprecipitation and hydrothermal method,using sodium aluminate and magnesium hydroxide as the raw materials.The samples were characterized by XRD,SEM,TG-DSC,and N2adsorption-desorption isotherms to study the effect of hydrothermal and sintering temperatures on the structures and properties of magnesium aluminate spinel.The results showed that the precursor is mainly magnesium aluminum hydroxyl compounds after coprecipitation and hydrothermal procedures.The good flake skeletal structure is formed by hydrothermal time of 24 h.The final magnesium aluminate spinel has well-crystalline mesoporous structure.Witnin experimental range,the promoted crystalline skeleton structure was formed at 600 ℃.And with the increment of calcination temperature,the XRD diffraction peak intensity of samples increased gradually and the flake skeletal structure was improved.When the sintering temperature was above 900 ℃,the skeleton structure of magnesium aluminate spinel collapses.So the best sintering temperature is 800 ℃ for magnesium aluminate spinel catalyst carriar.
magnesium aluminate spinel; catalyst support; hydrothermal method
2016-07-29
国家自然科学基金项目(51171096); 陕西省科技厅自然科学基金项目(2014JM6233)
张超武(1958-),男,陕西兴平人,教授,博士,研究方向:功能材料、环境材料
1000-5811(2016)06-0042-05
O64
A

