多层螺旋CT及磁共振成像对胰腺导管内乳头状黏液性肿瘤的诊断价值
伍翠云,方松华,蔡学祥,宋琼,钟建国
(浙江省人民医院放射科,杭州 310014)
多层螺旋CT及磁共振成像对胰腺导管内乳头状黏液性肿瘤的诊断价值
伍翠云,方松华,蔡学祥,宋琼,钟建国
(浙江省人民医院放射科,杭州 310014)
胰腺导管内乳头状黏液性肿瘤(IPMN)是一种较少见的好发于老年男性的胰腺外分泌、囊性肿瘤。IPMN按导管不同的受累部位分为主胰管型(MD)、分支胰管型(BD)及混合型(MIX)三型。IPMN影像学上与胰腺假性囊肿、慢性胰腺炎等原因导致的胰管扩张鉴别有一定的难度,且IPMN有恶变成胰腺导管癌的倾向[1],术前正确的诊断对临床有重要的价值。本文回顾性分析22例经手术切除并经病理证实的IPMN患者的影像学、临床和病理资料,探讨IPMN的MSCT及MRI影像学表现,以提高诊断的准确性。
1 资料与方法
1.1 一般资料 回顾性分析在本院有完整的影像学检查、手术资料,病理资料的IPMN有22例。术前行多层螺旋CT(MSCT)平扫、增强扫描有17例;行MRI平扫、增强扫描15例;行 磁共振胰胆管成像(MRCP)19例。22例患者中,男性17例,女性5例,年龄42~82岁。其中13例表现为上腹部腹痛、腹胀不适,9例为体检偶然发现,其中3例患者血CEA、CA19-9、细胞角蛋白19不同程度的增高。
1.2 检查方法 CT检查方法:扫描设备为德国Siemens Sensation 20 或Siemens Sensation 64螺旋CT扫描仪。扫描参数:管电压120kV,管电流150~220 mAs,螺距1.0,扫描层厚、层间距均为5mm。扫描前禁食6 h,并用阴性对比剂充盈胃肠道。对比剂为300 mgI/mL碘海醇,注射流率2.5~3.0 mL/s。注射对比剂后35s、70s增强扫描,范围包全胰腺。
MRI检查方法:扫描设备为Siemens Avanto 1.5T MR成像仪。患者行常规T1WI、 FSE T2WI平扫,层厚5 mm,层间距5 mm。增强对比剂为GD-DTPA,剂量0.1~0.2 mmol/kg,注射流率2.0~3.0 mL/s。注射对比剂后18、25、42 s分别各期增强扫描。二维MRCP序列,TR 4500 ms,TE 760 ms。
1.3 图像分析
1.3.1 图像影像学表现 由两位腹部副主任以上影像诊断医师采用双盲法对所有的影像学资料分别阅片,当结果存在分歧时,通过讨论达成一致共同评价。观察内容包括:(1)病变分型:按Sugiyama等[2]将IPMN分为3型:主胰管型,主胰管局部或全程扩张;分支胰管型,分支胰管呈簇状或葡萄状扩张,囊性病灶与主胰管相通;混合型,主胰管及分支胰管均有扩张。(2)病变部位:分为胰头(包括钩突)、胰体、胰尾和弥漫性(病变累及≥2个节段)。(3)病变最大径:测量病变最大直径。(4)壁结节、囊内分隔:观察有无壁结节、分隔及增强特点。
1.3.2 良恶性诊断 根据2010年WHO分类[3],将IPMN分为以下4 类:IPMN伴低度异型增生、伴中度异型增生、伴高度异型增生、伴相关性浸润性癌。即分为低级别、中级别、高级别异型增生及浸润癌。本研究中良性包含低级别、中级别异型增生,恶性包括高级别异型增生和浸润癌。
1.4 统计学处理 应用SPSS20统计软件对数据进行分析,计数资料采用Fisher确切概率法,计量资料采用t检验。P<0.05为差异有统计学意义。
2 结果
2.1 影像学表现与病理良恶性的对比 22例IPMN伴低级别异型增生10例、中级别异型增生5例、高级别异型增生5例及浸润性癌2例,其中MD、BD、MIX分别为4、10、8例,胰头、胰体、胰尾、弥漫性分别为12、3、2、5例,病变累及导管分型、病变部位与良恶性均差异无统计学意义(P>0.05);病变最大径、有无壁结节在判断BD-IPMN及MIX-IPMN的良恶性差异有统计学意义(P<0.05),恶性直径为(50.40±10.37)mm,明显大于良性(25.15±2.19)mm。见表1。
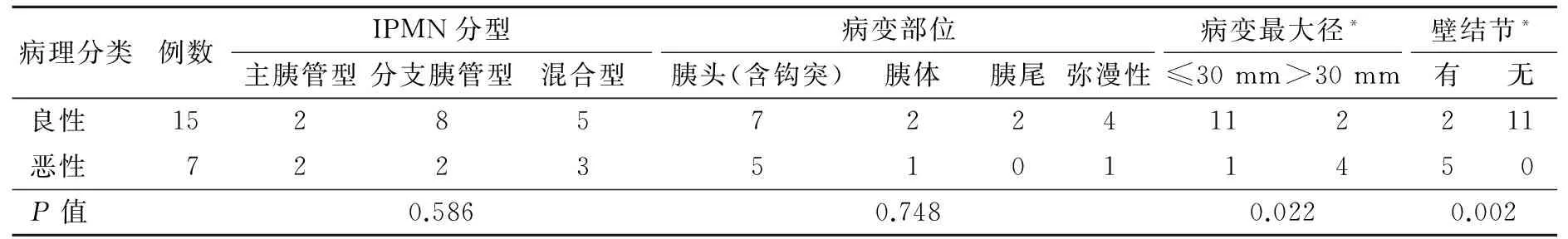
表1 IPMN影像学表现与病理良恶性的对比(例)
注:*指BD-IPMN和MIX-IPMN(分别为10例、8例)
2.2 影像学表现 主胰管型(MD)4例,影像学表现为主胰管全程或局部扩张,胰头区病变以实性成分为主,增强后轻中度强化,胰头部、胆总管下段均见低信号充盈缺损,MRCP显示肝内外胆管及胰管扩张,病理证实为IPMN伴浸润性腺癌。分支胰管型(BD)10例,表现为囊性或囊实性病灶,且与胰管相通,5例囊性病变内可见壁结节,6例可见分隔。其中1例表现为弥漫性病变(胰头+胰体),MRI检查显示胰头+胰体2个长T2囊性信号,CT、MR均可显示壁结节及分隔,但MR显示分隔更清晰,囊性灶与胰管相通在MRCP可清晰显示,主胰管轻度扩张约4mm,增强后囊性灶无增强,壁结节及分隔轻度增强。术后病理证实为IPMN伴轻度异型增生。混合型(MIX)8例,主胰管、分支胰管均扩张,病变为囊性或囊实性病灶,部分见分隔及壁结节。其中1例胰头区病灶内壁结节不规则,并见多发不规则分隔,CT与MR均可显示,MRCP显示主胰管扩张约10 mm,并与胰头囊实性病灶相通。术后病理证实为IPMN伴高度异型增生。
3 讨论
IPMN病灶来自胰腺导管上皮,黏液细胞增生,并分泌黏液引起胰管的扩张。IPMN存在肿瘤发展转化的特点,可以从不同程度异型性增生发展为浸润性癌[4]。2010年WHO根据IPMN的恶性倾向,取消了“交界性”一词。除了胰腺导管上皮内瘤变(PanIN)以外,IPMN是胰腺导管内癌最重要的癌前病变[5]。
3.1 临床特点 IPMN是一种胰腺囊性肿瘤,发生率较低,约占胰腺外分泌肿瘤的1%~2%,进展缓慢[6]。IPMN多见于老年男性[7],发病年龄60~70岁,平均63~66岁[8-9]。本研究中,男性占77.3%(17/22),明显多于女性,发病年龄42~82岁,平均年龄65.4岁。与文献相似,在发病年龄上比文献上报道的有更年轻的病例,可能跟近几年对IPMN的认识与重视越来越多有关。本病临床表现不一,可有上腹痛,腹胀不适,反复发作的胰腺炎症状,引起胆管梗阻可有黄疸,另有不少病例仅体检偶然发现。有文献报道侵袭性IPMN患者中血清肿瘤标记物CA19-9和/或癌胚抗原增高[10],本研究中1例患者肿瘤标志物CA19-9、CEA明显增高,术后病理证实为主胰管型IPMN伴浸润性癌。
3.2 影像学表现 IPMN的典型影像学表现为主胰管和(或)分支胰管不同程度的扩张,囊性病变内有或无实性成分(分隔及壁结节),囊性成分无增强,实性成分轻-中度增强。MSCT增强扫描可清晰显示扩张的胰管、囊变区、实性成分及与毗邻脏器、组织关系;MR的T2加权成像对囊性病灶(高信号)与囊内实性软组织成分(壁结节及分隔呈等信号)的显示有强大的对比度,利用MRI对软组织的分辨率较高,在显示壁结节及纤维分隔上比CT更具有优势[11]。MRCP可以直观立体地显示囊性病灶与扩张胰管之间的关系,这是其他检查方法不可比拟的[12]。
约30%的IPMN可进展为癌[3]。Crippa 等[13]报道主胰管型恶变率有49%~92%。本研究显示,病变累及导管分型、病变部位对良恶性的鉴别诊断价值无统计学意义(P=0.586、0.748),与报道不一致,可能与样本量不够大有关;有学者[14-16]提出,患者有黄疸或尿黄,肿瘤直径>30 mm,囊壁有较大的结节,主胰管明显扩张(直径>6.5 mm或>10 mm),胆总管扩张,以及病灶内不规则厚分隔,周围淋巴结肿大,可作为术前判断IPMN 恶性的指标。本研究中病变最大径(P=0.022)、有无壁结节(P=0.002)在判断BD-IPMN及MIX-IPMN的良恶性有明显差异,恶性病变最大径明显大于良性。本研究中有1例患者黄疸明显,病变呈囊实性,恶性BD-IPMN及MIX-IPMN均有壁结节,病变最大径45 mm,主胰管达8 mm,结果为浸润性腺癌。
3.3 鉴别诊断 IPMN主要应与以下等疾病鉴别:(1)胰腺假性囊肿:多有胰腺炎病史,直径较大,壁薄,囊壁光滑、无实性成分。(2)胰腺黏液性囊腺瘤:老年女性好发,胰腺体尾部多见,囊性病变区不与主胰管相通。囊性病灶与主胰管是否相通,是它们主要的鉴别点[11,17]。(3)胰腺实性假乳头状肿瘤囊变:中青年女性好发,病灶实性成分内伴出血、坏死。(4)胰腺癌:恶性度高,实性成分多见到坏死区,轻度不均匀强化,囊变不明显,病灶可引起胰管、胆总管扩张。金雷等[18]认为同时检测肿瘤标记物CA199、CA125联合增强CT或者MRI比单独的影像学检查可以提高胰腺癌的确诊率。
总之,IPMN表现为主胰管和(或)分支胰管扩张,囊性病灶与扩张的胰管相通,囊性病灶内可见到壁结节、分隔,增强后实性成分轻中度强化。病灶最大径>30 mm,且灶内有明显壁结节及不规则厚分隔、CA199增高等多提示恶性。IPMN的诊断及良恶性的鉴别影像学检查有重要的价值,可作为临床术前诊断的重要参考。
[1] GRüTZMANN R,POST S,SAEGER HD,et al.Intraductal papillary mucinous neoplasia (IPMN) of the pancreas :its diagnosis,treatment,and prognosis[J].Dtsch Arztebl Int,2011,108(46):788-794.
[2] SUGIYAMA M,ATOMI Y.Intraductal papillary mucinous tumors of the pancreas:imaging studies and treatment strategies[J].Ann Surg,1998,228(5):685-691.
[3] 周晓军,樊祥山.解读2010年消化系统肿瘤WHO分类(三)[J].临床与实验病理学杂志,2011,27(11):1158-1159.
[4] ADSAY NV,FUKUSHIMA N,FURUKAWA T,et a1.Intraductal neoplasm of the pancreas[M]//Bosman FT,Cameiro F,Hruban RH,et al.WHO classification of tumors of digestive system.Lyon:WHO Press,2010:304-313.
[5] HRUBAN RH.An illustrated consensus on the classification of pancreatic intraepithelialIial neoplasia and intraductal papillary mucinous neoplasms[J].Am J Surg Pathol,2004,28(8):977-987.
[6] 冯娟娟,袁德全,沈雪峰,等.胰腺导管内乳头状黏液性肿瘤CT与MRI表现及鉴别诊断[J].临床放射学杂志,2012,31(2):215-217.
[7] 尚建辉,王莉,陆建平,等.胰腺导管内乳头状黏液性肿瘤的CT诊断价值[J].中国医学计算机成像杂志,2010,16(2):129-134.
[8] SAWAI Y,YAMAO K,BHATIA V,et al.Development of pancreatic cancersd uring long-term follow-up of side-branch intraductal papillary mucinous neoplasms[J].Endoscopy,2010,42(12):1077-1084.
[9] NARA S,ONAYA H,HIRAOKA N,et al.Preoperative evaluation of invasive and noninvasive intraductal papillary-mucinous neoplasms of the pancreas:clinical,radiological,and pathological analysis of 123 cases[J].Pancreas,2009,38(1):8-16.
[10] FRITZ S,HACKERT T,HINZ U,et al.Role of serum carbohydrate antigen 19-9 and carcinoembryonic antigen in distinguishing between benign and invasive intraductal papillary mucinous neoplasm of the pancreas[J].Br J Surg,2011,98(1):104-110.
[11] 李仁峰,王中秋,郝楠馨,等.胰腺导管内乳头状黏液性肿瘤的CT及MRI表现[J].实用放射学杂志,2013,29(2):327-329.
[12] 尚建辉,陆建平.胰腺导管内乳头状黏液性肿瘤的影像学诊断进展[J].中国医学影像技术,2010,26(6):1182-1184.
[13] CRIPPA S,FERNANDEZ-DEL CASTILLO C,et al.Mucinproducing neoplasms of the pancreas:an analysis of distinguishing clinical and epidemiologic characteristics[J].Clin Gastroenterol Hepatol,2010,8(2):213-219.
[14] 范飞,胡先贵,张怡杰,等.良恶性胰腺导管内乳头状瘤的临床及影像特征[J].第二军医大学学报,2008,29(2):193-196.
[15] TANAKA M,FERNáNDEZ-DEL CASTILLO C,ADSAY V,et al.International consensus guidelines 2012 for the management of IPMN and MCN of the pancreas[J].Pancreatology,2012,12(3):183-197.
[16] 岳奎涛,刘剑羽,王智勇,等.胰腺导管内乳头状黏液性肿瘤的MSCT征象[J].中国医学影像技术,2012,28(7):1367-1370.
[17] 汪秀玲,程丽,徐凯,等.胰腺导管内乳头状黏液性肿瘤的MRI诊断[J].临床放射学杂志,2009,28(1):63-65.
[18] 金雷,韩真,王卫东,等.多项肿瘤标记物联合影像学检查在胰腺癌诊断中的价值[J].中国临床保健杂志,2014,17(6):609-611.
伍翠云,医师,Email:54342685@qq.com
R735.9
B
10.3969/J.issn.1672-6790.2016.06.027
2016-08-15)

