三个基于3-(2,5-二羧基苯基)-吡啶羧酸的Cu(II)、M n(II)配合物的结构及磁性
王淑菊 蔺明明 熊 刚 由立新 丁 茯 孙亚光
(沈阳化工大学辽宁省无机分子基化学重点实验室,沈阳110142)
三个基于3-(2,5-二羧基苯基)-吡啶羧酸的Cu(II)、M n(II)配合物的结构及磁性
王淑菊 蔺明明 熊 刚 由立新*丁 茯 孙亚光
(沈阳化工大学辽宁省无机分子基化学重点实验室,沈阳110142)
通过水热法合成了3个新型配位聚合物:[Cu(Hdppa)(H2O)]n(1)、{[Cu2(dppa)(μ2-OH)(H2O)]·H2O}n(2)和{[Mn3(dppa)2(H2O)4]· 2H2O}n(3),(H3dppa=3-(2,5-二羧基苯基)-吡啶羧酸),并对其进行了元素分析、红外光谱、粉末X射线衍射和热重分析表征。X射线单晶衍射分析结果表明:化合物1属于单斜晶系,P21/c空间群,a=1.371(2)nm,b=0.805(11)nm,c=1.266(19)nm,β=112.74(3)°,Z= 4;化合物2属于三斜晶系,P1空间群,a=0.839(4)nm,b=1.039(5)nm,c=1.110(5)nm,α=98.31°,β=110.630(3)°,γ=111.90(3)°,Z=2;化合物3属于三斜晶系,P1空间群,a=0.881(6)nm,b=0.939(6)nm,c=1.038(7)nm,α=100.29°,β=97.990(10)°,γ=111.13(7)°,Z=1。化合物1以配体Hdppa2-桥联Cu(II)形成一维链状结构;化合物2和3以配体dppa3-分别桥联Cu(II)和Mn(II)形成二维层状结构,并进一步通过氢键形成三维超分子结构。变温磁化率研究表明在化合物1和化合物2中存在较强的铁磁耦合作用,其磁交换常数分别为4.44和8.94 cm-1;而化合物3中Mn(II)离子之间存在反铁磁相互作用。
配位聚合物;3-(2,5-二羧基苯基)-吡啶羧酸;晶体结构;磁性
0 引言
配位聚合物的设计与合成是近些年配位化学领域研究的热点之一,不仅因为它们多样的结构,还因为它们具有高比表面积、高孔隙率、高化学稳定性和热稳定性,使其在光、磁、催化以及吸附等领域显示出诱人的应用前景[1-6]。作为一种新型的功能材料,构成配位聚合物的金属和有机配体均可灵活选择。氮杂环羧酸类配体由于具有多个配位点和良好的配位能力,常被用来构筑新型的配合物,已经引起了研究人员的广泛关注[7-10]。
吡啶羧酸类物质(如3-(2,4-二羧基苯基)-2,6-吡啶二羧酸和3-(4-羧基苯基)-2,6-吡啶二羧酸)作为配体构筑的系列配位聚合物已先后被报道[11-13]。而3-(2,5-二羧基苯基)-吡啶羧酸(H3dppa)作为吡啶羧酸类衍生物,含有吡啶环和3个羧基,具有丰富的配位点和多种配位方式,容易构筑新颖结构的化合物;同时,芳环上的羧基能够参与形成氢键,易于构筑高维配位聚合物[14-16]。
分子基磁性材料的研究一直是化学、物理、材料和信息等多学科领域热门的研究课题之一。配位聚合物结构稳定并易于合成,使其在分子磁学和分子磁体设计领域中具有重要地位[17-18]。本文以H3dppa为配体,与硝酸铜在不同溶剂体系中作用得到2种新型配位聚合物[Cu(Hdppa)(H2O)]n(1)和{[Cu2(dppa) (μ2-OH)(H2O)]·H2O}n(2);与氯化锰作用得到配位聚合物{[Mn3(dppa)2(H2O)4]·2H2O}n(3),并进一步研究3个化合物的结构和磁性。
1 实验部分
1.1 试剂与仪器
所用试剂均为分析纯试剂,未经进一步纯化处理。元素分析使用Perkin-Elemer 470型元素分析仪;红外光谱测定使用Nicolet IR-6700型红外光谱仪;粉末X射线衍射使用BRUKER D8 ADVANCE粉晶衍射仪,Cu Kα射线(λ=0.154 184 nm),管电压40 kV,管电流40 mA,扫描范围2θ为5°~55°;热重分析使用NETZSCH TG 209热重分析仪;金属配合物的变温磁化率测定使用Quantum Design MPMS-7 SQUID型磁量计,所有数据均经Pascals常数进行反磁校正;晶体结构测定使用Rigaku Pilatus 200K型X射线衍射仪和Bruker SMART 1000 CCD面探衍射仪。
1.2 化合物1~3的合成
[Cu(Hdppa)(H2O)]n(1)的合成及元素分析:取H3dppa 0.028 7 g(0.1 mmol),Cu(NO3)2·3H2O 0.024 2 g(0.1 mmol),9 m L蒸馏水和1 mL NaOH(0.1 mol· L-1)水溶液,搅拌10 min后置于密封25 mL聚四氟乙烯反应釜中,在150℃下反应72 h,然后冷却到室温,得到蓝色晶体。基于Cu(NO3)2·3H2O计算的产率为:56.4%。元素分析(C14H9CuNO7)理论值(%):C 45.85;H 2.47;N 3.82。实验值(%):C 45.36;H 2.12;N 3.18。
{[Cu2(dppa)(μ2-OH)(H2O)]·H2O}n(2)的合成及元素分析:除了将1 mL NaOH(0.1mol·L-1)水溶液换成1 mLDMF,其余步骤与1相同,得到深蓝色晶体。基于Cu(NO3)2·3H2O计算的产率为:61.8%。元素分析(C14H10Cu2NO9)理论值(%):C 36.29;H 2.18;N 3.02。实验值(%):C 36.19;H 2.03;N 2.99。
{[Mn3(dppa)2(H2O)4]·2H2O}n(3)的合成及元素分析:取H3dppa 0.057 6 g(0.2 mmol),MnCl2·4H2O 0.059 4 g(0.3mmol),9 mL蒸馏水和0.5mLDMF,搅拌10 min后置于密封25 m L聚四氟乙烯反应釜中,在120℃下反应48 h,然后在48 h内程序冷却到室温,得到无色透明晶体。基于MnCl2·4H2O计算的产率为:46.6%。元素分析(C28H24Mn3N2O18)理论值(%):C 39.97;H 2.88;N 3.33。实验值(%):C 39.88;H 2.65;N 3.12。
1.3 晶体结构测定
化合物1的晶体结构在113K下使用Rigaku Pilatus 200K型X射线衍射仪进行测定;化合物2和3的晶体结构在293 K下使用Bruker SMART 1000型X射线衍射仪进行测定,均采用石墨单色器单色化Mo Kα射线(λ=0.071 703 nm)作辐射源,以φ -ω扫描方式收集衍射点。晶体结构使用Olex2程序由直接法解出[19];用Olex2程序对非氢原子坐标及其各向异性热参数基于F2进行全矩阵最小而乘法精修;氢原子为理论加氢。在化合物2中,由于配位水分子具有较大热振动参数,因此将其分裂为2个原子O8和O8′,其占有率由软件自动分配。在化合物3中,游离水分子同样具有较大的热振动参数,因此将其分裂为2个原子O9a和O9b,其占有率由软件自动分配,难以找到合适的氢原子位置。化合物1~3的晶体学数据在表1列出,部分键长和键角列于表2。
CCDC:1442371,1;1442366,2;1442367,3。
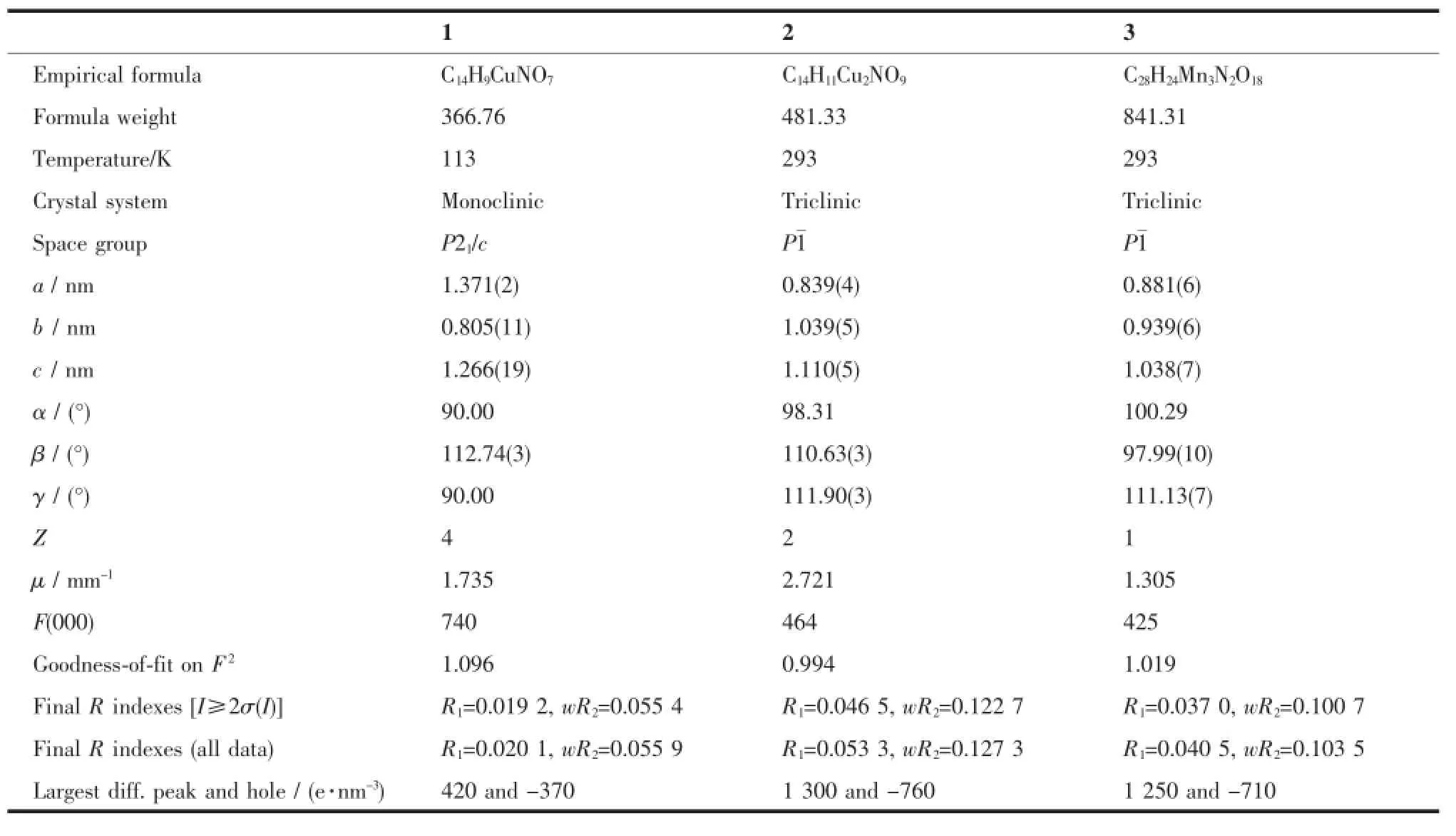
表1 化合物1~3的晶体学数据表Table 1 C rystal data and structure refinement of 1~3
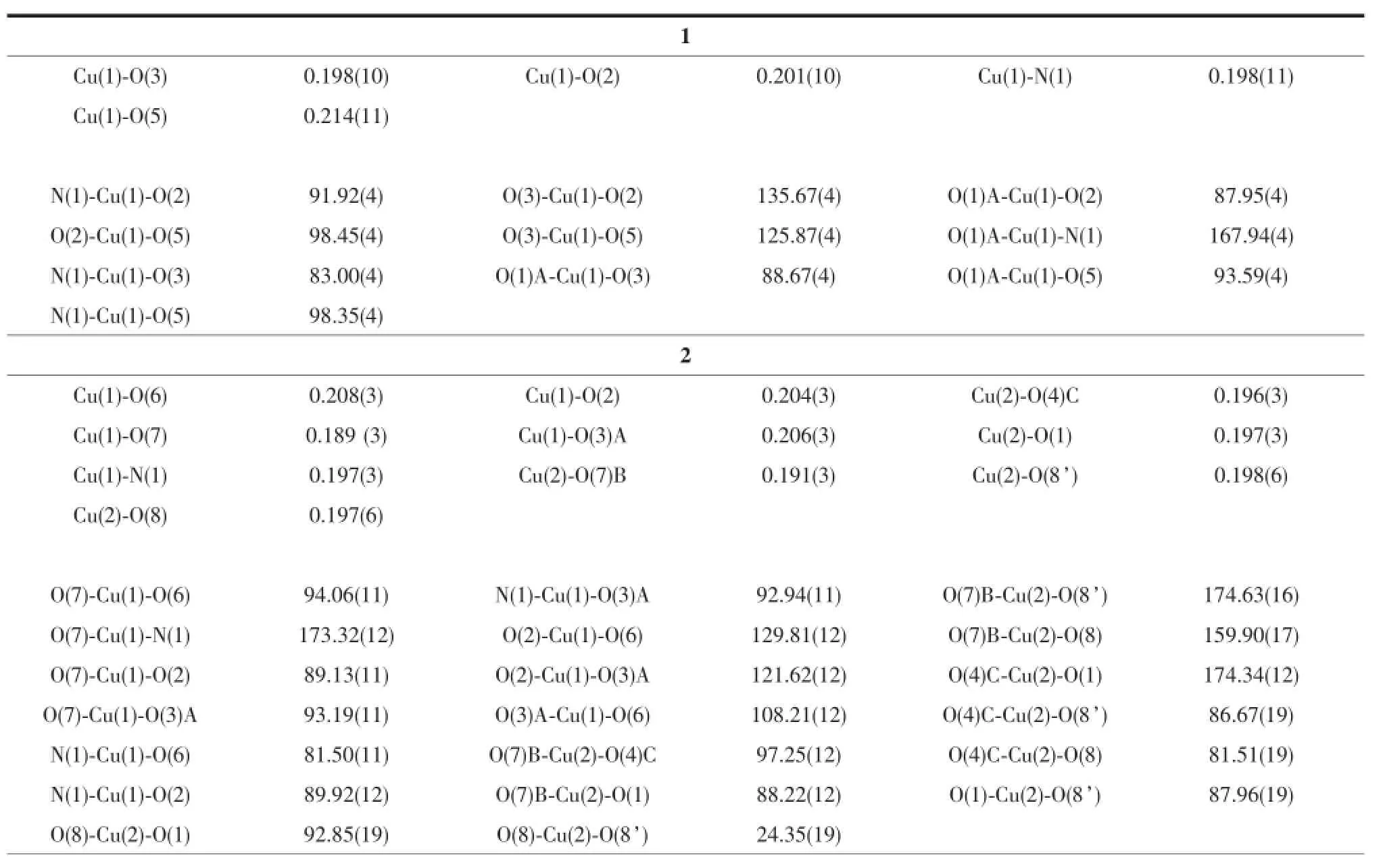
表2 化合物1~3结构中部分键长键角Tab le 2 Selected bond lengths(nm)and angles(°)for 1~3
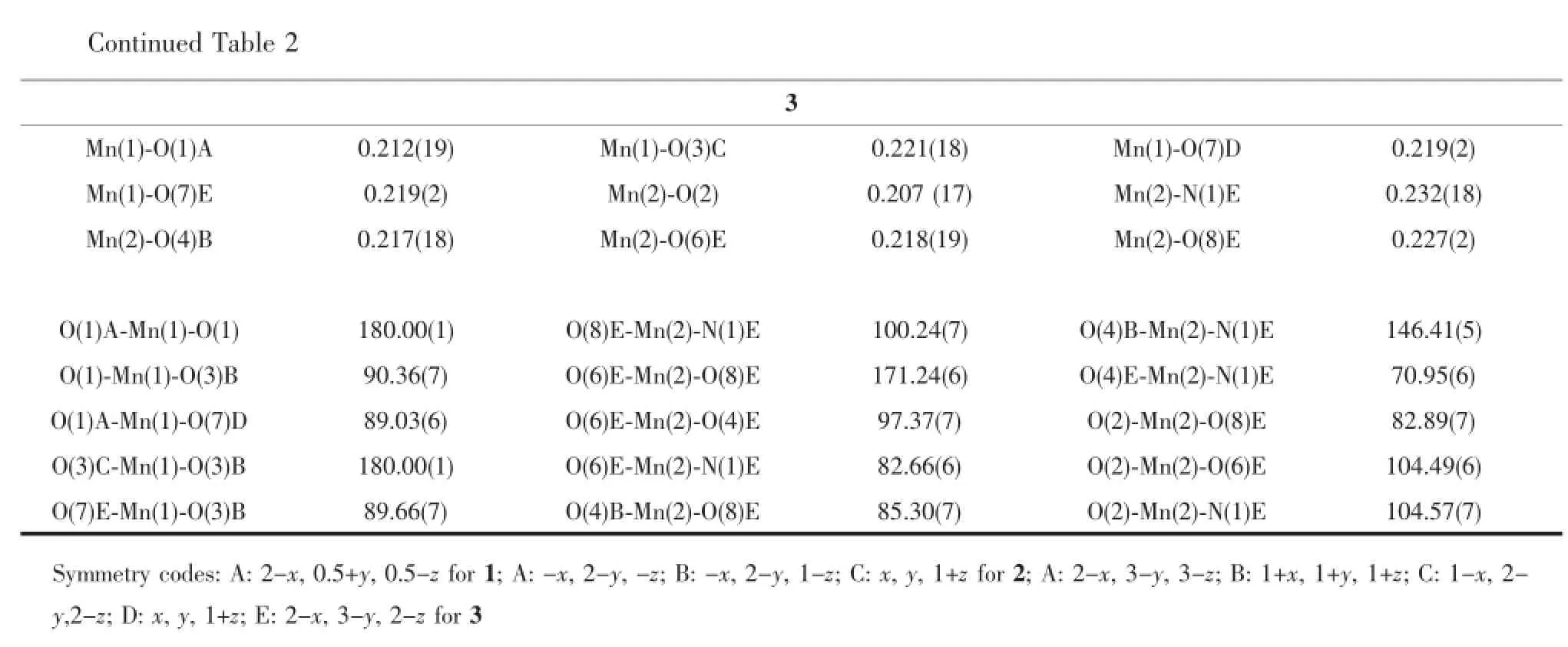
Continued Table 2 3 Mn(1)-O(1)A 0.212(19)Mn(1)-O(3)C 0.221(18)Mn(1)-O(7)D 0.219(2) Mn(1)-O(7)E 0.219(2)Mn(2)-O(2)0.207(17)Mn(2)-N(1)E 0.232(18) Mn(2)-O(4)B 0.217(18)Mn(2)-O(6)E 0.218(19)Mn(2)-O(8)E 0.227(2) O(1)A-Mn(1)-O(1)180.00(1)O(8)E-Mn(2)-N(1)E 100.24(7)O(4)B-Mn(2)-N(1)E 146.41(5) O(1)-Mn(1)-O(3)B 90.36(7)O(6)E-Mn(2)-O(8)E 171.24(6)O(4)E-Mn(2)-N(1)E 70.95(6) O(1)A-Mn(1)-O(7)D 89.03(6)O(6)E-Mn(2)-O(4)E 97.37(7)O(2)-Mn(2)-O(8)E 82.89(7) O(3)C-Mn(1)-O(3)B 180.00(1)O(6)E-Mn(2)-N(1)E 82.66(6)O(2)-Mn(2)-O(6)E 104.49(6) O(7)E-Mn(1)-O(3)B 89.66(7)O(4)B-Mn(2)-O(8)E 85.30(7)O(2)-Mn(2)-N(1)E 104.57(7) Symmetry codes:A:2-x,0.5+y,0.5-z for 1;A:-x,2-y,-z;B:-x,2-y,1-z;C:x,y,1+z for 2;A:2-x,3-y,3-z;B:1+x,1+y,1+z;C:1-x,2-y,2-z;D:x,y,1+z;E:2-x,3-y,2-z for 3
2 结果与讨论
2.1 配位聚合物的表征
红外光谱分析表明,化合物1在3 489 cm-1处的强宽峰为水的O-H伸缩振动吸收峰,1 715 cm-1处为羧基中C=O振动吸收峰,1 581和1 549 cm-1处为芳环碳骨架的振动吸收峰,见图S1。化合物2在3 568 cm-1处为羧基的O-H伸缩振动吸收峰,1 637 cm-1处为羧基中C=O振动吸收峰,1 577 cm-1为芳环碳骨架的振动吸收峰,见图S2。化合物3在3 392 cm-1处的强宽峰为水的O-H伸缩振动吸收峰,1 641 cm-1处为羧基中C=O振动吸收峰,1 600和1 572 cm-1处为芳环碳骨架的振动吸收峰,见图S3。
化合物1~3的粉末X射线衍射图谱与单晶结构模拟图谱基本吻合,见图S4~6,表明本实验得到的3个化合物样品均为纯相。
热重分析(TGA)是在氮气保护下,以10℃·min-1的升温速率,25~1 000℃范围内,在NETZSCH TG 209热重分析仪上测定的,见图S7。化合物1在30~260℃范围内失重率为4.51%,与每分子单元失去1个配位水的理论值4.91%相对应,当温度高于260℃时化合物开始分解。化合物2在30~270℃失重率为11.36%,为1个游离水和2个配位水(理论值11.57%),当温度高于270℃时化合物开始分解。化合物3在30~145℃范围内失重4.12%,为2个游离水(理论值4.34%),继续升高温度到270℃时失重12.39%,为4个配位水(理论值13.03%),当温度升高到450℃,化合物分解。
2.2 配位聚合物晶体结构
2.2.1 [Cu(Hdppa)(H2O)]n(1)晶体结构描述
X射线单晶衍射分析表明化合物1结晶在P21/c空间群,属于单斜晶系。化合物1的不对称单元包含1个Cu(II)离子,1个Hdppa2-配体和1个配位H2O分子。Cu1采用五配位模式,与其配位的原子来自1个Hdppa2-配体中的2个羧基氧原子和吡啶环上的氮原子(O2、O3、N1)和另一个配体中的氧原子(O1A),以及配位水中的氧原子(O5),如图1所示。
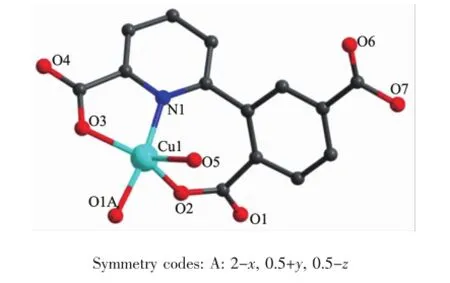
图1 化合物1中Cu(II)的配位环境Fig.1 Coordination environment of the Cu(II)in compound 1
其中,O2、O3和O5占据赤道平面的配位点,O1A和N1占据轴向上的配位点,形成一个略微变形的三角双锥结构,Cu-O键长范围为0.190~0.220 nm,Cu1-N1键长为0.198(15)nm,部分键长和键角见表2。每个Hdppa2-桥联2个Cu(II)离子沿b轴方向无限延伸,形成一维链状结构,如图2所示。
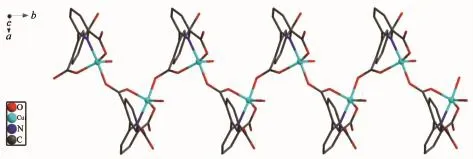
图2 化合物1的一维链状结构Fig.2 1D chain structure of the compound 1
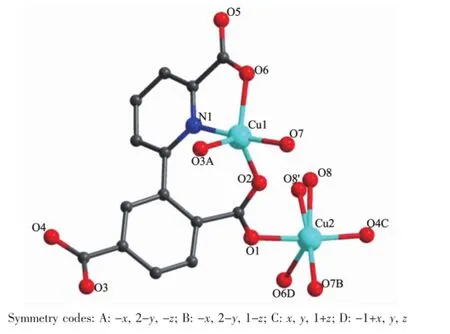
图3 化合物2中Cu(II)的配位环境Fig.3 Coordination environment of the Cu(II)in compound 2
2.2.2 {[Cu2(dppa)(μ2-OH)(H2O)]·H2O}n(2)晶体结构描述
X射线单晶衍射分析表明化合物1结晶在P1空间群,属于三斜晶系,Cu(II)配位环境如图3所示。化合物2的不对称单元包含2个Cu(II)离子,1个dppa3-配体,1个OH-,1个配位H2O分子和1个游离H2O分子。Cu1采用三角双锥结构的五配位模式,占据赤道平面配位点的O2、O3A和O6来自dppa3-配体中的羧基;占据轴向配位点的N1来自dppa3-配体的吡啶环,O7来自配位水。Cu2也采用五配位模式,分别来自dppa3-配体中的羧基氧原子(O1、O4C和O6D),以及配位水的氧原子(O7B和O8/O8′),其中O1、O4C、O7B和O8占据赤道平面的配位点,O6D则占据轴向上的配位点,形成变形的四棱锥结构,Cu-O的键长范围为0.180~0.210 nm,Cu1-N1键长为0.197(3)nm,部分键长和键角见表2。dppa3-配体桥联Cu1和Cu2沿a轴方向延伸形成一维链状结构,如图4a所示。配体中苯环上2-COO-的O1和O2以双齿顺-反(syn-anti)桥联方式连接相邻的2条一维链,形成二维层状结构(图4b)。二维层状结构通过羧基的氢键(O8-H8…O5)作用形成三维超分子结构(图4c)。
2.2.3 {[Mn3(dppa)2(H2O)4]·2H2O}n(3)晶体结构描述
X射线单晶衍射分析表明化合物3结晶在P1空间群,属于三斜晶系,Mn(II)配位环境如图5所示。化合物3的不对称单元包含1.5个Mn(II)离子,1个dppa3-配体,2个配位H2O分子和1个游离H2O分子。Mn1采用六配位模式,与其配位的原子来自dppa3-配体中羧基上的氧原子(O1、O1A、O3B和O3C)和配位水上的氧原子(O7D和O7E)。其中O1、O1A、O7D和O7E占据赤道平面的配位点,O3B和O3C则占据轴向上的配位点,形成畸变的八面体。
Mn2也采用八面体的六配位模式,占据赤道平面配位点的O2、O4E和O6E来自dppa3-配体中的羧基,O8E来自配位水;占据轴向上配位点的O4B来自dppa3-配体中羧基,N1E来自dppa3-配体的吡啶环,Mn-O键长范围为0.200~0.230 nm,Mn2-N1E键长为0.232(18)nm,部分键长和键角见表2。dppa3-配体吡啶环上6-COO-的O3B、O4B以双齿顺-反(syn-anti)方式桥联Mn1和Mn2形成沿a轴方向上的一维链状结构,如图6a所示。苯环上5-COO-的O1、O2以顺-顺(syn-syn)方式桥联相邻的两条一维链形成二维层状结构(图6c),二维层状通过羧基的氢键(O7-H7-O5)作用进一步形成三维超分子结构(图6c)。
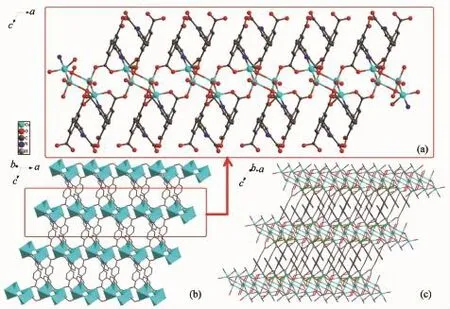
图4 化合物2的一维(a)、二维(b)和三维(c)结构Fig.4 Views of 1D(a),2D(b)and 3D(c)structure of the compound 2
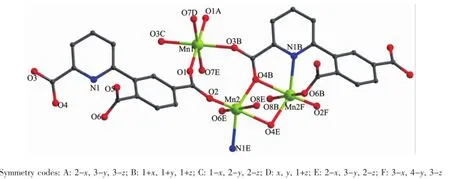
图5 化合物3中Mn(II)的配位环境Fig.5 Coordination environmentof the Mn(II)in compound 3
2.3 磁性
化合物1~3的变温磁化率是采用粉晶样品在1000Oe场强下,2~300 K温度变化范围内测定的,其χmT对T曲线如图7~9所示。当T=300 K时,化合物1的χmT值为0.367 cm3·K·mol-1,与没有耦合作用的1个Cu(II)离子(2D5/2,g=2)所对应的仅自旋值0.375 cm3·K·mol-1十分相近。温度在150~300 K之间,化合物1的χmT值几乎保持不变,随着温度继续下降,χmT迅速上升到2K时的0.826 cm3·K·mol-1。化合物1的χm-1对T的曲线如图7所示,该曲线是一条直线,符合Cure-Weiss定律χm-1=(T-θ)/C。利用χm-1(T-θ)/C对实验数据进行最小平方拟合得出的直线(图7的实线),最佳拟合参数Weiss常数θ=6.221 K,Curie常数C=0.367 cm3·K·mol-1。χmT值随T下降而上升的变化趋势和正的Weiss常数θ都表明化合物1存在铁磁耦合作用。由于在化合物1中存在
Cu-COO-Cu链,按各向同性的Heisenberg线性链磁交换模型[20]和引入分子场近似(为估算自旋中心间的磁相互作用),采用一个附加偶合参数zJ[21],拟合的结果得到Cu-Cu之间的超交换磁耦合常数J为4.44 cm-1,朗德因子g=2.01,Cu-COO-Cu链间的耦合常数zJ为-0.52 cm-1,一致性因子R=2.55×10-4(R=∑(χobsd-χcalcd)2/∑χobsd2)。
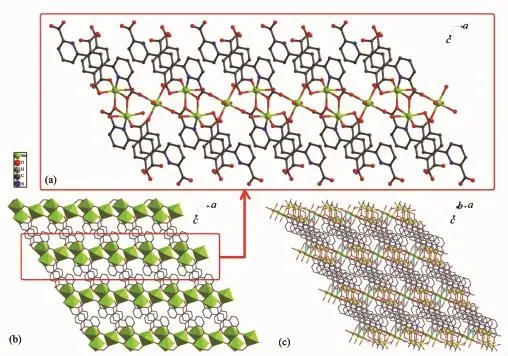
图6 化合物3的一维(a)、二维(b)和三维(c)结构Fig.6 Views of 1D(a),2D(b)and 3D(c)structure of the compound 3
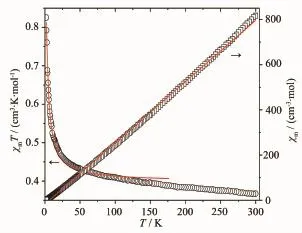
图7 化合物1的χmT对T和χm-1对T曲线Fig.7 Plots ofχmT vs T andχm-1vs T for 1
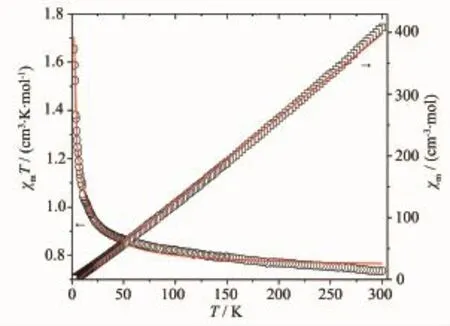
图8 化合物2的χmT对T和χm-1对T曲线Fig.8 Plots ofχmT vs T andχm-1vs T for 2
对于化合物2,当T=300 K时,2的χmT值为0.736 cm3·K·mol-1,比没有耦合作用的2个Cu(II)离子(2D5/2,g=2)所对应的仅自旋值之和0.75 cm3·K· mol-1略小。温度在20~300 K之间,化合物2的χmT值几乎保持不变,随着温度进一步下降,χmT迅速上升到2 K时的1.654 cm3·K·mol-1。化合物2的χm-1对T曲线如图8所示,该曲线是一条直线,符合Cure-Weiss定律χm-1=(T-θ)/C。利用χm-1=(T-θ)/C对实验数据进行最小平方拟合得出的直线(图8的实线)。最佳拟合参数Weiss常数θ=6.201 K,Curie常数C=0.739 cm3·K·mol-1。χmT值随T下降而上升的变化趋势和正的Weiss常数θ都表明化合物2存在铁磁耦合作用。由于在化合物2中存在着双核Cu和Cu-COO-Cu链,采用各向同性的Heisenberg磁交换模型[22]和分子场近似[21],得到双核Cu1-Cu2之间的超交换磁耦合常数J为8.94 cm-1,Cu1-Cu1之间的耦合常数为0.45 cm-1,朗德因子g=1.99,Cu-COOCu链之间的耦合常数zJ为-0.24 cm-1,R=5.8×10-5。
当T=300 K时,化合物3的χmT值为13.13 cm3·K·mol-1,与没有耦合作用的3个Mn(II)离子(6S5/2, g=2)所对应的仅自旋值之和(13.15 cm3·K·mol-1)十分相近。随着温度的下降,化合物3的χmT缓慢降到2 K时的6.66 cm3·K·mol-1。化合物3的χm-1对T曲线如图9所示,是符合Cure-Weiss定律χm-1=(T-θ)/C的一条直线。利用χm-1=(T-θ)/C对实验数据进行最小平方拟合得出的直线(图9的实线)。最佳拟合参数Weiss常数θ=-5.86 K,Curie常数C=13.27 cm3·K· mol-1。负的Weiss常数θ表明化合物3存在反铁磁耦合作用。由于化合物3结构较为复杂,没有找到合适的模型进行磁交换常数的拟合。
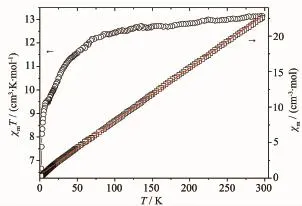
图9 化合物3的χmT对T和χm-1对T曲线Fig.9 Plots ofχmT vs T andχm-1vs T for 3
3 结论
本文报道了3个基于3-(2,5-二羧基苯基)-吡啶羧酸配体的Cu(II)、Mn(II)配合物,化合物1具有一维链状结构,化合物2和3具有二维层状结构并进一步通过氢键形成三维超分子网络。磁性研究表明,化合物1和化合物2中存在较强的铁磁耦合作用,化合物3中Mn(II)离子之间存在反铁磁相互作用。
Supporting information isavailableathttp://www.wjhxxb.cn
[1]White K A,Chengelis D A,Gogick K A,etal.J.Am.Chem. Soc.,2009,131:18069-18071
[2]Zhang Q J,Li B H,Chen L.Inorg.Chem.,2013,52:9356-9362
[3]Shultz A M,Farha O K,Hupp JT,et al.J.Am.Chem.Soc., 2009,131:4204-4205
[4]Alezi D,Belmabkhout Y,Suyetin M,et al.J.Am.Chem. Soc.,2015,137:13308-13318
[5]Black C A,Costa JS,FuW T,et al.Inorg.Chem.,2009,48: 1062-1068
[6]Cook T R,Zheng Y R,Stang P J.Chem.Rev.,2013,113: 734-777
[7]Crees R S,Cole M L,Hanton L R,et al.Inorg.Chem., 2010,49:1712-1719
[8]He Y P,Tan Y X,Zhang J.Cryst.Growth Des.,2013,13:6-9
[9]Pham T,Forrest K A,Hogan A,et al.Cryst.Growth Des., 2015,15:1460-1471
[10]Hu Z C,Pramanik S,Tan K,et al.Cryst.Growth Des., 2013,13:4204-4207
[11]You L X,Wang S J,Xiong G,et al.Dalton Trans.,2014,43: 17385-17394
[12]You L X,Li Z G,Ding F,et al.Inorg.Chem.Commun., 2014,46:340-343
[13]YOU Li-Xin(由立新),WANG Shu-Ju(王淑菊),XIONG Gang(熊刚),etal.Chinese J.Inorg.Chem.(无机化学学报), 2015,31:323-328
[14]Massoud S S,Junk T,Herchel R,et al.Inorg.Chem. Commun.,2015,60:1-3
[15]Liu B,Yu YH,JiangW H,etal.Inorg.Chem.Commun.,2015, 54:12-15
[16]Dai C,Zhou X Y,Jing X M,et al.Inorg.Chem.Commun., 2015,52:69-72
[17]ZHANG Chun-Li(张春丽),QIN Ling(覃玲),YANG Qing-Xiang(杨清香),etal.Chinese J.Inorg.Chem.(无机化学学报),2013,29:2157-2161
[18]YU Mei-Hui(于美慧),HU Ming(胡明),FENG Zhan-Yu (冯占宇),et al.Chinese J.Inorg.Chem.(无机化学学报), 2014,30:1261-1666
[19]Dolomanov O V,Bourhis L J,Gildea R J,et al.J.App l. Cryst.,2009,42:339-341
[20]Oshio H.Chem.Lett.,1991,20:227-230
[21]Kou H Z,Zhou BC,Liao D Z,etal.Inorg.Chem.,2002,41: 6887-6891
[22]Drillon M,Cornado E,Belaiche M,et al.J.Appl.Phys., 1988,63:3551-3553
Three Coordination Polymers of Cu(II)/M n(II)Based on 3-(2,5-Dicarboxylphenyl)picolinic Acid:Structure and M agnetism
WANG Shu-Ju LINMing-Ming XIONG Gang YOU Li-Xin*DING Fu SUN Ya-Guang
(Key Laboratory of Inorganic Molecule-Based Chemistry of Liaoning Province,Shenyang University of Chemical Technology,Shenyang 110142,China)
Three coordination polymers[Cu(Hdppa)(H2O)]n(1),{[Cu2(dppa)(μ2-OH)(H2O)]·H2O}n(2)and{[Mn3(dppa)2(H2O)4]·2H2O}n(3)(H3dppa=3-(2,5-dicarboxylphenyl)picolinic acid)have been synthesized by hydrothermalmethod and characterized by elemental analysis,IR spectra,PXRD and TGA.The single-crystal X-ray diffraction analysis showed that compound 1 crystalized inmonoclinic system,P21/c space group,a=1.371(2)nm,b=0.805(11)nm,c= 1.266(19)nm,β=112.74(3)°,Z=4.Compound 2 crystalized in triclinic system,P1 space group,a=0.839(4)nm,b= 1.039(5)nm,c=1.110(5)nm,α=98.31°,β=110.63(3)°,γ=111.90(3)°,Z=2.Compound 2 crystalized in triclinic system,P1 spacegroup,a=0.881(6)nm,b=0.939(6)nm,c=1.038(7)nm,α=100.29°,β=97.99(10)°,γ=111.13(7)°,Z= 1.For 1,Cu(II)were bridged by Hdppa2-ligands to form a 1D chain structure.For 2 and 3,Cu(II)and Mn(II)were respectively linked by dppa3-ligands to form 2D layersand furtherextend to a 3D supramolecular structure through the hydrogen bonding interaction.Magentic susceptibilitymeasurement indicated there were strong ferromagnetic interactions in 1 and 2,and their magnetic exchange constant was 4.44 and 8.94 cm-1respectively.There was antiferromagnetic interaction between theneighboringMn(II)ionsin 3.CCDC:1442371,1;1442366,2;1442367,3.
coordination polymers;3-(2,5-dicarboxylphenyl)picolinic acid;crystal structure;magnetism
O614.121;O614.7+11
A
1001-4861(2016)10-17830-08
10.11862/CJIC.2016.222
2016-05-09。收修改稿日期:2016-08-11。
国家自然科学基金(No.21201123)、辽宁省博士启动基金(No.201501075)、辽宁省高等学校杰出青年学者成长计划(No.LJQ2014043)和辽宁特聘教授项目(No.2013204)资助。
*通信联系人。E-mail:youlx@syuct.edu.cn