钴基双金属氧化物的制备及其在电化学储能领域的应用
黄国勇1 徐盛明*,3 杨 程永宾 李 娟
(1中南大学冶金与环境学院,长沙410083)
(2清华大学核能与新能源技术研究院,北京100084)
(3清华大学精细陶瓷北京市重点实验室,北京100084)
(4北京交通大学材料学院,北京100044)
HUANGGuo-Yong1,2XU Sheng-Ming*,2,3YANG Yue2CHENG Yong-Bin2,4LIJuan2
(1School of Metallurgy and Environment,Central South University,Changsha 410083,China)
(2Institute of Nuclear and New Energy Technology,Tsinghua University,Beijing 100084,China)
(3Beijing Key Lab of Fine Ceramics,Tsinghua University,Beijing 100084,China)
(4School of Science,Beijing Jiaotong University,Beijing 100044,China)
综述
钴基双金属氧化物的制备及其在电化学储能领域的应用
黄国勇1,2徐盛明*,2,3 杨越2 程永宾2,4李 娟2
(1中南大学冶金与环境学院,长沙410083)
(2清华大学核能与新能源技术研究院,北京100084)
(3清华大学精细陶瓷北京市重点实验室,北京100084)
(4北京交通大学材料学院,北京100044)
钴基双金属氧化物MCo2O4(M=Ni、Zn、Mn等)既继承了单一钴金属氧化物(Co3O4、CoO等)高比容量的优点,又引入了新的改性金属元素用于改善其导电性差、倍率性能不佳等缺点,是一种潜在的新型电化学储能材料。本文分类介绍了NiCo2O4、ZnCo2O4、MnCo2O4等钴基双金属氧化物及其复合物的现有研究(包括制备方法、形貌结构、颗粒尺寸及其电化学性能),阐述了改性手段的可能性机理,并对钴基双金属氧化物后续研究提出了一些看法。
钴基双金属氧化物;合成方法;形貌;改性;电化学性能
HUANGGuo-Yong1,2XU Sheng-Ming*,2,3YANG Yue2CHENG Yong-Bin2,4LIJuan2
(1School of Metallurgy and Environment,Central South University,Changsha 410083,China)
(2Institute of Nuclear and New Energy Technology,Tsinghua University,Beijing 100084,China)
(3Beijing Key Lab of Fine Ceramics,Tsinghua University,Beijing 100084,China)
(4School of Science,Beijing Jiaotong University,Beijing 100044,China)
0 引言
能源是保障社会发展的重要基础。随着世界经济的发展及人口数量的不断上涨,传统石化类能源资源经过上百年的开采已面临枯竭。因此,亟需开发高效能、低成本、可再生、环境友好的新能源资源及能源贮备装置。电池和电容器是当前最受关注并已广泛应用于日常生活的两类电化学储能装置。其中,高能量密度的锂离子电池和高功率密度的超级电容器更是当前研究的热门对象。而制约锂离子电池及超级电容器发展的瓶颈是储能材料。因此,储能材料的研发与升级换代迫在眉睫。
过渡金属氧化物因既可作锂离子电池负极材料,又可做超级电容器电极材料而备受关注[1-3]。其中,钴金属氧化物(Co3O4、CoO等)是最典型的过渡金属氧化物。其做锂离子电池负极材料时,具有较高的理论比容量,如Co3O4的理论比容量为890mAh·-1,远大于商用石墨的理论比容量,再加上其密度大,可大大缩小锂离子电池的体积,在新能源汽车领域有较大的潜在应用空间[4-6]。然而,其存在充放电时体积变化较大、导电性差等技术瓶颈,需要进一步改性提升性能。同时,钴金属氧化物做赝电容器电极材料时,具有比电容高、循环寿命长的特点,如Co3O4的理论比电容3 560 F·g-1,但其缺点是电阻偏大及成本较高[7-8]。为了提高钴金属氧化物的电化学性能,通常采用尺寸纳米化、微观结构特殊化及复合材料化,但改善效果是有限的,这是由于物质的固有性质决定了其应用性能[9-10]。
于是,通过引入活泼且相对廉价金属元素如镍、锌、锰、铜、铁、镁等,与钴、氧组成新的双金属氧化物,是一个非常有研究价值的方向。该类钴基双金属氧化物不断能继承单一钴金属氧化物(Co3O4、CoO等)高比容量、比电容的优点,又可以通过引入的改性金属元素提升材料的结构稳定性、导电性等,使其倍率性能、循环稳定性等得到同步提高,是一类潜在的新型电化学储能材料[11-13]。以该类钴基双金属氧化物为研究对象,进行材料的纳米化、特殊貌化构筑、复合化等,并研究微观结构与其电化学性能、反应机理之间的关系,将推动该类材料的实际应用,并为开发其它类似的过渡金属复合氧化物材料提供借鉴。因此,本文综述了NiCo2O4、ZnCo2O4、MnCo2O4等钴基双金属氧化物的研究进展及其在电化学领域的应用。
1 钴基双金属氧化物的研究进展及其在电化学领域的应用
1.1 NiCo2O4研究进展及其在电化学领域的应用
镍与钴的性质相似,故钴、镍双金属氧化物的制备相对较简单,易形成单一纯相。NiCo2O4主要用作超级电容器电极材料,Pu等[14]通过水热法合成了多孔六边形NiCo2O4纳米片(直径100 nm;厚度25 nm)。在1 A·g-1时,比电容为294 F·g-1;3 000次循环后,容量保留率为89.8%。Liu等[15]通过水热法在泡沫镍上制备了多孔阵列NiCo2O4。在40 A·g-1条件下,比电容为619 F·g-1;在2 A·g-1条件下,8 000次循环后,比电容仍维持在1 058 F·g-1(容量保持率为97.2%)。Wang等[16]通过类似水热法制备了海胆状纳米级NiCo2O4(直径约5μm;每根纳米线粗约100~200 nm,长度为2μm)。在1和15 A·g-1条件下,比电容分别是1 650和1 348 F·g-1;在8 A·g-1条件下,2 000次循环后,比电容损失仅为9.2%。Zou等[17]也通过水热法制备了相似结构的三维NiCo2O4微球(直径约4μm)。在2 A·g-1条件下,其比电容为1 284 F·g-1,3 000次循环后,仅有2.5%的容量损失。Padmanathan等[18]通过溶剂热法合成了不规则NiCo2O4纳米颗粒(10~20 nm),但其电化学性能一般。在0.5和10 A·g-1条件下,比电容分别为524和419 F·g-1。An等[19]通过溶剂热法制备了三维花状NiCo2O4(直径约为500 nm),具有极大的比表面积(212.6m2·g-1)。在1和10 A·g-1条件下,其比电容分别为1 191.2和755.2 F·g-1;当倍率从1 A·g-1增加至10 A·g-1,比电容仍然维持在63.4%。Yuan等[20]也通过类似溶剂热法制备了三维多孔网状NiCo2O4。在2和16 A·g-1条件下,其比电容分别为587和
518 F·g-1;3 500次循环后,其比电容衰减约为6%。Wu等[21]通过溶胶凝胶法制备了珊瑚状多孔亚微米尺寸NiCo2O4。在1 mA·cm-2条件下,其比电容为217 F·g-1,600次循环后,容量保持率为96.3%。Li等[22]通过静电纺丝法制备了NiCo2O4多孔纳米管(管径为250 nm)。在1 A·g-1条件下,其比电容为1 647 F·g-1;在25 A·g-1条件下,3 000次循环后,比电容损失率为6.4%。Ding等[23]通过液相沉淀及热分解法合成了不规则块状NiCo2O4,比表面积为190 m2·g-1,孔隙率为1.136 cm3·g-1。在1 A·g-1条件下,其比电容为351 F·g-1。Jiang等[24]通过类似方法合成了多孔NiCo2O4纳米线,在1 A·g-1时,比电容为743 F·g-1,3 000次循环后,比电容仅损失6.2%。Yuan等[25]把制备的超薄NiCo2O4纳米片(2~5 nm)固定到镍箔上。在20 A·g-1条件下,其比电容高达1 450 F·g-1(见图1)。Wang等[26]也将NiCo2O4纳米线阵列(直径80~200 nm;长度3μm)固定到镍箔上。在1mA·cm-2条件下,比电容为161mF·cm-2。用于超级电容器的不同类型NiCo2O4性能对比详见表1所示。
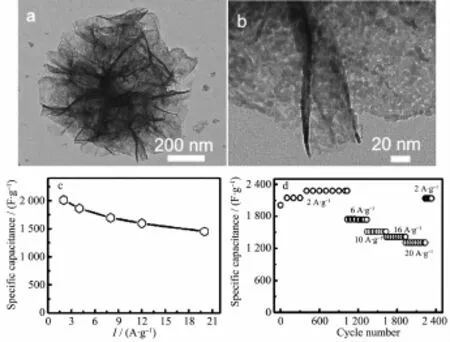
图1 (a,b)NiCo2O4的SEM图片;(c,d)NiCo2O4的电化学性能曲线[25]Fig.1(a,b)SEM images of the NiCo2O4;(c,d) Electrochemical performance of NiCo2O4[25]
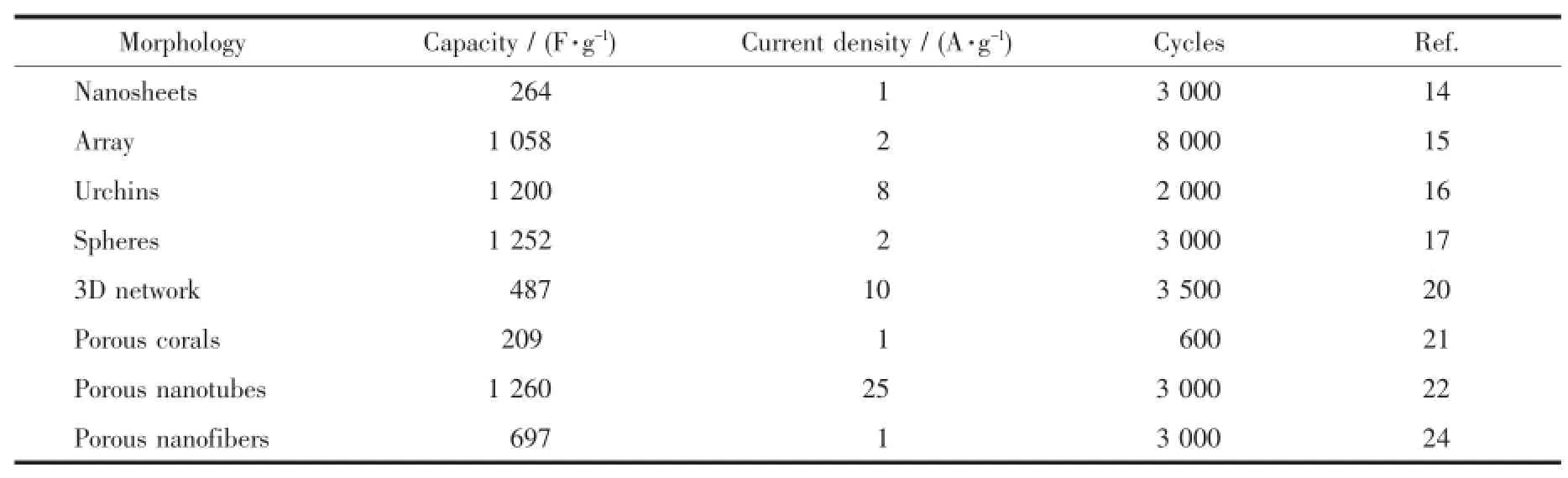
表1 用于超级电容器的不同种类NiCo2O4性能对比Table 1 Com parison of the performance of different NiCo2O4materials used in supercapacitor
同时,NiCo2O4也可用作锂离子电池负极材料。Li等[27]通过溶剂热法合成了单分散NiCo2O4介孔微球(直径2~3μm,平均孔径14.5 nm)。在0.2 A·g-1条件下,30次循环后,放电比容量仍高达1 198 mAh· g-1;在大电流0.8 A·g-1条件下,500次循环后,可逆比容量仍维持在705 mAh·g-1。Li等[28]通过溶剂热法制备了三维分级多孔花状NiCo2O4(直径约为1.5 μm)。在100mA·g-1条件下,60次循环后,其可逆比容量约为939mAh·g-1。Xu等[29]通过溶剂热法合成了NiCo2O4亚微米颗粒(0.5~1.0μm)。在100mA·g-1条件下,首次放电比容量大于1 200 mAh·g-1,100次循环后,可逆比容量为550 mAh·g-1。Chen等[30]通过模板法定向生长了NiCo2O4纳米线阵列(长2.0 μm,直径50~80 nm)。在100mA·g-1条件下,首次放电比容量为2 025mAh·g-1,但容量保持率一般。用于锂离子电池的不同类型NiCo2O4性能对比详见表2所示。
如上所述,目前制备NiCo2O4常用方法是溶剂热法和水热法,其他方法包括溶胶凝胶法、液相沉淀法、模板法、静电纺丝法等。制备的NiCo2O4微观结构各异,包括纳米线、纳米棒、纳米片、海胆状、微球、三维花状、多孔网状、珊瑚状等,主要应用在超级电容器上,锂离子电池领域研究相对较少。
1.2 ZnCo2O4的研究进展及其在电化学领域的应用
锌元素的化学性质较活波,且导电性好,钴、锌二元氧化物的研究也颇多。ZnCo2O4主要用作锂离子电池负极材料,Liu等[31]通过水热法合成ZnCo2O4纳米棒(直径15~22 nm,长度150~200 nm)。在0.2
mA·cm-2条件下,初始放电比容量为1 509 mAh·-1,50次循环后,容量为767 mAh·g-1;且EIS数据表明其具有较低的表层电阻(约为192Ω)。Mohamed等[32]通过水热法制备了由纳米线(直径约为70~100 m,长度约为2.5μm)组成的花状ZnCo2O4。在200 mA·g-1条件下,首次放电比容量为1 430 mAh·-1,50次循环后,放电比容量为900 mAh·g-1。Hao等[33]通过类似水热法制备了多孔花状ZnCo2O4微米球(平均直径约为1.2μm)。在0.7 A·g-1条件下,首次放电比容量1 209mAh·g-1,1 000次循环后,可逆比容量仍高达856mAh·g-1。Guo等[34]通过水热法制备了类似的多孔ZnCo2O4微米球(直径6~8μm,平均孔径30 nm)。在1 A·g-1条件下,首次放电比容量366 mAh·g-1,200次循环后,可逆比容量仍高达74 mAh·g-1。Xie等[35]通过水热法制备了双壳中空ZnCo2O4微米球(直径1.3μm,壳厚90~180 nm),在.1C条件下,其初始放电比容量值为1 025 mAh·-1,120次循环后,可逆比容量仍保持为1 019 mAh·g-1。Hu等[36]通过溶剂热法合成了由纳米片(5 m)组成的三维ZnCo2O4微米球(直径1.0~1.5μm)。在100 mA·g-1条件下,初始放电比容量为1 332 mAh·g-1,80次循环后,放电比容量维持在721 mAh·g-1;在大电流1 A·g-1条件下,初始比容量仍高达937 mAh·g-1,40次循环后,放电比容量为432 mAh·g-1。Guo等[37]通过溶剂热法合成了类菠萝状ZnCo2O4微球(直径5~6μm)。在大电流1 A·g-1条件下,初始放电比容量仍达到1 333 mAh·g-1,200次循环后,可逆比容量为800mAh·g-1。Kang等[38]通过类似溶剂热法合成了多孔ZnCo2O4微米棒(直径2 μm,长10μm)。在0.2 A·g-1条件下,初始放电比容量为1 293.7mAh·g-1,100次循环后,可逆比容量仍为937.3mAh·g-1;在大电流2.0 A·g-1条件下,初始放电比容量为925.0mAh·g-1。Song等[39]通过共沉淀法合成了多孔片状ZnCo2O4(厚度为30~80 nm)。在.1 A·g-1条件下,50次循环后,比容量为1 275 mAh·g-1;在0.5和3.0 A·g-1条件下,分别为1 130和730 mAh·g-1。Du等[40]通过常温液相沉淀及热分解法制备了多孔棒状ZnCo2O4(长几微米,直径100~300 nm),并发现煅烧温度影响其电化学性能。在100 mA·g-1条件下,500℃煅烧所得材料的电化学性能更好,其首次放电比容量高达1 331.5 mAh· g-1(见图2)。Liu等[41]通过模板法制备了海胆状的ZnCo2O4(直径约10μm)。在0.18 A·g-1条件下,100次循环后,比容量为1 180mAh·g-1;在高倍率18 A·g-1条件下,首次放电比容量仍为750 mAh·g-1。Luo等[42]通过静电纺丝法合成了孔状ZnCo2O4管(长度几毫米,直径200~300 nm,壁厚50 nm)。在100 mA·g-1条件下,首次放电比容量为1454 mAh·g-1,在大电流2 A·g-1条件下,30次循环后,可逆比容量为794mAh·g-1。Li等[43]通过回流热解法制备了均一的核壳结构ZnCo2O4微米球(壳厚50 nm,核直径600 nm)。在0.2 A·g-1条件下,首次放电比容量大于1 300mAh·g-1,100次循环后,放电比容量仍保持为950mAh·g-1;在大电流1 A·g-1条件下,500次循环后,放电比容量仍保持为331mAh·g-1。Sharma等[44]通过尿素燃烧法制备了ZnCo2O4纳米颗粒(15~20 nm)。在60mA·g-1条件下,温度分别为25℃和55℃时,其首次可逆比容量分别为900和960 mAh· g-1,即热稳定较好。Qu等[45]采用模板法在Ni箔上生长了三维ZnCo2O4纳米线,这种鹅毛状纳米线组成了疏松阵列。在1 A·g-1条件下,50次循环后,比容量仍保持为932mAh·g-1。Zhu等[46]采用微波法合成了二维超薄ZnCo2O4纳米层状物(比表面积高达181 m2·g-1)。在200mA·g-1条件下,200次循环后,可逆比容量仍保持约为960 mAh·g-1。用于锂离子电池的不同类型ZnCo2O4性能对比详见表3所示。
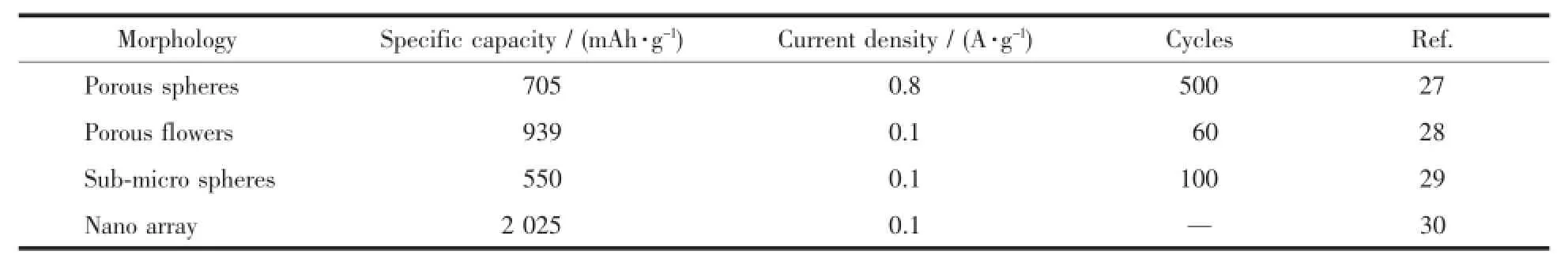
表2 用于锂离子电池的不同种类NiCo2O4性能对比Table 2 Comparison of the performance of different NiCo2O4materials used in Li-ion batteries
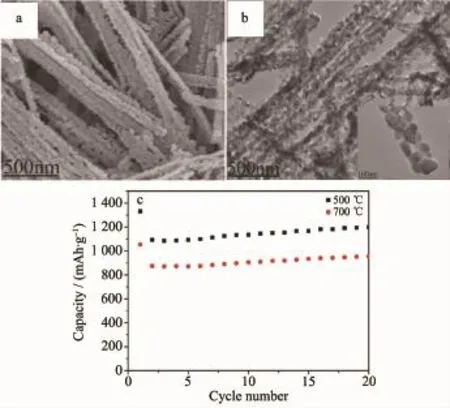
图2 (a,b)ZnCo2O4的SEM图与TEM图;(c)ZnCo2O4的电化学性能曲线[40]Fig.2(a,b)SEM and TEM images of the ZnCo2O4; (c)Electrochemical performance of ZnCo2O4[40]
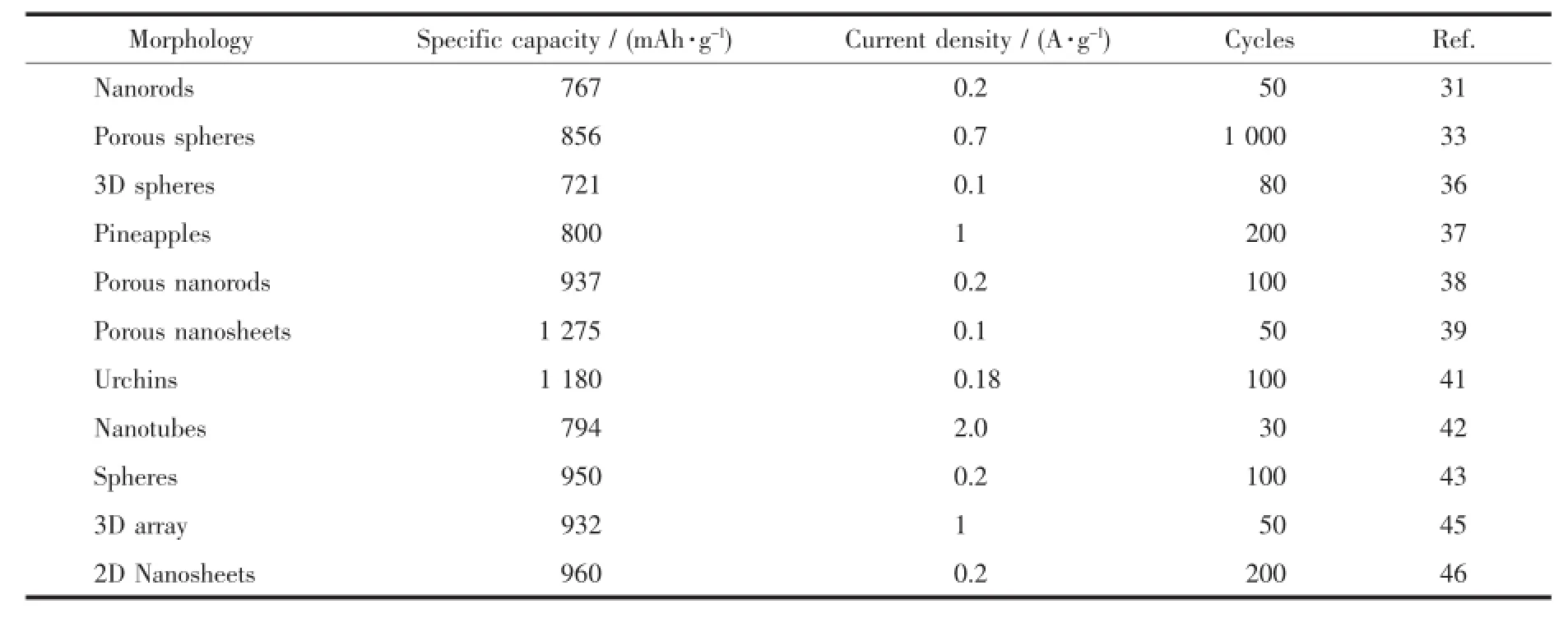
表3 用于锂离子电池的不同种类ZnCo2O4性能对比Table 3 Comparison of the performance of different ZnCo2O4materials used in Li-ion batteries
ZnCo2O4在超级电容器领域应用如下:Huang等[47]通过水热法制备了棒状ZnCo2O4颗粒(27 nm)。其在1 A·g-1条件下,比电容为604.5 F·g-1,3 000次循环后,比电容保持率为95.6%。Ratha等[48]通过水热法合成了自组装的ZnCo2O4纳米片。其在20 A· g-1条件下,比电容为1 691 F·g-1,5 000次循环后,比电容保持率大于75%。Liu等[49]通过溶剂热法制备了不规则ZnCo2O4纳米线。在1 A·g-1条件下,比电容约为1 400 F·g-1;在6 A·g-1条件下,1 000次循环后,仅有3%的容量损失。Wang等[50]通过溶剂热法合成了多孔ZnCo2O4微米球(直径5~10μm)。其在10 A·g-1条件下,比电容为440.6 F·g-1,2 000次循环后,比电容损失率仅为8%。Bao等[51]通过模板法在Ni箔上均匀生长了介孔ZnCo2O4纳米片阵列。其在30 A·g-1条件下,比电容为1 850 F·g-1,1 500次循环后,比电容保持率为96.3%。用于超级电容器的不同类型ZnCo2O4性能对比详见表4所示。
如上所述,制备ZnCo2O4的常用方法仍然是水热法、溶剂热法及热分解法,其他方法包括模板法、静电纺丝法等。ZnCo2O4的微观结构主要为常规的棒状、片状、球状及阵列,主要应用在锂离子电池领域,超级电容器研究较少。ZnCo2O4的电化学性能(特别是倍率性能)要明显优于单一的Co3O4与CoO[4-6,11-13],但其比容量要略低于NiCo2O4。

表4 用于超级电容器的不同种类ZnCo2O4性能对比Table 4 Com parison of the performance of different ZnCo2O4materials used in supercapacitor
1.3 M nCo2O4的研究进展及其在电化学领域的应用
锰的价态较多,加入锰元素形成钴、锰二元氧化物,易产生原子空位、占位等结构,可促进锂离子的迁移,提升电化学性能。Huang等[52]通过水热法合成了具有核壳结构与浓度梯度的MnCo2O4微米椭球(长轴2.5~4.5μm,短轴1.5~2.5μm;外壳层厚度
00~300 nm;外壳层钴含量要高于内核)。在0.1和.4 A·g-1条件下,首次放电比容量分别为1 433.3和1 248.4mAh·g-1;60次循环后,可逆比容量分别维持在900和620 mAh·g-1。Wu等[53]采用水热法合成了类似的不同形貌的核壳结构MnCo2O4颗粒。在.4 A·g-1条件下,其首次放电比容量最高达1 033.3 mAh·g-1,50次循环后,容量保持率最高为74.2%。Liu等[54]通过水热法制备了纳米尺寸的MnCo2O4(10~20 nm),XPS表征结果显示Mn和Co的化合价分别是+4和+2。在0.2 mA·cm-2条件下,首次放电比容量达到1 448mAh·g-1。Zhang等[55]采用液相沉淀结合水热法合成了MnCo2O4立方颗粒(直径4μm)。在0.8 A·g-1条件下,120次循环后,其可逆容量约为600mAh·g-1。Li等[56]采用溶剂热法结合热分解法合成了MnCo2O4和Mn2CoO4中空微米球(直径2.5~.5μm)。在0.2 A·g-1条件下,25次循环后,其可逆容量分别为755和706 mAh·g-1。Li等[57]采用溶剂热法结合热分解合成了多孔MnCo2O4球(直径200~00 nm)。在1 A·g-1条件下,其首次放电比容量最高达1 034mAh·g-1,1 000次循环后,可逆比容量约为40mAh·g-1。Li等[58]通过热分解法制备了类似的中空结构MnCo2O4亚微米球(直径250 nm)。通过控制升温速率,分别得到了介孔球、中空球、蛋黄-壳球、双壳球、多层壳球等。在0.4 A·g-1条件下,首次放电比容量最高能达到1 425 mAh·g-1;100次循环后,可逆比容量最大为850mAh·g-1(见图3)。Venkatachlam等[59]采用水热法合成MnCo2O4纳米线。在0.5 A·g-1条件下,其首次比电容为718.8 F·g-1;在2 A·-1条件下,1 000次循环后,比电容为500 F·g-1。ahoo等[60]采用模板法合成MnCo2O4纳米片阵列(厚度10~40 nm,长度1~2μm)。在0.25 A·g-1条件下,其首次比电容为250 F·g-1,1 000次循环后,比电容无衰减。用于锂离子电池的不同类型MnCo2O4性能对比详见表5所示。

表5 用于锂离子电池的不同种类MnCo2O4性能对比Table 5 Com parison of the performance of differen t M nCo2O4m aterials used in Li-ion batteries
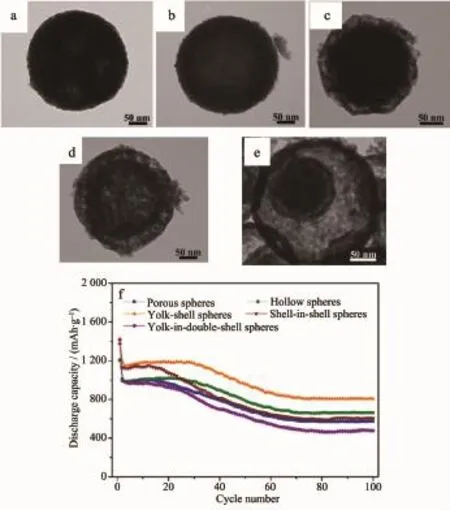
图3 (a~e)MnCo2O4的SEM图;(f)MnCo2O4的电化学性能曲线[58]Fig.3(a~e)SEM images of the MnCo2O4;(c)Electrochemical performance of MnCo2O4[58]
MnCo2O4的研究明显少于NiCo2O4与ZnCo2O4,这可能是由于锰元素的价态较多,易产生Mn2O3、MnO2等杂质,纯相的MnCo2O4较难合成。其合成方法主要为水热法、溶剂热法与热分解法等;结构为常见的球形,其他特殊形貌较少;且主要应用在锂离子电池领域,超级电容器研究较少。MnCo2O4的电化学性能尚可,具有一定的改性作用,但效果不及NiCo2O4与ZnCo2O4显著。
1.4 其它MCo2O4的研究进展及其在电化学领域的应用
除了常见的Ni、Zn、Mn与Co形成双金属氧化物,还有Fe、Mg、Cu等金属也能与Co形成双金属氧化物。Sharma等[61]通过尿素燃烧和草酸分解的方法合成了FeCo2O4与MgCo2O4。在60 mA·g-1条件下,FeCo2O4的首次比容量为827 mAh·g-1,MgCo2O4
的首次比容量为736mAh·g-1;50次循环后,FeCo2O4的容量保持率约90%,而MgCo2O4的容量保持率较差;该结果表明Fe作为复合元素要比Mg的效果更好。Liu等[62]采用液相沉淀法制备了中空FeCo2O4纳米球,在100 mA·g-1和1 A·g-1条件下,初始放电比容量分别为1 289和823 mAh·g-1。Sharma等[63]通过类似的尿素燃烧法合成了纳米CuCo2O4(10~20 nm)。在60 mA·g-1条件下,50次循环后,可逆比容量约为750 mAh·g-1。Sun等[64]采用模板法制备了有序介孔结构CuCo2O4,在60 mA·g-1条件下,初始放电比容量高达1 564mAh·g-1,但容量保持率一般。Ma等[65]采用水热法合成了CuCo2O4多面体颗粒,在1 A·g-1条件下,初始放电比容量约为1 000 mAh· g-1,100次循环后,可逆比容量约为500 mAh·g-1。Krishnan等[66]采用喷雾热分解法合成不规则MgCo2O4颗粒。在2 A·g-1条件下,其首次比电容约为350 F·g-1。Pendashteh等[67]采用模板法合成了多孔CuCo2O4纳米线阵列。在2 A·g-1条件下,其首次比电容约为3 000 F·g-1,接近理论值。Chen等[68]采用模板法合成了类似的CuCo2O4纳米线阵列。在1.7 A·g-1条件下,其首次比电容约为611 F·g-1,8 000次循环后,其比电容保持率为94.8%。其他类ZnCo2O4电化学性能对比详见表6所示。
其它MCo2O4的研究要远远少用NiCo2O4、ZnCo2O4与MnCo2O4。其合成方法主要为热分解法与模板法等,微观结构的设计构筑较少,在电化学储能领域的应用才刚刚起步。
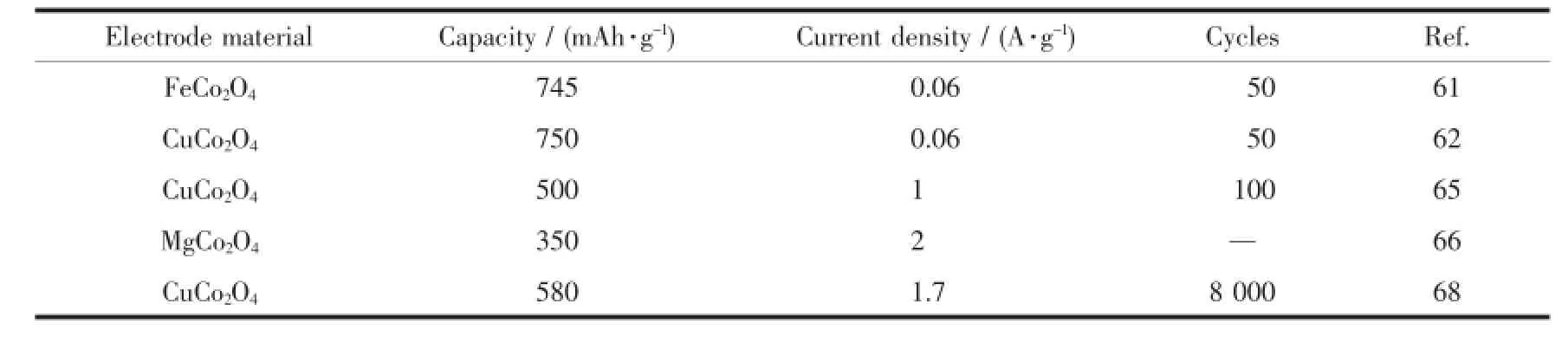
表6 其它类型M Co2O4电化学性能对比Table 6 Comparison of the electrochem ical performance of other MCo2O4materials
2 钴基双金属氧化物复合材料的研究进展及其在电化学领域的应用
在钴基双金属氧化物的基础上,通过复合改性可进一步提高其电化学性能。其与碳素类材料的复合研究如下:He等[69]通过水热法将NiCo2O4纳米线负载在还原氧化石墨烯(Reduced Graphene Oxide, RGO)上得到了NiCo2O4@RGO复合材料。在1 A·g-1条件下,比电容高达737 F·g-1;在4 A·g-1的条件下,3 000次循环后,比电容损失仅为6%。Wang等[70]也制得了类似的NiCo2O4/RGO复合材料,在20 A·g-1条件下,比电容为615 F·g-1;4 000次循环后,比容量维持在908 F·g-1(比初始值更高)。Yuan等[71]通过水热法制备了MnCo2O4@RGO复合材料。在1 A·g-1条件下,首次比电容为334 F·g-1,2 000次循环后,比电容保持率为98%。Huang等[72]制备了三维Ni(OH)2/NiCo2O4/C复合材料,在2 mA·cm-2条件下,面积比电容为5.2 F·cm-2。Yang等[73]采用模板法制备了NiCo2O4@NiO/C复合材料,在5 mA·cm-2条件下,比电容高达1 792 F·g-1,5 000次循环后,电容保留率为87.5%。Nguyen等[74]通过模板法在镍箔上制备了NiCo2O4/石墨烯复合材料。在7.5 A·g-1条件下,首次比电容为1 950 F·g-1;在3.0 A·g-1条件下,10 000次循环后,比电容保持率为92.8%。Zhou等[75]通过类似模板法在镍箔上制备了三维结构NiCo2O4/石墨烯复合材料。在6和200 A·g-1条件下,首次比电容分别为2 173和954 F·g-1;在100 A·g-1条件下,14 000次循环后,比电容保持率为94%。Zhang等[76]通过气相沉积法制备了花状NiCo2O4/石墨烯复合材料。在1 A·g-1条件下,首次比电容为1 402 F·g-1;在5 A·g-1条件下,5 000次循环后,比电容保持率为76.6%。Li等[77]通过模板法制备了NiCo2O4/碳纳米管(Carbon nanotubes,CNT)复合材料。在3和30 A·g-1条件下,首次比电容分别为1 533和1 335 F·g-1,2 000次循环后,比电容无衰减。Gao等[78]通过溶剂法将NiCo2O4沉积在多壁碳纳米管上形成复合材料。在1 A·g-1条件下,首次比电容为1 843.3 F·g-1;在10 A·g-1条件下,4 000次循环后,比电容衰减率为10%。Gao等[79]通过模板法制备了NiCo2O4/C复合二维阵列材料。在5mA·cm-2条件下,首次比电容为1 768 F·g-1,5 000次循环后,比电容保持率为96.8%。Li等[80]通过两步水热法合成了NiCo2O4/C核壳结构的亚微米球(250~300
m)。在1 A·g-1条件下,首次比电容分别为1 420 F·-1,3 000次循环后,比电保持率为98.5%。Bai等[81]通过模板法合成了ZnCo2O4/石墨烯/碳纳米管复合材料。在1 A·g-1条件下,首次比电容分别为1 802 F·g-1;在10 A·g-1条件下,4 000次循环后,比电容无衰减。用于超级电容器的不同MCo2O4复合材料性能对比详见表7所示。
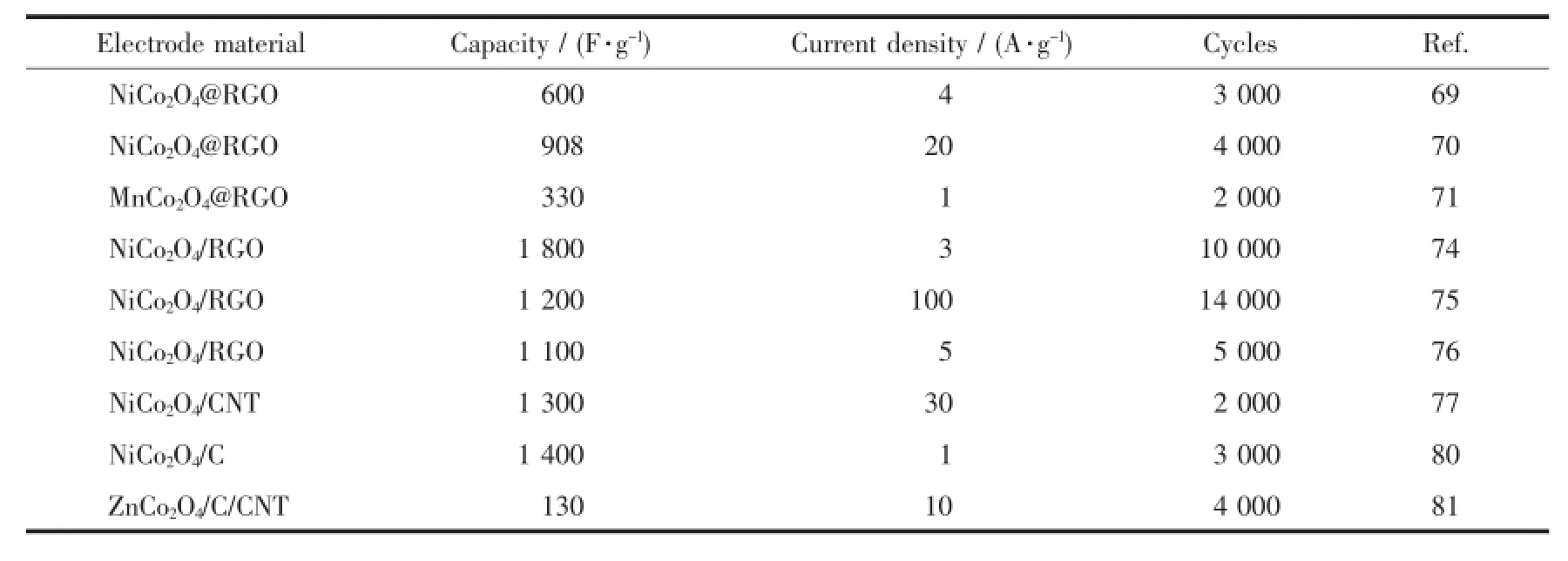
表7 用于超级电容器的不同MCo2O4复合材料性能对比Table 7 Comparison of the performance of different composites of MCo2O4and carbon m aterials used in supercapacitor
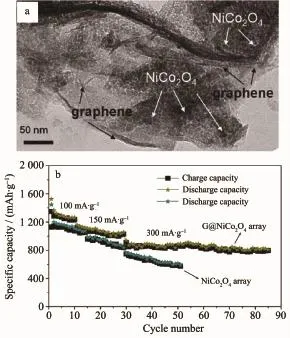
图4 (a)NiCo2O4/石墨烯的TEM图;(b)NiCo2O4/石墨烯的电化学性能曲线[82]Fig.4(a)TEM images of the NiCo2O4/Graphene; (b)Electrochemical performance of NiCo2O4/ Graphene[82]
同时,Chen等[82]通过模板法在镍箔上生长形成了NiCo2O4/石墨烯纳米片阵列。在100 mA·g-1条件下,首次放电比容量为1 216mAh·g-1,80次循环后,可逆比容量仍大于800mAh·g-1(见图4)。Liu等[83]制备了三维ZnCo2O4纳米线阵列/碳复合材料。在200 mA·g-1条件下,首次放电比容量大于1 300 mAh· g-1,160次循环后,比容量仍为1 200mAh·g-1。Rai等[84]通过液相沉淀法制备了ZnCo2O4/石墨烯复合材料。在100 mA·g-1条件下,首次放电比容量为1 124.8mAh·g-1,但容量保持率一般。Mo等[85]通过溶剂热法制备了NiCo2O4/C复合微球(平均粒径3.4 μm)。在400mA·g-1条件下,180次循环后,可逆比容量仍保持1 389mAh·g-1。Peng等[86]通过模板法制备了NiCo2O4/C纳米阵列(长2.5μm,直径10~30 nm)。在2 A·g-1条件下,首次放电比容量为664 mAh·g-1;在100mA·g-1条件下,200次循环后,比容量保持率为97%。用于锂离子电池的不同MCo2O4复合材料性能对比详见表8所示。
钴基双金属氧化物与其他材料的复合研究如下:Liu等[87]通过溶胶凝胶方法制备了介孔结构的NiO/NiCo2O4/Co3O4复合材料。在20 mA·cm-2条件下,比电容高达1 600 F·g-1;1 000次循环后,比电容保持率为94.9%。Lee等[88]通过氨气-蒸发-诱导方法制备了ZnO/ZnCo2O4亚微米棒阵列。在45mA· g-1条件下,首次放电比容量约为900 mAh·g-1。Li等[89]采用模板法制备了ZnCo2O4/ZnO/C复合材料。在100 mA·g-1条件下,首次放电比容量为1 400 mAh·g-1,140次循环后,可逆比容量为1 200mAh· g-1。Zou等[90]采用类似模板法制备了ZnCo2O4/MnO2纳米线阵列(长5μm,直径20 nm)。在10 mA·cm-2条件下,首次比电容为2 500 F·g-1,3 000次循环后,比电容损失率为1.6%。Zhai等[91]采用水热法制备了NiCo2O4/MnCo2O4亚微米球(直径约1μm)。在1 A·g-1条件下,600次循环后,可逆比容量为1 009
mAh·g-1;在5 A·g-1条件下,首次比电容为911.3 F· g-1,1 000次循环后,比电容为800 F·g-1。
如上所述,钴基双金属氧化物主要通过与石墨烯、碳纳米管、碳等炭素类材料复合。碳素类材料不仅可以弥补金属氧化物性导电差的缺陷,也可以缓冲双金属氧化物充放电过程中的体积变化,增大双金属氧化物材料的循环稳定性能和倍率性能;同时,碳素类材料自身可贡献一定的比电容或比容量。

表8 用于锂离子电池的不同M Co2O4复合材料性能对比Table 8 Com parison of the per formance of different composites of MCo2O4and carbon materials used in L i-ion batteries
3 总结与展望
综上所述,当前的钴基双金属氧化物主要围绕着“制备方法-微观结构控制-电化学性能-机理分析”这一路线展开。NiCo2O4、ZnCo2O4、MnCo2O4等钴基双金属氧化物的电化学性能(尤其是倍率性能及循环寿命)在一定程度上要优于单一钴金属氧化物(Co3O4、CoO等),起到了改性的作用[4-6];通过与碳素类、金属及其他金属氧化物复合,能进一步提高其电化学性能[92]。鉴于钴基双金属氧化物的诸多优点,其在锂离子电池、超级电容器、新型钠离子电池等能源存储设备领域有较大的应用潜力和优势[92-93]。
同时,不同形貌的钴基双金属氧化物的电化学性能存在明显差异。零维结构(量子点、球形、类球形等)材料的倍率性能普遍一般(高倍率下容量衰减快),采用空心结构可适当缓冲在充放电过程中的体积效应,达到改善效果。一维结构(管状、线状、纤维状等)材料的比表面积大,可有效增大电极材料与电解液接触面积,缩短了锂离子传输距离,表现出了良好的倍率性能。二维结构(层状、片状等)与三维结构(阵列、介孔等)的材料,多为与碳素类(石墨烯、碳纳米管等)的复合型材料,碳素成分可形成富有弹性的导电网络,可大幅缓解金属氧化物部分在高倍率充放电过程中体积的变化,并可提升活性材料与电解液的相溶性,使得循环寿命及循环稳定性均有大幅提升。另外,合成方法也一定程度上影响了材料的性能,水热法与溶剂热法是最常用的方法,这是由于其合成的材料结晶完整、颗粒一致性好,材料的电化学性能普遍较优异。
但是,钴基双金属氧化物仍然存在着过渡金属氧化物类负极材料的一些共性问题未解决:(1)电压平台较高(约1.0 V),只能与高电压平台的正极材料相匹配;(2)首次不可逆比容量损失较大(约30%);(3)充放电电压差较大[95-97]。且当前钴基双金属氧化物的研究较为分散,未横向对比研究不同种类钴基双金属氧化物的性能差异及反应机理区别;材料形貌、粒径、微观结构等与电化学性能之间尚无通用的规律与关系;没有深入研究金属元素之间的配比及相互作用的机理;材料的复合改性及表面修饰研究才刚刚起步[98-100]。因此,为了促进钴基双金属氧化物在电化学储能领域的商业化应用,亟需针对上述关键问题进行深入研究。
[1]Xie D,Yuan W W,Dong Z M,et al.Electrochim.Acta, 2013,92:87-92
[2]Mai Y J,Tu JP,Xia X H,et al.J.Power Sources,2011,196: 6388-6393
[3]Huang G Y,Xu SM,Cheng Y B,et al.Int.J.Electrochem. Sci.,2015,10:2594-2601
[4]Huang G Y,Xu S M,Lu S S,et al.ACS Appl.Mater. Interfaces,2014,6:7236-7243
[5]Huang G Y,Xu SM,Lu SS,et al.Electrochim.Acta,2014, 135:420-427
[6]Huang G Y,Xu SM,Yang Y,et al.Int.J.Electrochem. Sci.,2015,10:10587-10596
[7]Ujjain SK,Singh G,Sharma R K.Electrochim.Acta,2015, 169:276-282
[8]Yao M M,Hu Z H,Xu Z J,et al.J.A lloys Compd.,2015, 644:721-728
[9]Meng T,Xu Q Q,Wang Z H,et al.Electrochim.Acta,2015, 180:104-111
[10]Feng C,Zhang J F,He Y,et al.ACS Nano,2015,9:1730-1739
[11]Tholkappiyan R,Naveen A N,Sumithra S,et al.J.Mater. Sci.,2015,50:5833-5843
[12]Zhou X Y,Chen G H,Tang J J,et al.J.Power Sources, 2015,299:97-103
[13]Wang Y,Wang M S,Chen G,et al.Ionics,2015,21:623-628
[14]Pu J,Wang J,Jin X Q,et al.Electrochim.Acta,2013,106: 226-234
[15]Liu X Y,Zhang Y Q,Xia X H,et al.J.Power Sources, 2013,239:157-163
[16]Wang Q F,Liu B,Wang X F,et al.J.Mater.Chem.,2012, 22:21647-21653
[17]Zou R J,Xu K B,Wang T,et al.J.Mater.Chem.A,2013, 1:8560-8566
[18]Padmanathan N,Selladurai S.Ionics,2013,19:1535-1544
[19]An C H,Wang Y J,Huang Y N,et al.CrystEngComm, 2014,16:385-392
[20]Yuan C Z,Li JY,Hou L R,et al.J.Mater.Chem.A,2013, 1:11145-11151
[21]Wu Y Q,Chen X Y,Ji P T,et al.Electrochim.Acta,2011, 56:7517-7522
[22]Li L L,Peng S J,Cheah Y,et al.Chem.Eur.J.,2013,19: 5892-5898
[23]Ding R,Li Q,Jia M J,et al.Electrochim.Acta,2013,107: 494-502
[24]Jiang H,Ma J,Li C Z.Chem.Commun.,2012,48:4465-4467
[25]Yuan CZ,Li JY,Hou L R,etal.Adv.Funct.Mater.,2012, 22:4592-4597
[26]Wang Q F,Wang X F,Liu B,et al.J.Mater.Chem.A, 2013,1:2468-2473
[27]Li J F,Xiong S L,Liu Y R,et al.ACS Appl.Mater. Interfaces,2013,5:981-988
[28]Li L L,Cheah Y,Ko Y,et al.J.Mater.Chem.A,2013,1: 10935-10941
[29]Xu S,Lu L,Zhang Q,etal.J.Nanopart.Res.,2015,17:381-392
[30]Chen G H,Yang J,Tang J J,et al.RSC Adv.,2015,5: 23067-23072
[31]Liu HW,Liu J.Electrochim.Acta,2013,92:371-375
[32]Mohamed SG,Hung TF,Chen C J,etal.RSCAdv.,2013, 3:20143-20149
[33]Hao S J,Zhang BW,Ball S,et al.J.Power Sources,2015, 294:112-119
[34]Guo L Y,Ru Q,Song X,et al.RSC Adv.,2015,5:1924-1927
[35]Xie Q S,Li F,Guo H Z,et al.ACSApp l.Mater.Interfaces, 2013,5:5508-5517
[36]Hu L L,Qu B H,Li C C,et al.J.Mater.Chem.A,2013,1: 5596-5602
[37]Guo L Y,Ru Q,Song X,et al.J.Mater.Chem.A,2015,3: 8683-8692
[38]Kang W P,Feng F,Zhang M M,et al.J.Nanopart.Res., 2013,15:1891-1898
[39]Song X,Ru Q,Zhang B B,et al.J.Alloys Compd.,2014, 585:518-522
[40]Du N,Xu Y F,Zhang H,et al.Inorg.Chem.,2011,50:3320-3324
[41]Liu B,Wang X F,Liu B Y,et al.Nano Res.,2013,6:525-534
[42]Luo W,Hu X L,Sun Y M,et al.J.Mater.Chem.,2012,22: 8916-8921
[43]Li JF,Wang JZ,Wexler D,etal.J.Mater.Chem.A,2013, 1:15292-15299
[44]Sharma Y,Sharma N,Subba R G V,et al.Adv.Funct. Mater.,2007,17:2855-2861
[45]Qu B H,Hu L L,LiQ H,etal.ACSAppl.Mater.Interfaces, 2014,6:731-736
[46]Zhu Y Q,Cao C B,Zhang J T,et al.J.Mater.Chem.A, 2015,3:9556-9564
[47]Huang T F,Zhao C H,Zheng R J,et al.Ionics,2015,21: 3109-3115
[48]Ratha S,Rout CS.RSCAdv.,2015,5:86551-86557
[49]Liu B,Liu B Y,Wang Q F,et al.ACS Appl.Mater. Interfaces,2013,5:10011-10017
[50]Wang Q H,Zhu L X,Sun L Q,et al.J.Mater.Chem.A, 2015,3:982-985
[51]Bao F X,Wang X F,Zhao X D,et al.RSC Adv.,2014,4: 2393-2397
[52]Huang G Y,Xu S M,Xu Z H,et al.ACS Appl.Mater. Interfaces,2014,6:21325-21334
[53]Wu X Y,Li SM,Wang B,et al.New J.Chem.,2015,39: 8416-8423
[54]Liu HW,Wang J.J.Electron.Mater.,2012,41:3107-3110
[55]Zhang YW,Wang X Y,Zhao Q L,et al.Electrochim.Acta, 2015,180:866-872
[56]Li JF,Xiong S L,Li X W,et al.Nanoscale,2013,5:2045-2054
[57]LiGD,Xu LQ,Zhai Y J,etal.J.Mater.Chem.A,2015,3: 14298-14306
[58]Li JF,Wang JZ,Liang X,etal.ACSAppl.Mater.Interfaces, 2014,6:24-30
[59]Venkatachalama V,Alsalme A,A lghamdi A,et al.J. Electroanal.Chem.,2015,756:94-100
[60]Sahoo S,Naik K K,Rout C S.Nanotechnology,2015,26: 455401-455409
[61]Sharma Y,Sharma N,Rao S G V,et al.Solid State Ionics, 2008,179:587-597
[62]Liu L,Hu Z B,Sun L M,et al.RSC Adv.,2015,5:36575-36581
[63]Sharma Y,Sharma N,Subba R G V,et al.J.Power Sources, 2007,173:495-501
[64]Sun S J,Wen Z Y,Jin J,et al.Microporous Mesoporous Mater.,2013,169:242-247
[65]Ma J J,Wang H J,Yang X,et al.J.Mater.Chem.A,2015, 3:12038-12043
[66]Krishnan S G,Reddy M V,Harilal M,et al.Electrochim. Acta,2015,161:312-321
[67]Pendashteh A,Moosavifard S E,Rahmanifar S M,et al. Chem.Mater.,2015,27:3919-3926
[68]Chen H Y,Chen X H,Zeng Y,et al.RSC Adv.,2015,5: 70494-70497
[69]He G Y,Wang L,Chen H Q,et al.Mater.Lett.,2013,98: 164-167
[70]Wang H W,Hu Z A,Chang Y Q,et al.J.Mater.Chem., 2011,21:10504-10511
[71]Yuan Y,Bi H P,He G Y,et al.Chem.Lett.,2014,43:83-85
[72]Huang L,Chen D C,Ding Y,et al.ACS Appl.Mater. Interfaces,2013,5:11159-11162
[73]YangW L,Gao Z,Ma J,et al.J.Mater.Chem.A,2014,2: 1448-1457
[74]Nguyen V H,Shim JJ.J.Power Sources,2015,273:110-117
[75]Zhou J,Huang Y,Cao X H,et al.Nanoscale,2015,7:7035-7039
[76]Zhang C F,Kuila T,Kim N H,et al.Carbon,2015,89:328-339
[77]Li X C,Sun W,Wang L Q,et al.RSC Adv.,2015,5:7976-7985
[78]Gao SN,Liao F,Ma SZ,et al.J.Mater.Chem.A,2015,3: 16520-16527
[79]Gao Z,Yang W L,Wang J,et al.Nano Energy,2015,13: 306-317
[80]Li D L,Gong Y N,Zhang Y P,et al.Sci.Rep.,2015,5: 12903-12911
[81]BaiW L,Tong H,Gao Z Z,et al.J.Mater.Chem.A,2015, 3:21891-21898
[82]Chen Y J,Zhu J,Qu B H,et al.Nano Energy,2014,3:88-94
[83]Liu B,Zhang J,Wang X F,et al.Nano Lett.,2012,12:3005-3011
[84]Rai K A,Kim J.Solid State Sci.,2015,48:90-96
[85]Mo Y D,Ru Q,Song X,et al.Electrochim.Acta,2015,176: 575-585
[86]Peng L,Zhang H J,Bai Y J,et al.J.Mater.Chem.A,2015, 3:22094-22101
[87]Liu M C,Kong L B,Lu C,et al.ACSApp l.Mater.Interfaces, 2012,4:4631-4636
[88]Lee CW,Seo SD,Kim DW,et al.Nano Res.,2013,6:348-355
[89]Li ZQ,Yin LW.J.Mater.Chem.A,2015,3:21569-21577
[90]Zou R J,Yuen M F,Zhang Z Y,et al.J.Mater.Chem.A, 2015,3:1717-1723
[91]Zhai Y J,Mao H Z,Liu P,et al.J.Mater.Chem.A,2015,3: 16142-16149
[92]Ni JF,Li Y.Adv.Energy Mater.,2016,6:1600278(1-21)
[93]Ni J F,Fu S D,Wu C,et al.Adv.Mater.,2016,28:2259-2265
[94]Ni JF,Fu S D,Wu C,et al.Adv.Energy Mater.,2016,6: 1502568(1-8)
[95]Huang G Y,Xu SM,Yang Y,et al.Mater.Lett.,2014,131: 236-239
[96]Huang G Y,Xu S M,Yang Y,et al.RSC Adv.,2016,6: 10763-10774
[97]HUANG Guo-Yong(黄国勇),XU Sheng-Ming(徐盛明),LI Lin-Yan(李林艳),etal.Acta Phys.-Chim.Sin.(物理化学学报),2014,30:1121-1126
[98]HUANG Guo-Yong(黄国勇),XU Sheng-Ming(徐盛明), WANG Jun-Lin(王俊莲),et al.Acta Chim.Sinica(化学学报),2013,71:1589-1597
[99]Bai L,Fang F,Zhao Y Y,et al.RSC Adv.,2014,4:43039-43046
[100]Mujtaba J,Sun H Y,Huang G Y,et al.Sci.Rep.,2016,6: 20592(1-8)
Preparation of Cobalt-Based Bi-M etal-Oxides and the App lication in the Field of Electrochem ical Energy Storage
The development of new electrodematerials are required due to the high performance Li-ion batteries (LIBs)and supercapacitors(SCs)for application in electric vehicles(EVs)and hybrid electric vehicles(HEVs). Among a wide variety of electrodematerials,transition metal oxides(Co3O4,CoO,NiO,et al.)are accounted as promising ones for both LIBs and SCs owing to the high theoretical capacities.However,its practical use is hindered because of the low electronic conductivity,the large volume change during charge/recharge progress and fair rate capability.With the purpose to improve the electrochemical performance,many researchers have focused on studying cobalt-based bi-metal-oxides(MCo2O4,M=Ni,Mn,Zn,et al.)due to the chemical and thermal stability,low costand good electrical conductivity.Therefore,it ismeaningful to review the recent developmentof MCo2O4in the field of electrochemical energy storage including their energy densities,cycling stability and rate capability.In this paper,the recent advances of MCo2O4and these composites as electrodematerials of LIBs and SCs are reviewed.The researches are classified by types,preparation method and characteristics of materials
cobalt-based bi-metal-oxides;preparation method;morphology;modification;electrochemical energy storage
O646;O614.81+2
A
1001-4861(2016)10-1693-11
10.11862/CJIC.2016.244
2016-04-04。收修改稿日期:2016-08-21。
国家自然科学基金项目(No.51604306,51274130)、教育部长江学者和创新团队发展计划项目(No.IRT13026)和中南大学升华猎英人才计划项目(No.502035031)资助。
*通信联系人。E-mail:smxu@tsinghua.edu.cn
ncluding NiCo2O4,ZnCo2O4,MnCo2O4,and so on.Their advantages and disadvantages are summarized and the ossible electrochemical reaction mechanisms are explained.In addition,it is also discussed how to improve the lectrochemical performance of MCo2O4in the future.