南极磷虾油微胶囊的制备
赵鑫鹏,陈京美,王松,苗钧魁,刘小芳,高华,赵宪勇,冷凯良,*
(1.青岛大学药学院药物化学系,山东青岛266021;2.中国水产科学研究院黄海水产研究所,山东青岛266071)
南极磷虾油微胶囊的制备
赵鑫鹏1,2,陈京美1,2,王松2,苗钧魁2,刘小芳2,高华1,赵宪勇2,冷凯良2,*
(1.青岛大学药学院药物化学系,山东青岛266021;2.中国水产科学研究院黄海水产研究所,山东青岛266071)
以海藻酸钠与壳聚糖为壁材,采用锐孔法制备南极磷虾油微胶囊。以南极磷虾油微胶囊的包埋率作为指标,选取海藻酸钠溶液浓度、壳聚糖溶液浓度、氯化钙溶液浓度和芯壁质量比4个因素,采用四因素三水平正交试验确定最佳微胶囊化工艺。结果得到最佳工艺参数:海藻酸钠溶液浓度为1%,壳聚糖溶液浓度为0.5%,氯化钙溶液浓度为3%,芯壁质量比为1∶1,包埋率可达86.45%。
南极磷虾油;微胶囊;锐孔法
南极磷虾油是从南极磷虾(Euphausia superba)中提取的脂质,主要成分包括:甘油酯、磷脂、虾青素、甾醇等;其中磷脂含量可达20.4%~32.7%,极性非磷脂含量占64%~77%,甘油三酯占1.0%~3.2%[1]。同时南极磷虾油中含有天然的抗氧化剂虾青素,含量可达100 mg/kg~300 mg/kg[2];南极磷虾油中还含有丰富的ω-3系列多不饱和脂肪酸(DHA、EPA),且以磷脂形式存在[3-4]。因此,磷虾油有着较好的保健功效,具有很大的开发潜力和广阔的市场前景。但不饱和脂肪酸极易氧化变质,造成磷虾油品质下降,使其开发受到了限制。
为了南极磷虾油的开发和利用,可采用微胶囊化技术将磷虾油制备成微胶囊。微胶囊化技术即将磷虾油包封在5 μm~200 μm的小胶囊中,形成球状或者卵状[5]。使磷虾油由油状物转化为粉末状,既可保护磷虾油不被氧化,又方便运输和贮存,同时可以掩蔽令人不愉快的气味或味道。目前,国内制备微胶囊的方法主要有复合凝聚法[6-8]、锐孔法[9-11]、喷雾干燥法[12-13]等。其中复合凝聚法在制备过程中需要加入一定的化学交联剂,对芯材品质有影响。而喷雾干燥法在制备过程中瞬间温度可达200℃,对芯材品质也有一定影响,而锐孔法相较其他制备方法,反应条件温和,操作简单。本研究选取海藻酸钠和壳聚糖为包封壁材,使用锐孔法制备微胶囊,操作简单可行,对南极磷虾油综合利用具有一定的指导意义,可为工业化生产工艺提供理论参考。
1 材料与方法
1.1材料与试剂
南极磷虾油(从南极磷虾粉提取精制):黄海水产研究所;海藻酸钠:青岛聚大洋有限公司;壳聚糖(脱乙酰度80%~95%)、氯化钙:上海国药集团化学试剂有限公司;其他试剂均为分析纯。
1.2仪器与设备
FJ200-SH数显高速分散均质机:上海标本模型厂;FD-1B-50冷冻干燥机:上海比朗仪器有限公司。
1.3微胶囊制备工艺路线
取壳聚糖与氯化钙混合水溶液置于烧杯中,磁力搅拌;取海藻酸钠水溶液与精制南极磷虾油混合,加入乳化剂(吐温80与司盘80质量比为4∶1),高速均质(10 000 r/min),形成乳化液,将上述乳化液,以锐孔匀速连续滴入壳聚糖-氯化钙水溶液中,静置,水洗,过滤除去溶液后冷冻干燥。

1.4微胶囊制备工艺参数的优化
分别对乳化剂用量,海藻酸钠溶液浓度,氯化钙溶液浓度,壳聚糖溶液浓度浓度,芯壁质量比5个因素进行单因素试验;再选取海藻酸钠溶液浓度、氯化钙溶液浓度、壳聚糖溶液浓度浓度、芯壁质量比4个因素,作三水平的正交试验,优化微胶囊制备工艺。
1.5微胶囊化评价方法
采用包埋率这一指标对南极磷虾油微胶囊化效果进行评价,公式如下:

总油提取方法[14]:采用碱性乙醚法测定。
表面油提取方法:精确称取质量M(约1 g~2 g)的微胶囊产品,用30 mL乙醚准确浸提1min后,立即抽滤,用20 mL乙醚洗涤滤渣,收集滤液,将滤液真空浓缩即得到表面油,其质量记做m(g)。

2 结果与分析
2.1单因素试验
2.1.1乳化剂用量对包埋率的影响
南极磷虾油微胶囊包埋过程中确定海藻酸钠溶液浓度为1%、壳聚糖溶液浓度为1%、氯化钙溶液浓度为1%、芯壁质量比为1∶1的条件下,分别考察乳化剂用量为0.5%、1%、1.5%、2%时对包埋率的影响。

图1 乳化剂添加量对包埋率的影响Fig.1 Effect of emulsifier content on encapsulation efficiencies
从图1可知,包埋率随着乳化剂添加量的增加先上升后下降,乳化剂含量为1.5%时,包埋率最高,但乳化剂用量继续增加,包埋率出现下降,这是因为乳化剂用量过大,致使乳化液过于黏稠,均质效果欠佳,且会影响微胶囊的风味,增大成本。故适当增大乳化剂用量,利于均质,且乳化液均匀。最终选取乳化剂用量为1.5%。
2.1.2海藻酸钠溶液最佳浓度的确定
南极磷虾油微胶囊包埋过程中确定壳聚糖溶液浓度为1%、氯化钙溶液浓度为1%、芯壁质量比为1∶1的条件下,分别考察海藻酸钠溶液浓度为0.5%、1%、2%、3%时,对微胶囊产品的影响。结果见表1。
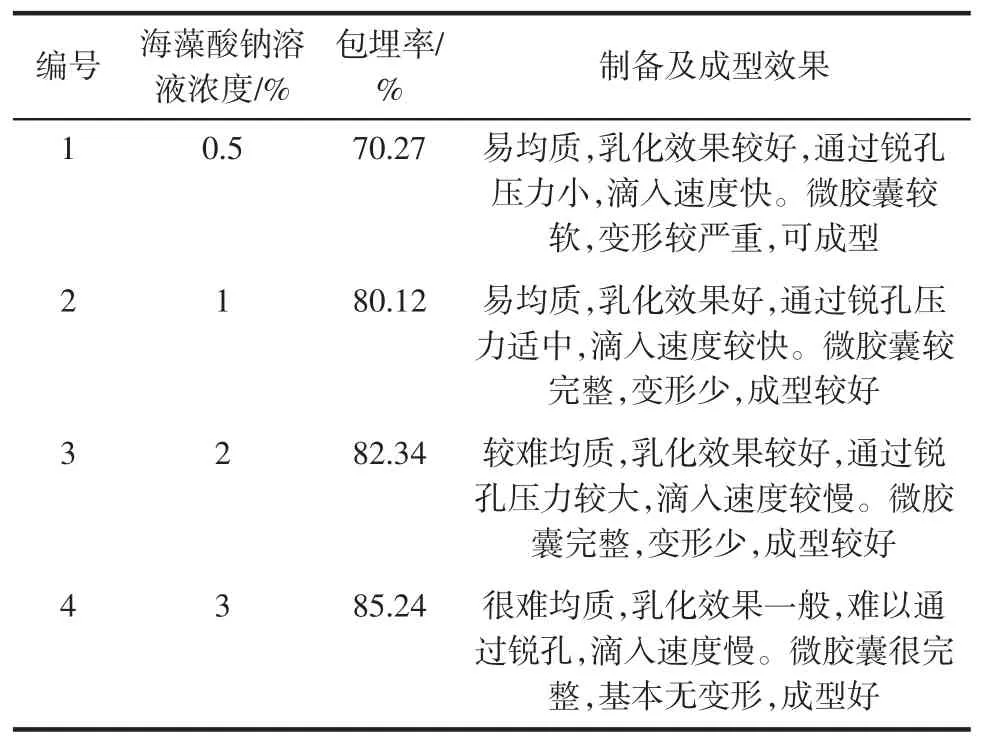
表1 海藻酸钠溶液浓度对微胶囊的影响Table 1 Effect of concentration of sodium alginate on microcapsules properties
由表1可知,适当增大海藻酸钠溶液的浓度可以提高微胶囊的包埋率,因为随着海藻酸钠溶液浓度的增大,黏度上升,可将虾油包裹在其中,乳化效果好。若海藻酸钠溶液浓度过低,影响乳化效果,导致包埋率下降;但海藻酸钠溶液浓度过高,导致黏度过大,不利于乳化均质,且难以形成均匀的乳液滴,增加成本且对后续操作产生影响。故选取1%~2%的海藻酸钠溶液浓度为佳。
2.1.3氯化钙溶液最佳浓度的确定
南极磷虾油微胶囊包埋过程中确定海藻酸钠溶液浓度为1%、壳聚糖溶液浓度为1%、芯壁质量比为1∶1的条件下,分别考察氯化钙溶液浓度为0.5%、1%、2%、3%、5%时,对微胶囊产品的影响。结果见表2。

表2 氯化钙溶液浓度对微胶囊的影响Table 2 Effect of concentration of CaCl2on microcapsules properties
由表2可知,增大钙离子浓度,可以加速海藻酸钠凝胶珠的形成,减少虾油的暴露时间,但如果钙离子浓度过高,会导致壳聚糖包膜难以形成,影响包埋率。且微胶囊的质地,也与钙离子浓度有关,钙离子浓度越大,微胶囊越硬,且壁材较厚。
2.1.4壳聚糖溶液最佳浓度的确定
南极磷虾油微胶囊包埋过程中确定海藻酸钠溶液浓度为1%、氯化钙溶液浓度为1%、芯壁质量比为1∶1的条件下,分别考察壳聚糖溶液浓度为0.5%、1%、1.5%、2%、3%时,对微胶囊包埋率的影响。结果见图2。

图2 壳聚糖溶液浓度对包埋率的影响Fig.2 Effect of chitosan concentration on encapsulation efficiencies
由图2可知,增大壳聚糖溶液浓度,微胶囊包埋率先上升后下降。分析可能的原因是:壳聚糖在溶液中显正电,可以与显负电的海藻酸钠产生静电作用,从而影响了海藻酸钠与钙离子形成凝胶珠,使微胶囊成形时间变长,导致包埋率下降。
2.1.5芯壁质量比的确定
南极磷虾油微胶囊包埋过程中确定海藻酸钠溶液浓度为1%、壳聚糖溶液浓度为1%、氯化钙溶液浓度为1%的条件下,分别考察芯壁质量比为1∶2、1∶1、2∶1、2.5∶1、3∶1时,对微胶囊包埋率的影响。结果见图3。
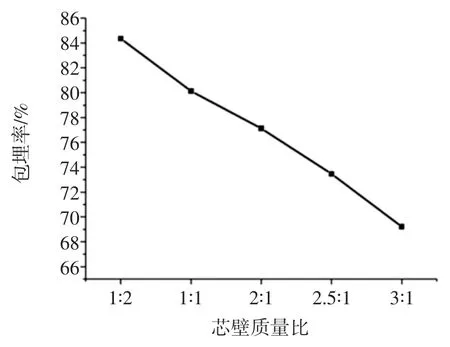
图3 芯壁质量比对包埋率的影响Fig.3 Effect of core/wall mass ratio on encapsulation efficiencies
由图3可知,芯壁质量比的改变会影响包埋率,随着芯材的增加,包封率下降,微胶囊表面渗油较为明显。芯材含量的多少从侧面显示了微胶囊的承载能力[15],即微胶囊所能包埋虾油的能力。当芯材含量过少时,壁材过厚,造成壁材浪费;当芯材含量过多时,壁材难以包裹完全,导致表面油过多,包埋率较差,所以选取芯壁质量比1∶1、2∶1为佳。
2.2南极磷虾油微胶囊制备工艺的优化
结合上述单因素试验。选取海藻酸钠溶液浓度,壳聚糖溶液浓度,氯化钙溶液浓度,芯壁质量比这4个因素,采取四因素三水平进行正交试验,以微胶囊的包埋率作为参考指标,分析试验结果,得到最佳南极磷虾油制备工艺。正交设计见表3。

表3 正交试验因素水平表Table 3 Factors and levels of orthogonal test
正交试验结果及方差分析见表4和表5。
由表4可知,南极磷虾油微胶囊最佳工艺参数为A2B1C3D2,即海藻酸钠溶液浓度1%,壳聚糖溶液浓度0.5%,氯化钙溶液浓度3%,芯壁质量比1∶1。由方差分析可得影响南极磷虾油微胶囊包埋率的工艺条件的主次顺序依次为:海藻酸钠溶液浓度>芯壁质量比>壳聚糖溶液浓度>氯化钙溶液浓度。从正交试验结果及方差分析可以看出,海藻酸钠溶液浓度对微胶囊包埋率的影响程度最大,因为海藻酸钠溶液浓度的改变影响了均质与乳化效果,与单因素试验结果相符合;芯壁质量比与氯化钙溶液浓度对微胶囊包埋率的影响程度居中,适当地提高芯材含量与钙离子浓度,有利于微胶囊的形成;而壳聚糖溶液浓度对微胶囊包埋率的影响程度最小,使用较少的壳聚糖便可达到较好的包埋效果,也符合单因素试验结果。

表4 正交试验与结果Table 4 Result of orthogonal test

表5 正交试验方差分析Table 5 Analysis variance of orthogonal test
2.3验证试验
通过上述正交试验分析得到最佳微胶囊制备工艺进行验证实验,制备得到南极磷虾油微胶囊,产品包埋率可达86.45%。微胶囊产品呈颗粒状,颗粒大小均一,色泽呈鲜红,略有虾腥味,无其他异味。
3 结论
以海藻酸钠、壳聚糖为壁材,采用锐孔法制备南极磷虾油微胶囊,以微胶囊包埋率为主要指标,对海藻酸钠溶液浓度、壳聚糖溶液浓度、氯化钙溶液浓度、芯壁质量比4个因素进行正交优化后得到南极磷虾油微胶囊化的最佳制备工艺:海藻酸钠溶液浓度1%,壳聚糖溶液浓度0.5%,氯化钙溶液浓度3%,芯壁质量比1∶1。在此条件下,南极磷虾油微胶囊包封率可达86.45%。通过正交分析,得到工艺条件的主次顺序依次为:海藻酸钠溶液浓度>芯壁质量比>壳聚糖溶液浓度>氯化钙溶液浓度。最终得到产品呈颗粒状,颗粒大小均一,色泽呈鲜红,略有虾腥味,无其他异味。南极磷虾油的微胶囊化,使其形成稳定的固态,在方便运输和贮存的同时,还可防止磷虾油的酸腐变质,提高了南极磷虾油的应用价值,使南极磷虾油拥有更广泛的开发利用前景。
[1] Gigliotti J C,Davenport M P,Beamer S K,et al.Extraction and characterisation of lipids from Antarctic krill(Euphausia superba)[J].Food Chemistry,2011,125(3):1028-1036
[2]Ali-Nehari A,Kim S B,Lee Y B,et al.Characterization of oil including astaxanthin extracted from krill(Euphausia superba)using supercritical carbon dioxide and organic solvent as comparative method[J].Korean Journal of Chemical Engineering,2012,29(3):329-336
[3]Phleger C F,Nelson M M,Mooney B D,et al.Interannual and between species comparison of the lipids,fatty acids and sterols of Antarctic krill from the US AMLR Elephant Island survey area[J]. Comparative Biochemistry&Physiology Part B Biochemistry& Molecular Biology,2002,131(4):733-747
[4]Tou J C,Jaczynski J,Chen Y C.Krill for Human Consumption:Nutritional Value and Potential Health Benefits[J].Nutrition Reviews,2007,65(2):63-77
[5]杨海燕,于蒙,刘姗姗,等.冷冻干燥法制备甜杏仁油微胶囊[J].食品科学,2012(18):36-40
[6]盖旭,李荣,姜子涛.大豆分离蛋白—海藻酸钠复凝聚法制备芥末油微胶囊[J].中国调味品,2012,37(2):51-54
[7]路宏波,张冲,冯岩,等.复合凝聚法制备鱼油微胶囊技术的研究[J].食品工业科技,2008(6):120-123
[8]谢艳丽,蒋敏,陈鸿雁.复凝聚法制备明胶/阿拉伯胶含油微胶囊工艺过程的研究[J].化学世界,2010,51(1):33-37
[9]Matsumoto S,Kobayashi H,Takashima Y.Production of monodispersed capsules[J].Journal of Microencapsulation,2008,3(1):25-31
[10]Sarah K,Johns E J.Alginate encapsulation of genetically engineered mammalian cells:comparison of production devices,methods and microcapsulecharacteristics[J].Journal of Microencapsulation,2003,20(3):303-316
[11]Brandenberger H,Widmer F,Brandenberger H,et al.A new multinozzle encapsulation/immobilisation system to produce uniform beads of alginate[J].Journal of Biotechnology,1998,63(1):73-80
[12]马云标,周惠明.VE微胶囊的制备及性质研究[J].食品科学,2010,31(2):1-5
[13]姚翾,陶宁萍,王锡昌.宝石鱼油的微胶囊化研究[J].食品科学,2008,29(9):254-259
[14]大连轻工业学院,华南理工大学,西北轻工业学院,等[M].食品分析,北京:中国轻工业出版社,1994:143
[15]Pinheiro A C,Bourbon A I,Cerqueira M A,et al.Chitosan/fucoidan multilayer nanocapsules as a vehicle for controlled release of bioactive compounds[J].Carbohydrate Polymers,2015,115:1-9
Preparation of the Antarctic Krill Oil Microcapsules by Piercing Method
ZHAO Xin-peng1,2,CHEN Jing-mei1,2,WANG Song2,MIAO Jun-kui2,LIU Xiao-fang2,GAO Hua1,ZHAO Xian-yong2,LENG Kai-liang2,*
(1.Department of Pharmaceutical Chemistry,School of Pharmacy,Qingdao University,Qingdao 266021,Shandong,China;2.Yellow Sea Fisheries Research Institute,Chinese Academy of Fishery Sciences,Qingdao 266071,Shandong,China)
Microencapsulation of krill oil using sodium alginate and chitosan as wall materials by piercing method.Taking encapsulation efficiency as the main evaluating index,the optimum processing conditions of microencapsulation of krill oil by L9(34)orthogonal test were determined as follows:sodium alginate solution con centration 1%,chitosan solution concentration 0.5%,CaCl2solution 3%,core/wall mass ratio 1∶1,and the encapsulation efficiency was 86.45%.
krill oil;microcapsules;piercing method
10.3969/j.issn.1005-6521.2016.21.019
青岛市应用基础研究自主创新计划项目(15-9-1-113-jch);农业部南极海洋生物资源开发利用项目(2016年度)
赵鑫鹏(1991—),男(汉),硕士研究生,研究方向:生物活性成分的改性及修饰应用。
冷凯良,男,硕士生导师,研究员。
2015-12-17

