桑椹的质量分析方法研究
陈诚广西中医学校530023南宁市东葛路61号王柳萍辛华广西中医药大学530001
桑椹的质量分析方法研究
陈诚广西中医学校530023南宁市东葛路61号王柳萍辛华*广西中医药大学530001
目的:建立桑椹药材的质量分析方法。方法:采用高效液相色谱法同时测定桑椹药材中的白藜芦醇和芦丁含量;采用改良后pH示差分光光度法测定桑椹花色苷的含量;采用薄层色谱法对桑椹进行理化鉴别。结果:10批白藜芦醇含量为0~0.0143mg/g,芦丁含量为0.2922~2.3680mg/g,花色苷含量为0~21.11mg/g;薄层色谱供试品色谱中,在与对照药材色谱及对照品色谱相应的位置上,显相同颜色的斑点,专属性良好。结论:本研究建立的质量分析方法专属性强、重复性好,可为桑椹的质量评价提供科学依据。
桑椹;白藜芦醇;芦丁;花色苷;HPLC;薄层色谱;光谱鉴别
桑椹为桑科植物桑的果穗,是药食同源类中药,具有滋阴补血、生津润燥的功效。目前,《中华人民共和国药典》2015年版关于桑椹药材的质量控制项目尚无专属性强的薄层鉴别及含量测定项目。为了更好地控制药材的质量,本实验在前期研究[1]的基础上,进一步建立桑椹药材薄层色谱鉴别方法,并采用高效液相色谱法同时测定桑椹药材中白藜芦醇和芦丁的含量,采用改良后pH示差分光光度法测定桑椹花色苷的含量,旨为桑椹药材的质量评价提供科学依据。
1 仪器与试药
1.1仪器Agilent 1200高效液相色谱仪(美国安捷伦);BP211D电子天平(德国赛多利斯公司);LG16-W型高速离心机(北京京立离心机有限公司);KQ5200E型超声波清洗仪(江苏省昆山市超声仪器有限公司);雷磁pHS-3C精密pH计(上海精密科学仪器有限公司);Agilent 8453紫外-可见分光光度计(美国安捷伦)。
1.2试药桑椹药材样品共10批,经广西蚕业技术推广总站朱方容研究员鉴定为桑科桑属植物广东桑Morus atropurpurea Roxb.的果穗,经低温干燥后置于干燥器中,备用。桑椹对照药材(批号121158-200602),购于中国药品生物制品检定所;白藜芦醇(批号111535-2 00502)、芦丁(批号100080-200707),均购自中国药品生物制品检定所,供含量测定用;乙腈(色谱纯);薄层层析硅胶G(青岛海洋化工有限公司);甲醇、CMC-Na、乙酸乙酯、甲酸、三氯化铝(国药集团),实验用水(娃哈哈)。
2 方法与结果
2.1芦丁、白藜芦醇的含量测定
采用高效液相色谱法同时测定。
2.1.1色谱条件色谱柱:Agilent ZORBAX SB-C18柱(250 mm× 4.6 mm,5μm),Phenomenex KJO 4282保护柱;流动相:乙腈-水,采用梯度洗脱程序,0 min(12∶88)~13 min(12∶88)~16 min(19∶81),后运行5 min;流速:1.0 m l/min;检测波长:306 nm;柱温:35℃。
2.1.2对照品溶液的制备分别取白藜芦醇对照品和芦丁对照品适量,精密称定,加甲醇制成每1 m l含白藜芦醇0.033 mg、芦丁1.353mg的混合溶液,即得。
2.1.3供试品溶液的制备取桑椹药材粉末(过三号筛)约0.2 g,精密称定,置于50m l具塞锥形瓶中,精密加入甲醇10m l,称定重量,超声处理(功率200 W,频率40 kHz)10 min,冷却,再称定重量,用原提取溶液补足减失的重量,10 000转/分钟高速离心10 min,取上清液作为供试品溶液。
精密吸取对照品溶液、供试品溶液和空白溶剂各10μl,按2.1.1项色谱条件进样测定,空白溶剂、对照品及供试品色谱图见图1。
2.1.4线性关系考察精密吸取上述混合对照品溶液适量,稀释5倍、10倍、25倍、50倍、100倍,分别取上述6个不同浓度的混合对照品溶液各10μl注入高效液相色谱仪测定,以对照品浓度(mg/m l)为横坐标,峰面积(Area)为纵坐标绘制标准曲线,得到回归方程。白藜芦醇:Y=43788.3X-1.3,r= 1.0000,线性范围为0.33~33.00mg/L;芦丁:Y=8 599.3X-41.1,r=0.99992,线性范围为13.53~1 353.00 mg/L。
2.1.5精密度试验精密吸取同一混合对照品溶液10μl,连续进样6次,测定白藜芦醇和芦丁的峰面积,其RSD分别为1.11%和0.38%,结果表明仪器精密度良好。
2.1.6重复性试验取6份同一批次桑椹样品粉末0.2 g,精密称定,按供试品溶液的制备方法制备,进样10μl测定峰面积,计算含量。白藜芦醇和芦丁含量的RSD分别为1.95%和1.56%,结果表明样品重复性良好。
2.1.7稳定性试验取同一供试品溶液,分别于制备后0 h、2 h、4 h、6 h、8 h、12 h、18 h、24 h进样10μl测定,白藜芦醇和芦丁含量的RSD分别为1.72%和0.50%。表明供试品溶液在24 h内稳定。
2.1.8加样回收率试验分别取已知含量的桑椹样品粉末6份,每份0.1 g,精密称定,分别加入适量对照品,按照供试品溶液制备方法制备,测定含量后计算加样回收率。结果显示白藜芦醇和芦丁的加样回收率分别为100.8%、102.2%,RSD分别为2.3%、1.8%。表明该方法同时测定芦丁和白藜芦醇含量的准确性较好。
2.1.9样品含量测定取10批不同产地的药材,按照上述“供试品溶液的制备”方法制备样品溶液,进样10μl测定峰面积,以外标法计算含量,测定结果见表1。
2.2花色苷的含量测定采用pH示差分光光度法进行测定。
2.2.1缓冲溶液的配制醋酸-醋酸钠缓冲液(pH4.5):取醋酸钠18 g,加冰醋酸9.8 ml,再加水稀释至1 000 m l,即得[2]。盐酸-氯化钾缓冲液(pH1.0):移取250 m l 0.2mol/LKCl溶液,670m l0.2mol/L HCl溶液,稀释至1 000ml[3],即得。
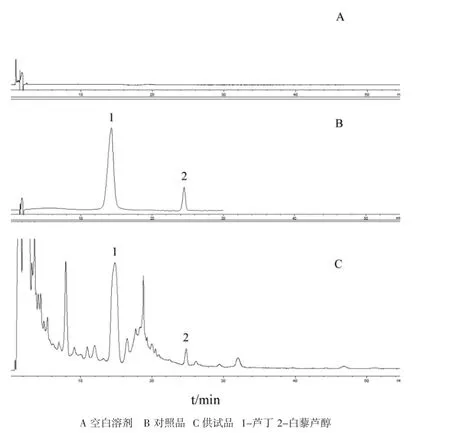
图1 HPLC色谱图
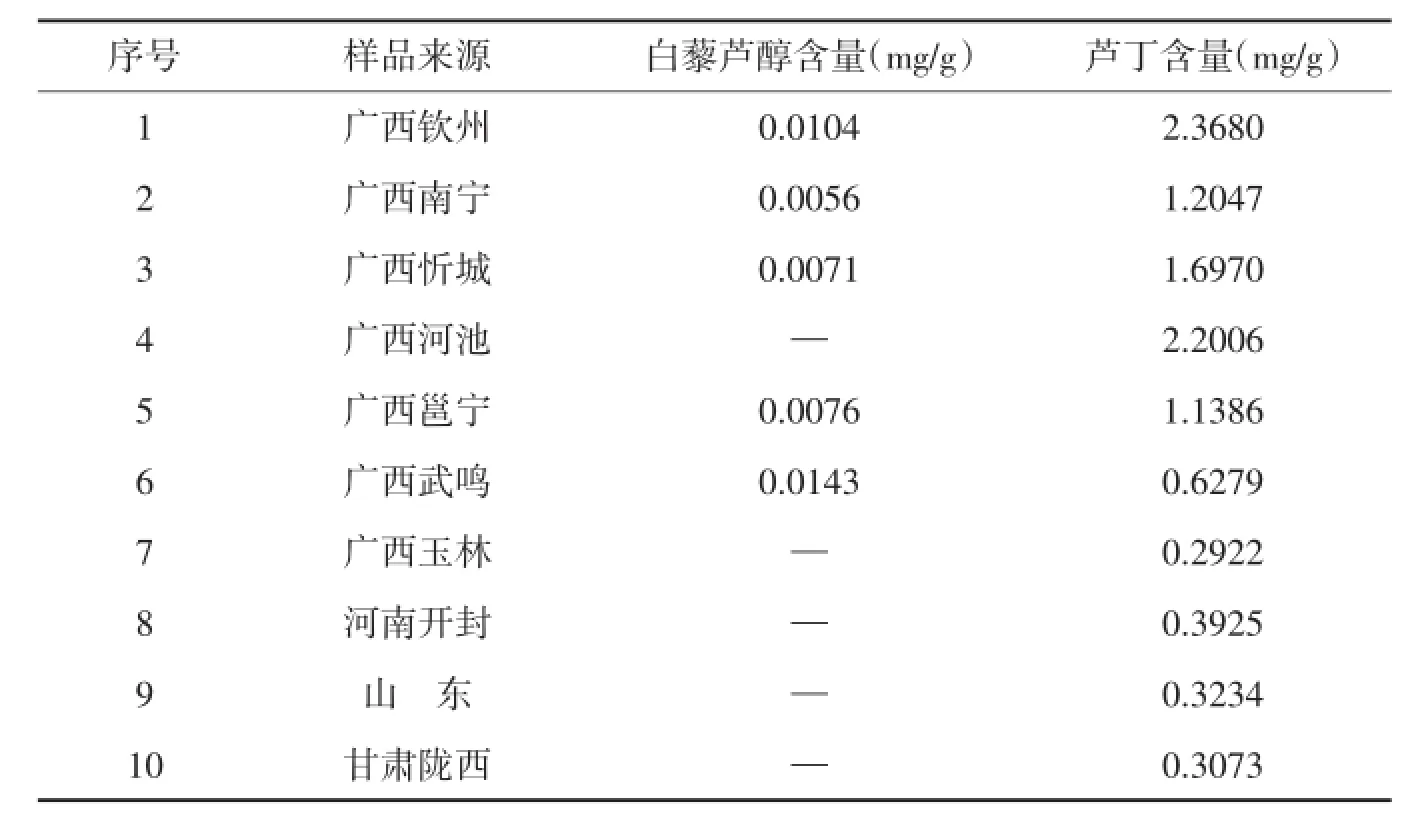
表1 白藜芦醇和芦丁含量测定结果(n=3)
2.2.2供试原液的制备取已干燥备用的桑椹粉末(过三号筛)约0.2 g,精密称定,置于50 ml具塞锥形瓶中,精密加入2%HCl甲醇溶液10m l,称定重量,超声(功率200W,频率40 kHz)处理40 min,放冷,再称定重量,用2%HCl甲醇溶液补足减失的重量,精密加入10 ml蒸馏水,摇匀,滤过,取续滤液作为供试原液。
2.2.3供试品溶液的制备精密吸取2份供试原液各1 m l,分别用盐酸-氯化钾缓冲液(pH1.0)和醋酸-醋酸钠缓冲液(pH4.5)定容至10 m l,摇匀,平衡50 min,即得供试品溶液。用蒸馏水做空白,分别测定两种供试液(pH1.0和pH4.5)在最大吸收波长(514 nm)和参比波长处(700 nm)的吸光度值,色谱图见图2。测定3次取平均值,按照经验公式计算含量[4]。在pH1.0时,桑椹花色苷以红色的2-苯基苯并吡喃的形式存在,吸收很大;pH=4.5时,则以无色假碱式花色苷的形式存在,没有吸收。
A=(Amax-A700)pH1.0-(Amax-A700)pH4.5;C(mg/ml)=(A×M×DF)/(a×L);花色苷含量(mg/g)=(C×V)/m;式中:C为花色苷的质量浓度,A为吸光度;M为分子量,桑椹花色苷以矢车菊素-3-葡萄糖苷计算(C21H21O11),其分子量为449.2;DF为稀释倍数;a为消光系数,26 900;L为光程:1.0;V为溶剂体积;m为取样量。
2.2.4样品含量测定分别称取不同批次的桑椹药材粉末,一式3份,按“供试原液的制备”方法制备样品溶液,再按上述方法进行测定并计算含量。测定结果见表2。
2.3薄层鉴别
2.3.1供试品、对照药材、对照品溶液的制备称取不同批次桑椹粉末(过三号筛)0.2 g,加甲醇10m l,加热回流30 min,趁热过滤,滤液浓缩至1ml,作为供试品溶液。另取桑椹对照药材0.2 g,同法制备对照药材溶液。再取芦丁对照品适量,加甲醇制成每1 ml含1 mg的溶液,作为对照品溶液。
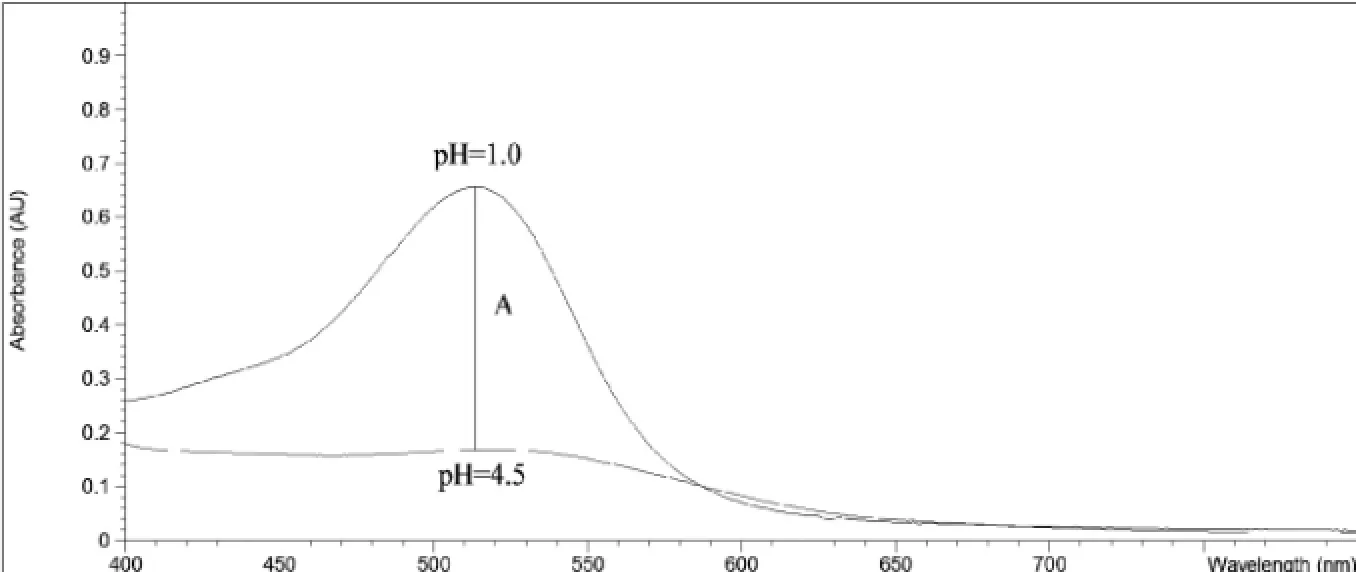
图2 桑椹pH示差分光光谱图(A为吸光度差值)
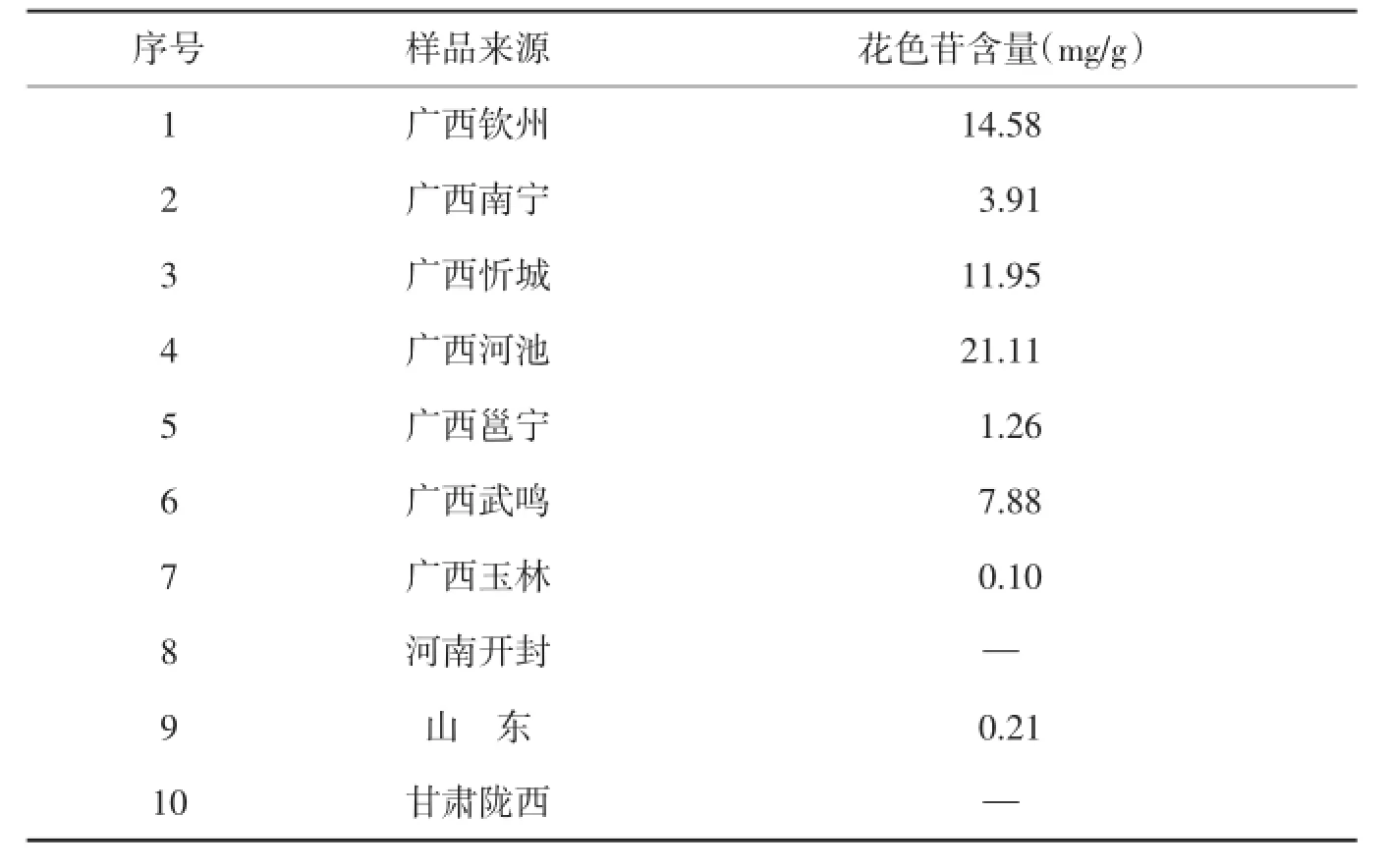
表2 花色苷含量测定结果(n=3)
2.3.2 TLC鉴别方法照《中华人民共和国药典》2010年版薄层色谱法(附录VIB)[2]进行试验,将硅胶G按1∶2.7的比例与0.7% CMC-Na混合,研磨均匀,铺板(20 cm×10 cm),阴干,105℃活化30 min,置干燥器中保存备用。分别吸取上述三种溶液各2μl,点于同一硅胶G薄层板上,以乙酸乙酯-甲酸-水(8∶1∶1)为展开剂,展开,取出,晾干,喷以5%三氯化铝乙醇溶液,晾干,待乙醇挥干后,在105℃加热5 min,取出,置紫外灯(365 nm)下检视。供试品色谱中,在与对照药材色谱及对照品色谱相应的位置上,显相同颜色的斑点。结果见图3。
3 讨论
3.1在HPLC测定实验中,对芦丁、白藜芦醇对照品溶液进行全波长扫描,芦丁有3个吸收峰,分别为206 nm、257 nm、358 nm,白藜芦醇有2个吸收峰,分别为217 nm、306 nm。由于样品中白藜芦醇的含量较低,必须优先提高其灵敏度,故选择306 nm作为检测波长。预试验中曾对乙腈-水洗脱系统和甲醇-水洗脱系统、等度洗脱和梯度洗脱都进行了考察对比。结果甲醇-水洗脱系统出峰晚,溶剂消耗大,用时长,且峰型差;等度洗脱保留时间过长,峰变宽;梯度洗脱比等度洗脱节省溶剂和时间,出峰良好,分离度高。结果选择以乙腈-水洗脱系统为流动相,并采用梯度洗脱。
3.2国内外有关桑椹花色苷含量测定的参考文献中多以桑椹鲜果、桑椹酒、桑椹提取物或者是经过大孔树脂纯化过的桑椹红色素作为实验对象,而未见直接用干燥后的桑椹药材作为实验对象的报道。本实验采用pH示差分光光度法测定花色苷的含量,在样品前处理上稍做改进,采用两步稀释法。由于花色苷易溶于水,所以溶剂提取后,在过滤前先加入定量的蒸馏水将醇相稀释,放出热量,再过滤除去析出的干扰物质。这样处理后,既可以避免在容量瓶中产生大量的热,又可以提前除去析出的干扰物质,稀释后的待测溶液澄清、透明,无白色浑浊干扰,能满足测定要求。在平衡时间的考察方面,本实验通过每隔5 min测定一次吸光度值,最后确定平衡时间为50min,并经过多批样品测定,重复性很好。此外,由于花色苷的光稳定性很差,所以整个操作过程都要注意避光。
3.3在薄层色谱鉴定实验中,对芦丁的提取方法、展开剂的选择、湿度、显色方法等进行考察。
3.3.1芦丁的提取方法加入甲醇分别以超声30min和回流30min两种方式进行提取,结果显示回流方法提取效果较超声提取好。其主要原因是芦丁难溶于冷水,而在沸甲醇中的溶解度(1∶7)较大。
3.3.2展开剂的选择在实验中曾对比过乙酸乙酯-甲酸-水、三氯甲烷-甲醇、三氯甲烷-丙酮、丙酮-甲醇等展开剂,实验结果表明,以乙酸乙酯-甲酸-水(8∶1∶1)为展开剂最好,斑点分离较好且清晰,位置适宜,其Rf值在0.5左右。
3.3.3湿度对展开效果的影响在相同的色谱条件下,湿度大于85%的环境下展开效果较差,斑点的清晰度不够,甚至观察不到斑点。因此,应把湿度控制在85%以下。
3.3.4显色方法的选择在相同色谱条件下,分别用氨熏和三氯化铝乙醇溶液进行显色,比较了两种不同的显色方法。结果氨熏后在对应位置上,日光下可见淡黄色斑点,斑点较清晰,但短时间内斑点颜色变浅,不易观察,且紫外(365 nm)下在相应位置未观察到荧光斑点。而喷以三氯化铝乙醇溶液,待乙醇挥干之后,在日光下隐约可见淡黄色斑点,置紫外灯(365 nm)下可见淡黄色斑点但不够清晰。若在烘箱中105℃干燥5 min后于再置紫外灯(365 nm)下观察可在相应位置明显看到到黄色荧光斑点。因此,采取喷以三氯化铝后,105℃干燥5 min的显色方法较好,能观察到明显斑点。
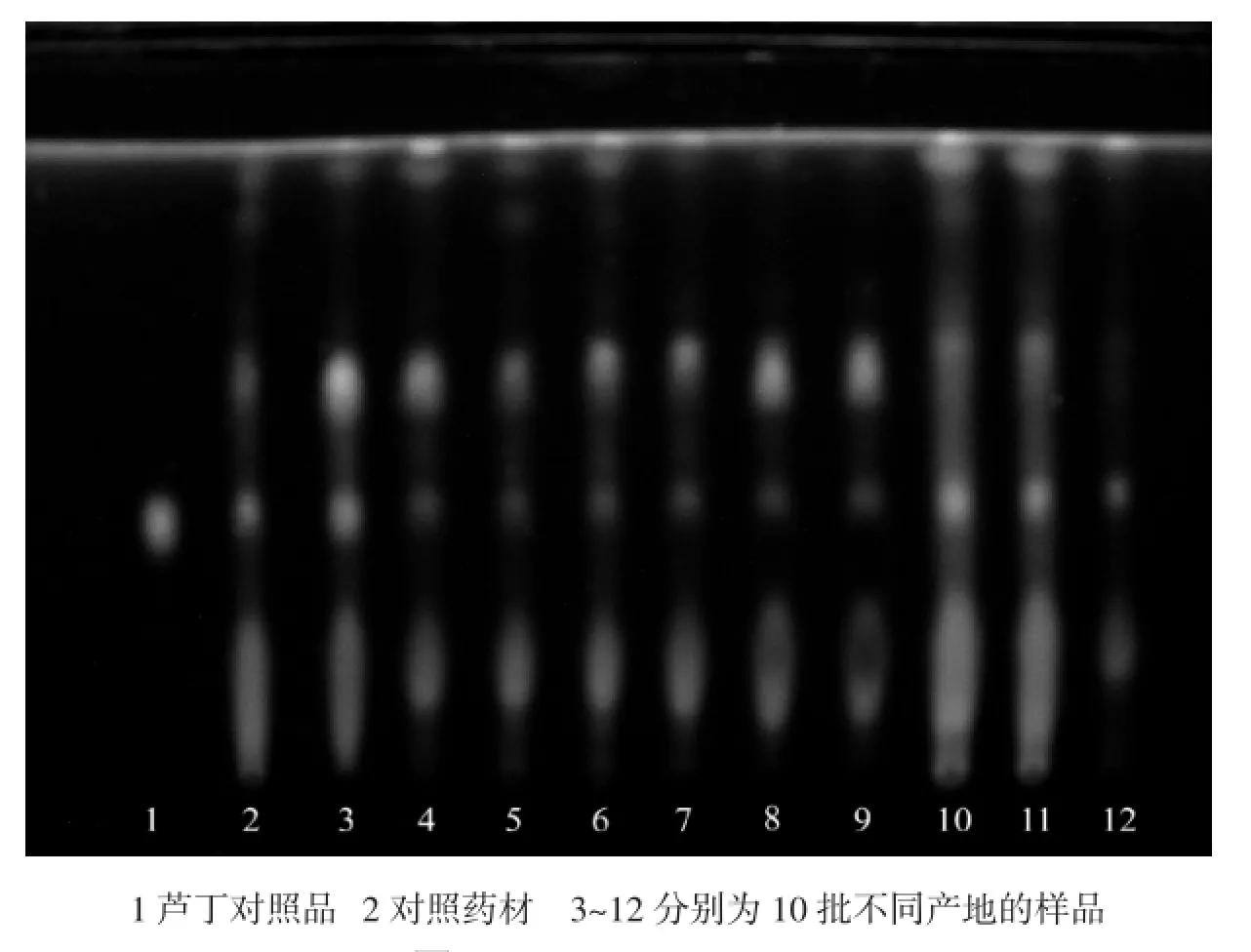
图3 桑椹薄层色谱图
[1]陈诚,李洪波,杨欣,等.中药桑椹活性物质的研究进展[J].中药材,2010,33(10):1660-1662.
[2]国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2010:附录68-71;附录110.
[3]全国化学标准化技术委员会化学试剂分会.GB/T 604-2002.化学试剂酸碱指示剂pH变色域测定通用方法[S].北京:中国标准出版社,2002:50.
[4]Lee J,Durst R W,Wrolstad R E.Determination of totalmonomeric anthocyanin pigment content of fruit Juices,beverages,natural colorants,and wines by the pH differentialmethod:collaborative study[J].Journal of AOAC international,2005,88(5):1269-1278.
(2016-09-13收稿/编辑陈明伟)
R284.1
A
1003-0719(2016)05-0076-04
广西卫生厅医疗卫生重点科研课题(编号:重2010092)
,副教授,研究方向:中药商品质量与标准研究;E-mail:1004605269@qq.com

