高含量痢菌净溶液的制备
侯美如,高俊峰,冯万宇,徐馨,周庆民
(黑龙江省兽医科学研究所,黑龙江齐齐哈尔161006)
高含量痢菌净溶液的制备
侯美如,高俊峰,冯万宇,徐馨,周庆民
(黑龙江省兽医科学研究所,黑龙江齐齐哈尔161006)
通过了解痢菌净在不同溶剂及助溶剂的溶解情况,筛选并组合最佳溶剂,以制备高含量痢菌净溶液,为临床药剂开发提供参考依据。运用全波长扫描选取最适痢菌净检测波长,并建立痢菌净含量检测方法,测定不同溶剂及助溶剂对痢菌净的最大溶解量,组合形成可溶解高含量痢菌净溶液的混合溶剂。结果表明,痢菌净在373.0 nm、368.0 nm、356.0 nm、254.0 nm、241.0 nm均有吸收峰,经与其他所选溶剂及助溶剂全波长扫描图谱比较,选取373为最适检测吸收波长。建立的痢菌净含量检测方法在1.25~20 μg/mL浓度范围内,吸收度与浓度呈良好的线性关系,R2=0.9992。不同溶剂及助溶剂中,单一溶剂或助溶剂对痢菌净的溶解程度均较混合溶剂差,且以水杨酸钠效果最好,但其在350.0~500.0 nm区间有较低的吸收峰,对运用紫外分光光度法测定痢菌净含量有一定的影响,2种混合溶剂均有较好的溶解效果,混合溶剂1溶解量最大,达54.37 mg/mL。为以后痢菌净缓释药剂的开发奠定了基础。
痢菌净;溶剂;助溶剂;溶解
1试验材料
1.1仪器WT-1003H型电子天平(赛多利斯科学仪器有限公司);ZNCL-S自能恒温磁力搅拌器(上海羌强仪器设备有限公司);PINE-TREE帕恩特标准试剂级超纯水机(北京湘顺源科技有限公司);UV-1900PC/UV-1901双束紫外可见分光光度计(上海佑科仪器仪表有限公司)。
1.2试剂水杨酸钠、N,N-二甲基甲酰胺、二甲亚砜、丙二醇、甘油、聚乙二醇及苯甲醇均为分析纯。
1.3对照品乙酰甲喹,中国兽医药品监察所,批号:H0111008,纯度:99.6%。
1.4样品痢菌净原粉,南通天辰药业公司。
2方法
2.1痢菌净全波长扫描取经105℃干燥恒重的痢菌净标准品用超纯水制成20 μg/mL水溶液,以超纯水为空白对照,置于1 cm石英吸收池中,用双光束紫外分光光度计在200~500 nm波长间扫描,扫描间隔1.0 nm,绘制痢菌净紫外吸收图谱,记录最大吸收峰。
2.2标准曲线的绘制利用电子天平精密称取痢菌净标准品0.027 g,置于10 mL离心管中,加纯水8.1 mL溶解,为母液备用。待完全溶解后,取36 μL痢菌净母液加水6 mL即得浓度为20 μg/mL的痢菌净溶液,并对其进行2倍倍比稀释分别得浓度为10、5、2.5、1.25 μg/mL痢菌净溶液,于“2.1”试验结果中选取最大吸收峰时波长,进行吸收度测定。
2.3溶剂、助溶剂及混合溶剂全波长扫描溶剂:N,N-二甲基甲酰胺、二甲亚砜、丙二醇、甘油、聚乙二醇及苯甲醇分别配制成浓度为40%、20%、30%、25%、20%及1%溶液。
助溶剂:取水杨酸钠25 g,置于100 mL容量瓶中,加超纯水溶解,待完全溶解后定容至刻度。
混合溶剂1、2(专利申请中):量取混合溶剂50 mL加水定容至100 mL。
以超纯水为空白对照,将以上溶液分别置于1 cm石英吸收池中,用双光束紫外分光光度计在200~500 nm波长间扫描,绘制各药剂吸收图谱。
2.4不同溶剂及助溶剂对痢菌净的溶解程度
分别按“2.3”试验配制不同溶剂、助溶剂及混合溶剂1、2的溶液100 mL,分别加入过量的痢菌净于溶液中,使其达到饱和溶液,于室温磁力搅拌72 h,静置取上层清液,经0.22 μm有机相滤膜过滤后,用紫外分光光度计于“2.1”试验中选定的最大吸收峰来测定痢菌净在该溶剂、助溶剂或混合溶剂中的最大溶解量。
3结果
3.1痢菌净全波长扫描由吸收光谱可知在373.0 nm、368.0 nm、356.0 nm、254.0 nm、241.0 nm等处均有最大吸收峰。
3.2溶剂、助溶剂及混合溶剂全波长扫描由全波长扫描图谱可以看出波长200~350 nm处痢菌净与其他药物均有吸收值,为避免其他药物吸收对所建检测方法的影响,选取373 nm为痢菌净含量的检测波长。
3.3标准曲线的绘制将以上数据以痢菌净浓度为X(μg/mL)轴,吸光值为Y(Abs)轴进行回归分析,其回归曲线见图1。
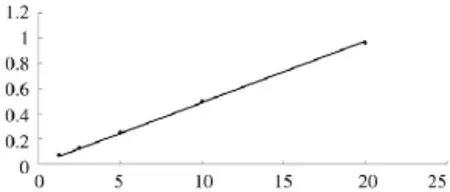
图1痢菌净标准曲线
回归方程为:Y=0.0488XR2=0.9992
试验结果表明,在1.25~20 μg/mL浓度范围内,吸收度与浓度呈良好的线性关系。
3.4不同溶剂及助溶剂对痢菌净的溶解程度
将检测吸光度值代入“3.2”所得方程,其不同溶剂及助溶剂对痢菌净的溶解量见表1。
由表1可知,混合溶剂1对痢菌净的溶解能力最大,为54.37 mg/mL,单一溶剂或助溶剂中水杨酸钠溶解效果最好,可达35.69 mg/mL,但均较3种混合溶剂少。

表1不同溶剂或助溶剂痢菌净的最大溶解量
4讨论
4.1对痢菌净在200~500 nm全波长扫描结果,共有5个吸收峰,分别为373.0 nm、368.0 nm、356.0 nm、254.0 nm、241.0 nm,241.0 nm及254.0 nm较高,373.0 nm、368.0 nm及356.0 nm较低,均可单独作为检测波长使用,实践中应结合所配伍药品的最大吸收峰来选取特定的检测波长。
4.2对常用溶剂、助溶剂及混合溶剂的全波长扫描,仅水杨酸钠在350.0~500.0 nm区间有较低波峰的干扰,其他仅在200.0~350.0 nm区间处有吸收曲线且吸收数值较高,混合溶剂也未显示在350.0~500.0 nm处有吸收峰。为此,373.0 nm将作为痢菌净检测时的最佳检测波长。
4.3本试验在选定的检测波长373.0 nm绘制痢菌净水溶液标准曲线,其在1.25~20 μg/mL有良好的线性关系,R2为0.9992,在一定范围内吸光度值与浓度符合比尔-郎伯尔定律。
4.4单一溶剂或助溶剂对痢菌净的溶解程度均较混合溶剂差,且以水杨酸钠效果最好,但其在350.0~500.0 nm区间有较低的吸收峰,对运用紫外分光光度法测定痢菌净含量有一定的影响,本试验同时也运用40%乙醇溶液代替纯水来配制不同溶剂及助溶剂,观察对痢菌净的溶解情况,其结果显示,会大幅度提升痢菌净的溶解量,二甲亚砜、苯甲醇、甘油、聚乙二醇、丙二醇、N,N-二甲基甲酰胺及水杨酸钠可分别形成浓度为14.55 mg/mL、19.80 mg/mL、12.73 mg/mL、14.26 mg/mL、16.01 mg/mL、29.74 mg/mL及46.18 mg/mL。2种混合溶剂均有较好的溶解效果,混合溶剂1溶解量最大,达54.37 mg/mL。为以后痢菌净缓释药剂的开发奠定了基础。
[1]中国兽药典委员会.中华人民共和国兽药规范(一部,1992年版).北京:中国农业出版社,1-2,附16.
[2]中国兽药典委员会编.兽药手册(第3版).北京:中国农业出版社,1992,96-97.
[3]李荣誉,王红霞.利用助溶性辅料制备2%痢菌净注射液的研究[J].河南畜牧兽医,1999,6(20):7-9.
S859.7911H10N2O3),对牛、猪细菌性肠炎及猪短螺旋体引起的痢疾均有良好的疗效[1-2],但因其水溶性较差[3],难以制备高浓度药液,使其剂型较为单一,生物利用率低,影响了该药物在临床上的使用。为此,本试验选取多种常用溶剂、助溶剂及混合溶剂,为以后该药剂高浓度溶液的配制提供参考依据。
B
0529-6005(2016)08-0113-03痢菌净又名乙酰甲喹(C
2015-05-20
侯美如(1985-),女,助理研究员,硕士,主要从事动物疫病防控工作,E-mail:houmeiru168@126.com
周庆民,E-mai:ssyzqm@163.com

