遗传性心肌疾病的诊断及治疗
闻松男,刘 念*
(首都医科大学附属北京安贞医院,北京 100029)
遗传性心肌疾病的诊断及治疗
闻松男,刘 念*
(首都医科大学附属北京安贞医院,北京 100029)
遗传性心肌疾病是一组原发性的、以累及心肌结构和功能为主要病理生理基础的心脏疾病,通常由一种或多种编码心肌细胞、组织的基因发生变异引起,有较强的遗传倾向。遗传性心肌疾病主要包括肥厚型心肌病(HCM)、致心律失常性右室心肌病/发育不良(ARVC/D)、左室心肌致密化不全(LVNC)、遗传性心肌淀粉样变等,以前二者最常见。
1 致心律失常性右室心肌病
致心律失常性右室心肌病(ARVC)是一种原因不明的心肌疾病,病变主要累及右心室(RV),以RV心肌不同程度地被脂肪或纤维脂肪组织代替为特征。临床主要表现为室性心律失常或猝死,也可无症状。ARVC在文献中曾被称为“羊皮纸心”、“Uhl氏畸形”、RV脂肪浸润或脂肪过多症、右心室发育不良、致心律失常性右室发育不良(ARVD)、右室心肌病、ARVC,以后三种使用较广泛。文献中,一些ARVC常被描述为Uhl畸形,两者须加以鉴别。Uhl畸形是真性先天畸形,为先天性右室心肌完全缺如,心室壁薄如纸,仅存心内膜和心外膜,婴幼儿多见,常早年死于充血性心力衰竭。而ARVC多见于成年人,临床主要表现为室性心律失常或猝死,右室心肌不是先天性缺如,而是灶性或弥漫性地被脂肪或纤维脂肪组织代替,可累及左室,是一种进行性心肌病,在病理学和法医学上称之为脂肪心或心肌脂肪浸润。
ARVC具有遗传性,家族性ARVC发生率达30~50%,多呈常染色体显性遗传。目前的研究表明桥粒基因突变及伴随的缝隙连接组成蛋白异常可能是导致绝大部分ARVC的发病机制。
1.1 致心律失常性右室心肌病的病理特点
尸检所见,病变呈灶性或弥漫性,主要累及右室前壁漏斗部、心尖部及后下壁,三者构成了所谓的“发育不良三角”。右心室多呈球形增大,心腔扩张,可伴室壁瘤形成。切面心壁肌层变薄,可见层状、树枝状或云彩状分布的黄色脂肪浸润区。部分(20-50%)病例病变可累及室间隔和左室。Corrade等[1]在多中心的尸检报告中发现ARVC病人76%有左室受累,且为年龄依赖性,并认为ARVC不应被看作是独立发生于右室的疾病。心瓣膜及冠状动脉等无形态异常。镜下以右室心肌不同程度地被脂肪或纤维脂肪组织代替为特征。脂肪组织呈条索状或片块状浸润、穿插于心肌层,残存的心肌纤维萎缩,呈不规则索团状,与脂肪组织混存。在2010年Task Force诊断标准中[2],组织学指标成为ARVC的诊断指标之一,其主要指标为至少1个标本经形态学分析残留心肌细胞<60%(或估计<50%),伴右室游离壁心肌被纤维组织替代,心内膜活检发现有或无心肌细胞脂肪替代;次要指标为至少1个标本经形态学分析残留心肌细胞<60%~75%(或估计50%~65%),伴右室游离壁心肌被纤维组织替代,心内膜活检发现有或无心肌细胞脂肪替代。
1.2 致心律失常性右室心肌病的临床表现
ARVC好发于青壮年,男性多见,有家族倾向。患者可无症状,或表现为心律失常引起的心悸、头晕及运动相关的晕厥,部分患者可能以心搏骤停为首发表现,严重者心功能受累表现为充血性心力衰竭。室性心律失常是ARVC最常见的临床表现,以反复发作的持续性或非持续性室速为特征,室速多起源于右心室,可发展为室颤导致病人猝死。
根据ARVC的临床特点,常将其自然病程分为四个阶段:隐匿期:无症状或轻微心律失常,右室轻微结构改变,多局限于“发育不良三角”(右室前壁漏斗部,心尖部,后下壁)。不稳定期:可发生症状性室性心律失常,室性早搏和室速多呈左束支阻滞图形。或以猝死为首发表现。右室明显的形态、结构、功能改变。右心衰竭期:弥漫性右心室结构改变,出现右心功能不全。终末期:疾病进入终末阶段,顽固性右心甚至全心衰竭,可有无休止性室速。
1.3 致心律失常性右室心肌病的诊断标准
当患者有心悸和晕厥症状,且出现LBBB 型室性期前收缩(PVC),并且下壁导联(Ⅱ,Ⅲ,aVF)主波向下,临床上应该高度怀疑AVC诊断[3]。
ARVC的诊断主要根据:①相关病史:如既往史、家族史和家族中有无早年(≤35岁)猝死者;②可疑征兆:注意运动后有否心悸、频发室性早搏、发作性晕厥等;③临床表现:主要是不明原因的以右心室为主的心脏增大和室性心律失常;④各项实验室检查结果。在排除其他各类心脏病和各种胸、肺疾病后,临床可诊断本病。
1.4 致心律失常性右室心肌病的辅助检查
X线胸片:心脏正常或增大,轮廓呈球形,肺动脉或流出道扩张,多数患者心胸比率≥0.5。
心电图:①窦性心律时常呈完全性或不完全性右束支阻滞表现,右心导联出现右室晚激动波(Epsilon波),T波倒置。②发作室速时,QRS波呈左束支阻滞图形,常伴有电轴右偏。③心室晚电位阳性检出率高。
电生理学检查:对有自发性室速史的患者,大多数程序电刺激可诱发单形性或多形性持续性室速,呈左束支阻滞图形,部分可见碎裂电位。但心内电生理检 查诱发出室速并非确诊ARVC所必须。
超声心动图:①右心室扩大,流出道增宽。②右心室运动异常或障碍,舒张期呈袋状膨突或呈室壁瘤样改变。③右心室节制带结构异常,肌小梁紊乱。超声心动图可重复性好,是筛查ARVC的首选影像学检查方法。
右心导管及右心室造影检查:右房和左、右室压力正常或升高;右房压力可升高,重者可超过肺动脉舒张压;心脏指数降低,提示心搏出量减少;左室受累者舒张末期压力稍高,容积指数增大,伴左室射血分数降低。造影显示右心室扩大,伴收缩功能降低或运动障碍,室壁膨突,造影剂排泄缓慢,射血分数降低。
放射性核素血池显像:也可见右心室扩大、收缩功能减退;对判断右心室的病变特征、范围及其解剖学定位和左心受累情况,具有敏感性高、特异性强等优点,而且属于无创性检查。
CT:可显示①右心室扩大,游离壁呈扇贝形图象,可见心内膜下低衰减的肌小梁横过右室腔。②能直接显示心外膜脂肪和心肌内脂肪浸润程度。③可显示左室受累的各种形态异常。
磁共振显像:可精确测定右心室各种形态和功能改变以及左室受累情况。可鉴别正常心肌与脂肪或纤维脂肪组织。MRI取代心脏超声成为这种疾病无创显像检查的金标准。(图1)
心内膜心肌活检:是确诊ARVC的有效方法。活检取材部位应是病变最常累及的右心室游离壁。但由于该处心壁变薄,质脆而软,有发生穿孔的危险,故应在超声心动图引导下进行,并应有心外科作后盾。
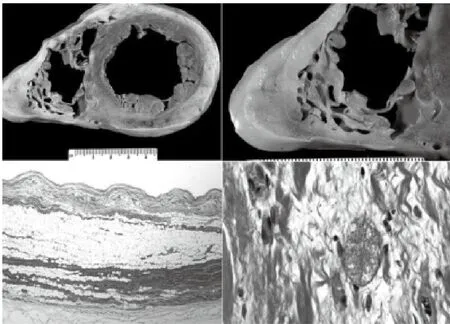
图1 ARVC的病理改变(一例ARVC猝死患者的尸检心脏标本)
上图:左、右心室短轴切面,右心室腔扩大、室壁薄,右心室游离壁、左心室后侧壁的脂肪组织明显增多(左);其中右心室前壁心肌几乎完全被脂肪组织替代,后壁有大量脂肪纤维化组织(右)。下图:Masson染色见右心室壁全层为脂肪或纤维化组织,仅残存少量带状心肌组织(左);高倍镜下可见典型的心肌细胞空泡样变性(右)。
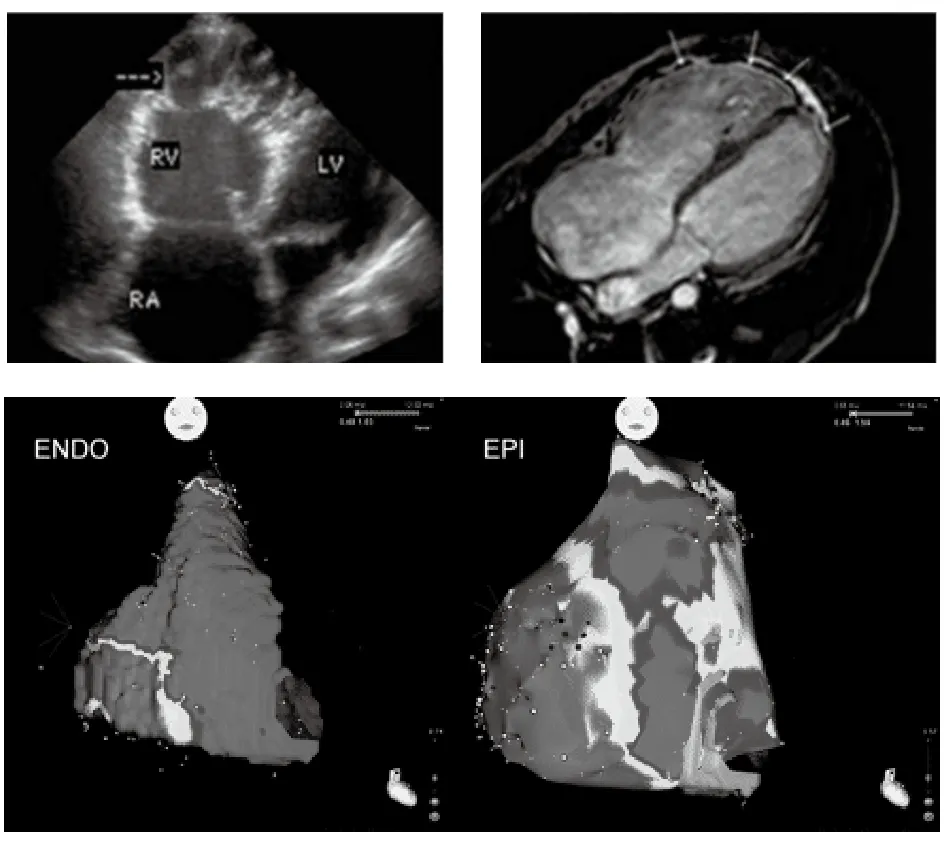
图2 ARVC的影像学。
上图:一例ARVC患者的经胸心脏超声示右心室明显扩大,心尖室壁瘤形成(左);心脏长轴MRI延迟显像见右心室壁及左心室心尖区广泛脂肪纤维化(右)。一例ARVC患者的心内膜(Endo)和心外膜(Epi)电压标测见大面积低电压区(红色区域)。
1.5 ARVC伴发的室速与起源右心室的特发性室速鉴别要点
右室特发性室速与ARVC室速均好发于青年人,且都与情绪激动和运动有关,有相似之处。鉴别的要点是:
ARVC室速发作时常伴严重血流动力学紊乱,甚至演变成室颤。心源性晕厥常见,为年轻人猝死的主要原因之一,有家族遗传倾向。而右室特发性室速发作时多血流动力学稳定,晕厥少见,无家族遗传倾向。
ARVC室速发作时多呈多形性,室速多来源于心尖部和右室前壁。而右室特发性室速绝大部分来源于右室流出道。
大部分ARVC患者在窦律时心电图有异常改变,如Epsilon波,右胸导联QRS增宽,右束支阻滞等。而右室特发性室速患者在窦律时心电图多正常。
绝大部分ARVC患者心室晚电位阳性。而右室特发性室速患者心室晚电位为阴性。
ARVC室速对抗心律失常药物反应欠佳,导管消融成功率低,易复发。右室特发性室速导管消融成功率高,不易复发。
1.6 致心律失常性右室心肌病预后
提示ARVC预后不良的因素包括既往有心搏骤停史、持续性室速伴晕厥者、QRS波离散度增加(12导联QRS最大时限和最小时限>40 ms)、症状出现早、右室严重扩张及左室受累者。
1.7 致心律失常性右室心肌病的治疗
对ARVC的治疗目标是减少或控制心律失常的发生,预防猝死,减轻心力衰竭的症状。
1)一般处理:限制体力活动和情绪激动,避免诱发室性心律失常。避免劳累和呼吸道感染,预防心衰。
2)室性心律失常的治疗:β受体阻滞剂可减少ARVC室速发作,降低猝死风险,是主要的基础治疗。效果不佳时可合用IA、IC或III类抗心律失常药。对于无法耐受药物或药物治疗效果不佳者可行电生理检查确定室速起源部位进行导管消融治疗,但疗效不确切,受患者病变部位、进展程度等多因素的影响。一项ARVC注册研究[4]提示,胺碘酮在预防ARVC室性心律失常方面优于索他洛尔和β受体阻滞剂。ARVC/D患者经历过一次以上引起血流动力学不稳定的持续性室速或室颤发作、严重右室和(或)左室收缩功能障碍无论是否存在心律失常,均推荐植入ICD治疗(Ⅰ类);经历过一次以上血流动力学稳定的室速发作及存在“主要”危险因素如原因未明的晕厥、中度心室功能障碍或NSVT的患者应考虑植入ICD治疗(Ⅱa类);在仔细评价ICD植入的长期风险及获益后,存在“次要”危险因素的ARVC/D患者可考虑植入ICD(Ⅱb类);而对于无症状且无危险因素或健康的基因携带患者,不推荐进行预防性ICD植入术(Ⅲ类)[5]。对无休止性室速发作者,心脏移植是最后的选择。
3)心衰的治疗:按照心力衰竭的常规处理,终末期可考虑心脏移植。
2 肥厚型心肌病
肥厚型心肌病是以左心室和(或)右心室肥厚(通常为非对称性)、心室腔变小、左室充盈受损和舒张期顺应性下降为特征的原发性、遗传性心肌病,为青年猝死的常见原因之一。肥厚型心肌病的特征性表现为非对称性室间隔肥厚,光镜下见心肌细胞肥大,肌束排列紊乱构成独特漩涡状,局限性或弥漫性间质纤维化。心肌壁内冠状动脉管壁增厚、管腔变小。肥厚型心肌病患者常伴心肌缺血,心肌缺血引起心肌损伤、坏死,最终可出现心室扩张和收缩力降低,发生心力衰竭;肥厚型心肌病患者易发各种心律失常、尤其是恶性室性心律失常,导致患者猝死。
2.1 肥厚型心肌病临床表现
肥厚型心肌病的临床表现因其肥厚部位及程度的不同差异较大,半数患者可无症状。常见症状为呼吸困难,90%以上有症状的患者出现劳力性呼吸困难,夜间阵发性呼吸困难较少见。胸闷、胸痛及心悸较常见。重症患者可有恶性心律失常、心力衰竭甚至猝死。左心室流出道有梗阻的患者在运动时因交感神经兴奋,肥厚心肌收缩力增强,同时因加速喷射的血流产生吸引力,使二尖瓣前叶前向运动,流出道梗阻更加严重,心排出量瞬间骤降,患者可出现黑曚及晕厥。猝死也可为首发症状,也是肥厚型心肌病的主要死亡原因。
肥厚型心肌病的自然病程可以很长,最高年龄超过90岁,75岁以上的达到23%。肥厚型心肌病的主要死亡原因包括心脏性猝死(51%),心力衰竭(36%),卒中(13%);其中16%的猝死是在中等到极量体育活动时发生[6]。
肥厚型心肌病猝死的高危因素有:心搏骤停生还者;反复发作的晕厥史;持续性室性心动过速;运动时血压不升反降;左心室壁或室间隔厚度≥30 mm;左室流出道压力阶差>50 mmHg;非持续性室速或心房颤动;家族性肥厚型心肌病恶性基因型(α-MHC、cTnT和cTnI某些突变位点)。
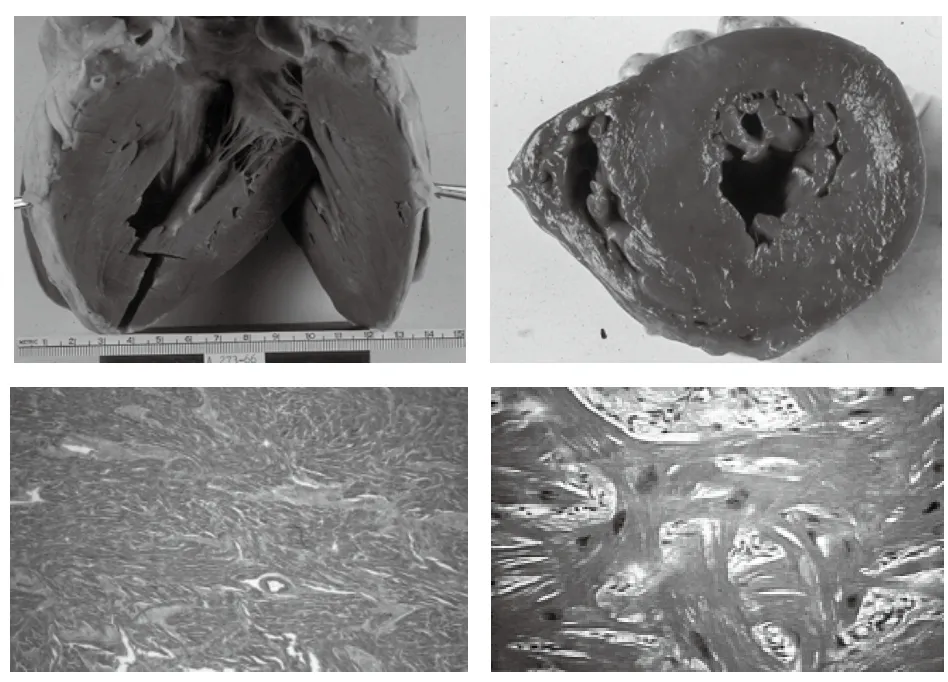
图1 HCM的病理改变
上图:一例HCM患者的尸检心脏标本。左心室显著肥厚,以室间隔肥厚更为明显,乳头肌粗大,左心室心腔变小(左:长轴观;右:短轴观)。下图:心肌细胞排列紊乱(左);高倍镜下可见心肌细胞肥大(右)。
2.2 肥厚型心肌病诊断
2007年中华医学会肥厚型心肌病的诊断标准[7]:
主要标准:(1)超声心动图左心室壁或(和)室间隔厚度超过15 mm。(2)组织多普勒、磁共振发现心尖、近心尖室间隔部位肥厚,心肌致密或间质排列。
次要标准:(1)35岁以内患者,12导联心电图I、aVL、V4-V6导联ST下移,深对称性倒置T波。(2)二维超声室间隔和左室壁厚11-14 mm。(3)基因筛查发现已知基因突变,或新的突变位点,与HCM连锁。
排除标准:(1)系统疾病,高血压病,风湿性心脏病二尖瓣病,先天性心脏病(房间隔、室间隔缺损)及代谢性疾病伴发心肌肥厚。(2)运动员心脏肥厚。
临床确诊HCM标准:符合以下任何一项者:1项主要标准+排除标准;1项主要标准+次要标准3即阳性基因突变;1项主要标准+排除标准2;次要标准2和3;次要标准1和3。
FHCM的诊断:除发病就诊的先证者以外,三代直系亲属中有两个或以上成员诊断HCM或存在相同DNA位点变异。FHCM诊断后对其遗传背景筛查和确定,随访无临床表现的基因突变携带者,及时确定临床表型十分重要。
2.3 肥厚型心肌病治疗
肥厚型心肌病的治疗以改善左室舒张功能,减轻左室流出道梗阻,缓解症状,预防猝死,提高长期生存率为目标。
无症状的肥厚型心肌病患者应尽量生活规律,限盐低脂饮食,避免过量饮酒、过度劳累,不宜剧烈运动。有症状的患者应避免劳累、激动及突然用力,应规律监测血压、心率,以及避免使用增强心肌收缩力和减轻心脏负荷的药物。严重心功能减退的患者应绝对卧床休息,避免一切可能加重心脏负荷的因素。
β受体阻滞剂为肥厚型心肌病的一线治疗药物之一[8],通过抑制心脏交感神经兴奋性,减慢心率,降低左心室收缩力,降低心肌需氧量来减轻流出道梗阻,可使1/3~2/3患者改善症状。但对肥厚性梗阻型心肌病无确切疗效,许多患者远期疗效差。目前认为β受体阻滞剂能改善症状但不能减少心律失常与猝死,不能改善肥厚型心肌病患者的预后。
非二氢吡啶类钙离子拮抗剂能选择性抑制细胞膜钙内流,降低钙结合力和细胞内钙利用度,降低左心室收缩力,改善心室顺应性和心室流出道梗阻,在对β受体阻滞剂不能耐受或存在禁忌症时推荐,首选维拉帕米[8]和地尔硫卓,由于这类药物有扩血管作用,严重流出道梗阻的患者用药初期需要严密观察。
ACEI类药物能有效阻止心室肥厚与心肌纤维化,增加缓激肽含量,促进一氧化碳和前列腺生成,有抗有丝分裂作用,有助于遏制心肌肥厚进展;但ACEI类药物扩张外周动脉,在严重左室流出道梗阻患者可能使梗阻部位两侧压力阶差增大,需谨慎从小剂量开始使用。
抗心律失常药通常应用于有室性心律失常与心房颤动的患者。胺碘酮可改善症状,增加运动量。丙吡胺是一种有负性肌力作用的IA类抗心律失常药,可减轻流出道梗阻,降低流出道压力阶差,抑制心房颤动,维持窦性心律,增加心室充盈;因其可缩短房室传导时间,在心房颤动可加快心室率,必要时与β受体阻滞剂联用减慢心室率。但丙吡胺并不能改善心室舒张功能。在用药期间应检测QT间期,防止致心律失常作用及其他不良反应。
洋地黄和利尿剂[8]因可加重左室流出道梗阻而被禁用,但对于心腔扩大、收缩功能不全而流出道梗阻不明显的患者可用。
14%~16%肥厚型心肌病患者随年龄增长逐渐出现扩张型心肌病症状和体征,称肥厚型心肌病的扩张型(心肌病)相,此时应按扩张性心肌病伴心衰治疗。
静息状态下流出道梗阻或负荷运动时左室流出道压力阶差≥50mmHg,HYHA心功能III~IV级且药物治疗不能改善者,可考虑室间隔化学消融或外科手术治疗[8]。前者通过导管向左冠状动脉前降支的间隔支内注入无水酒精0.5~3ml,引起可控范围的室间隔上部心肌梗死,扩大左室流出道,降低压力阶差。外科手术方法包括室间隔部分心肌切除术和室间隔心肌剥离扩大术等。
双腔起搏器通过起搏右室心尖,使肥厚的室间隔与左室游离壁在收缩期同向运动,一定程度上减轻流出道梗阻,改善临床症状及心功能,但该治疗不能作为肥厚型梗阻性心肌病的主要治疗方式,在内科药物治疗无效,症状严重或出现不良反应、左室流出道压力阶差>50mmHg,或出现房室传导阻滞、交界性逸搏伴或不伴心功能不全,基因筛选存在恶性突变的可选择双腔起搏器植入治疗[8]。
植入性复律除颤器(ICD)可预防猝死,对猝死高危患者建议使用ICD进行一级预防,对心搏骤停生还者或反复自发性持续性室性心动过速者,ICD植入可作为猝死的二级预防措施[9]。
2.4 肥厚型心肌病患者预后
可从心室肥厚与流出道梗阻程度、是否存在心肌缺血及心律失常等方面初步判断。总的来说,HCM的中长期预后相对较好,以心肌肥厚仅累及心尖部者预后最佳。约1/4的患者可发生心血管事件,诊断年龄≥60岁及左心房内径≥36 mm 是发生心血管事件的独立危险因素。
[1] Corrade D,Bassoc N,Thiene G,et al.Spectrum of clinicopathologic manifestations of ARVD:a multicenter study.J Am Coll Cardiol,1997,15:1512-1520.
[2] Marcus FI, McKenna WJ, Sherrill D, et al. Diagnosis of arrhythmogenic right ventricular cardiomyopathy/dysplasia: proposed modification of the Task Force Criteria. Eur Heart J. 2010;31(7):806-14.
[3] Basso C,Thiene G,Corrado D,et al. Hypertrophic cardiomyopathy and sudden death in the young: pathologic evidence of myocardial ischemia. Hum Pathol,2000,31: 988-898.
[4] Saguner AM,Brunckhorst C,Duru F. Arrhythmogenic ventricular cardiomyopathy: A paradigm shift from right to biventricular disease. World J Cardiol,2014,6: 154-174.
[5] Corrado D, Wichter T, Link MS, et al. Treatment of arrhythmogenic right ventricular cardiomyopathy/dysplasia: an international task force consensus statement. Circulation. 2015 Aug 4;132(5):441-53.
[6] Frenneaux MP. Assessing the risk of sudden cardiac death in a patient with hypertrophic cardiomyopathy. Heart. 2004 May. 90(5): 570-5.
[7] 中国心肌病诊断与治疗建议工作组.心肌病诊断与治疗建议.中华心血管病杂志2007年1月第35卷第1期:6-7.
[8] Perry M. Elliott, Aris Anastasakis, MichaelA.Borger, et al. 2014 ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy. European Heart Journal (2014) 35, 2733-2779.
[9] Brignole M, Auricchio A, Baron-Esquivias G, et al. 2013 ESC guidelines on cardiac pacing and cardiac resynchronization therapy[J]. Rev Esp Cardiol(Engl Ed), 2014, 67(1):58.

R542
A
ISSN.2095-6681.2016.17.009.02
闻松男,首都医科大学附属北京安贞医院副主任医师、医学博士。擅长心律失常导管消融与器械植入的围术期管理和术后随访,主要从事心律失常的转化与心电学研究。承担“国家自然科学基金”1项。2015年入选北京市委组织部“北京市优秀人才计划”。以第一作者在SCI及核心期刊发表科研论文20余篇。参与多项国际临床研究。

