导向有机化合物对氟康唑发明的贡献
吴建良,李永福
(1.杭州立佳环境服务有限公司,浙江杭州311101;2.Techemax,LLC,Oregon 97330,USA)
导向有机化合物对氟康唑发明的贡献
吴建良1*,李永福2
(1.杭州立佳环境服务有限公司,浙江杭州311101;2.Techemax,LLC,Oregon 97330,USA)
以降低化合物的亲脂性、提高代谢稳定性为出发点,在导向化合物的基础上勇于改进,脱颖而出新一代的高效抗真菌药—氟康唑。
氟康唑;抗真菌药物;导向化合物
0 引言
真菌感染的治疗,特别是对于免疫系统缺陷的病人,是当今医疗界面临的一大难题[1]。我们的周围布满了真菌。它们存在于土壤、空气以及人的胃肠道。它们通常不会致病,因为我们的免疫系统保护着我们。但是,医疗技术的发展,诸如器官和骨髓的移植,以及对于癌症的化疗措施,导致了深部真菌感染病人数目的增加[2-4]。那些接受白血病、某些癌症治疗和器官移植的病人以及艾滋病人,由于他们的免疫系统受到了抑制,各种真菌感染会危及他们的生命[5]。
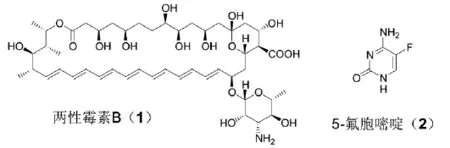
早在20世纪的70年代,辉瑞(Pfizer)公司在英国的研究中心开始了一个研究项目,旨在发明一个能治疗深部真菌感染的药物。由于真菌和人体的生物化学类似,使得寻找安全高效的抗真菌药物更为困难。当时仅有的药物是两性霉素B(1)和5-氟胞嘧啶(2)。两性霉素B是一个多烯的抗生素,能与细胞膜上的真菌甾醇—麦角甾醇结合,使细胞失去必需的离子。不幸的是,两性霉素B对胆固醇也能结合。这一选择性的缺乏导致人体许多副作用,如发抖、风寒、发烧、恶心和肾脏损害[6]。这些副作用,加上两性霉素B给药时静脉输注长达数小时,使得许多病人不愿使用。那时两性霉素B是万不得已的一项选择。另外一个广泛使用的深部有效的药物是5-氟胞嘧啶,它具有良好的口服生物利用度和低毒性的优点,但是只对有限的真菌有效,而且长期使用常常产生抗药性[7]。显然,对于治疗真菌感染迫切需要一个安全、高效的药物。
1 导向化合物
许多不同的结构类型具有抗真菌活性。大部分化合物不能选择性地对抗真菌,而咪唑类化合物对广泛的真菌病原体有很强并且有选择性的体外活性[8]。它们的抗真菌作用是由于抑制了真菌C-14脱甲基酶——一个含有细胞色素P450的酶,从而阻止了羊毛甾醇(3)生成麦角甾醇(4)(图1)。麦角甾醇能保持真菌膜的流体性,因而对于真菌的存活至关重要[9]。

图1
由于咪唑类化合物对于真菌的C-14脱甲基酶具有显著的选择性,而不是对非常相近的哺乳动物的酶,因而这类化合物会具有其固有的安全性。早期研究工作取得了噻康唑(Tioconazole,5),它的局部用药对皮肤和阴道的真菌感染临床上非常有效[8]。但是,当口服或静脉给药时,对动物的真菌感染治疗效果很差。研究表明这些咪唑类抗真菌剂特别容易代谢失活,导致低的口服生物利用度和低的血浆浓度。另外,噻康唑是亲脂性的(logP≈5),与血浆蛋白高度结合导致游离的、活性的形式以非常低的浓度在体内循环。
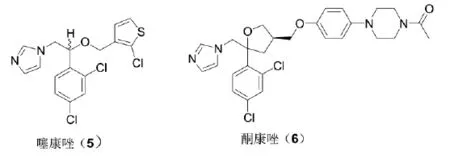
为使所合成的化合物代谢稳定、亲脂性低,以提高口服生物利用度,降低蛋白结合,从而提高游离药物的血浆浓度,引入了一系列极性的烷基、芳环和杂环基团替代噻康唑的氯代噻吩部分,取得了一些进展。其中,酮康唑(6)口服对动物真菌感染的治疗相当有效[10]。这一发现使得研究重点集中到了酮康唑的结构改造上。对酮康唑的研究发现,尽管它比以前咪唑类抗真菌化合物在代谢上稳定性增加,使得口服生物利用度有所提高,但是,它的稳定性仍然不够,在尿中的原药浓度很低。酮康唑比以前的咪唑类化合物亲脂性低,具有较高的血药浓度,但它仍然与血浆蛋白高度结合,只有不到1%以游离形式存在。总之,酮康唑相比于以前咪唑类抗真菌化合物是一个重要进展[5],但是对于进一步改进尚有广阔的余地[11]。

图2
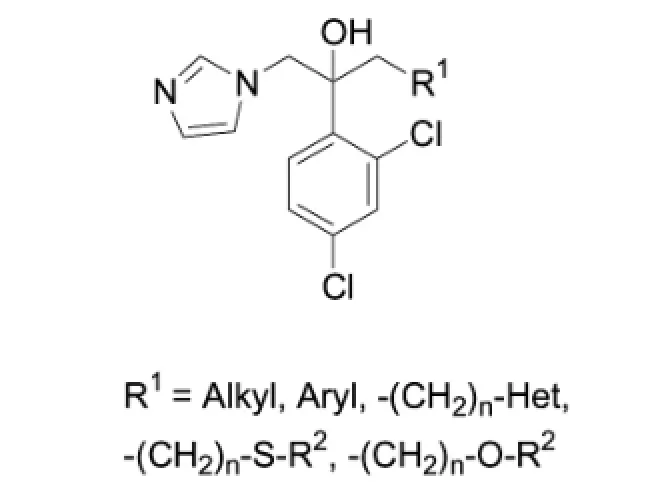
图3
正如图1所示,当时对抗真菌药物机理的一致认识是,咪唑基团可以阻止真菌的C-14脱甲基酶,因而,在结构改造中,咪唑作为一个固定的基团而得以保留。在酮康唑的结构基础上,合成了一系列结构类型,如二氧杂环(7)、羟基衍生物(8)、四氢呋喃类(9)、二硫杂环(10)等(图2)以降低亲脂性、提高代谢稳定性。引入极性官能团如酰胺、砜、氰和极性杂环也都具有一定的活性。其中某些化合物能达到与酮康唑相似的体内抗真菌活性,但是却没有一个具有明显的优势。其中羟基衍生物(8)为非环结构,与酮康唑结构相比差别较大,羟基的存在可以降低亲脂性、增加水溶性,而且在合成工艺上相对容易,便于构效关系的研究。因此,在此羟基衍生物的基础上合成了大约300个化合物(图3)。其中许多显示出与酮康唑相似的活性,但是却无法超越酮康唑。
2 氟康唑的发明
药物研究工作者逐渐认识到,咪唑基团作为抗真菌药物设计中一个经典而又不能改变的策略,似乎束缚着进一步创新的思维,限制着寻找更高效、更安全的抗真菌药物的突破。
要想在酮康唑的基础上打开一个新的局面,如果不对咪唑环进行更换似乎已经到了山穷水尽的地步。图4中选择了一系列基团,它们相应的咪唑衍生物具有与酮康唑等效的体内体外活性。替代之后,如果能改善咪唑化合物代谢不稳定的缺陷,那么新的化合物有可能会在药效上超过酮康唑。
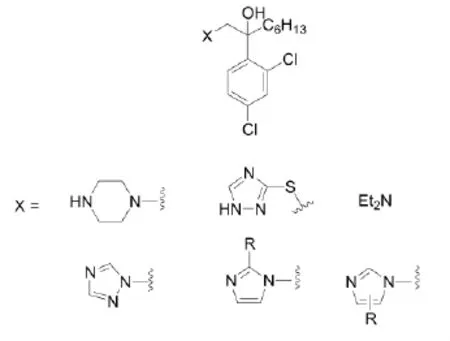
图4
在所尝试的咪唑取代基中,唯一具有较好活性的是1,2,4-三唑。当1,2,4-三唑-1-基替代咪唑基团以后,得到代号为UK-46,245的化合物(11),其对抗深部念珠菌的活性是相应咪唑类似物的两倍。这一结果表明三唑基团比咪唑基团在代谢的稳定性上有了提高,而且仍然保持着与在真菌C-14脱甲基酶中的细胞色素P450相互作用的能力。既然引入一个三唑可以提高抗真菌活性,那么引入两个三唑自然是下一个策略。用第二个三唑取代化合物11中一个亲脂性高又代谢不稳定的烷基,得到一个对称的双三唑化合物UK-47,265(12)。这是一个独特的化合物。当它在小鼠深部念珠菌模型上试验时,口服或静注,其活性比酮康唑强100倍。这一活性结果完全是前所未有的。对小鼠和大鼠的阴道念珠菌病、小鼠和豚鼠的皮肤真菌病、以及免疫缺陷的小鼠和大鼠的深部念珠菌病,都显示出理想的效果。药动学研究表明:体内活性不是由于生成了活性的代谢物,而是由于该化合物特别稳定,有30%的原药在尿中排出,这与酮康唑的1%形成了鲜明的对照[12]。因而,化合物12被过渡到临床前安全评价。
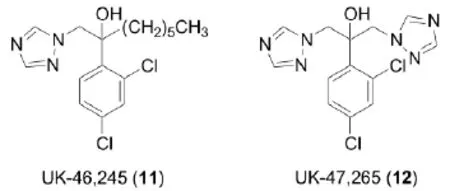
临床前试验结果大失所望,因为化合物12被发现对小鼠和狗有肝脏毒性,对大鼠有致畸作用。尽管受到这一挫折,研究人员非常坦然,因为他们从咪唑到三唑的突破所获得的结果已经确信一个比酮康唑强得多、比两性霉素B更优越的抗真菌药物已经近在咫尺。只要在原有的结构上进一步改进以降低毒性,一个高效安全的抗真菌药即可脱颖而出。实际上,在对化合物12进行抗真菌药动学和安全评价的同时,又合成了100多个双三唑类似物。一系列芳环和杂环基团替代了二氯苯基(表1)。许多化合物显示出很好的体内抗念珠菌活性,其中又择优进行阴道念珠菌病和皮肤真菌病的小鼠模型评价。最佳的三个化合物,2,4-二氟苯基、2-氯-4-氟苯基和4-氯苯基类似物过渡到小鼠的药动学评价。其中2,4-二氟苯基类似物拔得头筹(表1)。它的血浆半衰期为5.1 h,75%的原药在尿中排出,另外它的水溶性(室温时,8 mg/mL)极佳,有利于静注给药。这一化合物,UK-49,858,即氟康唑(13)在正常免疫功能的动物和免疫功能抑制的动物中对所有的真菌感染模型显示出高效的活性[13-14]。安全评价表明,氟康唑既无肝脏毒性,又无致畸作用,因而过渡到人体试验。
在健康志愿者中,氟康唑口服吸收很好,食物并不影响生物利用度。血浆半衰期大约是30 h。这样每日用药,药物可在4~5 d内达到稳定态[15]。氟康唑口服给药,大约有90%的原药经尿液排出,并且没有副作用。
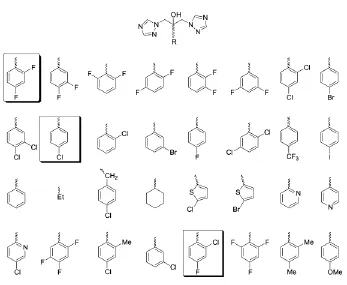
表1 双三唑化合物部分结构汇总
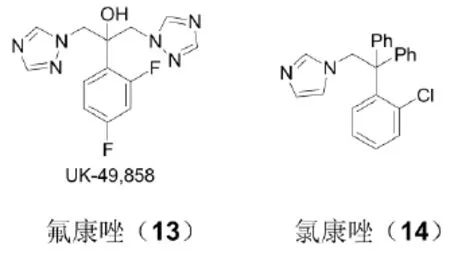
氟康唑因而过渡到对有真菌感染的人体评价。起初药效研究是对患有急性阴道念珠菌病的病人,半数人一次口服氟康唑150mg,另一半人与氯康唑(Chlotrimazole,14)阴道片一起在阴道内给药(每日200mg,连用三天)。两种药物都产生了很好的临床效果(氟康唑100%,氯康唑97%),并且没有副作用[16]。氟康唑从而过渡到对免疫缺陷病人的研究。这些病人极大多数是艾滋病患者,受到口腔念珠菌的感染。经过5~7 d的治疗后,临床治疗成功率达到100%,并且没有显著的副作用[17]。后来研究表明,对于HIV阳性的病人,单用氟康唑比单用酮康唑或先用酮康唑后用氟康唑更简单有效[18]。对于危及生命的真菌感染的病人研究,五名由于患癌症进行化疗或器官移植后免疫抑制的病人用氟康唑治疗念珠菌感染,在经过两个星期治疗后感染全部治愈[19]。进一步的研究表明,对于艾滋病、癌症、白血病和器官移植病人的念珠菌感染,氟康唑都有很好的疗效[20-23]。
隐球菌脑膜炎是危及生命的真菌感染,艾滋病人中多达30%有这种感染。对此氟康唑取得了临床上的成功[24-25]。最近的一项研究表明,氟康唑与5-氟胞嘧啶合用,与单用氟康唑或单用两性霉素B相比,临床效果进一步提高[26]。艾滋病人需要抗真菌药的维持以防复发或再度感染。研究表明用氟康唑防治效果很好,因而,现在它是这类病人的专用药品[27]。与先用两性霉素B治疗艾滋病人的隐球菌脑膜炎再用每周静注两性霉素B作为防止复发的治疗相比,口服氟康唑效果则要好得多[28]。
3 对药物研究的启发
氟康唑的发明使真菌病的治疗发生了根本性的变化,它对浅部和深部真菌感染具有同等疗效,并且既可口服又可静脉注射,给接受器官移植者、烧伤病人、接受化疗病人、艾滋病人和其他免疫系统减弱易受真菌感染的人带来了福音。作为当今世界一号抗真菌药,从该药问世以来,对于危及生命的真菌感染的治疗,它已经拯救了全世界成千上万的生命,减轻了无以计数的人的痛苦。
纵观氟康唑发明的整个过程,咪唑基团作为抗真菌机理中一个不可缺少的基本结构,曾经催生出以酮康唑为代表的一代抗真菌药物。但是,如果墨守成规,不敢挑战经典,那么抗真菌药物的研究只能在原地徘徊。三唑基团的引入无疑使抗真菌药物的研究和开发上升到了一个崭新的层面。如何从原来对事物的认知向前突破而又不落入“谬误”的陷阱,需要勇气和谋略。勇气是敢于大胆尝试,谋略则源于经验积累。从这个意义上说:退一步,前功尽弃;进一步,海阔天空。
更高效、更低毒、更广谱、更专一的抗真菌药物的研究仍在继续[29]。本文所呈现的理念,即在探索真理的道路上不断地超越自我,在新药开发的过程中应该还会继续发挥它的作用,更广泛地说,对于其它科学研究也不会例外。
[1]Robinson P A,Knirsch A K,Joseph J A.Fluconazole for life-threatening fungal infections in patientswho cannot be treated with conventional antifungal agents[J].Rev Infect Dis,1990,12(Suppl.3):S349-S363.
[2]Eilard T,Norrby R.Clinical diagnosis of systemic fungal infections[J].Scand J Infect Dis,1978,10(Suppl.16): 15-22.
[3]Hart P,Russel E,Remington J.The compromised host and infection.II.deep fungal infection[J].J Infect Dis,1969,120(2):169-191.
[4]Young R C,Bennett J E,Geelhoed G,et al.Fungemia with compromised host resistance:a study of 70 cases[J]. Ann Intern Med,1974,80(5):605-612.
[5]Heeres J in M edicinal Chemistry.The Role of Organic Chemistry in Drug Research ed.Roberts SM,Price B J,Academic Press,London,1985,p249.
[6]Maddux M S,Barriere S L.A review of complications of amphotericin B therapy:recommendations of prevention and management[J].Drug Intell Clin Pharmacol,1980,14:177-181.
[7]Block E R,Jennings A E,Bennett JS.5-Fluorocytosine resistance in Cryptococcus neoformans[J].Antim icrob A gents Chemother,1973,3(6):649-656.
[8]Jevons S,Gymer G E,Brammer K W,et al.Antifungal activity of tioconazole(UK-20,349),a new imidazole derivative[J].Antimicrob Agents Chemother,1979,15(4): 597-602.
[9]Van den Bossche H,Willemsens G,CoolsW,etal.Biochemical effects of miconazole on fungi.II.Inhibition of ergosterol biosynthesis in Candida albicans[J].Chem-Biol Interact,1978,21:59-78.
[10]Thienpont D,Cutsem JV,Gerven F V,et al.Ketoconazole-a new broad spectrum orally active antimycotic[J]. Experientia,1979,35:606-607.
[11]Holt R J in Antifungal Chemotherapy ed.Speller D C E,John Wiley,New York,1980,p107.
[12]Richardson K,Cooper K,Marriott M S,et al.Discovery of fluconazole,a novel antifungal agent[J].Rev Infect Dis,1990,12(Suppl.3):S267-S271.
[13]Richardson K,Brammer KW,MarriottM S,etal.Activity of UK-49,858,a bis-triazole derivative,against experimental infectionswith Candida albicans and Trichophyton mentagrophytes[J].Antimicrob Agents Chemother,1985,27(5):832-835.
[14]Troke PF,Andrews R J,Brammer KW,et al.Efficacy of UK-49,858(fluconazole)against Candida albicans experimental infections inmice[J].Antimicrob Agents Chemother,1985,28(6):815-818.
[15]Brammer K W,Farrow P R,Faulkner JK.Pharmacokinetics and tissue penetration of fluconazole in humans[J]. Rev Infect Dis,1990,12(Suppl.3):S318-S326.
[16]Brammer K W,Lees L J.In recent trends in the discovery,development and evalua tion of antifungal agents ed. From tling R A,Prous JR,Barcelona,1987,p151.
[17]Dupont B,Drouhet E.Fluconazole in the management of oropharyngeal candidosis in a predom inantly HIV antibody -positive group of patients[J].JMed Vet Mycol,1988,26(1):67-71.
[18]Rabeneck L,Laine L.Esophageal candidiasis in patients infected with the human immunodeficiency virus.A decision analysis to assess cost-effectiveness of alternativemanagement strategies[J].Arch Intern Med,1994,154(23):2705-2710.
[19]Cohen J.Treatment of systemic yeast infection with fluconazole[J].JAntimicrob Chemother,1989,23(2):294-295.
[20]Kujath P,Lerch K.Secondary mycosis in surgery:treatmentwith fluconazole[J].Infection,1989,17:111-117.
[21]Van’t Wout JW,Mattie H,van Furth R.A prospective study of the efficacy of fluconazole(UK-49,858)against deep-seated fungal infections[J].JAntimicrob Chemother,1988,21(5):665-672.
[22]Gritti F M,Raise E,Bonazzi L,et al.Fluconazole treatment for candidiasis and cryptococosis in patients with AIDSand AIDS-related complex[J].Curr Ther Res,1990,47:1049-1062.
[23]Kauffman C A,Bradley S F,Ross S C,et al.Hepatosplenic candidiasis:successful treatment with fluconazole[J].Am JMed,1991,91(2):137-141.
[24]Dupont B,Drouhet E.Cryptococcal meningitis and fluconazole[J].Ann Intern Med,1987,106(5):778-778.
[25]DismukesW,Cloud G,Thompson S,etal.In proceedings of the 35th Interscience Conference on Antimicrobial A-gents and Chemotherapy at Houston American Society for Microbiology,1325 Massachusetts Avenue,NW,Washington DC 20005,1989,Abstract 1065.
[26]Larson R A,Bazette S A,Jones B E,et al.Fluconazole combined with flucytosine for treatment of cryptococcal meningitis in patients with AIDS[J].Clin Infect Dis,1994,19(4):741-745.
[27]Diamond R D.The growing problem ofmycoses in patients infected with the human immunodeficiency virus[J].Rev Infect Dis,1991,13:480-486.
[28]Powderly W G,Saag M S,Cloud G A,et al.A controlled trial of fluconazole or amphotericin B to prevent relapse of cryptococcal meningitis in patients with the acquired im munodeficiency syndrome[J].New England JMed,1992,326(12):793-798.
[29]Roemer T,Krysan D J.Antifungal drug development: challenges,unmet clinical needs,and new approaches[J]. Cold Spring Harb PerspectMed,2014,4(5):a019703.
Advancing the Lead Com pounds towards the Discovery of Fluconazole
WU Jian-liang1*,LIYong-fu2
(1.Hangzhou Lijia Environmental Services Co.,Ltd.,Hangzhou,Zhejiang 311101,China;2.Techemax,LLC,Oregon 97330,USA)
This article reviewed the strategies ofmodifying the lead compounds for improvement to reduce the lipophilicity and enhance themetabolic stability in search formore effective antifungal agents.Fluconazole was thus invented,representing a novel class of triazole-containing derivatives,a superior generation of highly effective antifungal drugs.
fluconazole;antifungals;lead compounds
1006-4184(2016)9-0010-06
浙江力普GWM150纤维素粉碎烘干一体机列入2016科技计划
2016-07-25
吴建良(1962-),男,浙江杭州人,高级工程师,长期从事有机化工科研及环保工作。E-mail:717545975@qq.com。
日前,国家高新技术企业,中国粉碎技术的领航者——浙江力普粉碎设备有限公司研发的GWM150纤维素粉碎烘干一体机列入2016嵊州市科技计划。这是该公司持续在纤维素领域创新开发新品取得的又一成果。在此之前,力普研发的“短纤维粉碎机”、“高效纤维素剪切粉碎机”和“精制棉粉碎成套生产线”相继获得国家专利;“医药辅料纤维素醚专用高效剪切粉碎机的研究和产业化项目”、“GWM-730纤维素高效剪切磨开发”被列入省市科技项目,评为浙江省新产品。浙江力普独有的纤维素醚粉碎加工新技术获得了中国纤维素行业协会领导的充分肯定,协会领导曾于今年4月专程到公司进行了实地考察,并对力普当前取得的业绩和对行业的贡献,给予了很高评价,希望继续努力,提升我国纤维素生产设备的整体技术水平。(丁文供稿)

