去氢表雄酮合成研究进展
何智鹏,金灿
(浙江工业大学药学院,浙江杭州310014)
去氢表雄酮合成研究进展
何智鹏,金灿*
(浙江工业大学药学院,浙江杭州310014)
去氢表雄酮对生命代谢活动起着重要的调节作用,具有抗衰老、抗肿瘤、抗抑郁等作用。综述了去氢表雄酮的几种合成方法,并对合成方法进行了分析总结。
去氢表雄酮;化学合成;生物合成
0 前言
去氢表雄酮(Dehydroepiandrosterone),化学名(3β)-3-羟基-5-烯-17-甾酮,简称DHEA(Figure 1)。去氢表雄酮是20世纪的重要发现之一,是人体血液循环中最为丰富的甾体物质,是人体内40多种激素合成所必需的前提物质,在人体内的含量会随年龄的变化而变化[1]。DHEA具有广泛的生理活性,可预防心血管、糖尿病[2]等疾病,也应用于治疗抑郁症[3]、提高免疫力、抗衰老和抗肿瘤等方面,同时它也是合成米非司酮、曲螺酮、炔诺酮、醋酸阿比特龙[4]等甾体药物的一个关键中间体。近几年来,DHEA在临床上的应用是当前的热门。

Figure 1
1 合成路线
目前,去氢表雄酮获得方法主要有化学合成,生物合成和从天然产物中提取。以下就国内外对DHEA的研究概况作一概述。
1.1化学法合成DHEA
化学法合成去氢表雄酮主要以薯蓣皂苷元,4-AD以及各种甾醇为原料合成。其中薯蓣皂苷元是传统生产甾体激素类药物的重要基础原料,近年来薯蓣资源日益短缺,因此寻求以其他方法或原料制备DHEA具有较大意义。
1.1.1以薯蓣皂苷元为原料

以薯蓣皂苷元的酯化物为原料,经过高温裂解,氧化,碱性水解,得到醋酸妊娠双烯醇酮酯,再经肟化、贝克曼重排、水解得到DHEA[5],总收率60%,这也是现在工业上用得较多的一种方法(Scheme 1)。该工艺用到毒性大的吡啶,在重排时用到了苯和三氯氧磷,危险性大,且环境污染严重。
1.1.2以醋酸妊娠双烯醇酮酯为原料
与前一工艺(Scheme 1)相比,此工艺[6]肟化反应时用醋酸钠作为碱,不但价格比吡啶低,而且环境污染小,后处理方便。重排反应用对甲苯磺酰氯替代POCl3,三乙胺做缚酸剂,CH3OH替代苯做溶剂,有利于减少对环境的污染,降低成本,而且毒性也较低。再经过碱水解,酸中和,活性炭脱色得到DHEA,收率86%(Scheme 2)。

Scheme 2
1.1.3以胆固醇为原料
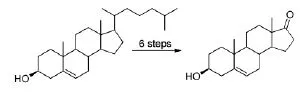
Scheme 3
1935年,Everett S[7]等人尝试用胆固醇等甾醇通过6步反应合成DHEA,但反应过低,且过程复杂,污染较大,该方法的尝试也为后续DHEA合成多了一种原料选择(Scheme 3)。
1.1.4以雄甾-5-烯-3β,17β-二醇为原料

Scheme 4
1973年,Hosoda H[8]等用雄甾-5-烯-3β,17β-二醇,利用位阻效应选择性地保护3位羟基,再用三氧化铬氧化17位羟基,之后脱保护得到DHEA。这条路线(Scheme 4)在硅试剂保护时部分17位的羟基也会被保护,降低了反应收率,也增加了硅试剂的使用,硅试剂较昂贵,三氧化铬的使用对环境污染也较大,收率64%。
1.1.5以4-AD为原料

Scheme 5
以4-AD为原料合成DHEA(Scheme 5),这工艺的开发有助于减少对传统原料薯蓣皂苷的需求,这有助于对野生资源的保护和减少对环境的污染[9]。该工艺先将三位共轭羰基乙酰化,再保护17位羰基,之后经过还原,水解得到DHEA,工艺环保且操作简单,精炼后的收率80.8%。
1.2生物法合成DHEA

Scheme 6
此条路线[10]是利用微生物发酵生产DHEA(Scheme 6),原料是植物甾醇(菜籽甾醇,菜油甾醇等),先将3位羟基保护,再利用微生物发酵脱去17位饱和支链,最后经过水解得到DHEA。生物合成具有原料来源广,反应步骤简短等优点,解决了传统化学合成路线中原料来源紧缺等问题,不过反应液成份较复杂,后处理分离繁琐。
Stephanie JW[11]等人在1958年运用生物法合成DHEA、睾酮、雌酮及雌二醇-17β硫酸酯。系统中需Mg2+和三磷酸腺苷或被还原二磷酸吡啶核苷酸增强活性。
1.3从天然产物中提取DHEA
1936年,德国专利报道,用丙酮溶除类脂和脂肪,剩余物再用稀盐酸或醋酸在50°C下水解,从孕妇尿液和血液中可以分离得到DHEA[12]。
2001年,姚菊英[13]等从薯渣中提取得到DHEA(Scheme 7)。预发酵对提高产率有明显效果,但时间需要两天,所需时间较长。该提取方法存在几个问题:成本较高,废弃物较多,DHEA含量很低,在万分之五左右。
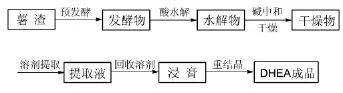
Scheme 7
2010年,Hu G[14]运用自然发酵法在山药中提取DHEA。先通过内源酶的酶解,然后加酸水解,水解物用石油醚提取,得出较佳的提取条件为料液比1:20,60℃水浴发酵48 h,然后用硫酸90℃下酸解24 h,索式提取24 h,最终DHEA收率可达5.73mg/100 g。
DHEA大都集中于动物器官,组织内,含量低,提取困难。天然产物内含有其他与DHEA结构类似的化合物,如薯蓣皂苷等,这造成了DHEA提取收率低,分离困难等问题。
2 小结
综上所述,从天然产物中提取DHEA收率较低,在提取过程中容易受薯蓣皂苷干扰,且总流程冗长,耗时较多,难以实现大规模推广使用。用生物法制备DHEA,以植物甾醇为原料,成本较低,反应路线较短,环境污染较少,但后处理较为繁琐,产物种类较多,不易分离。化学方法合成DHEA具有操作简单,后处理简单,收率高等优点,相比于其他两种具有较好的工业化前景。以4-AD替代传统工艺中的薯蓣皂苷元,有助于对野生资源的保护,且成本较低,具有较好的研究价值。
[1]马志民,刘兰服,姚海兰,等.脱氢表雄酮研究进展[J].河北农业科学,2014,18(3):60-62.
[2]Goncharov N P,Katsya G V.Neurosteroid dehydroepiandrosterone and brain function[J].Fiziologiya Cheloveka,2013,39(6):120–128.
[3]Parson,T D,Kpatz K M,Thompson E.DHEA supplementation and congnitin in postmenopausalwomen[J].Intern.J. Neuroscience,2006,116:141-155.
[4]Potter G A,Hardcastle IR,Jarman M.Aconvenient,large-scale synthesis of abiraterone aetate[3β-acetoxy-17-(3-pyrid l)androsta-5,16-diene],a potential new drug for the treatment of prostate cancer[J].Org.Prep.Proced. Int.,1997,29:123-128.
[5]Testa F,Fava L.Preparazione del△5-androsten-3β-ol-17-one acetato dal△5,16-pregnandien-3β-ol-20-on acetato[J].Gazz.Chim.Ital.,1957,87:971-975.
[6]申利群,左前进,雷福厚,等.去氢表雄酮的合成:CN,102212099A[P].2011-10-12.
[7]Everett S,Wallis E F.The preparation of dehydroan-drosterone from cholesterol[J].J.Amer.Chem.Soc.,1935,57: 1504-1506.
[8]Hosda H,David K,Fukushima F J.Convenient,high yield conversion of androst-5ene-3β-17β-diol to dehydroisoandrosterone[J].J.Org.Chem.,1973,38(24):4209-4211.
[9]刘喜荣,蒋青锋.去氢表雄酮的制备方法:CN,102603841A[P].2012-7-25.
[10]刘喜荣,孟浩,杨坤.用微生物发酵制备去氢表雄酮的方法:CN,102816825A[P].2012-12-12.
[11]Stephanie JW,Thomas E G,Russell A P.The biological actions of dehydroepiandrosterone involvesmultiple receptors[J].Drug.Metab.Rev.,2006,38:89-116.
[12]秦学孔,李楠.天然植物性激素DHEA的研究进展[J].中草药,2000,31(11):871-873.
[13]姚菊英,彭辉.红薯中DHEA的提取[J].江西教育学院学报(自然科学),2001,22(6):39-40.
[14]Hu G,Linning R,McCallum B et al.Generation of a wheat leaf rust,Puccinia triticina,ESTdatabase from stage-specific cDNA libraries[J].MolPlantPathol,2007,8(4):451-467.
The Synthesis Development of Dehydroepiandrosterone
HE Zhi-peng,JIN Can
(College of Pharmaceutical Sciences,Zhejiang University of Technology,Hangzhou,Zhejiang 310014,China)
Dehydroepiandrosterone(DHEA)plays an important regulation role in life metabolic activities,it shows anti-aging,anti-neoplastic and anti-depressant activities.This article summarized several representative the syntheticmethods of DHEA and reviewed the advantages and disadvantages of thesemethods.
dehydroepiandrosterone;chemical synthesis;biosynthesis
1006-4184(2016)9-0007-03
2016-02-29
何智鹏(1991-),男,硕士研究生在读,研究方向:药物中间体合成。
金灿,E-mail:jincan@zjut.edu.cn。

