手性对映体超分子单晶的制备与手性识别
曾小清 郭 媛 杨季冬,2*
手性对映体超分子单晶的制备与手性识别
曾小清1郭 媛1杨季冬1,2*
(1.重庆三峡学院环境与化学工程学院,重庆万州 404100)(2.长江师范学院化学与化工学院,重庆涪陵 408100)
诺贝尔奖获得者Lehn等创建的超分子化学揭示了自组装和自聚集的自发过程,为探索生命体系中自然的手性匹配、手性降解和手性转化的选择性行为,以及自发的手性拆分和自聚集的手性复制的自然规律提示了明径.文章以环糊精及其衍生物为主体,讨论了手性对映体超分子包合物制备的研究进展和实践操作,且对环糊精(主体)与手性对映体分子(客体)形成包合物单晶体做了展望,并探讨了手性物质的手性识别和不对称合成以及其分离分析的实际应用.
超分子化学;手性对映体;环糊精;包合物;手性识别
1 引 言
1848年,发现酒石酸盐对映体结晶的Louis Pasteur说:“分子的旋光性也许是生命的唯一判据,因为天然有机物分子的不对称性,是至今在死的化学和活的化学之间唯一的分界线.[1-2]”他试图以这种来自生命活力的结晶体阐释生命体中的手性环境,揭示生命的起源,但那时也没有人工制备出手性对映体的单晶.然而从1987年Lehn、Pederson和Cram获得诺贝尔化学奖,到《超分子化学大全》[1]出版以来,超分子化学[3]崛起.多个分子之间通过非共价的弱相互作用结合的自组装、自聚集,形成了复杂有序且具有特定功能的超分子体系,这为人工制备手性对映体单晶开辟了道路.
自然生命环境是具有显著手性特征的生物大分子构筑起各向异性的手性环境,正是在手性均一性的主导下生命过程中的手性对映体无论是本源的或外来的都能够被自然识别.在生命组织的各相间各表面都有识别区分标识和分离对映体的向导,因此也有分别接纳手性药物或标识毒物的靶标功能,可以说手性识别正是生命过程的自发表现.本文无意深入讨论生命力学说与非生命学说有关手性起源以及影响生命进化延续的争议,但希望在超分子化学的主导下,分子间非化学键的弱相互作用(主要包括vander Waals力,氢键,电荷转移,静电相互作用,疏水相互作用等),形成了各种化学、生物过程中的高选择性的识别、变换和易位过程[4].探索生命体系中自然的手性匹配、手性降解和手性转化的选择性行为,以及自发的手性拆分和自聚集的手性复制的自然规律.
2手性对映体超分子单晶的制备
分子识别[5-7]是超分子化学研究的新兴领域,研究的热点又集中在大分子空腔主体包结小分子客体的包合物超分子[8].其中的大分子有冠醚、环糊精、大环多胺、环番、穴芳烷、杯[n]芳烃、卟啉等,其中环糊精包合物研究报道得最多,因此下面主要探讨环糊精(cyclodextrins,常简称CDs)包合物制备过程.
2.1 环糊精包合物
环糊精,常见的是α-CD、β-CD、γ-CD由6,7,8个(船式)-D-吡喃葡萄糖单元以α-1,4-苷键首尾相连形成的大环化合物,是继冠醚后超分子化学研究的第二代主体化合物.CD拥有“外亲水,内疏水”的结构,其空腔可以结合形状和大小合适的模型底物客体化合物,而这种主客体配位化合物β-CD的结构式如图1所示,即CD截锥状结构的主面(较小口面)由葡萄糖单元的6位羟基构成,具有亲水性;而另一侧,即CD截锥状结构的次面(较大口面)由葡萄糖单元的2、3位羟基构成,具有疏水性.即CD是两端开口中空的上宽下窄的圆筒状化合物,圆台顶端和空腔内部具有疏水性质,圆台低端和外缘具有亲水性,如图2所示.CD的空间结构和性质,可使其与一个或者多个受体(无机分子、有机分子和离子分子类客体)通过分子间非共价键力相互作用形成超分子包合物,并且会改变包合物的物理和化学性质.
2.2 CDs包合物分子间力分析
CD与客体分子形成包结配合物的过程是先释放CD空腔的溶剂分子,然后主体与客体形成弱键,最后客体分子脱溶剂化并且与溶剂分子重组.在溶液中,CD与客体分子形成配合物需要以下几种分子间相互作用作为驱动力.
(1)疏水作用:在水溶液中,CD的非极性空腔包结的极性水分子在能量上不相适宜,所以,能与CD的空腔几何形状、大小、性质和非极性相匹配的客体分子会自发进入CD空腔,进而取代水分子形成包合物,而形成的几何形状和体积以及与主客体形成的紧密程度会影响CD环的旋转.
(2)范德华力:由偶极相互作用和色散力两种构成的.偶极相互作用包括偶极-偶极和偶极-诱导的两种相互作用,主要是由电子因素引起的;色散力主要由客体分子空间结构因素引起的.
(3)氢键:因为CD包含很多羟基,能与电负性大的一些原子或基团形成氢键,从而使主体与客体分子间形成稳定结构.如前所述,α/β/γ-CD与其空腔内的水分子难以形成完整的氢键,次面的羟基有些可以形成完整的氢键.但这种主客体间的相互作用较弱,客体分子只有部分移动并且还保持原有的旋转自由度.
还有其它释放高能水和释放构型张力能等对CD包合物的形成也会有一定的影响,所以,CD选择性地与客体分子形成超分子体系需要各分子间力协同作用,超分子体系的组装和分子识别与其有关,并且还决定了包合物的稳定性.但主客之间的相互作用力最大取决于主客间的形状、尺寸和性质的匹配.
2.3 CDs包合物的影响因素
主客体匹配性:即分子间形状尺寸匹配性会影响形成包合物的稳定性.如α–CD、β–CD、γ–CD的空腔内径不同,其选择匹配的客体分子种类也不同;如小聚碱与小腔径的α–CD形成的包合物稳定性要大于与中腔径的β–CD的包合物稳定性,因为小聚碱分子的大小与α–CD的内腔径接近.由于客体分子的立体效应不同,主体与之形成包合物的几何形状和稳定程度会受到很大的影响.
介质:理论上形成包合物只需要主体和客体,但要使客体分子与CD溶解并且镶嵌入CD空腔内,或者增加主客体间驱动力等,就不得不引入水或其它溶剂作为助溶剂.由于疏水性的溶剂易与CD形成稳定的包合物,使主体空腔内的疏水溶剂不宜被其他客体分子驱出或取代,从而溶剂与客体分子形成一种竞争关系.因此制备包合物时,一般选择强亲水性的溶剂,如水、甲醇或2-甲氧基乙醇等.但有时在CD溶液中,为了增强溶解度较低客体分子的溶解性,需要加入少量有机溶剂或者是纯有机溶剂.
分子间作用力:CD包合物分子间的力包括范德华力、氢键、释放高能水、释放构型张力能,但都比较弱.一般主客体间作用力越大,越易形成包合物,其作用力是上述几种分子间作用力的总和.
电荷及极性:如果主体分子与客体分子所带电荷相反,那么它们形成的包合物会更加稳定.CD分子的空腔是疏水性的,所以包合物的形成依赖于客体分子的极性,极性小、疏水性大的离子化客体分子容易与CD包合.
其它外界条件:pH值、温度、防腐剂、表面活性剂以及渗透压调节剂都在一定程度上影响客体分子的包结率.如在pH = 9左右时,对硝基苯酚与CD的配位作用最大,很可能是因为对硝基苯酚在酸性和碱性条件下存在可逆平衡;在强碱溶剂中CD的羟基脱去质子或者空腔的疏水性遭到破坏,所以包结客体分子的配位能力减小,客体分子在碱性条件下可以发生解离.溶液的酸碱性会影响主体与客体分子间配位能力,影响了包合物的稳定性.同样,其他外界条件也会影响包合物的稳定性.
2.4 CDs包合物的制备
CD与客体分子形成包结配合物,是CD空腔溶剂的释放、客体分子的脱溶剂、主客体分子间非共价键的形成及重新组装的协作过程.制备CD包合物的方法较多,主要有溶液法、固相法及一些特殊方法.其中溶液法包括共沉淀法、悬浮液法等.共沉淀法[9-10]又称为重结晶或饱和水溶液法,是常用的方法.
共沉淀法:先称取适量的CD,溶解在温水中使其达到饱和,之后再向其饱和溶液加入客体分子进行包合,并用磁力搅拌器或电动搅拌器不断搅拌,最后静止冷却并完全析出晶体后进行过滤、洗涤和干燥就可得到CD包合物,而这种包合物是不溶物.
悬浮液法:当客体分子没有合适的溶剂时,可以先配置50%的CD细悬浮液,然后将客体分子直接加入其中,不断搅拌几小时,对于密度大的油状物甚至会搅拌几天,使其充分包结.李柱等[11]在β–CD制备微胶囊化甜橙油的研究中采取悬浊液法制备包合物,其产品产率达到60.3%.在水溶液环境中,还有喷雾干燥法、渗透法、气液界面法以及冷冻干燥法等.
固相法:包括共研磨法、密闭容器内加热法、室温摇动法和胶体磨法等;对于固相法制备CD包合物,共研磨法[12-14]是最常用的.共研磨法是将结晶CD分子与结晶客体或液态客体分子在室温下机械混合,相对湿度一般在60%~70%下充分研磨,形成糊状后强力再研磨数小时,最后使糊状物干燥并用合适的洗涤剂洗涤脱落.使用这种包结技术方法简单,但CD的含湿量很重要,且只适合于水溶性较大的包结络合物的制备.M. Spulber等[15]和袁曦等[4]运用这种方法将硫康唑和氯化血红素分别包结入CD空腔内.在食品和医药方面也常会采用这种包合技术,比如香精或益妇灵胶囊中挥发油等的包合[12-14],其产率高于97%.对升华性客体分子常采用密闭容器内加热法[16],也就是在微量水存在条件下将CD与客体分子置于密闭容器内进行加热的方法,客体分子可以是芳香酸类化合物,其条件是必须存在微量水,因为在完全干燥的条件下CD不能得到包结络合物,且一般加热温度为43~142 ℃,加热时间为10~90 min,便获得CD包合物.还有一些其它固相法制备包结物,如室温摇动法和胶体磨法等.
还有其它的一些特殊方法包括超声波法、微波法、旋转蒸发法和超临界流体法等,这些方法操作简单,效率高,包结效果好.
3 β-CD包合物单晶体
诺贝尔获得者Lehn曾说:“分子识别、转换和运输是超分子物种的基本功能”[3],这表明超分子对分子识别起着核心作用[17].就如生命体中抗原和抗体、激素和受体、免疫抑制剂和免疫亲体间的作用.分子识别指受体(如CD主体)对底物(如氨基酸客体)的选择性键合并表达出特定功能的过程.CD及其衍生物是一类重要的超分子主体,具有不同大小的疏水空腔和亲水外缘的手性微环境,可以在溶液中或固体中选择性地键合各种有机、无机、惰性气体以及生物等分子而形成主—客体或者超分子配合物.包合就是主体化合物与客体化合物通过分子间非共价键相互作用,完成彼此识别的过程,使客体分子部分或全部进入主体内部的现象[14].因为微环境的变化,客体被包结后,客体分子的物理、化学、生物性质发生了显著的改变,譬如:溶解性[15]、稳定性、扩散性、化学性、光和电化学性、紫外可见、荧光和核磁等.作用是相互的,客体的结构和性能特点也会影响包合物的结构和性能.
3.1 β–CD包合物对映体单晶体
3.1.1 手性对映体小分子
氨基酸是构成蛋白质的基本单元,被广泛用于医药等方面.大多数氨基酸都具有手性,D-/L-氨基酸对映体的生理活性截然不同,组成蛋白质的氨基酸大多都是L型α-氨基酸;蛋白质氨基酸(参与蛋白质合成的氨基酸)可转换为非蛋白氨基酸,有些是β、γ、δ-氨基酸,有些是D-氨基酸.但近年研究发现,在人和动物体内存在着多种由细胞直接合成的D-氨基酸,在生物体内起着重要的生理作用.
不同类型D-氨基酸在体内转化的程度有所不同,如果摄入过多就会引起D-氨基酸中毒,甚至会危及生命.如治疗帕金森病时,当左旋多巴胺中的D-多巴胺成分含量较多时,病人服用后可能会产生副作用甚至造成生命危险;而右旋甲状腺氨基酸可降低血脂,使用时必须达到光学纯以防对甲状腺产生副作用;在医学方面,如D-氨基酸类抗生素很难被细菌降解,不会产生抗药性,为抗生素的利用提供广阔的前景.因此,在生命的起源、发育、病变和衰老中,研究氨基酸的拆分和检测很有意义,本文用诱导结晶法将外消旋体中手性氨基酸中的一种对映体进行分离研究.
3.1.2 研发环糊精-色氨酸对映体超分子包合物单晶
我们在考察环糊精与D-/L-色氨酸(Trp)反应体系的分子光谱时,发现其D-色氨酸和L-色氨酸分别与环糊精(CD)形成的超分子包合物的吸收光谱、荧光光谱和共振瑞利散射光谱均有明显差异.于是我们推测CD-D-Trp和CD-L-Trp在形成包合物的空间结构上有差异,如图3所示.
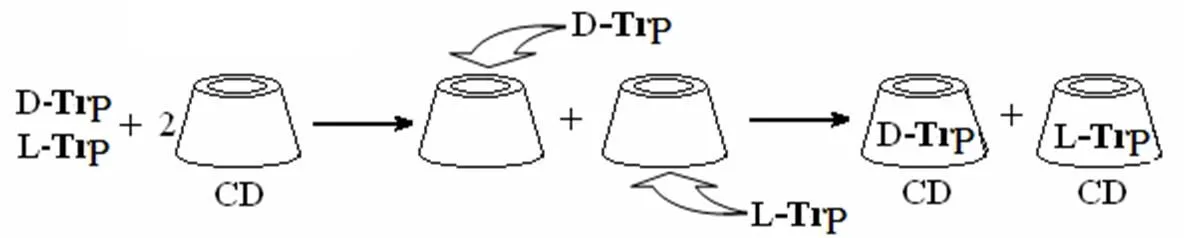
图3 CD-D-Trp和CD-L-Trp反应机理示意
于是我们试验制备β-CD-D-Trp和β-CD-L-Trp的超分子包合物单晶,如能制作出有明显参数差异的单晶,则可证明我们的推测机理是正确的.经文献查阅,对于超分子包合物单晶,由于它的晶格不对等,且环糊精个体的七糖环相对独立,缺乏有效的键合力,导致我们的制备总是失败,但目前我们用多次重结晶提纯环糊精并以色氨酸为客体分子入手,用自创的扩散+挥发溶剂法制作成功.制作步骤是以β-CD分别与D-Trp和L-Trp等量混合,混合后39 ℃恒温36小时,再冷却静置在小安碚瓶里,然后外面套上盛有不良溶剂(环已烷)的大烧杯,密封静置在低温状态下,第9天后分别生长出两种大小和数量不同的晶体,肉眼能清晰地辨别,如图4和图5.用TEM显示证实L-Trp+β-CD的晶形与D-Trp+β-CD迥然不同.现正准备进一步送检求证,与此同时,申报β-CD-D-Trp和β-CD-L-Trp的超分子包合物单晶制备方法专利已在受理审查中.
4 手性对映体超分子单晶的应用
手性在自然界中普遍存在,在生命体系中的生物大分子多数仅以一种对映形态存在,并与手性环境、医学、生物、食品和化妆品密切相关[18].立体异构体的构型不同表达出的作用也不同,如在医药上,D型对映体药物与L型对映体药物参与反应所表现的作用效果不同——拮抗作用、协同作用、竞争作用、副作用等,可能与生命体本身的手性有关,比如生命体内的手性氨基酸具有自我识别能力.如早期我们所熟知的“欧洲悲剧”——用于减轻孕妇早期妊娠反应的镇静剂和止吐药“反应停”,很多服用过此药的孕妇产下畸形婴儿.经研究,在动物体中其外消旋中的(R)-异构体分子才具有有效作用,(S)-异构体分子能致畸.又如D型对映体的氯霉素具有杀菌药效,而L型对映体却完全没有;(-)-尼古丁对人体的毒性要比(+)-尼古丁大很多;在化疗中(S)-普萘洛尔作β-受体阻断药,比(R)-普萘洛尔活性高;苯丙氨酸氮芥(L-溶肉瘤素)可被细胞摄取,D-溶肉瘤素则不被摄取.1995年,Shinkai等很早研究超分子组装进行手性识别,他们用LB膜实现了手性分子的识别[19].超分子主体化合物与客体化合物进行包合的过程一般与电子得失无关,而与客体化合物间的非共价键的缔合作用有关,当主体与客体分子形成超分子或者超分子体系后可能会产生光电效应或发生化学变化.
CD拥有“外亲水,内疏水”的结构,其空腔可以结合合适形状和大小的模型底物客体化合物,这种主—客体配位化合物的化学反应性能以及光、电、磁等物理性能在特定条件下可能会发生改变.与不同形态的手性氨基酸包合形成的不对称化合物晶体,可以有效识别和分离手性化合物.研究单晶形成的过程和机理,可改善合成不同形态的手性对映体单晶的新技术,并建立手性识别的新方法,将对环境治理手性污染物(自然溢出的天然手性污染物、滥用扩散的手性药物、残留的手性农药等)具有重要意义.研究手性氨基酸与CD的包合物单晶的结构,对理解CD类大分子形成超分子包结物机制很重要,可以通过核磁共振、荧光光谱、紫外吸收光谱、红外吸收光谱、差热分析和色谱等方法来表征包合物晶体的组成结构和形成机理.但是,培养CD包结物非常困难,加上包结物单晶极不稳定,在空气中极易失水风化,增大了晶体结构数据测定的难度,因此,国内对CD包合物晶体结构数据的报道很少,对CD包结成的不对称化合物更少.所以,培养和解析CD包结手性分子的超分子化合物并总结出形成超分子包合物的规律,对国内外科学家提供有力的数据显得尤为重要.
5 CD-手性氨基酸包结物的展望
手性物质的分离和识别一直是药学、化学、生物、食品和环境等众多领域中重要的研究课题,随着对单一手性化合物需求的日益增加,手性化合物的分离识别已成为重大的科学任务和挑战之一,而寻求简单、快速、准确以及高效手性分离和灵敏手性识别的方法是分离分析的重中之重.目前常用的分离分析手性对映体的技术手段主要包括色谱法、光谱法以及电化学方法.利用手性对映体为客体与CD或其衍生物主体形成超分子包合物,再缔合生成两种不同形态、具有显著的物化差异的对映体包合物单晶为手性识别提供了新的方向.研究手性氨基酸形成手性超分子体系的反应机制和过程,探索形成手性超分子包合物单晶的特征、稳定条件和优化条件,进而探索手性对映体超分子包合物单晶形成的过程和机理,确立合成制备手性对映体超分子包合物单晶新技术,建立同时制备外消旋手性对映体超分子包合物单晶的新方法,将对环境治理手性污染物提供新的途径.
[1] Perez-Garcia L, Amabilino D B. Spontaneous resolution under supramolecular control. Chem. Soc. Rev., 2002, 31(6): 342.
[2] María Asensio-Ramos, Javier Hernández-Borge, Teresa M. Borges-Miquel, et al. Ionic liquid-dispersive Liquid-liquid microextraction for the simultaneous determination of pesticides and metabolites in soils using high-performance liquid chromatography and fluorescence detection[J]. Journal of Chromatography A., 2011, 1218: 4808-4816.
[3] Lehn J M, Atwood J L, Davies L E, et al. Comprehensive Supramolecular Chemistry[M]. New York: Pergamon, 1996.
[4] Harada A, LI J, Kamachi M, et al. The molecular necklace: a rotaxane containing many threaded α-cyclodextrins [J]. Nature, 1992, 356: 325 - 327.
[5] Lehn J M. Perspectives in Supramolecular Chemistry-From Molecular Recognition towards Molecular Information Processing and Self-Organization [J]. Angew. Chem. Int. Ed Engl., 1990, 29: 1304-1319.
[6] 杨季冬,杨琼,周尚.共振瑞利散射光谱法同时测定手性对映体的研究进展[J].重庆三峡学院学报,2012,28(3):90-94.
[7] 杨季冬,谭选平,杨琼,等.研发光散射探针拓展光谱手性识别的研究进展[J].食品安全质量检测学报,2014, 5(10):3064-3070.
[8] Nicolas E, Russell K C, Knollenberg J, et al. Efficient method for the total asymmetric synthesis of the isomers of P-methyltyrosine [J]. J. Org. Chem., 1993, 58: 7565-7571.
[9] Ozkan Y., Atay T., Dikmen N., et al. Ement of water solubility and vitro dissolution rate of gliclazide by complexation with β-cyclodextrin[J]. Pharm. Acta. Helv., 2000, 74(5): 365-370.
[10] 王潮霞,刘丽雅,陈水林.β-CD制备香精微胶囊的机理及其应用[J].印染助剂,2003,4(20):5-7.
[11] 李柱,陈正行,罗昌荣,等.β-CD制备微胶囊化甜橙油的研究[J].香精香料化妆品,2004(6):17-21.
[12] 钱星文,雷晓林,张小红.益妇灵胶囊中挥发油β-CD包合工艺的研究[J].安徽医药,2009,13(2):141-142.
[13] 王锦玉,仝燕,马振山,等.香薷油β-CD包合物制备工艺的研究[J].中国实验方剂学杂志,2008,1(14):23-26.
[14] Gedye R, Smith F, Westaway K. The use of mierowave ovens for rapid organic synthesis [J]. Tetrahedron Lett., 1986, 27: 279-282.
[15] M. Spulber, M. Pinteala, V. Harbagiu, B. C. Simionescu. Inclusion complexes of Sulconazole with Q-cyclodextrin and hydroxypropyl, β-cyclodextrin: characterization in aqueous solution and in solid state[J]. J. lncl. Phenom. Macrocycl. Chem., 2008, 61: 41-51.
[16] 袁曦,洪清,林功舟,等.氯化血红素节β-CD包合物的研制[J].中国药学,2001,36(6):389-391.
[17] Charoenchaitrakool M, Dehghani F, Foster NR. Utilization of supercritical carbon dioxide for complex formation of ibuprofen and methyl-β-cyclodextrin [J]. Int. J. Pharm., 2002, 239(1-2): 103-112.
[18] 赵艳梅,吴环,杨季冬.环境分析中的手性识别方法展望[J].重庆三峡学院学报,2015,31(5):99-103.
[19] James T D, Kawabata H, Ludwig R, Murata K, Shinkai S. [J]. Tetrahedron, 1995,51(2) : 555-566.
(责任编辑:张新玲)
The Preparation of Chiral Enantiomers Supramolecular Single Crystal and Chiral Recognition
ZENG Xiaoqing1GUO Yuan1YANG Jidong1,2
(
Supramolecular chemistry, built by Lehn who obtained the Nobel Prize, revealed the process of self-assemble and self-aggregation. It offers a way to explore the natural chiral matching in living systems, the degradation of chiral and the selectivity behavior of chiral transform. This paper discusses the preparation and the application of chiral enantiomers supramolecular inclusion compound and cyclodextrin and its derivatives as the host. In addition, the prospect of the cyclodextrin host and the chiral enantiomers guest formed inclusion compoundl. It also leads to the discussion of practical application of chiral recognition and asymmetric synthesis of chiral separation and extraction analysis.
supramolecular chemistry; chiral enantiomers; cyclodextrin; inclusion compound; chiral recognition
O641
A
1009-8135(2016)03-0051-06
2016-01-11
曾小清(1992-),女,重庆开县人,重庆三峡学院硕士研究生,主要研究环境分析.
杨季冬(1956-),男,重庆丰都人,重庆三峡学院教授,博士生导师,主要研究分子光谱分析.
国家自然科学基金(项目编号21175015、21475014)阶段性成果

