青荚叶指纹图谱的研究
庞新莉,郭欢迎,李峰丽
(1.西安市儿童医院,西安 710083;2.陕西省食品药品检验所,西安 710065;3.北京康远制药有限公司,北京 100071)
青荚叶指纹图谱的研究
庞新莉1,郭欢迎2,李峰丽3
(1.西安市儿童医院,西安710083;2.陕西省食品药品检验所,西安710065;3.北京康远制药有限公司,北京100071)
目的 建立青荚叶的高效液相(HPLC)指纹图谱,为其制药、采收、利用及质量评价提供依据。方法以木犀草素为对照品,采用反相高效液相色谱法测定10批不同商家的青荚叶,绘制色谱图,确立参照指纹图谱,并用中药指纹图谱相似度评价系统,计算其相似度。色谱条件:色谱柱:ODS C18(250 mm×4.6 mm,5 μm);流动相:甲醇-2 mL·L-1磷酸水溶液;柱温:25 ℃;流速:1.0 mL·min-1;检测波长:350 nm;记录时间:30 min。结果共标示出青荚叶的5个特征指纹峰;各批样品相似度介于0.80~0.99之间。表明不同批次的青荚叶组成相似,但含量稍有差异。结论所建立的青荚叶HPLC指纹图谱测定方法稳定性及重复性较好,为青荚叶的应用及质量评价提供依据。
青荚叶;反相高效液相色谱法;指纹图谱
青荚叶Helwingiajaponica(Thunb)来源于山茱萸科青荚叶属,又名叶上花、叶上果等,其茎、叶、根都可入药[1]。青荚叶中含有表儿茶素、β-胡萝卜苷、棕榈酸、甘油酯、桂皮酸、木犀草素和7-O-β-D-吡喃葡萄糖苷等成分[2-3]。指纹图谱是一种顺应中药中组分多、靶点多、从“全成分”的角度出发的现代中药质量控制方法,能够全面评价中药的化学成分[4],反映中药材的质量,在中药材及制剂质量控制领域受到广泛关注[5-6]。国内外现有文献中仅对青荚叶的含量测定有报道,而对青荚叶指纹图谱研究的论文未见报道。为了能更全面地控制青荚叶的质量,本文选择木犀草素作为对照品,利用HPLC法建立了10批青荚叶药材的指纹图谱,以木犀草素为对照品特征峰,建立青荚叶的指纹图谱测定方法,为青荚叶的质量控制提供依据。
1 仪器与试药
1.1仪器Agilent 1220高效液相色谱仪(安捷伦科技公司),配置:Thermo C18柱(250 mm×4.6 mm,5 μm),手动进样器,真空在线脱气,VWD紫外检测器,恒温柱温箱;SENCOR系列旋转蒸发器(上海申生科技有限公司);SXKW数显控温电热套(北京市永光明医疗仪器厂);SHZ-D(Ⅲ)循环水式真空泵(上海予申仪器有限公司);KQ-300B型超声波清洗器(昆山市超声仪器有限公司);SQP124型电子天平(赛多利斯科学仪器有限公司)。
1.2试药甲醇、乙醚、磷酸均为分析纯;甲醇为色谱纯;娃哈哈纯净水;木犀草素对照品(上海金穗生物科技有限公司,JS90108-20mg);10批青荚叶药材分别在不同时间、不同商家购买于陕西省中药材批发市场,经鉴定为山茱萸科青荚叶。
2 方法与结果
2.1色谱条件色谱柱: Thermo C18柱(250 mm×4.6 mm,5 μm);流动相是甲醇-2 mL·L-1磷酸溶液(75∶25),等度洗脱;流速:1.0 mL·min- 1;检测波长:350 nm;柱温:25 ℃;进样量:20 μL。
2.2制备对照品溶液精密称取木犀草素对照品8.5 mg,置于25 mL量瓶中,用甲醇定容(1 mL甲醇溶液中含0.34 mg木犀草素),摇匀,用0.45 μm滤膜滤过,备用。
2.3制备青荚叶样品溶液取青荚叶,干燥粉碎后,过20目筛,精密称取3.0 g,加30 mL甲醇在80 ℃水浴中加热回流2次,每次2 h,过滤后合并滤液,采用旋转蒸发仪蒸干,残渣加50 mL水溶解,用乙醚萃取3次,每次乙醚的用量为30 mL。将3次乙醚萃取液合并后水浴蒸干[7],用甲醇溶解并定容于100 mL量瓶中,即为供试品溶液。
2.4方法学考察
2.4.1线性关系考察分别精密吸取2.2项下对照品溶液1.0,5.0,10.0,15.0和20.0 μL,按照2.1项下色谱条件进样测定,以峰面积值(Y)对木犀草素进样量 (X)进行线性回归,得回归方程Y=1 975.6X-2 211.6(r=0.999 8)。结果表明,木犀草素进样量在0.34~6.8 μg范围内线性关系良好。
2.4.2木犀草素含量测定按照2.1项下色谱条件对10个批次的青荚叶样品进行含量测定,并根据回归方程计算出木犀草素在青荚叶样品中的含量,结果S1~S10中木犀草素的含量分别为0.15%,0.12%,0.13%,0.14%,0.13%,0.15%,0.14%,0.12%,0.14%和0.14%。2.4.3精密度实验称取青荚叶药材粉末(S1),按照2.3项下方法制备青荚叶样品溶液,在同一天连续进样5次,测出各共有峰的相对保留时间和保留峰面积,计算出RSD值分别为1.0%~2.4%和0.82%~2.7%。RSD值均小于5%,达到指纹图谱对色谱条件的技术要求。2.4.4稳定性实验称取青荚叶药材粉末(S1),按照2.3项下方法制备青荚叶样品溶液,分别在0,4,8,12,16,20和24 h进行取样检测,测出各共有峰的相对保留时间和保留峰面积,计算出RSD值分别为1.1%~1.9%和1.3%~2.7%。RSD值均小于5%,表明青荚叶样品溶液在24 h内稳定,达到指纹图谱对色谱条件的技术要求。
2.4.5重复性实验称取青荚叶药材粉末(S1), 按照2.3项下方法制备青荚叶样品溶液,进行取样检测,测出各共有峰相对保留时间和保留峰面积的RSD值分别为0.8%~1.6%和1.3%~2.8%,表明此方法重复性良好,符合指纹图谱对色谱条件的技术要求。
2.4.6加样回收率实验称取已知含量的青荚叶粉末6份(S1),加入1 mL对照品溶液,按照2.3项下方法制备青荚叶样品溶液后按照选定的色谱条件进行测定。测出木犀草素的加样回收率范围为99.85%~100.5%, RSD值为0.10%,结果见表1。
表1木犀草素加样回收率实验
Tab.1 The results of luteolin recovery test

样品号取样量/mL供试品含量/μg加入量/μg测得总含量/μg回收率/%平均回收率/%RSD/%10.517.04340357.24100.1099.950.1020.517.04340357.13100.0030.517.04340357.0099.9940.517.04340356.8799.9550.517.04340356.4599.8360.517.04340356.5699.85
2.5青荚叶指纹图谱分析与评价
2.5.1青荚叶指纹图谱分析方法的建立及共有峰的标定取青荚叶药材粉末,按照2.3项下方法制备青荚叶样品溶液,将木犀草素对照品和10个青荚叶样品溶液按照选定的色谱条件分别进样测定分析,得到青荚叶样品对照HPLC色谱图,见图1A[8]。经木犀草素对照品定性,鉴定出2号色谱峰为木犀草素,见图1B。2.5.2木犀草素对照图谱利用中药色谱指纹图谱相似度评价系统 (2004 版A)对不同的10批青荚叶药材中木犀草素HPLC图谱进行处理,选择青荚叶色谱图中的5个共有峰作为校正点,建立青荚叶药材的对照指纹图谱,见图2。由图1B可知,木犀草素的色谱峰出峰时无拖尾,分离度较好,峰面积值所占比例较大且出峰保留时间相对稳定,因此选择木犀草素色谱峰为参照峰,计算出各共有峰的相对保留时间和相对峰面积值,结果见表2~3。
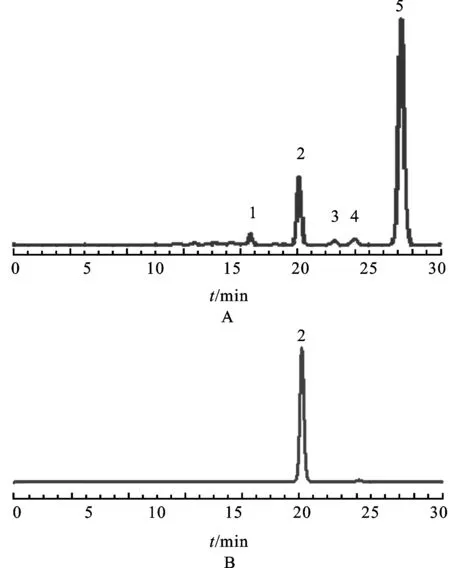
图1HPLC图
A.10 批青荚叶样品;B.木犀草素对照品;2.木犀草素
Fig.1 HPLC chromatograms
A.10 batchesHelwingiajaponicasamples;B.reference substances;2.luteolin
表210批青荚叶药材指纹图谱共有峰的相对保留时间
Tab.2 The 10 batches ofHelwingiajaponicafingerprint of the relative retention time of common peaks
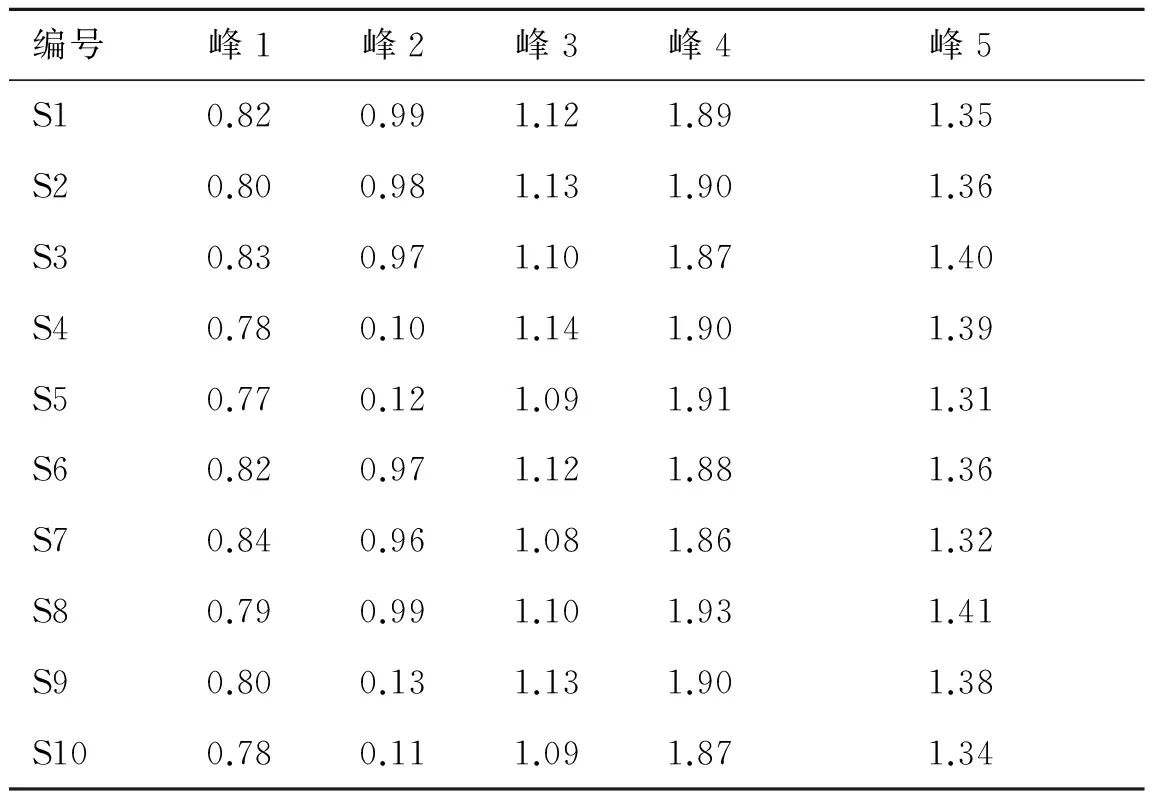
编号峰1峰2峰3峰4峰5S10.820.991.121.891.35S20.800.981.131.901.36S30.830.971.101.871.40S40.780.101.141.901.39S50.770.121.091.911.31S60.820.971.121.881.36S70.840.961.081.861.32S80.790.991.101.931.41S90.800.131.131.901.38S100.780.111.091.871.34
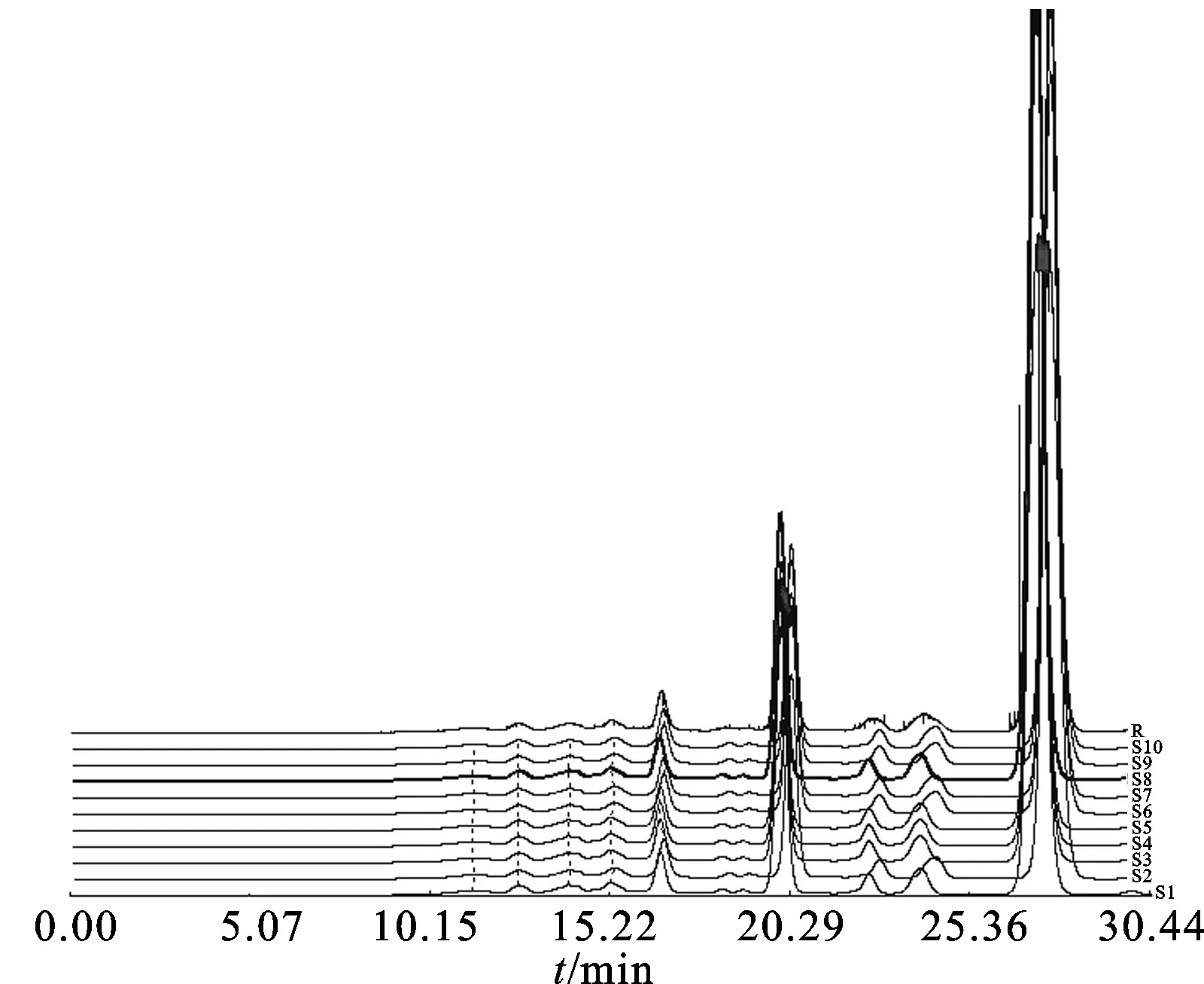
图210批青荚叶药材对照指纹图谱共有模式
Fig.2 10 batchesHelwingiajaponicaherbs fingerprints of the control model
2.5.31青荚叶指纹图谱相似度评价采用中药色谱指纹图谱相似度评价系统(2004版A),使用中位数
法对所得的10批青荚叶药材的HPLC 指纹图谱全谱进行相似度计算。结果显示,10批青荚叶药材的HPLC指纹图谱与对照指纹图谱相比,相似度分别为:0.922,0.943,0.997,0.978,0.957,0.962,0.947,0.982,0.963和0.919。充分证明,10批青荚叶药材与对照峰R的相似度较大,差异不显著,因此所选择的5个共有峰可以作为青荚叶药材指纹图谱的特征峰进行青荚叶药材的鉴别,相似度结果见表4。
表310批青荚叶药材指纹图谱共有峰的相对峰面积
Tab.3 The 10 batches ofHelwingiajaponicafingerprints of common peaks
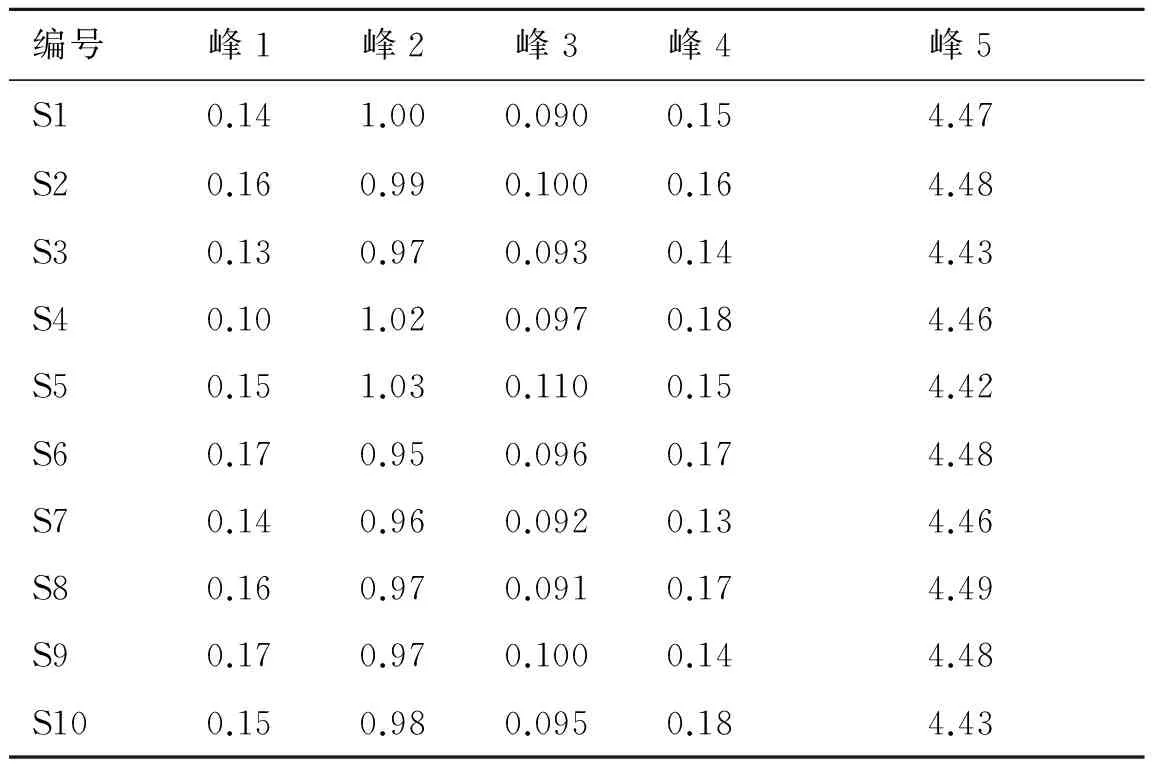
编号峰1峰2峰3峰4峰5S10.141.000.0900.154.47S20.160.990.1000.164.48S30.130.970.0930.144.43S40.101.020.0970.184.46S50.151.030.1100.154.42S60.170.950.0960.174.48S70.140.960.0920.134.46S80.160.970.0910.174.49S90.170.970.1000.144.48S100.150.980.0950.184.43
3 结论与讨论
3.1流动相的选择本实验曾采用甲醇-2 mL·L-1磷酸水溶液,以比例58∶42,60∶40和65∶35作为流动相,流速为1.0 mL·min-1,但由于样品未能很好地分离且峰形有前沿现象。最后采用甲醇-2 mL·L-1磷酸水溶液(75∶25)为流动相,木犀草素出峰保留时间适中(20 min),峰形较为理想,分离度好。
表4青荚叶药材相似度结果
Tab.4 The similarity results ofHelwingiajaponicaherbs
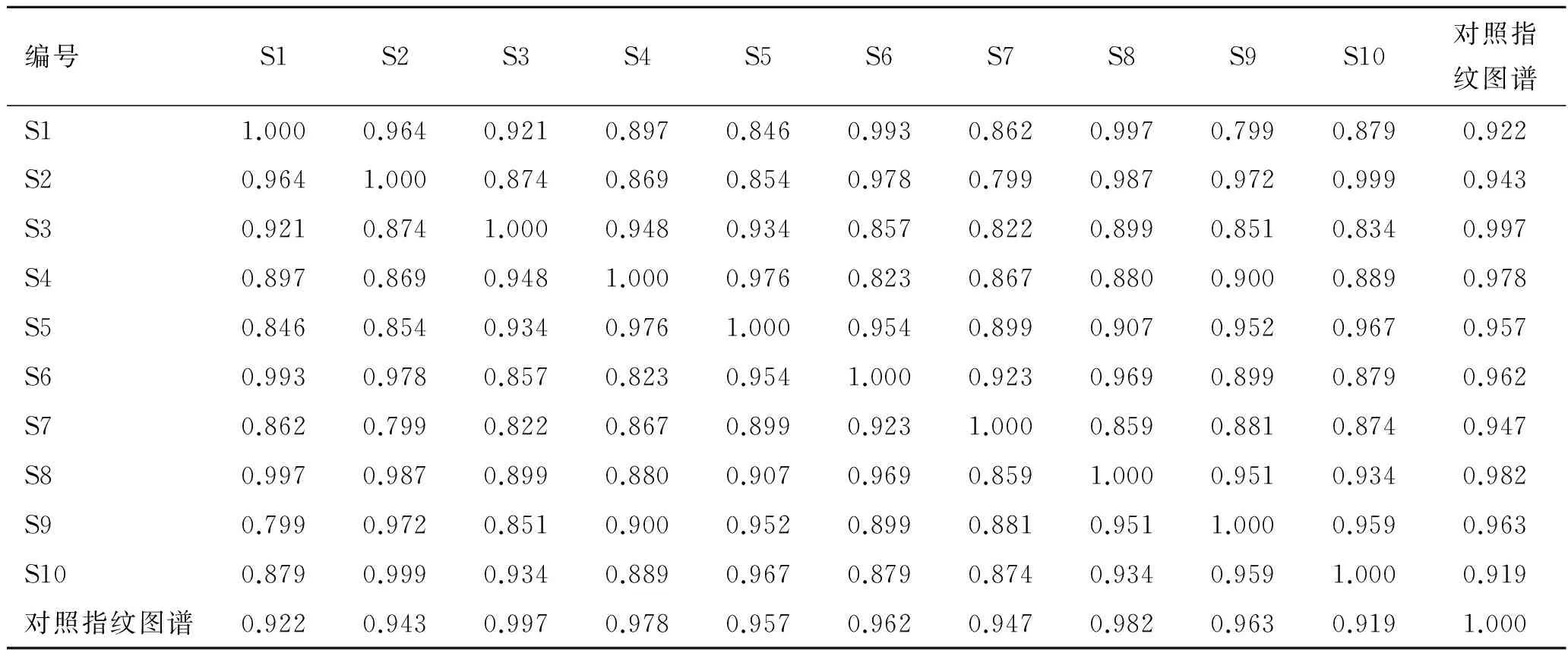
编号S1S2S3S4S5S6S7S8S9S10对照指纹图谱S11.0000.9640.9210.8970.8460.9930.8620.9970.7990.8790.922S20.9641.0000.8740.8690.8540.9780.7990.9870.9720.9990.943S30.9210.8741.0000.9480.9340.8570.8220.8990.8510.8340.997S40.8970.8690.9481.0000.9760.8230.8670.8800.9000.8890.978S50.8460.8540.9340.9761.0000.9540.8990.9070.9520.9670.957S60.9930.9780.8570.8230.9541.0000.9230.9690.8990.8790.962S70.8620.7990.8220.8670.8990.9231.0000.8590.8810.8740.947S80.9970.9870.8990.8800.9070.9690.8591.0000.9510.9340.982S90.7990.9720.8510.9000.9520.8990.8810.9511.0000.9590.963S100.8790.9990.9340.8890.9670.8790.8740.9340.9591.0000.919对照指纹图谱0.9220.9430.9970.9780.9570.9620.9470.9820.9630.9191.000
3.2样品前处理优化本实验供试品前处理方法采用甲醇加热回流2次,合并滤液,最后定容至100 mL量瓶中,作为储备液备用。但在进行HPLC分析时,发现供试品进样后出峰效果不好,分离度差,所需的主峰有拖尾现象,最后采用乙醚对供试品精制萃取3次后,发现供试品出峰效果好,分离度高,所需主峰峰形完整。
3.3青荚叶药材指纹图谱评价本实验对10批青荚叶药材进行了HPLC色谱分析,选择了稳定性较好、紫外吸收较强的5个色谱峰作为共有峰。结果显示,10批青荚叶药材相似度数值均大于0.919,证明这10批药材的液相图谱差异不显著,因此所选择的5个共有峰可以作为青荚叶药材指纹图谱的特征峰进行青荚叶药材的鉴别。
[1]李双妹.青荚叶多糖的提取及含量测定[J].温州职业技术学院学报,2010,10(2):49-52.
[2]杨小录,王瀚.中国青荚叶属植物资源及其开发利用[J].甘肃高师学报,2010,15(5):28-30.
[3]杨娟,娄方明,牛煜坤.中华青荚叶化学成分研究[J].中国中药杂志,2007,32(14):1416-1418.
[4]崔誉文,杨黎彬,杨静,等.黄翘HPLC指纹图谱研究[J].西北药学杂志,2014,29(5):446-449.
[5]孔祥玲,张曜武,王超.中药色谱指纹图谱研究的回顾与展望[J].西北药学杂志,2010,25(1):74-76.
[6]刘文,蒋世云.中药指纹图谱研究与应用进展[J].中国药房,2011,22(19):1819-1822.
[7]陈志红,徐美奕,龚先玲.紫荆花黄酮类化合物的HPLC指纹图谱研究[J].中国药房,2010,21(31):2927-2928.
[8]朱婕,洪俊丽,秦民坚.紫花地丁HPLC指纹图谱研究[J].中国野生植物资源,2011,30(4):46-49.
HPLC fingerprint of Helwingia japonica
PANG Xinli1,GUO Huanying2,LI Fengli3
(1.Children′s Hospital of Xi′an,Xi′an 710083,China;2.Shaanxi Provincial Institute for Food and Drug Control,Xi′an 710065,China;3.Beijing Kangyuan Pharmaceutical Limited Company,Beijing 100071,China)
Objective To establish HPLC fingerprint ofHelwingiajaponicaand to provide a reference for harvest,application and quality evaluation ofHelwingiajaponica.Methods RP-HPLC method was used to determine the content of 10 batchesHelwingiajaponicafrom different habitats with rutin and quercetin as control.The similarity was calculated using fingerprint similarity evaluation system.The separation was performed on a Hypersil ODS C18(250 mm×4.6 mm,5 μm) column with mobile phase consisted of methanol-2 mL·L-1phosphoric acid solution(gradient elution)at a flow rate of 1.0 mL·min-1lasting for 30 min.The UV detection wavelength was set at 350 nm and column temperature was at 25 ℃.Results The results showed that 5 peaks were recognized as common peaks.The similarity index of 10 batchesHelwingiajaponicasamples were between 0.80~0.99.The results indicated the chemical components were similar but the contents of the compounds was different.Conclusion The established HPLC fingerprint ofHelwingiajaponicais stable,reliable and reproducible,which is valuable for harvest,application and quality evaluation ofHelwingiajaponica.
Helwingiajaponica;RP-HPLC;fingerprint
国家自然科学基金项目(编号:81202492)
10.3969/j.issn.1004-2407.2016.05.002
R284
A
1004-2407(2016)05-0444-05
2016-03-10)

