氯气制备及性质实验的一体化设计
李猛 王世存
摘要:鉴于教材中氯气性质实验存在用料多、耗时长、污染大等不足,在文献梳理的基础上,结合中学化学教学实际,遵循可操作性原则,对氯气制备及性质实验进行了一体化改进设计。该一体化实验可以通过一次实验连续完成氯气制备及漂白性、酸性、氧化性、与金属反应等性质的验证。减少了试剂用量,防止了环境污染,体现了绿色化学思想、培养了学生环保意识,并为其他性质实验的改进提供了思路。
关键词:氯气制备;性质实验;一体化;实验设计;实验改进
文章编号:1005–6629(2016)8–0060–04 中图分类号:G633.8 文献标识码:B
1 问题的提出
《普通高中化学课程标准(实验)》实施建议中指出:“要鼓励教师和实验管理人员开发实验仪器,研究低成本、少污染的化学实验,同时也鼓励学生和教师设计富有特色的实验和实践活动。[1]”为此对人教版化学1(必修)第四章第二节[实验4-4]和[实验4-5] [2]进行实验改进的优化设计。
教材上的实验方法存在以下问题:
(1)氯气制备和性质实验是分开进行的,存在试剂用量大、仪器多、操作繁等不足。
(2)需要课前制备氯气并保存在广口瓶中,实验操作中氯气易逸散,污染教室内环境,危害师生身体健康,不利于培养学生的环保意识。
(3)该实验只验证了氯水的漂白性,对氯气的酸性、氧化性、与金属反应等并未涉及,而这些性质又是氯气的重要性质,不利于学生形成系统全面的知识。
针对以上问题,查阅了大量文献,发现已有不少学者对氯气的性质实验做了改进研究,取得了较多成果。
如:李海燕的“新课标下的氯气漂白性质的实验改进”[3],见图1。这是一个封闭的实验装置,能防止氯气对空气的污染,能够完成氯气制备及漂白性的验证,是对教材实验较好的改进。但是该装置并未对氯气的氧化性、酸性、与金属反应等性质作验证。
罗兵的“氯气制备及性质实验装置的组合化与微型化设计”[4],见图2。这个组合化、微型化的实验装置,一次实验就能够完成氯气制备及漂白性、酸性、氧化性、与金属反应等性质的验证,同时尾气处理装置能防止氯气对空气的污染。但是,该装置不能对氯气漂白作用的不可逆性进行验证,且所用材料仪器较多,课堂搭建装置较复杂。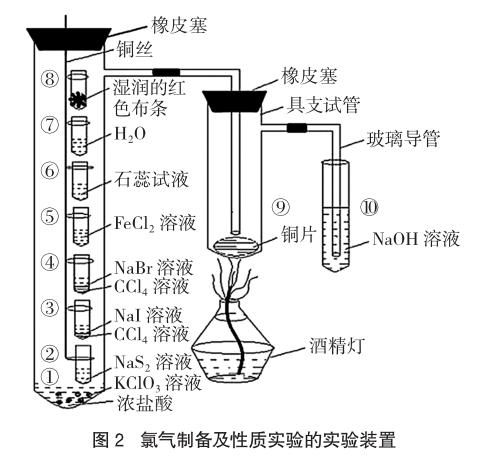
于永民的“氯气的制备及其性质实验的微量化设计”[5],见图3、图4、图5、图6。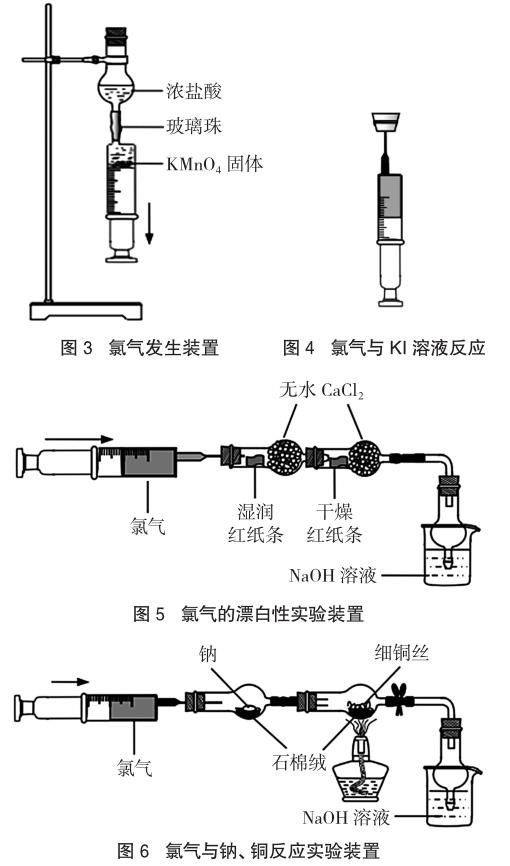
该装置利用注射器、球型干燥器巧妙地完成了氯气制备及漂白性、酸性、氧化性、与金属反应等性质的验证。但是,该装置每次只能完成氯气一个性质的验证,实验耗时长,不利于节约课堂时间,也不能对氯气漂白作用的不可逆性进行验证。
通过对文献的梳理,确保设计的实验装置能够一次完成氯气的制备及漂白性、酸性、氧化性、与金属反应等性质实验,且能够对氯气漂白性的不可逆性进行验证。采用Y型试管与长颈漏斗结合完成氯气的制取;采用Y型试管、硬质玻璃管和球型干燥器结合完成氯气诸多性质的验证;采用Y型试管A端褪色后,加热红色不恢复,验证氯气漂白性的不可逆性,为后面学习二氧化硫使品红溶液褪色的不同反应机理做铺垫;采用倒置的普通漏斗与烧杯结合组成氯气的尾气处理装置,确保尾气的吸收,防止空气污染,体现了绿色化学的思想。
根据以上设计思路,结合中学化学教学实际,设计了氯气制备及性质实验一体化的实验装置。该装置的使用能够连续完成氯气制备及漂白性、酸性、氧化性、与金属反应等性质以及对氯气漂白作用的不可逆性的验证。实验过程中试剂用量少、防止环境污染、现象较明显,充分体现了绿色化学的理念,突出了化学学科特征,发挥了实验的教育功能。
2 实验部分
2.1 实验原理
实验室通常采用浓盐酸和二氧化锰在加热的条件下制取氯气。浓盐酸在加热的条件下,容易挥发出HCl气体,对氯气性质验证造成干扰。KClO3与稀盐酸几乎不反应或反应很慢,与浓盐酸反应也不理想且会挥发出HCl气体。KMnO4反应较快较剧烈,但不易控制反应速率,且试剂有颜色。而漂粉精片[Ca(ClO)2]反应速率较适中,且不需加热,容易获得,较低浓度的盐酸就能与漂粉精片反应,速度适中易于观察,挥发性杂质较少,适合中学化学做演示实验或学生实验。反应方程式为:
Ca(ClO)2+4HCl=CaCl2+2Cl2↑+2H2O
2.2 实验用品
仪器:铁架台(带铁夹)、分液漏斗、Y形试管、酒精灯、硬质玻璃管、球型干燥器、导管、普通漏斗、烧杯、滤纸、胶头滴管、剪刀、止水夹、镊子、木块、石棉绒
药品:漂粉精片[Ca(ClO)2]、2 mol/L盐酸、紫色石蕊试液、品红溶液、淀粉碘化钾溶液、NaOH溶液
2.3 实验装置
实验装置见图7。
2.4 实验步骤与现象
(1)铁架台连接Y形试管,如图7搭建实验装置,检查装置气密性,在A端加入约2mL品红溶液,在B端加入约2g漂粉精片,在分液漏斗中加入适量的2 mol/L盐酸。
(2)在硬质玻璃管上取等距的C、D、E三点。对应地用剪刀把滤纸剪成大小相同的三张滤纸片C、D、E,用胶头滴管滴加石蕊试液于C、D上,其中C烘干备用。滴加淀粉碘化钾溶液于E上浸湿备用。
(3)用镊子夹取制备好的滤纸片C、D、E放在对应的硬质玻璃管的C、D、E三点。球型干燥器F处石棉绒上加入约0.1g金属钠。连接装有氢氧化钠溶液的尾气处理装置。
(4)打开止水夹和分液漏斗的上口塞和玻璃活塞,向B端加入适量的2 mol/L盐酸。待黄绿色气体充满整个装置,观察到A端品红溶液褪色,C点滤纸无明显变化,D点滤纸先变红后褪色,E点滤纸由白色变蓝色,蓝色变浅直至褪色,金属钠与氯气很容易反应,可观察到金属钠自动燃烧(可微热),发出黄色火焰,并产生白色固体。
(5)加热Y形试管A端,褪色的品红溶液不能恢复成红色。
2.5 实验结论
(1)硬质玻璃管C、D处滤纸颜色的变化和Y形试管A端品红溶液褪色,证明氯气本身没有漂白性,氯水有漂白性;加热Y形试管A端,褪色的品红溶液不能恢复成红色,证明氯水漂白性的不可逆性。
一体化:通常能在6~8分钟内一次完成氯气制备及漂白性、酸性、氧化性、与金属反应等性质以及对氯气漂白作用的不可逆性进行验证。
防污染:采用倒置的普通漏斗能充分吸收尾气,防止污染环境,保护师生身体健康,培养学生环保意识。
节约性:该设计用试液浸湿的滤纸片与传统实验相比,既减少了试液的用量,又减少了氯气的需要量,从而节约了漂粉精片[Ca(ClO)2]和盐酸的用量。
灵活性:硬质玻璃管中C、D、E的滤纸可以换成pH试纸、滴有KSCN的新制FeCl2溶液、Na2S溶液、NaBr溶液等。球型干燥器F处可换成铜丝、铁丝,底部垫上石棉绒,可验证氯气的诸多性质。
普适性:该装置稍加改装可完成SO2等气体的制取和诸多性质的验证。例如把漂粉精片(次氯酸钙)和盐酸换成亚硫酸钠粉末和硫酸,可完成SO2气体制备及其漂白性、氧化性、酸性、还原性等性质的验证。
3 实验说明
(1)分液漏斗下端应紧贴Y形试管B端的试管壁,防止盐酸滴入品红溶液中。可在C点前安装装有CaCl2球型干燥器,吸收少量的水蒸气,排除干扰。
(2)待品红溶液褪色后,再用酒精灯加热A端,且品红溶液加入量不要过多,防止褪色现象不明显。
(3)在与金属反应时,将金属切成金属片或金属丝,有利于反应的进行,现象较明显。同时从安全性角度考虑,金属钠用量要控制在0.1g以内,且在金属下面垫上石棉绒。
(4)尾气处理的NaOH溶液浓度不宜过稀。实验结束后加热装置或在B端加入稍过量的锌粒,把剩余氯气排到尾气处理装置中,保证剩余的氯气被吸收,防止污染环境,保护师生身体健康。
参考文献:
[1]中华人民共和国教育部制定.普通高中化学课程标准(实验)[S].北京:人民教育出版社,2013:41.
[2]宋心琦.普通高中课程标准实验教科书·化学1(必修)(第3版)[M].北京:人民教育出版社,2012:84.
[3]李海燕.新课标下的氯气漂白性质的实验改进[J].化学教育,2009,(10):68.
[4]罗兵.氯气制备及性质实验装置的组合化与微型化设计[J].化学教学,2012,(5):50.
[5]于永民.氯气的制备及其性质实验的微量化设计[J].化学教学,2013,(5):40~42.

