基于脑网络分析的轻度认知障碍患者脑电变异感兴趣脑区研究
陈丹彦,段火强,刘庭伟,蒋皆恢,2,★(. 上海大学通信与信息工程学院,上海 200444;2. 上海市生物医学工程研究所,上海 200444)
基于脑网络分析的轻度认知障碍患者脑电变异感兴趣脑区研究
陈丹彦1,段火强1,刘庭伟1,蒋皆恢1,2,★
(1. 上海大学通信与信息工程学院,上海200444;2. 上海市生物医学工程研究所,上海200444)
轻度认知障碍(mild cognitive impairment, MCI) 是介于正常老年人和阿尔茨海默病(Alzheimer’s disease, AD)患者之间的一种临床状态,MCI的早期诊断对AD预防和治疗具有非常重大意义。目前,临床经常使用脑电(Electroencephalogram, EEG)技术对MCI患者进行筛查和诊断,但是缺少感兴趣脑区是医生针对MCI 的EEG信号诊断中遇到的一个临床问题。为了研究感兴趣脑区,本实验选取了18名老年人参与京剧体验任务,记录了他们在听京剧任务后闭眼状态下的脑电信号,并通过脑网络分析方法对数据进行了分析。结果表明,MCI组的网络参数与正常老年组的基本保持一致,但MCI组节点介数相较于正常老年组却发生较为明显的改变,MCI患者在任务状态下相较于正常老人在CP3和P4两个节点发生显著改变。
轻度认知障碍;脑电;脑网络分析;感兴趣脑区
0 引言
阿尔茨海默病(Alzheimer’s disease, AD)是老年人最常见的神经变性疾病之一,现已成为我国继心血管疾病、恶性肿瘤、脑卒中之后老年人的第四大疾病[1]。截至2015年,全球大约有AD患者4800万名,我国AD患者超过800万,位居世界之首[2]。AD患者多伴有失忆、认知障碍、平衡能力缺失等机能衰退,导致走失、跌倒、甚至轻微家庭暴力等,易引发一系列社会问题。由于 AD 是一种不可逆转的神经变性疾病,因此 AD 的早期诊断、干预以及防治就显得尤为重要[3]。
轻度认知障碍(mild cognitive impairment, MCI) 是介于正常老年人和AD患者之间的一种临床状态[4]。相较于AD患者,MCI患者日常能力没有受到明显影响,但患者存在轻度认知功能减退,是痴呆的高危人群。随着病情的发展,部分MCI患者将转化为AD。因此,研究轻度认知损害对AD的预防和治疗具有非常重大意义,已成为当前老年痴呆症早期诊断关注的重点[5]。
目前临床上对于MCI的研究主要包括量表筛查,脑影像技术比如结构磁共振(Magnetic Resonance Imaging, MRI),功能磁共振(functional MRI, fMRI),正电子发射型计算机断层显像(Positron Emission Computed Tomography, PET),以及脑电(Electroencephalogram, EEG)等[6-8]。其中EEG信号广泛被应用于AD及MCI患者的大脑研究中,例如,祝本菊等通过脑电非线性复杂度分析,发现认知功能障碍患者其各脑区复杂度的降低并非一致,与认知相关脑区退化较其他脑区更为明显[9]。翟静波等将脑电指标用于阿尔兹海默病的发病机制和早期预警研究,发现脑电指标与认知功能有较强的关联性,MCI患者不同脑波活动可能存在代偿机制,而且代偿时期可能不同[10]。王佳等通过探讨MCI在工作记忆时脑电图功率值改变与神经心理学特点及其相互关系,发现MCI患者颞叶与其他脑区之间存在联系障碍且这种障碍在正常衰老过程中可能已经出现[11]。
尽管目前基于EEG信号对于MCI患者大脑信号变异研究正成为热点,EEG方法也开始用来对MCI患者进行筛查和诊断,但是医生在临床应用过程中却遇到信号分析相关的问题[9],其中最常见也最函待解决的是感兴趣脑区(Region of Interest, ROI)的定位问题。由于每位患者的EEG信号具有特异性,而学界暂时没有公认的针对EEG的感兴趣脑区研究,无法针对ROIs进一步开展定量研究和客观追踪MCI患者病情发展,因此,ROIs的定位具有明显的临床意义。
脑网络分析方法是近年来神经科学领域提出的用于定位大脑ROIs的新方法,目前被广泛地应用在基于MRI、fMRI、EEG等信号的分析中。因此,本文基于EEG信号,拟应用脑网络分析方法对MCI患者大脑的感兴趣区域进行定位研究,尤其聚焦MCI患者大脑在任务状态下的感兴趣区域。与之前的文献研究相比,本文拟实现两个创新点:1.通过对比正常组(Normal, NOR)与MCI组老人EEG信号,研究任务状态下MCI患者EEG信号变异明显的ROIs;(2)应用脑网络分析方法定位任务状态下MCI患者EEG信号变异明显的ROIs。
1 材料与方法
1.1实验材料
1.1.1被试选取
参与实验的18位被试均招募自上海某社区,其年龄均超过60周岁,实验前所有被试进行了MMSE(the mini.mental state examination,MMSE)测评,满分为30分。其中27分以上及以上为正常人,低于27分即被认定为患有认知障碍。结果正常老年人组和MCI患者组各9人,且两组被试的MMSE值具有显著性统计差异(n=9,P=0.002,F=19.692)。

表1 数据来源基本信息
两组被试具体信息如表1所示。其中,正常组9人,4男5女(平均年龄62.3±2.23,3人半年前被诊断为MCI患者,6人为正常人);MCI组9人,2男7女(平均年龄68.2±7.38,7人半年前被诊断为MCI患者,2人为正常人),所有被试均无精神病史,视力正常或矫正正常。本实验通过了人类伦理委员会的审查批准。
1.1.2数据记录与预处理
本实验采用京剧体验认知任务,对于京剧的选择,本小组选择《定军山》片段来对老年被试进行刺激。用选定的京剧片段对前面所述的两组被试进行刺激。在京剧刺激前后,对两组被试进行主观性应激量表评价,无显著性统计差异。
整个实验在光线较暗、安静的封闭室内进行,被试坐在舒适的靠背椅上,心情放松。被试根据声音提示按照如下步骤进行测试:
(1)静息状态下闭上眼睛保持3分钟;
(2)要求被试专心体验一段时间长度为2分钟的京剧,此过程中不记录脑电数据;
(3)静息状态下闭上眼睛保持3分钟,并同时记录脑电数据;
(4)实验结束;
实验使用武汉格林泰克科技生产的32导电极帽,用NeuroScan公司生产的放大器采集脑电信号。电极分布采用遵循国际标准的10-20导联系统,垂直和水平眼电也被同时记录。实验过程中,电极阻抗保持在5kn以下,采样率为1000Hz。实验结束后,分别从每段数据中选取2min最佳信号,进行DC校正、去眼电、基线校正和0~lO0Hz低通滤波等离线预处理。然后,使用小波分解得到所有被试theta频段的EEG信号。
1.2构建脑网络
在本实验中,30个电极导联被作为网络中的30个节点,基于皮尔森相关的方法[12]构建了theta频段正常老年组和MCI组的脑功能连接网络。两组网络的皮尔森相关系数矩阵如下图1所示,其中横纵轴坐标代表30个导联,颜色对应于相关系数,颜色越亮代表相关性越强,越暗则代表相关性越弱。
在得到连接系数矩阵后,通过设定稀疏度(Sparsity)阈值[13]的方法来确定两个节点(即两个导联)之间是否存在连接。由于没有合适的方法确定一个单一的阈值,在本实验中,我们设定一系列阈值来将系数矩阵转化成二值矩阵,阈值范围为0.1-0.5,步长为0.01,总共41个阈值[14]。在二值矩阵中。“1”代表两个节点之间有连接,“0”代表无连接,如下图1所示。
1.3网络特征参数
为了探究MCI组和正常老年组两组网络的差异,聚类系数、特征路径长度、小世界系数、局部效率、全局效率和节点介数被选择为网络特征参数。所有的参数都是通过网上开源的工具箱GRETNA[15]和The Brain Connectivity Toolbox (BCT, http://www.nitrc.org/projects/bct/)[16]计算获取。
1.3.1聚类系数
在网络中,节点的聚类系数是指与该节点相邻的所有节点之间相互连接的比例,而网络的聚类系数则是指网络中所有节点聚类系数的平均值,它反映了网络中节点的连接聚集情况。其求解公式如下所示,其中N代表网络的节点数,ki代表节点i所连接的节点个数,E(i)代表ki个节点之间实际连接的边数[17],如公式1所示:
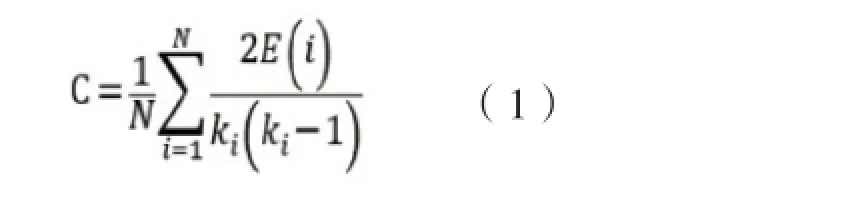
1.3.2特征路径长度
在网络中,两点之间的最短路径定义为连接两点所需要的最少边数,而网络的特征路径长度L指网络中所有节点对的最短路径的平均值,它表明网络中节点间的分离程度。其求解公式如下所示,其中N代表网络的节点数,i,j代表网络V中的节点,dij代表节点i和j之间的最短路径[18],,如公式2所示:

1.3.3Gamma,Lambda和小世界系数
通过综合聚类系数C和特征路径长度L这两个特征参数,我们可以得到另外一个小世界网络参数:小世界系数。其具体定义如下:定义一个网络的聚类系数与其相应随机网络聚类系数的比Gamma= C/Crand,特征路径长度与其相应随机网络特征路径长度的比Lambda= L/Lrand,小世界系数则定义为Sigma= Gamma/Lambda[19]。由于小世界网络本身拥有大的聚类系数和小的路径长度特性,因此若一个网络满足以下条件:Sigma>1,其中Gamma>1且Lambda ≈1,我们认为该网络是具有小世界特性的。在本实验中,考虑到每次生成的随机网络是不一样的,我们总共生成了100次相应的随机网络来计算小世界系数。
1.3.4全局效率和局部效率
在网络中,全局效率被定义为节点间最短路径的的倒数的平均值,反映了信息在网络全局中传递的效率;局部效率为子图Vi内所有节点对最短路径的平均值,代表了网络中所有子图内部信息交换的效率。其计算公式分别如下所示[20]:
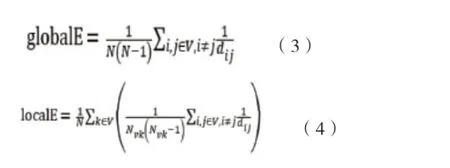
1.3.5节点介数
在网络中,节点i的节点介数Bi定义为网络中所有最短路径中经过该节点的路径数目占最短路径总数的比例。即任意选两点,若发现m条最短路径,有n条通过你关注的点的话,则记为n/m,将所有节点对计算得到的值依次相加则得到相应节点的介数。其求解公式如下所示[21]:
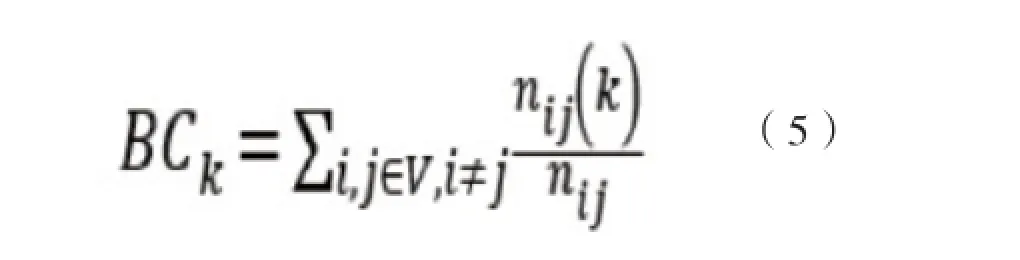
其中j,k代表网络V中的节点,nij代表节点i和j之间最短路径的数量,nij(k)代表节点i和j之间的最短路径通过节点k的数量。通常,我们把网络中所有节点的点介数平均值作为网络的介数B,并使用这一数值对点介数进行归一化计算,归一化的点介数bi=Bi/B。因此节点介数反映了相应的节点在整个网络中的作用和影响力,bi值越大的区域其节点中心行越强。
为了确定在信息传递过程中的关键脑区,需要确定一个阈值来分析网络的节点介数。根据文献,阈值确定的规则为在保证网络处于全连通的状态下的最小阈值。在本实验中,我们选取阈值为0.19。
对正常组和MCI组两组数据,我们分别计算在阈值为0.19时每个脑区的归一化节点介数bi,bi>1.5时被认为是hub节点,表明该节点在整个网络的信息传递过程中起到了关键作用。
2 结果
2.1网络参数
在本实验中,网络参数包括聚类系数、特征路径长度、全局效率、局部效率、gamma、lambda以及小世界系数均被计算用于分析网络特性的改变。图2显示了theta频段下正常老年组和MCI组两组网络的参数平均值计算结果。结果表明,无论是正常老年组还是MCI组,两组网络的sigma参数均大于1,意味着两组网络均表现出小世界特性。但相对于正常老年组,MCI组的网络参数与正常老年组的基本保持一致,没有发生明显改变。

图2 正常老年组和MCI组网络参数
2.2网络hub节点
图3以地形图的方式显示了两组网络节点介数参数计算结果,具体数值及统计结果如表2所示。结果表明,在正常老年组中,hub节点(bi>1.5)主要集中在左侧顶叶与枕叶,包括C3,CP3,CP4,T5,P3,Pz和O1电极;在MCI组中,hub节点主要集中在顶叶后半部,包括FC3, CP3, CP4,P3,Pz和P4电极。经统计表明,CP3和P4节点在MCI组发现显著改变。其中,对于CP3节点,在正常老年组其归一化后的bi值为1.98,在MCI组中为3.30,双样本t检验P值计算结果为0.03(P < 0.05);对于P4节点,在正常老年组其归一化后的bi值为1.02,在MCI组中为2.01,双样本t检验p值计算结果为0.04 (P < 0.05)。此外,在本实验中,结果表明大脑额叶区域在两组网络中没有发生显著改变。由此可见,CP3和P4节点为任务状态下MCI患者但挠变化较明显的ROIs。

图3 正常老年组(左)和MCI组(右)的节点介数地形图

表2 节点介数计算结果
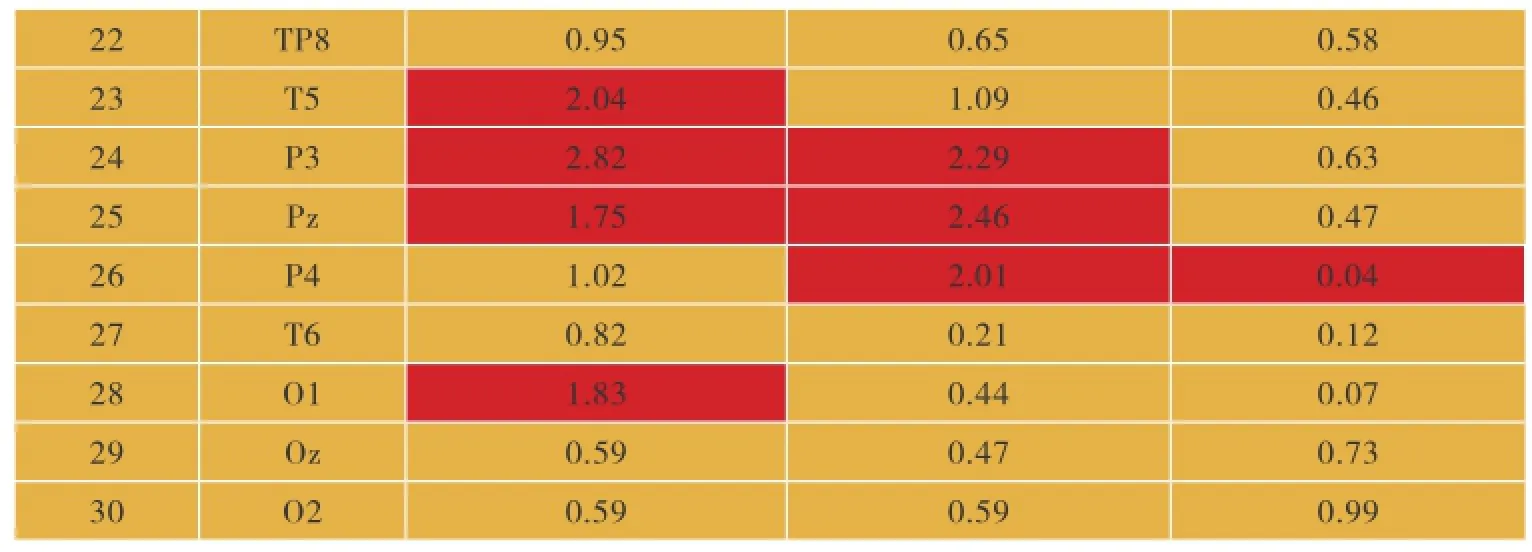
22 TP8 0.95 0.65 0.58 23 T5 2.04 1.09 0.46 24 P3 2.82 2.29 0.63 25 Pz 1.75 2.46 0.47 26 P4 1.02 2.01 0.04 27 T6 0.82 0.21 0.12 28 O1 1.83 0.44 0.07 29 Oz 0.59 0.47 0.73 30 O2 0.59 0.59 0.99
3 讨论
本文基于皮尔森相关方法分析了theta频段下正常老年组和MCI组的脑网络特性,定位了两组网络在theta频段的hub节点,最后找到MCI患者在任务状态下相较于正常老人在CP3和P4两个节点发生显著改变。
在本实验中,尽管MCI组的网络参数与正常老年组的基本保持一致,但MCI组节点介数相较于正常老年组却发生较为明显的改变。这个现象表明,基于网络分析的方法研究MCI,从网络参数比如聚类系数、路径长度、网络效率以及小世界系数的角度,或许不是一个好的选择,很多时候从上述参数中并不能发现MCI患者问题所在。相较于计算上述参数,计算节点介数从而定位网络hub节点或许是一个更优的选择。从网络参数本身特性来讲,上述现象是可以被如下解释:无论是聚类系数还是路径长度等,这些参数都是所有节点的平均结果,它们从网络整体出发而弱化了具体每个节点的差异。与之相反,节点介数基于每个节点,反映了每个节点在网络信息传输的重要程度。事实上,MCI患者也正是因为某些特定脑区的改变从而导致大脑功能受损。
在正常老年组中,7个节点被发现为hub节点,包括C3,CP3,CP4,T5,P3,Pz和O1节点;在MCI组中,FC3, CP3, CP4, P3, Pz和P4被发现为hub节点。其中CP3, CP4, P3和Pz在两组网络中均被发现为hub节点,表明这四个节点在整个网络的信息传递过程中起到了关键作用,为大脑的正常的信息处理以及脑区之间的信息交流提供了中转站。然而,双样本t检验结果表明,MCI组的CP3和P4节点与正常老年组相比发生显著改变并具有统计差异。因此,我们可以推测,这两个节点的变化或许是导致MCI患者存在认知功能减退的一个关键因素,在后续对MCI的研究中,需要对这两个节点加以关注。
尽管本文较为系统的对MCI患者theta频段EEG网络进行了分析,但仍然存在以下不足之处。第一,本文基于皮尔森相关的方法构建EEG脑网络,但事实上,构建EEG脑网络的方法并不仅此一种。偏相关、相位同步、频域相干等方法也广泛被应用于EEG网络的构建,本文并没有使用不同的构网方法对MCI患者进行网络研究。不同的方法所得到的结果或许不尽相同,这还有待进一步研究。第二,本文仅对theta频段网络进行分析,对EEG信号中其它频段的网络特性尚未完全清楚。第三,本文仅对10例正常老年人和10例MCI患者进行研究,数据样本过少,统计结果不一定有足够的说服力。在后续的研究中,增加样本进行更为深层的研究是十分有必要的。
4 结论
本文基于皮尔森相关方法构建了theta频段下正常老年组和MCI组的脑网络,较为系统的对比了两组网络的网络特征参数,分别定位了两组网络在theta频段下的hub节点,结果表明MCI患者相较于正常老人在CP3和P4两个节点发生显著改变。
5 致谢
感谢上海大学生物医学工程专业李颖洁教授学术团队提供的实验数据并在文章撰写过程中给予的支持。
[1]Chan K Y, Wang W, Wu J J, et al. Epidemiology of Alzheimer’s disease and other forms of dementia in China, 1990-2010: a systematic review and analysis [J]. The Lancet, 2013, 381(9882): 2016-2023.
[2]Thompson C A, Spilsbury K, Hall J, et al. Systematic review of information and support interventions for caregivers of people with dementia [J]. BMC geriatrics, 2007, 7(1): 18.
[3]Waldemar G, Dubois B, Emre M, et al. Recommendations for the diagnosis and management of Alzheimer’s disease and other disorders associated with dementia: EFNS guideline [J]. European Journal of Neurology, 2007, 14(1): e1-e26.
[4]Petersen R C, Smith G E, Waring S C, et al. Mild cognitive impairment: clinical characterization and outcome[J]. Archives of neurology, 1999, 56(3): 303-308.
[5]Suk H I, Shen D. Deep learning-based feature representation for AD/MCI classification[C]//International Conference on Medical Image Computing and Computer-Assisted Intervention. Springer Berlin Heidelberg, 2013: 583-590.
[6]Baker M, Akrofi K, Schiffer R, et al. EEG patterns in mild cognitive impairment (MCI) patients [J]. The open neuroimaging journal, 2008, 2(1).
[7]Risacher S L, Saykin A J, Wes J D, et al. Baseline MRI predictors of conversion from MCI to probable AD in the ADNI cohort [J]. Current Alzheimer Research, 2009, 6(4): 347-361.
[8]Mosconi L, Tsui W H, Herholz K, et al. Multicenter standardized 18F-FDG PET diagnosis of mild cognitive impairment, Alzheimer’s disease, and other dementias [J]. Journal of Nuclear Medicine, 2008, 49(3): 390-398.
[9]祝本菊. 基于复杂度分析的阿尔茨海默病、轻度认知功能障碍与正常老年人的脑电研究[D].天津医科大学,2012.
[10]翟静波. 老年轻度认知功能障碍向阿尔兹海默病转归的脑电特征研究[D].山西医科大学,2011.
[11]王佳. 轻度认知功能障碍患者在工作记忆时的脑电图功率值及相干性研究[D].浙江大学,2005.
[12]Li Y P, Qin Y, Chen X, et al. Exploring the functional brain network of Alzheimer’s disease: based on the computational experiment [J]. PloS one, 2013, 8(9): e73186.
[13]Seo E H, Lee D Y, Lee J M, et al. Whole-brain functional networks in cognitively normal, mild cognitive impairment, and Alzheimer’s disease[J]. PloS one, 2013, 8(1): e53922.
[14]He Y, Chen Z, Evans A. Structural insights into aberrant topological patterns of large-scale cortical networks in Alzheimer’s disease[J]. The Journal of neuroscience, 2008, 28(18): 4756-4766.
[15]Wang J, Wang X, Xia M, et al. GRETNA: a graph theoretical network analysis toolbox for imaging connectomics [J]. Frontiers in human neuroscience, 2015, 9.
[16]Rubinov M, Sporns O. Complex network measures of brain connectivity: uses and interpretations [J]. Neuroimage, 2010, 52(3): 1059-1069.
[17]Inoue H, Liu Y Y. Revealing the intricate effect of collaboration on innovation[J]. PloS one, 2015, 10(3): e0121973.
[18]He Y, Chen Z J, Evans A C. Small-world anatomical networks in the human brain revealed by cortical thickness from MRI[J]. Cerebral cortex, 2007, 17(10): 2407-2419.
[19]Watts D J, Strogatz S H. Collective dynamics of ‘small-world’ networks [J]. nature, 1998, 393(6684): 440-442.
[20]Achard S, Bullmore E. Efficiency and cost of economical brain functional networks [J]. PLoSComputBiol, 2007, 3(2): e17.
[21]Bullmore E, Sporns O. Complex brain networks: graph theoretical analysis of structural and functional systems [J]. Nature Reviews Neuroscience, 2009, 10(3): 186-198.
Study of Altered Brain Regions of EEG networks in Mild Cognitive Impairment
Danyan Chen1, Huoqiang Duan1, Tingwei Liu1, Jiehui Jiang1,2,*
(1. School of Communication and Information Technology, Shanghai University, Shanghai, 200444; 2. Shanghai Institute of Biomedical Engineering, Shanghai, 200444)
As a middle state between normal and Alzheimer’s disease(AD) elderly people, the early diagnosis of mild cognitive impairment(MCI) is greatly significant for AD prevention and treatment. Currently, Electroencephalogram (EEG)technology has been widely used to detect and diagnose MCI patients in clinic. However, lackingregions of interest in brains is a challenge in the analysis of EEG signals for physicians. In order to identify altered brain regions in MCI patients, this study investigated 18 subjectsby carrying Peking Opera tasks. EEG signals of each subject were recorded underthe state of eyesclosed, and brain network method was applied for EEG signal analysis. The experimental results showed that network parameters in MCI group were similar with normal group, while betweenness centrality was significantly changed in MCI group. As a result, betweenness centrality of CP3 and P4 nodes in MCI group were significantly changed compared withnormal group.
Mild cognitive impairment; EEG, Brain network; Region of interest
上海市科委生物医药专项(16441906200)、教育部回国人员科研启动基金、上海市教委青年骨干教师计划、上海市大学生创新创业训练计划项目。
蒋皆恢。

