HPLC法同时测定玉泉丸中5个成分的含量
李少光, 蔡林雪, 姚 宏, 黄丽英, 陈 冰, 林新华
HPLC法同时测定玉泉丸中5个成分的含量
李少光1, 蔡林雪2, 姚宏1, 黄丽英1, 陈冰1, 林新华1
目的建立同时测定玉泉丸中5个成分(葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸)的方法。方法采用反相高效液相色谱-二极管阵列紫外检测器(RP-HPLC-DAD),在UltimateTMXB-C18色谱柱(250×4.6 mm,5 μm)上,优化获得以乙腈(B)-水(0.2%甲酸)(A)为流动相的梯度洗脱条件;流速1.0 mL/min;检测波长为254,280和340 nm,柱温30 ℃。结果5个活性成分的分离度良好,在各自测定的浓度范围内具有良好的线性关系(r≥0.997),平均加样回收率为87.5%~104.3%。相对标准偏差≤3.3%(n=6)。结论本方法操作简便、快速,具有较好的稳定性和重复性,可为玉泉丸质量控制提供定量分析方法。
玉泉丸; 葛根素; 甘草; 异黄酮类; 甘草酸; 色谱法, 高压液相
玉泉丸,源于《仁斋直指》(宋代)、《古今医鉴》(明代)和《种福堂公选良方》(清代)的三朝名方“玉泉散”,是由葛根、天花粉、地黄、麦冬、五味子及甘草六味中药组方而成的现代制剂——浓缩丸。主治“消渴”症(胰岛功能减退的糖尿病),具有辨因求治,对证治疗的独特优势。玉泉丸属国家中药保护品种、国家医保甲类用药,但卫生部药品标准中未收载其含量测定项[1],且已有文献检测指标单一(1~2个成分)或分析耗时较长[2-4]。因此,本实验旨在建立同时测定玉泉丸中5个活性成分葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸含量的高效液相色谱方法(其中葛根素和大豆苷元为君药葛根中已报道的主要降血糖药效成分;甘草苷、异甘草苷和甘草酸归属使药甘草,也有明确的降血糖活性报道[5-8]),为玉泉丸的质量控制提供更简便、准确、高效的检测,也为其质量标准的提升提供方法学参考。
1 材料与方法
1.1仪器和试剂高效液相色谱仪(Agilent 1260型,美国安捷伦科技有限公司),配备自动进样器、柱温箱、四元低压混合泵、二极管阵列紫外检测器。色谱柱(UltimateTMXB-C18,250 × 4.6 mm,5 μm,上海月旭科技股份有限公司)。电子天平(BS124S,德国赛多利斯集团),数控超声微波清洗器(KQ-250DE型,功率250 W,频率40 KHz,昆山市超声仪器有限公司)。乙腈(美国Sigma公司)、甲酸(上海晶纯生化科技股份有限公司)、双蒸水为实验室自制,其他试剂均为分析纯。葛根素对照品(批号:MUST-14061203,北京恒元启天化工技术研究院与北京世纪奥科生物技术研究公司);甘草苷对照品(批号:0633)、异甘草苷对照品(批号:0401)和大豆苷元对照品(批号:1302)均购自北京索莱宝科技有限公司;甘草酸对照品(批号:MUST-14081812,北京恒元启天化工技术研究院与北京世纪奥科生物技术研究公司),纯度均≥98%。玉泉丸浓缩丸(成都九芝堂金鼎药业有限公司,批号121103,130103和140301)购自福建省福州市回春药店。
1.2对照品溶液的制备精密称取葛根素20 mg、甘草苷10 mg、异甘草苷10 mg、大豆苷元20 mg和甘草酸20 mg,分别置于2 mL容量瓶中,葛根素加50%甲醇,甘草苷加甲醇,异甘草苷、大豆苷元及甘草酸加无水乙醇超声溶解并稀释至刻度,摇匀,得单一对照品储备液,质量浓度分别为10,5,5,10和10 mg/mL。
1.3供试品溶液的制备精密称定玉泉丸6 g,置于具塞锥形瓶,加水10 mL,震荡10 min使成混悬液,加入40 mL甲醇,称总质量后超声提取60 min(功率250 W,频率40 kHz),用甲醇补足减失质量,静置10 min,取上清液13 mL于离心管中加盖离心10 min(3 000 r/min),用0.45 μm微孔滤膜过滤后,精密移取10 mL置蒸发皿中,水浴蒸干,用甲醇复溶后定容于10 mL容量瓶。进样分析前微孔滤膜(0.45 μm)过滤,取续滤液为供试品溶液。
1.4阴性对照样品的制备根据待测目标组分归属,葛根素和大豆苷元为葛根中的主要成分,甘草苷、异甘草苷和甘草酸为甘草中的主要成分,故进行专属性试验时,只需设定不含葛根组和不含甘草组。由于玉泉丸为国家中药保护品种,其组方剂量尚未公开,参照其古方“玉泉散”中各味药组方剂量范围(10~60 g),设定天花粉、地黄、麦冬和五味子各30 g,再加入葛根或甘草30 g,组成上述2组药材缺失的阴性样品。分别剪碎后,用250 mL 80%的甲醇溶液浸泡12 h,参照1.3项下提取方法制备。
1.5色谱条件在高效液相色谱仪(配备四元低压混合泵、自动进样器、柱温箱、二极管阵列检测器)上,采用UltimateTMXB-C18色谱柱,以乙腈(B)-水(0.2%甲酸)(A)为流动相,线性洗脱梯度为B:12%~34%(0~8 min),34%等度(8~15 min),34%~53%(15~16 min),53%等度(16~22 min),53%~99%(22~22.1 min),99%等度(22.1~27 min),99%~12%(27~27.1 min),12%等度(27.1~33 min),平衡时间为10 min。流速1.0 mL/min;检测波长为254,280和340 nm,柱温30 ℃,进样10 μL。上述玉泉丸供试液的色谱结果如图1所示:供试液中大多数成分实现了很好的基线分离,两组阴性对照样品分别在葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸的色谱峰位置无干扰峰出现,且一次色谱分析时间<33 min。
2 结 果
2.1标准曲线的绘制分别精密吸取1.2项下各单一对照品储备液适量于容量瓶中,加入80%乙醇稀释至刻度得每1 mL含葛根素500 μg、甘草苷250 μg、异甘草苷25 μg、大豆苷元100 μg和甘草酸750 μg的混合对照品溶液备用。
分别精密吸取2,4,6,8,10,15和20 μL依次进样,以进样量(μg/mL)为横坐标,峰面积为纵坐标,分别绘制标准曲线,计算出5个对照品的回归方程和线性范围,详见表1。
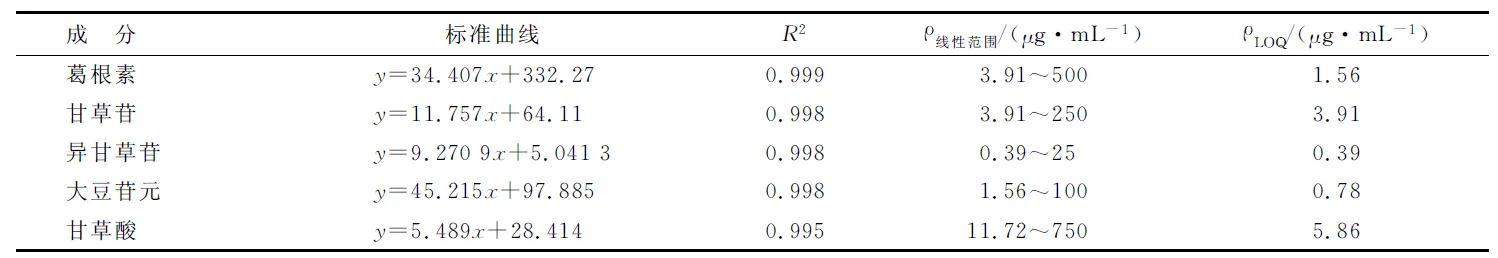
表1 5个对照品的标准曲线和定量限
y:对照品的峰面积;x:对照品的含量.LOQ:定量限.
2.2精密度试验取2.1项下对照品溶液,按1.5项下色谱条件,连续进样6次,根据峰面积分别计算得葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸的RSD为0.16%,0.25%,1.5%,0.19%及0.25%。
2.3重复性试验取同批次(批号为121103)玉泉丸浓缩丸6份,分别按1.3项下方法平行制备供试品溶液6份,按1.5项下色谱条件进样分析,测得样品中葛根素、甘草苷、异甘草苷、大豆苷元、甘草酸的RSD分别为0.29%,0.62%,1.9%,0.45%及1.2%。
2.4稳定性试验取供试品溶液1份,室温放置,按1.5项下色谱条件,于0,2,4,6,8,10,24,36,48 h各进样1次分析,记录峰面积,计算得葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸含量的RSD分别为1.2%,0.9%,2.1%,0.7%及1.6%。结果表明供试液中葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸在48 h内稳定性良好。
2.5加样回收率试验取已测定含量的样品(批号:140301)6份,每份6.0 g。精密称定,每份加入相同量的葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸混合对照品(含量分别为:0.025,0.012 5,0.001 25,0.005和0.037 5 mg),按1.3项下方法处理得到供试液,分别按1.5项下色谱条件进行分析,计算平均加样回收率分别为98.8%,96.1%,104.3%,103.5%和87.5%。RSD分别为1.3%,1.1%,2.8%,1.5%和3.3%。
2.6样品含量测定取3批待测样品,按1.3项下方法制备成供试液,按1.5项下色谱条件,进样分析。以外标法分别计算样品中葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸的含量,结果见表2。
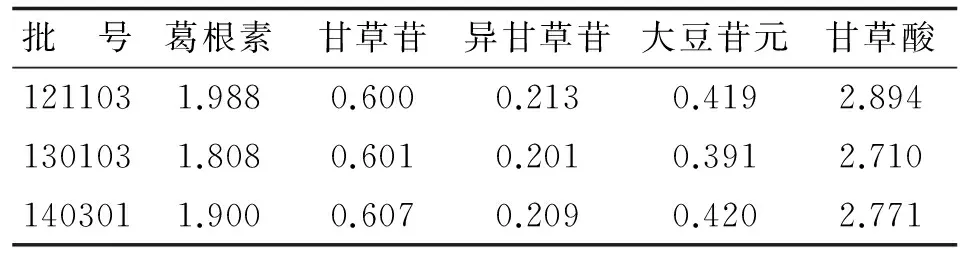
表2 5个化合物在3批玉泉丸中的含量
3 讨 论
在色谱条件的考察过程中,对检测波长和流动相组成均做了考察。葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸对照品的紫外光谱扫描结果显示:葛根素、大豆苷元和甘草酸在210,254 nm有最大吸收,甘草苷在280 nm有最大吸收,异甘草苷在340 nm有最大吸收。故设置3个检测波长为254,280和340 nm。
对比甲醇-水和乙腈-水体系,发现乙腈-水体系能在较短时间内实现较好的色谱分离。同时,为避免成分色谱峰拖尾及缩短分析时间,水相体系加入适当比例的甲酸或乙酸,结果表明乙腈-水(0.2%甲酸)体系能满足色谱峰出峰早、分离度好、峰形尖锐、基线波动较小的色谱分离要求。故用于玉泉丸供试液HPLC分析。
玉泉丸由葛根、天花粉、地黄、麦冬、五味子及甘草六味中药组方而成。其中葛根为君药,生津止渴,主消渴;天花粉、地黄为臣药,可滋阴清热,生津止渴;麦冬和五味子为佐药,麦冬主清肺养阴,益胃生津,五味子可益气生津,宁心止烦渴;甘草为使药,调和全方药材适用于消渴病,肺胃阴亏。中药复方制剂化学成分复杂,课题组前期采用高相液相-质谱联用技术分析了玉泉丸供试液中的化学成分,明确鉴定了葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸等多个成分。已有文献报道,葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸具有明确降糖作用[5-8],是方中含量较高且较稳定的活性成分。故选取该5种活性成分为含量测定指标成分,可更全面、准确地评价玉泉丸质量。
该研究建立了RP-HPLC同时测定玉泉丸中葛根素、甘草苷、异甘草苷、大豆苷元和甘草酸这5个有效成分含量的方法。经上述方法学实验证明该方法精密度和准确性均良好,完全符合药品检测要求。并将其成功应用于3个批次(121103,130103和140301)的玉泉丸中5个有效成分的含量测定。结果显示在检测时间内(该研究在2015年),这3个批次玉泉丸中的5个活性成分含量较稳定。该含量检测方法可用于玉泉丸的质量检测及相关研究。
[1]中华人民共和国卫生部. WS3-B-3802-98《中华人民共和国卫生部药品标准》中药成方制剂第二十册[S].北京:人民卫生出版社,1998:Z20.
[2]胡守莲,张红伟.HPLC测定玉泉丸中葛根素的含量[J].中华中医药学刊,2011,29(2):398.
[3]库尔班江,罗新泽.高效薄层双波长扫描法测定玉泉丸中葛根素和大豆甙元的含量[J]. 伊犁师范学院学报,2000,3:93.
[4]史培颖,林逢林,陈芳美,等. 高效液相色谱法同时测定玉泉丸中的葛根素及甘草酸[J]. 中国医院药学杂志,2013,33(20):1657.
[5]马运明,李大鸣,张静,等.葛根素对糖尿病小鼠降血糖功能的研究[J]. 中国慢性病预防与控制,2010,18(4):373.
[6]Yasuo M,Tomoko M,Akiko O. Combination effects of pioglitazone and bofutsushosan on body weight and blood glucose levels in diabetic KKAy mice[J].JTraditionalMedicines,2010,27(4):157.
[7]Guo Y Q, Wu G Z, Su X,etal. Antiobesity action of a daidzein derivative on male obese mice induced by a high-fat diet[J].NutritionResearch,2009,29(9):656.
[8]陈洁,彭仁琇,杨静,等.18α-甘草酸二铵与格列本脲联用对实验性糖尿病大鼠糖代谢的影响及其机制[J].中国药理学与毒理学杂志,2005,19(4):274.
(编辑:张慧茹)
Simultaneous Determination of Five Bioactive Components in Yuquan Pills by RP-HPLC
LI Shaoguang1, CAI Linxue2, YAO Hong1, HUANG Liying1, CHEN Bing1,LIN Xinhua1
1.Faculty of Pharmacy, Fujian Medical University, Fuzhou 350108, China;2.No 476 Hospital of Fuzhou General Hospital of Nanjing Army,Fuzhou 350002,China
ObjectiveTo establish a quality control method by using reversed-phase high performance liquid chromatography coupled with DAD detector (RP-HPLC-DAD) to simultaneously determine five components (puerarin, liquirtin, isoliquiritin, daidzein, glycyrrhizic acid) in Yuquan pills.MethodChromatographic experiment was carried out on an UltimateTMXB-C18 column(250×4.6 mm, 5 μm)with a gradient elution composed of acetonitrile (B) and 0.2% formic acid(A).The flow rate was 1.0 mL/min and the detection wavelength were 254, 280, 340 nm.The column temperature was set at 30 ℃.ResultsThe calibration curves of five components (puerarin, liquirtin, isoliquiritin, daidzein, glycyrrhizic acid) showed good linearity in their concentration ranges withr≥0.997.The average recovery was 87.5%~104.3% with relative standard deviation (RSD) less than 3.3%(n=6).ConclusionThe method is rapid, simple, and with good repeatability and stability, and it can be used in quality control of Yuquan pills.
Yuquan pill; puerarin; glycyrrhiza uralensis; isoflavones; glycyrrhizic acid; chromatography, high pressure liquid
2016-01-29
国家863项目(2012AA022604);国家自然科学基金项目(81202987);福建省高校新世纪优秀人才支持计划(JA14128);福建省科技厅自然科学基金项目(2016J01368);福建省教育厅科技项目(JA15209);福建医科大学苗圃科研基金(2014MP010)
1.福建医科大学 药学院,福州 350801;2.南京军区福州总医院第四七六医院 药剂科,福州350002
李少光(1984-),女,讲师,药理学博士
林新华. Email:Xhlin1963@sina.com
R284;R284.1;R285.5;R289.5;R927.2
A
1672-4194(2016)03-0155-04

