硅胶负载壳聚糖/海藻酸钠(SiO2-CTS/SA)脱除扇贝废弃物酶解液重金属的研究
任丹丹,张海丽,曲 词,李佰磊,郭晓茜,任先见
(大连海洋大学食品科学与工程学院,辽宁大连 116023)
硅胶负载壳聚糖/海藻酸钠(SiO2-CTS/SA)脱除扇贝废弃物酶解液重金属的研究
任丹丹,张海丽,曲词,李佰磊,郭晓茜,任先见
(大连海洋大学食品科学与工程学院,辽宁大连 116023)
研究了硅胶负载壳聚糖/海藻酸钠(SiO2-CTS/SA)对扇贝废弃物酶解液中重金属的脱除作用。以扇贝加工废弃物为原料,SiO2-CTS/SA为实验材料,对酶解液进行处理,利用原子吸收石墨炉法测定处理液中各种重金属的含量。结果显示:在投加量为5 g/L,pH为6,吸附时间2 h条件下,SiO2-CTS/SA对Cr、Cd、Pb的脱除率分别为92.5%、82.3%和84.6%;在10~50 ℃间,吸附热力学较好的符合Langmuir方程式;吸附动力学均符合Lagergren准二级动力学模型。动态过柱实验表明,在流动过柱状态下SiO2-CTS/SA对Cr、Cd、Pb的吸附量分别为0.678、0.523、0.457 mg/g,在流速1 BV/h,流动过柱2 h时后,脱除率接近100%;通过定量过柱实验,SiO2-CTS/SA可完全脱除酶解液中Cr、Cd和Pb;蛋白质、氨基酸态氮保存率分别为90.86%和92.39%。硅胶负载壳聚糖/海藻酸钠(SiO2-CTS/SA)能有效脱除扇贝酶解液中重金属Cr、Cd、Pb。
硅胶负载壳聚糖/海藻酸钠,重金属,扇贝废弃物,酶解液,吸附
随着人口的迅速增长和人类社会经济的加速发展,大量工业废水和生活污水排入到近岸海域,使得海域污染总体形势严峻,其中具有强毒性的Cr、Cd、Pb易在贝类体内富集成为贝类食品安全的重大隐患之一[1]。因此,寻找有效减少或脱除Cr、Cd、Pb在双壳贝类体内残留的方法,对保证水产品质量安全、保障人们饮食健康和解除我国贝类食品出口贸易技术壁垒具有重要意义。
化学沉淀法、电解法和离子交换与吸附等是目前常用的重金属脱除方法[2]。但这些脱除方法主要是针对处于游离状态下的重金属离子,而对于脱除与蛋白质等有机质结合的重金属离子的研究方法较少。吸附法是一种既简单又具有发展前景,而且已经被广泛应用的脱除方法。壳聚糖是甲壳素在碱性条件下水解并脱去部分乙酰基后生成的衍生物,可溶于大多数稀酸溶液。它是目前发现唯一的一种天然碱性多糖,已被广泛应用于食品、医药、化工、环保等行业中[3-6]。Muzzarelli[7]研究了壳聚糖与重金属离子的作用机理,认为其除具有螯合作用外,还包括离子交换和物理吸附两种方式。壳聚糖来源丰富,吸附效率高,可生物降解,无毒,是一种十分理想的重金属离子脱除剂。因此,壳聚糖已成为未来研究的重点,尤其在其增强对重金属的选择性及可再生的改性壳聚糖树脂方面的研究。本文以硅胶负载壳聚糖/海藻酸钠(SiO2-CTS/SA)为吸附材料,考察其对酶解液中重金属的脱除作用,旨在促进我国贝类废弃物利用和贝类产品的开发。
1 材料与方法
1.1材料与仪器
扇贝加工废弃物由大连獐子岛渔业集团公司提供;壳聚糖(CTS)、海藻酸钠(SA)为生化试剂;硅胶(200-300目)青岛海洋化工有限公司;氢氧化钠、浓盐酸、浓硝酸、冰乙酸、无水氯化钙、高氯酸,硫酸钾、碳酸钾等均为国产分析纯;铅、镉和铬标准溶液购自国家标准物质中心。
KSW-5-12A水浴恒温振荡器金坛市顺华仪器有限公司;pHs-25C数字式酸度计上海理达仪器厂;FW100高速万能粉碎机天津市泰斯特仪器有限公司;KSW-5-12A马弗炉天津市中环实验有限公司;SB-电热板龙口市先科仪器公司;KDN-04消化炉上海新嘉电子有限公司;SBS-100自动计滴部分收集器上海沪西分析仪器厂有限公司;79-2磁力搅拌器常州国华电器有限公司;中空纤维超滤膜正泰集团成套设备制造有限公司;TAS-990 AFG型原子吸收分光光度计北京普析通用仪器有限公司。
1.2实验方法
1.2.1实验材料制备
1.2.1.1扇贝酶解液的制备制备方法参考文献[8]。
1.2.1.2硅胶负载壳聚糖/海藻酸钠凝胶颗粒(SiO2-CTS/SA)的制备分别称取2 g海藻酸钠、壳聚糖,溶于质量分数为2%的100 mL醋酸溶液,脱泡、静置过夜,让其充分溶解,分别配成海藻酸钠溶液和壳聚糖溶液。在搅拌下向壳聚糖溶液中加入等体积的海藻酸钠溶液,20 min后,边搅拌边加入2 g烘干至恒重的硅胶,持续搅拌1 h。用胶头滴管将均匀混合溶液滴加到2%的氯化钙溶液中,滴状物胶化成粒径为(3.0±0.2) mm的颗粒。在氯化钙溶液中固化4 h。用蒸馏水将所得到的颗粒洗涤数次至中性,70 ℃烘干,轻轻研磨,过100目筛,即得淡黄色颗粒状固体硅胶负载壳聚糖/海藻酸钠(SiO2-CTS/SA)复合材料[9]。
1.2.2静态吸附实验
1.2.2.1投加量对吸附效果的影响取SiO2-CTS/SA,分别按质量0.00、0.01、0.02、0.03、0.05、0.07、0.10、0.20、0.40 g分别投入9个100 mL锥形瓶中,并做好编号。将扇贝酶解液解冻后,用1 mol/L的NaOH或HCl溶液调节溶液初始pH6,向每个锥形瓶中分别加入10 mL扇贝酶解液,用保鲜膜罩住瓶口,在温度25 ℃条件下震荡3 h,震荡结束后3000 r/min离心15 min,取上清液。消化,定容后待测。
1.2.2.2溶液初始pH对吸附性能的影响取7个100 mL锥形瓶,分别向其中加入10 mL解冻后的扇贝酶解液,用1 mol/L的NaOH或HCl溶液调节溶液pH分别为2、3、4、5、6、7、8,然后向每个锥形瓶中各加入0.1 g吸附材料,用保鲜膜罩好瓶口,在温度25 ℃条件下震荡3 h,震荡结束后3000 r/min离心15 min,取上清液。消化,定容后待测。
1.2.2.3吸附时间对吸附性能的影响取8个锥形瓶,分别向其中加入10 mL解冻的扇贝酶解液,用1 mol/L的NaOH或HCl溶液调节溶液pH为6加入0.1 g吸附材料,用保鲜膜罩住瓶口,在温度25 ℃条件下分别震荡0、10、30、60、90、120、240、360 min,震荡结束后3000 r/min离心15 min,取上清液。消化,定容后待测。
1.2.2.4温度对吸附效果的影响分别取5份扇贝酶解液溶液20 mL于锥形瓶中,用1 mol/L的NaOH或HCl溶液调pH为6,然后定容至50 mL,分别加入0.1 g 吸附材料。在摇床中恒温振荡反应4 h,振荡速度为200 r/min,温度分别为10、20、30、40、50 ℃,然后3000 r/min离心15 min,取上清液。消化、定容过程同上。
1.2.3动态吸附实验
1.2.3.1流动过柱向(Ф1.6 cm×60 cm)的玻璃柱中加入20 mL(柱高10 cm)充分吸水溶胀的硅胶负载壳聚糖/海藻酸钠(SiO2-CTS/SA)复合材料,装柱完毕后,温度25 ℃,用恒温蠕动泵维持动态平衡半小时。扇贝酶解液(pH6)持续地以1 BV/h从吸附柱顶端流入,流出液在吸附柱底收集,测定流出液中重金属和氨基酸态氮、蛋白质含量。
1.2.3.2定量过柱将吸附材料装柱,玻璃柱规格为Ф1.6 cm×60 cm,吸附材料高度为50 cm,装柱完毕后,动态平衡半小时后,定量加入20 mL的扇贝酶解液进行洗脱,流速通过调节阀控制在1 BV/h,分部收集流出液,直至流出液在280 nm下吸光值小于0.05,合并流出液。将流出液浓缩为过柱前体积,测定流出液中重金属和氨基酸态氮、蛋白质含量。
1.2.4测定方法氨基酸态氮的测定[10]:采用甲醛滴定法测定;蛋白质含量的测定[11]:采用280 nm紫外吸收法测定;重金属含量的测定:Cd、Pb、Cr的含量均采用原子吸收分光光度计石墨炉法测定。
1.2.5脱除率及吸附量的计算根据以下公式计算吸附量Qt:Qt=V(C0-Ct)/W
脱除率R的计算公式为:
R(%)=(C0-Ct)/C0×100
式中:V为溶液体积(mL);W为SiO2-CTS/SA干重(mg);C0、Ct为吸附前、吸附t分钟后重金属浓度(mg/L)。
2 结果与分析
2.1投加量对吸附效果的影响
由图1可知,随着SiO2-CTS/SA投加量的增加,各种重金属离子的脱除率不断增加,这是由于SiO2-CTS/SA量增多,对金属的吸附表面积增大,吸附重金属离子的结合点和吸附功能基团增多,使脱除率增大。当用量为3 g/L时,Cr、Cd、Pb的脱除率均不及40%,增加用量至5 g/L时,Cr、Cd、Pb的脱除率均在65%以上,当SiO2-CTS/SA量继续增加至7 g/L,虽然Cr、Cd、Pb脱除率达到70%左右,但是吸附容量有所降低,综合考虑脱除率和吸附容量两个因素,SiO2-CTS/SA的用量应控制为5 g/L。
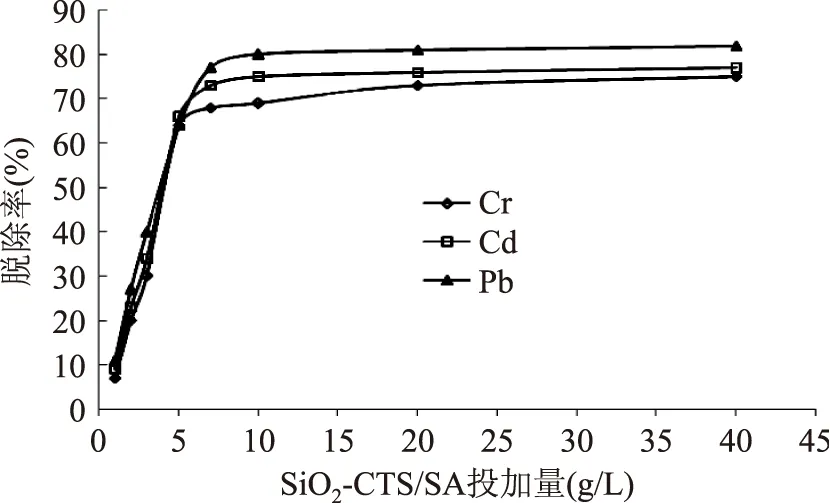
图1 SiO2-CTS/SA投加量对Cr、Cd、Pb脱除率的影响Fig.1 Effect of SiO2-CTS/SA weight on removal rate of Cr,Cd,Pb
2.2pH对吸附性能的影响
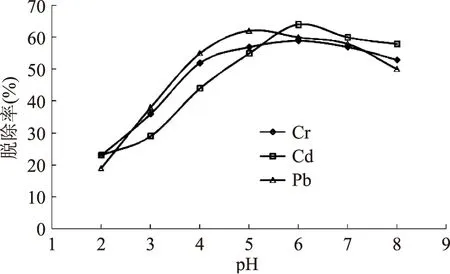
图2 pH对Cr、Cd、Pb脱除率的影响Fig.2 Effect of solution pH on removal rate of Cr,Cd,Pb
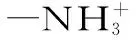
2.3时间对吸附性能的影响
由图3知,SiO2-CTS/SA对Cr、Cd、Pb的去除率趋势均随着时间的延长而增大,前60 min,吸附过程进行较快,90 min时,吸附已趋于平衡,为保证吸附充分进行,实验中选择时间应为2 h。经实验在投加量5 g/L,pH6吸附时间2 h时,SiO2-CTS/SA对Cr、Cd、Pb的脱除率分别为92.5%、82.3%、84.6%。经计算,t/Qt与t呈线性关系,以t/Qt对t作图(见图4)。
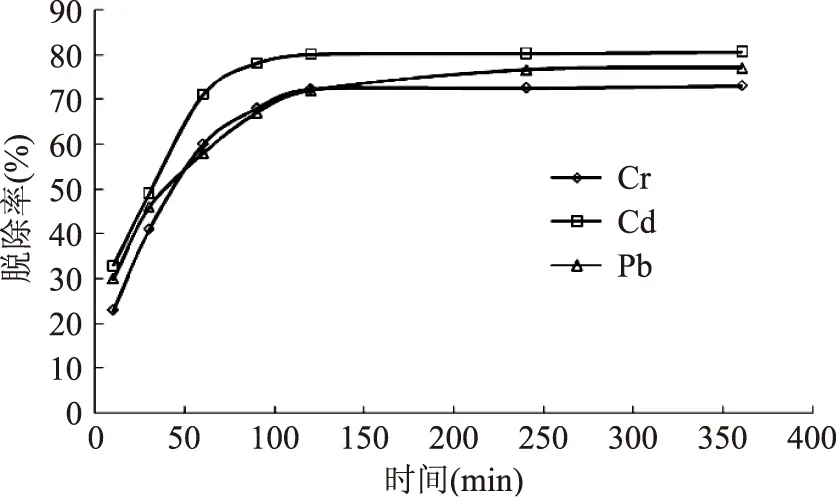
图3 吸附时间对Cr、Cd、Pb脱除率的影响Fig.3 Influence of time on removal rate of Cr,Cd,Pb
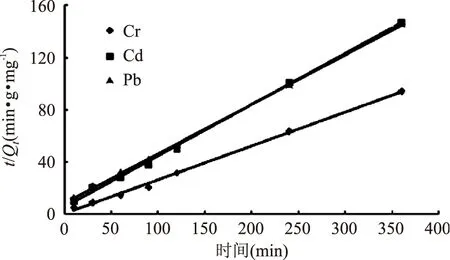
图4 Cr、Cd、Pb的准二级动力学模型Fig.4 Pseudo second-order kinetic of Cr,Cd,Pb
动力学常数K和平衡吸附量Qeq可由t/Qt对t作图所得直线方程的截距和斜率求得(见表1)。
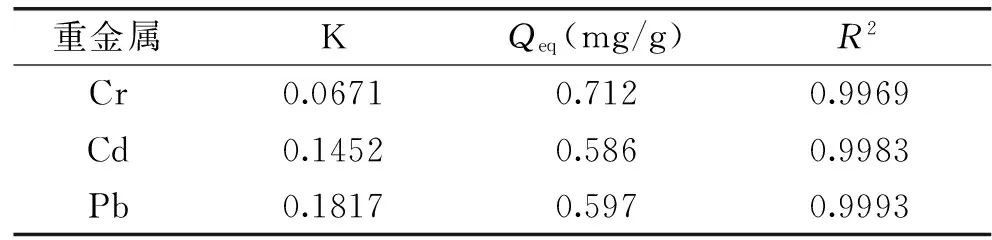
表1 SiO2-CTS/SA吸附Cr、Cd、Pb的动力学参数
由图4和表1知,在SiO2-CTS/SA投加量5 g/L,pH为6,温度25 ℃条件下,SiO2-CTS/SA对酶解液中Cr、Cd和Pb的平衡吸附量Qeq分别为0.712、0.586和0.597 mg/g。t/Qt与t相关系数分别为0.9969、0.9983和0.9993,t/Qt与t呈线性关系,说明SiO2-CTS/SA对Cr、Cd、Pb的吸附很好的符合Lagergren准二级动力学模型,吸附过程主要为化学吸附。
2.4温度的影响
以Qe对Ce作图,分别用Langmuir和Freundlich方程对相关数据进行拟合,SiO2-CTS/SA对Cr、Cd、Pb的吸附热力学曲线Langmuir模型和Freundlich模型分别如图5、图6所示。
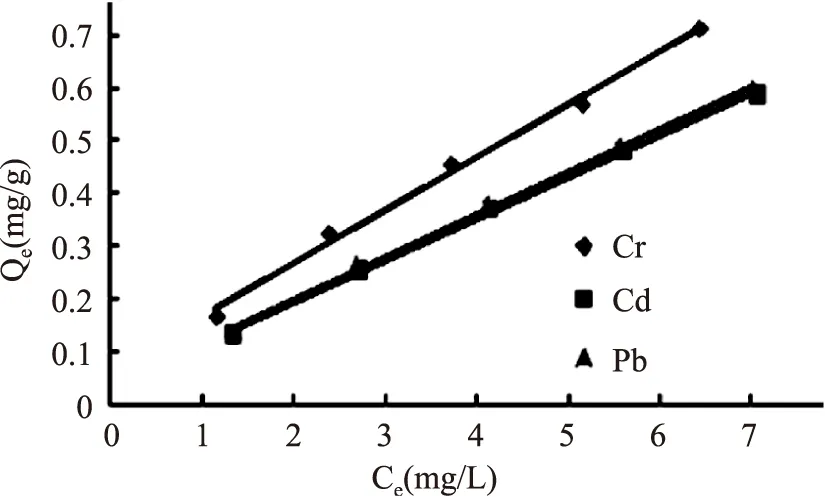
图5 Cr、Cd、Pb等温吸附线Langmuir模型Fig.5 Langmuir isotherm model of adsorption of Cr,Cd,Pb

图6 Cr、Cd、Pb等温吸附线Freundlich模型Fig.6 Freundlich isotherm model of adsorption of Cr,Cd,Pb
通过比较图5和图6知,SiO2-CTS/SA对Cr、Cd、Pb的吸附等温线更加符合Langmuir模型,拟合参数和相关数据见表2。

表2 Langmuir和Freundlich方程参数值(pH=6.0)
注:R2为相关系数。
由表2可知,SiO2-CTS/SA对Cr、Cd、Pb的吸附等温线对Langmuir公式比Freundlich公式拟合得更好,其相关系数均大于0.99,SiO2-CTS/SA对扇贝酶解液中Cr、Cd、Pb的吸附主要为单分子层吸附。Freundlich方程中n<1,说明SiO2-CTS/SA对扇贝酶解液中Cr、Cd、Pb的吸附属于容易吸附。
2.5动态过柱吸附效果
SiO2-CTS/SA流动过柱实验结果如图7所示。

图7 SiO2-CTS/SA流动过柱吸附曲线Fig.7 Adsorption curve of SiO2-CTS/SA flowing through the column
由图7可知,其吸附整体趋势为当扇贝酶解液连续通过吸附柱时,SiO2-CTS/SA不断吸附扇贝酶解液中重金属离子。在最初阶段,吸附柱顶端的SiO2-CTS/SA能够迅速有效脱除重金属,因此初始收集液中重金属浓度很低,几乎为零。随着酶解液持续流入,吸附不断进行,顶部吸附带达到饱和,吸附带不断下移,当吸附带下移到柱底端时,酶解液中重金属浓度不断增加,当吸附柱整体达到饱和时,酶解液未经脱除而直接穿出。经计算,SiO2-CTS/SA在流动过柱状态下对Cr、Cd、Pb的吸附量分别为0.678、0.523、0.457 mg/g,在流动过柱2 h时,收集到过柱后的酶解液中Cr、Cd和Pb含量很少,脱除率接近100%。
2.6蛋白质、氨基酸态氮含量的变化
由表3可知,定量过柱实验表明,在玻璃柱规格为1.6 cm×60 cm,SiO2-CTS/SA高度为50 cm,流速1 BV/h,定量加入20 mL扇贝酶解液,温度25 ℃,pH6条件下,能较好的保留酶解液中主要营养物质,对蛋白质、氨基酸态氮保存率分别为90.86%和92.39%。
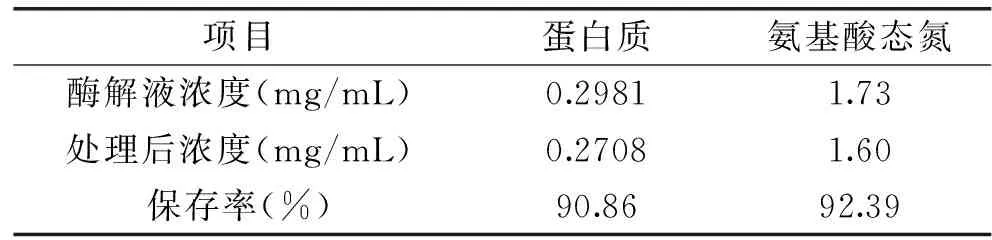
表3 扇贝酶解液过柱前后蛋白质、氨基酸态氮含量变化
3 结论
本文制备了硅胶负载壳聚糖/海藻酸钠SiO2-CTS/SA这种新型的吸附材料,通过静态吸附实验、动态洗脱实验等研究了这种材料对扇贝废弃物酶解液中重金属的吸附性能。研究结果表明,SiO2-CTS/SA能较好的脱除酶解液重金属;综合考虑pH、投加量、吸附时间及温度等因素,SiO2-CTS/SA脱除扇贝酶解液中重金属的最适宜条件为:投加量5 g/L,pH为6,吸附时间2 h,该条件下,对Cr、Cd、Pb的脱除率分别为92.5、82.3%、84.6%。动态过柱实验表明,利用SiO2-CTS/SA对扇贝废弃物酶解液进行动态洗脱以脱除其中的重金属Cr、Cd和Pb效果较好,且对酶解液中的蛋白质和氨基酸态氮的影响较小,从而说明今后将硅胶负载壳聚糖/海藻酸钠SiO2-CTS/SA这种吸附材料应用在扇贝废弃物酶解液的加工过程中是可行的,SiO2-CTS/SA具有一定的应用前景。
[1]Metian M,Warnau M,Oberhänsli F,et al. Interspecific comparison of Cd bioaccumulation in European Pectinidae
(Chlamys varia and Pecten maximus)[J]. Journal of Experimental Marine Biology and Ecology,2007,353(1):58-67.
[2]邱兆富,吕树光,洪丽云,等. 蟹壳生物吸附剂对水中镍离子的吸附研究[J]. 净水技术,2008,27(1):50-53.
[3]Wang Z K,Hu Q L,Wang Y X. Preparation of chitosan rods with excellent mechanical properties:One candidate for bone fracture internal fixation[J].Science China Chemistry,2011,54(2):380-384.
[4]Ravi Kumar M N V,Muzzarelli R A A,Muzzarelli C,et al. Chitosan chemistry and pharmaceutical perspectives[J]. Chem Rev,2004,104:6017-6084.
[5]Ren D D,Wang Q K,He Y H,et al. Heavy metals removal of modified chitosan from scallop processing waste hydrolyzate[J]. Glycobiology. 2013,23(11):1353-1354.
[6]Rinaudo M. Chitin and chitosan:properties and applications[J]. Prog Polym Sci,2006,31(7):603-632.
[7]Muzzarelli R A A. Carboxymethylated chitins and chitosans[J]. Carbohydrate Polymers,1988,8(1):1-21.
[8]任丹丹,李佰磊,王添娇,等. D401树脂脱除扇贝废弃物酶解液重金属的研究[J]. 食品工业科技,2013,34(17):139-141.
[9]Azlan K,Wan Saime W N,Lai Ken L. Chitosan and chemically modified chitosan beads for acid dyes sorption[J]. Journal of Environmental Sciences,2009,21(3):296-302.
[10]韩雅珊. 食品化学实验指导[M]. 北京:中国农业大学出版社,1996:61-63.
[11]张梅村. 蛋白质定量方法[J]. 山东食品科技.2004,6(12):11-13.
Study on heavy metals removal from hydrolyzate of scallop processing waste by SiO2-CTS/SA
REN Dan-dan,ZHANG Hai-li,QU Ci,LI Bai-lei,GUO Xiao-xi,REN Xian-jian
(College of Food Science and Engineering,Dalian Ocean University,Dalian 116023,China)
The removal of heavy metals from scallop waste by silica-supported chitosan/alginate(SiO2-CTS/SA)was studied. Scallop processing wastes were used as raw materials and SiO2-CTS/SA was utilized to be experimental materials to treat enzymatic hydrolysate. Atomic absorption spectrometry was used to measure heavy metal contents in the liquid. It was found that the removal rate of Cr,Cd,Pb was 92.5%,82.3% and 84.6% in the condition dosage of 5 g/L,pH 6 and adsorption time of 2 h. The adsorption thermodynamics was well in accordance with the Langmuir equation between 10 ℃ to 50 ℃. The adsorption isotherm was conformed to the Langmuir equation. The pattern of adsorption was single molecular adsorption,and the adsorption kinetic followed the pseudo-second-order dynamics. Flow velocity of 1Bv/h,time of 2 h,the adsorption amount of SiO2-CTS/SA to Cr,Cd,Pb was 0.678,0.523,0.457 mg/g,respectively. Heavy metals of enzymolysis liquid collected after column cannot be detected. The retention rate of protein and amino acid nitrogen attained 90.86% and 92.39%. SiO2-CTS/SA can remove Cr,Cd,Pb of scallops enzymolysis liquid effectively.
SiO2-CTS/SA;heavy metals;scallop waste;enzymatic hydrolysis;adsorption
2015-09-17
任丹丹(1980-),女,博士,副教授,研究方向:海洋生物资源利用,E-mail:rdd80@163.com。
国家自然科学基金资助项目(31301449);辽宁省高校优秀人才支持计划项目(LJQ2014077);辽宁省海洋与渔业厅科研计划项目(201004)。
TS254.9
A
1002-0306(2016)11-0109-05
10.13386/j.issn1002-0306.2016.11.014

