混合熔融Li2CO3-Na2CO3-K2CO3体系表面张力计算*
李建朝,齐素慈,许继芳,王 璟,翁文凭
(1.河北工业职业技术学院材料系,河北石家庄050091;2.苏州大学沙钢钢铁学院)
混合熔融Li2CO3-Na2CO3-K2CO3体系表面张力计算*
李建朝1,齐素慈1,许继芳2,王璟2,翁文凭2
(1.河北工业职业技术学院材料系,河北石家庄050091;2.苏州大学沙钢钢铁学院)
熔融碳酸盐是一种良好的热载体和反应介质,其表面张力直接影响反应体系中熔盐分布和界面反应。在熔融盐离子半径和Butler方程的基础上,建立了熔融混合碳酸盐Li2CO3-Na2CO3-K2CO3体系的表面张力计算模型,考察了温度和熔盐组分对表面张力的影响。结果表明:模型计算的表面张力值与实际测量值比较吻合;熔融碳酸盐纯物质的表面张力随着阳离子的静电势(Z/r)的增大而逐渐减小;Li2CO3-Na2CO3-K2CO3体系中,熔盐的表面张力随着温度的升高而减小;混合熔融盐表面张力随着Li2CO3含量的增加而逐渐增大,随着K2CO3含量的增加而逐渐减小。
熔融碳酸盐;表面张力;模型;Butler方程
碳酸熔盐是一种良好的热载体和反应介质的离子型熔体,且价格便宜、熔点低、相变潜热高、比热大、对环境影响小,可广泛应用于材料制备、催化反应、燃料电池等领域[1]。碳酸熔盐常用体系为Li2CO3-Na2CO3和Li2CO3-K2CO3体系[2]。针对二元熔融碳酸盐的基本性质如密度、表面张力、电导等的研究较多[3]。熔盐密度决定能量转换过程的能量密度,表面张力影响电解质在电池中隔膜和电极间的分配和电极界面反应效率,黏度影响熔融盐在流动时的能量损失和反应物在融体内传输的传质阻力,电导直接决定着燃料电池的输出效率[4]。而且这些基本物理性质对理解熔体微观结构、研究离子间作用力和熔盐中离子运动规律和实际使用过程的高效利用具有重要意义。
Li2CO3、Na2CO3和 K2CO3的熔点分别为 996、1 124、1 164 K。在二元体系中添加其他碳酸盐可形成低熔点共熔物,Li2CO3-Na2CO3-K2CO3作为最基本的三元体系受到广泛重视[5]。该体系温度范围为670~1 174 K,混合熔盐的物理性质变化范围比较大,为熔盐成分控制和性质优化提供了较大便利。J. Mohamedi等[6]研究了该体系作为燃料电池电解质时的氧溶解度和Warburg阻抗。S.G.Kim等[7]报道了Li2CO3-Na2CO3-K2CO3体系的相图和蒸汽压。但是,该体系的密度、表面张力和电导率数据比较缺乏,且物理性质与熔融组分之间关系的报道也很少。
表面张力是熔融盐的基本特性,是表征液体性质的重要参数,其大小与温度、界面两相物质的性质有关[8]。可靠的物性数据是熔盐作为传热蓄热介质在工业中应用的重要前提,但高温熔融下表面张力实验测量比较困难,数据准确度不高,致使有关数据至今还很缺乏[9]。一种可行的解决途径是建立合理的模型来对各种温度和组分的熔盐物理性质进行估算。因此,笔者基于熔融碳酸盐离子结构和熔体表面张力的Butler方程,建立 Li2CO3-Na2CO3-K2CO3体系表面张力的计算模型,并将计算结果与实验结果进行对比以验证模型的准确性。在此基础上,计算Li2CO3-Na2CO3-K2CO3三元体系及其二元子体系的表面张力,考察了温度和熔盐组分对表面张力的影响,以期为熔融碳酸盐设计和优化提供数据支持和理论参考。
1 混合熔盐表面张力计算模型
J.A.V.Bulter[10]根据化学势和表面能推出了表面张力计算方程(Bulter方程):
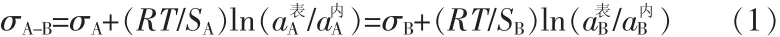
式中,σA、σB、σA-B分别为纯物质A、B和A-B二元系的表面张力;R、T分别表示气体常数和绝对温度;SA、SB分别表示纯组元A、B的摩尔表面积;、分别表示组元A在表面和内部的活度;、分别表示组元B在表面和内部的活度。
基于上述基本理论,T.Tanaka等[8]将熔体中组元有效阴离子和阳离子半径比作为模型参数来计算熔体表面张力。该模型考虑将组元的离子半径比作为模型参数,采用纯组元的表面张力和摩尔体积。其表达式:
1)ACO3-BCO3二元碳酸盐体系:
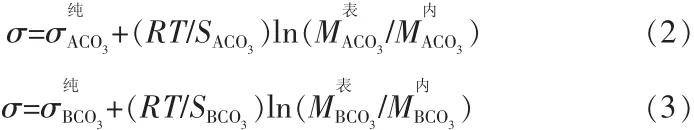
2)ACO3-BCO3-DCO3三元碳酸盐体系:
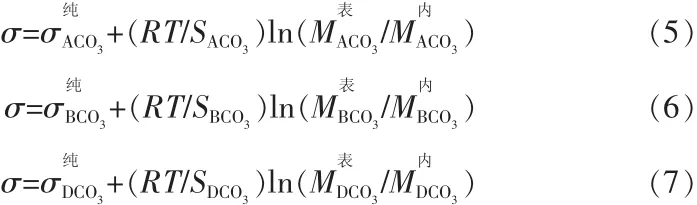

表1 阳离子半径及碳酸根半径 nm

表3 碳酸盐纯物质的表面张力与温度的关系
另外,对于混合熔融盐的物理性质,一般可运用Arrhenius混合规则来计算,以表面张力为例,计算方程如下:

式中,σi表示纯物质组元i的表面张力,xi为纯物质组元i的物质的量分数。
2 计算结果及讨论
2.1二元体系表面张力计算结果
1 073 K和 1 123 K下Li2CO3-Na2CO3、Li2CO3-K2CO3和Na2CO3-K2CO3二元体系表面张力的计算结果如图1~3所示。由于Na2CO3和K2CO3的熔点高于此温度值,因此模型采用的纯物质熔融盐的物理性质数据(如物质的量分数和表面张力)由实验数据与温度的关系外推得到。为了验证计算结果的准确性,相关二元体系的测量结果也如图1~3所示。
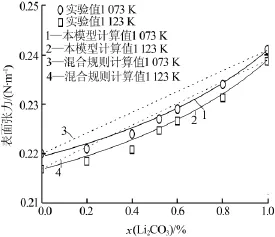
图1 Li2CO3-Na2CO3二元碳酸盐体系的表面张力
对比模型计算值与实际测量值表明,本模型计算结果与实验测量结果完全吻合,熔盐表面张力随温度和组分的变化关系完全一致,从而验证了模型的正确性。二元体系中,随着温度的升高,熔盐表面张力逐渐减小;随着Li2CO3含量的增加,熔盐表面张力逐渐增大;随着K2CO3含量的增加,熔盐表面张力逐渐减小。通过Arrhenius混合规则计算出的混合碳酸盐的表面张力结果也如图1~3所示。结果显示,混合规则计算出的混合碳酸盐表面张力随着熔融组分的变化而呈现线性变化,且与实际测量结果偏离较大,混合规则计算值偏高。

图2 Li2CO3-K2CO3二元碳酸盐体系的表面张力
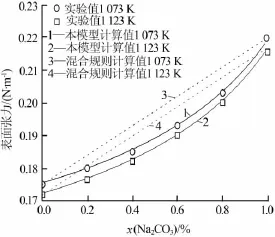
图3 Na2CO3-K2CO3二元碳酸盐体系的表面张力
2.2三元体系表面张力计算结果
采用模型计算了Li2CO3-Na2CO3-K2CO3三元体系表面张力。图4为1 073 K和1 123 K条件下由计算结果绘制的三元体系等表面张力线。为了验证计算结果的准确性,相关的实验测量结果也在图4中做了标注[11]。对比模型计算值与实际测量值发现,本模型计算结果与实验测量结果基本一致,进一步证明本模型可应用于熔融碳酸盐表面张力计算。Li2CO3-Na2CO3-K2CO3三元体系中,熔盐的表面张力随着温度的升高逐渐减小;随着混合熔融盐表面张力Li2CO3含量的增加而逐渐增大,随着K2CO3含量的增加而逐渐减小。

图4 三元碳酸盐体系中计算的等表面张力线
2.3结果讨论
1)熔盐性质与熔体中离子的静电势(Z/r)大小有关。在Li2CO3-Na2CO3-K2CO3三元熔融碳酸熔盐中,阴离子均为CO32-,因而熔盐性质与阳离子的静电势大小密切相关,其中阳离子的静电势大小关系为Li+>Na+>K+。1 073 K和1 123 K温度下熔融碳酸盐纯物质表面张力与阳离子静电势的关系见图5。
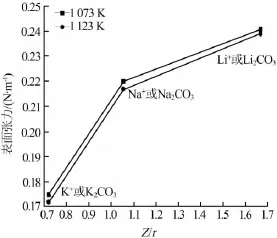
图5 碳酸盐纯物质表面张力与阳离子静电势的关系
熔融盐表面张力与离子间的作用力有关,在其他条件相同时,熔融盐中阳离子半径越大,阳离子的静电势越小,则熔融盐的表面层中聚集的离子数量就越少,因此熔体内部的离子对表面离子的吸引力越小,从而熔融盐表面张力也越小。因而熔融碳酸盐纯物质的表面张力随着Li+、Na+、K+静电势的减小而增大。
2)混合熔融盐的物理性质估算时,常运用Arrhenius混合规则来计算。但是混合熔融碳酸盐二元体系的实验结果显示,该体系中熔融盐表面张力与组分含量的关系并不符合简单的混合法则,即随着体系中某一组元含量的改变,熔融盐表面张力并不呈现单调性变化。因此,在混合熔融碳酸盐物理性质估算时,不适合仅采用简单的混合规则对混合熔融盐的物理性质进行估算。
3)熔融盐的易得性和成本也是熔融盐应用时需要考虑的环节,3种碳酸盐的商业价格由高到低依次为Li2CO3>K2CO3>Na2CO3[12]。虽然LiNO3的加入能够显著降低熔融盐的表面张力,但是考虑到实际使用的成本,在满足应用要求的前提下,实际使用时应尽量降低Li2CO3的含量。
4)本模型计算时,由于熔融碳酸盐纯物质的熔点一般高于混合熔融盐使用的温度,因此计算使用温度下混合熔融盐的表面张力时,需对已有纯物质的实验数据进行合理的外推,但这也可能为模型计算结果带来一定的误差。考虑到多元体系表面张力实验测量的范围和难度,且实验中二元体系及三元体系的模型计算结果与实际测量结果基本一致,因此本模型可对熔融碳酸盐表面张力进行估算。鉴于本模型在多元熔盐体系中较为成功的应用[8],本模型可推广到多元熔融碳酸盐表面张力的计算,以期为高温熔融碳酸盐的实际应用提供较为准确的表面张力数据,也为多元熔融碳酸盐设计和优化提供数据支持和理论参考。
3 结论
1)在熔融盐离子半径和Butler方程的基础上,建立了Li2CO3-Na2CO3-K2CO3体系表面张力计算模型,且模型计算结果与实际测量值比较吻合。
2)熔融碳酸盐纯物质的表面张力与阳离子的静电势(Z/r)大小密切相关,表面张力随着静电势的减小而逐渐增大。
3)Li2CO3-Na2CO3-K2CO3体系中,熔盐表面张力随着温度的升高逐渐减小,随着混合熔融盐中Li2CO3含量的增加而逐渐增大,随着K2CO3含量的增加而逐渐减小。
[1]赵倩,王俊勃,宋宇宽,等.熔融盐高储热材料的研究进展[J].无机盐工业,2014,46(11):5-8.
[2]尹辉斌,丁静,杨晓西,等.碳酸熔盐传热蓄热材料的制备与热性能[J].工程热物理学报,2013,34(5):952-956.
[3]Kojima T,Miyazaki Y,Nomura K,et al.Electrical conductivity of molten Li2CO3-X2CO3(X:Na,K,Rb,and Cs)and Na2CO3-Z2CO3(Z:K,Rb,and Cs)[J].J.Electrochem.Soc.,2007,154(12):F222-F230.
[4]辛嘉余,王华,何方,等.几种碳酸盐熔融体的粘度计算[J].工业加热,2006,35(1):22-24.
[5]廖敏,丁静,魏小兰,等.高温碳酸熔盐的制备及传热蓄热性质[J].无机盐工业,2008,40(10):15-17
[6]Mohamedi M,Hisamitsu Y,Uchida I.Ternary alkali carbonate composition-oxygen solubility relationship under atmospheric and pressurized conditions-A utility model for MCFC[J].J.Appl.Electrochem.,2002,32(1):111-117.
[7]Kim S G,Jun J H,Jun J H.Predictions of the optimum ternary alkali-carbonate electrolyte composition for MCFC by computational calculation[J].J.Power Sources,2006,160(2):805-810.
[8]Tanaka T,Kitamura T,Back I A.Evaluation of surface tension of molten ionic mixtures[J].ISIJ Int.,2006,46(3):400-406.
[9]Raade J,Padowltz D.Development of molten salt heat transfer fluid with low melting point and high thermal stability[J].J.Sol.Energy Eng.,2011,33(3):91-96.
[10]Butler J A V.The thermodynamics of the surfaces of solutions[J]. Proc.R.Soc.A,1932,135:348-375.
[11]Kojima T,Miyazaki Y,Nomura K,et al.Density,surface tension,and electrical conductivity of ternary molten carbonate system Li2CO3-Na2CO3-K2CO3and methods for their estimation[J].Journal of The Electrochemical Society,2008,155(7):F150-F156.
[12]丁晶,魏小兰,彭强,等.中高温传热蓄热材料[M].北京:科学出版社,2013.
联系方式:wlzcn15@163.com
Evaluation of surface tension for molten Li2CO3-Na2CO3-K2CO3system
Li Jianchao1,Qi Suci1,Xu Jifang2,Wang Jing2,Weng Wenping2
(1.Material Department,Hebei Institute of Vocational and Technique,Shijiazhuang 050091,China;2 Shagang School of Iron and Steel,Soochow University)
Molten carbonate salt is a good thermal carrier and reaction medium.Surface tension directly affects the interfacial reaction and the distribution of molten salt in reaction system.On the basis of the ionic radii of the components and Butler′s equation,a calculating model is developed for determining the surface tension of the molten Li2CO3-Na2CO3-K2CO3carbonate ternary system.The effects of temperature and composition on surface tension of molten salt were investigated.Compared with the calculated values of surface tension as well as the data available in the literature,the results showed that the present model was working well.The surface tension of the pure molten carbonate decreased with increasing the electrostatic potential of cations in molten salt.The surface tension in Li2CO3-Na2CO3-K2CO3system increased with in increasing of the Li2CO3content.And with the increasing of the K2CO3content,the surface tension decreased.
molten carbonate;surface tension;model;Butler equation
TQ127.13
A
1006-4990(2016)05-0016-04
河北省教育厅青年基金项目(QN2015252)、国家自然科学基金资助项目(50874072,51204115)、苏州大学大学生创新创业训练计划项目(2014xj044)。
2015-12-24
李建朝(1979—),男,博士研究生,主要从事无机盐物理性质研究,已公开发表文章6篇。
齐素慈

