达比加群酯中间体3-【【【2-{[(4-氰基苯基)氨基]甲基}-1-甲基-1H-苯并咪唑-5-基】羰基】(吡啶-2-基)氨基】丙酸乙酯的合成
蔡志强, 侯 旭, 侯 玲, 张晓妍, 胡志泉, 金正盛
(1. 沈阳工业大学 石油化工学院,辽宁 辽阳 111003; 2. 辽宁省核与辐射监测中心,辽宁 辽阳 110161)
·研究简报·
达比加群酯中间体3-【【【2-{[(4-氰基苯基)氨基]甲基}-1-甲基-1H-苯并咪唑-5-基】羰基】(吡啶-2-基)氨基】丙酸乙酯的合成
蔡志强1*, 侯旭1, 侯玲1, 张晓妍2, 胡志泉1, 金正盛1
(1. 沈阳工业大学 石油化工学院,辽宁 辽阳111003; 2. 辽宁省核与辐射监测中心,辽宁 辽阳110161)
以对氨基苯腈为起始原料,经胺化反应制得N-( 4-氰基苯基) 甘氨酸(4); 4与N-[3-氨基-4-(甲基氨基)苯甲酰基]-N-2-吡啶-β-丙氨酸乙酯(5)经酰胺化后经闭环反应,合成了达比加群酯的关键中间体——3-【【【2-{[(4-氰基苯基)氨基]甲基}-1-甲基-1H-苯并咪唑-5-基】羰基】(吡啶-2-基)氨基】丙酸乙酯,总收率79.6%,其结构经1H NMR和ESI-MS确证。
对氨基苯腈; 苯并咪唑; 达比加群酯; 中间体合成
苯并咪唑及其衍生物是一类重要的活性物质,在医药和农药领域有广泛应用,如抗凝血,抗癌、杀菌、抗氧化、抗寄生虫及除草等[1-2]。其合成研究一直倍受人们关注。德国勃林格殷格翰公司开发的新药达比加群酯(Pradaxa©)就是具有苯并咪唑母核结构的新型凝血酶抑制剂。该药于2008年被欧盟批准上市,主要用于髋关节和膝关节置换时的血栓预防。2010年被美国FDA批准用于预防成人非瓣膜性房颤患者的卒中和全身性栓塞[3-6]。
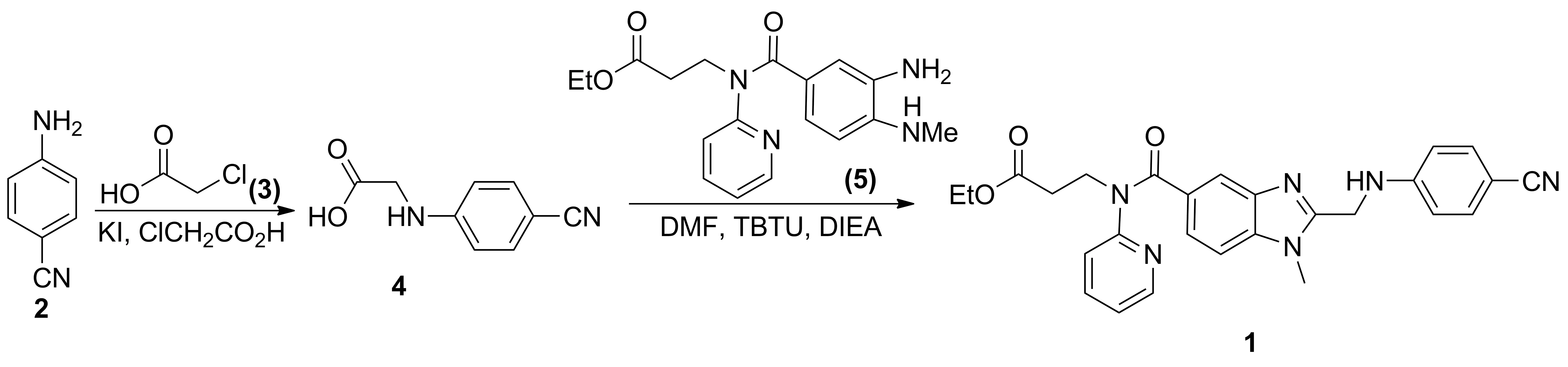
Scheme 1
达比加群酯的合成报道相对较多[2-9],但对其关键中间体3-【【【2-{[(4-氰基苯基)氨基]甲基}-1-甲基-1H-苯并咪唑-5-基】羰基】(吡啶-2-基)氨基】丙酸乙酯(1)的合成工艺研究较少。文献方法多以N-(4-氰基苯基)甘氨酸(4)和3-[(3-氨基-4-甲胺基苯甲酰基)(吡啶-2-基)氨基]丙酸乙酯(5)为原料,N,N-羰基二咪唑(CDI)或1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDCI)与1-羟基苯并三氮(HOBt)联用作缩合剂进行酰胺化反应。该方法后处理复杂,需柱层析纯化,不适合工业化生产。
本文在文献[2-3]方法的基础上,以对氨基苯腈(2)为起始原料,先与氯乙酸(3)经胺化反应制得4; 4与N-[3-氨基-4-(甲基氨基)苯甲酰基]-N-2-吡啶-β-丙氨酸乙酯(5)经酰胺化后经闭环反应合成了1(Scheme 1),总收率79.6%,其结构经1H NMR和ESI-MS确证。该方法具有操作简单,收率较高,无需柱层析纯化等优点,为工业化生产提供了借鉴。
1 实验部分
1.1仪器与试剂
X-4型熔点仪(温度未校正);Bruker ARX-400 NMR型核磁共振仪(DMSO-d6为溶剂,TMS为内标);Agient 1100型四级杆液质联用仪。
O-苯并三氮唑-N,N,N′,N′-四甲基脲四氟硼酸酯(TBTU), HOBt, EDCI, CDI, 4-二甲氨基吡啶(DMAP),二异丙基乙胺(DIEA),分析纯;其余所用试剂均为分析纯。
1.2合成
(1) 4的合成
在反应瓶中加入2 5.0 g(42.32 mmol),碘化钾0.7 g(4.23 mmol),氯乙酸4.4 g(46.56 mmol)和水100 mL,搅拌使其溶解;回流反应3 h。冷却至室温,过滤,滤饼依次用水(3×10 mL)和无水乙醚(20 mL)洗涤,干燥得白色固体4 6.5 g,收率87.2%, m.p.224.1~225.6 ℃;1H NMRδ: 3.92(s, 2H, CH2), 6.68(d,J=8.4 Hz, 2H, ArH), 7.45(d,J=8.4 Hz, 2H, ArH), 12.11(br s, 1H, COOH); ESI-MSm/z: 177{[M+H]+}。
(2) 1的合成
在反应瓶中加入4 3.0 g(17.0 mmo1)和DMF 10 mL,搅拌使其溶解;氮气保护,冰水浴下加入TBTU 5.7 g(17.8 mmo1)和DIEA 1 mL,反应30 min。滴加5 5.8 g(17.0 mmo1)的DMF(5 mL)溶液,滴毕,缓慢升至室温,反应4 h。蒸除溶剂,残余物加入二氯甲烷30 mL,用饱和盐水(3×5 mL)洗涤,无水硫酸镁干燥,过滤,滤液浓缩,剩余物加入冰乙酸30 mL,回流反应1 h。减压浓缩,剩余物加入浓氨水10 mL,于室温反应30 min。蒸除溶剂,剩余物加入二氯甲烷30 mL,用饱和盐水(3×10 mL)洗涤,无水硫酸镁干燥,过滤,滤液浓缩得黄褐色油状液体1 7.5 g,收率91.3%;1H NMRδ: 1.12(t,J=6.8 Hz, 3H, CH3), 2.66(t,J=6.8 Hz, 2H, CH2), 3.73(s, 3H, NCH3), 3.86(t,J=6.8 Hz, 2H, CH2), 4.18(t,J=6.8 Hz, 2H, CH2), 4.43(s, 2H, CH2), 6.79(d,J=8.8 Hz, 2H, ArH), 6.85(d,J=8.8 Hz, 1H, ArH), 7.14(m, 2H, ArH), 7.43(d,J=8.8 Hz, 2H, ArH), 7.48(d,J=8.8 Hz, 2H, ArH), 7.58(m, 1H, ArH), 8.38(m, 1H, ArH); ESI-MSm/z: 483{[M+H]+}。
2 结果与讨论
2.1合成4的反应条件优化
为优化4的合成条件,研究了催化剂和溶剂对4收率的影响,结果见表1。由表1可以看出,催化剂对4收率影响较大,溶剂相同,不加催化剂,反应时间超过24 h,收率低于30%(No.2, No.4)。加入催化剂,收率显著提高(No.1, No.3, No.5),可见碘可活化氯原子。此外,溶剂极性和沸点对4收率也有一定影响,如以丙酮为溶剂,即便加入碘化钾催化,收率均<60%(No.5和No.6)。以水为溶剂,收率较高(No.3和No.4),其可能原因为:(1)水的沸点较高,回流状态下使本反应正好达到其能量壁垒;(2)水的极性较强,有利于取代反应进行。
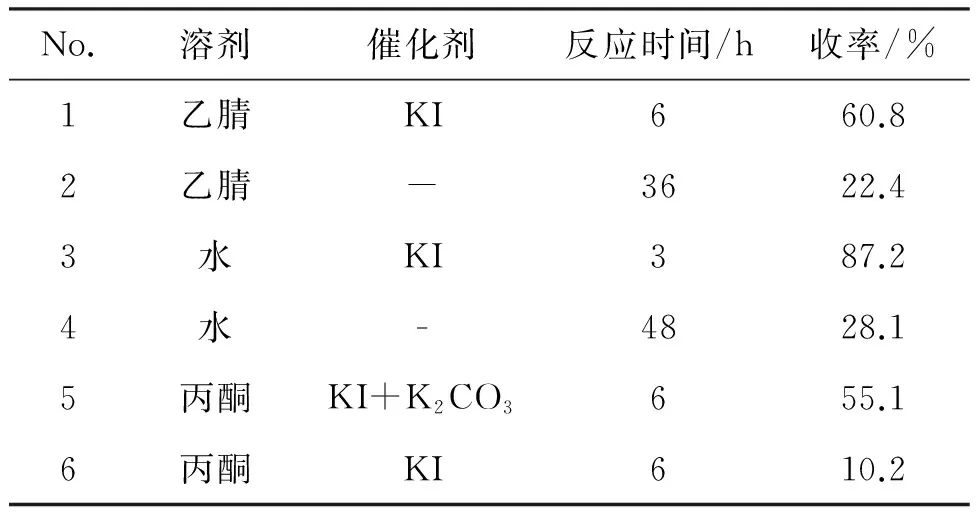
表1 4的合成条件优化
综上所述,合成4的最佳条件为:水为溶剂,碘化钾为催化剂,回流反应3 h,收率87.2%。
2.2合成1的反应条件优化
在合成1的过程中,研究了缩合剂对1收率的影响,结果见表2。
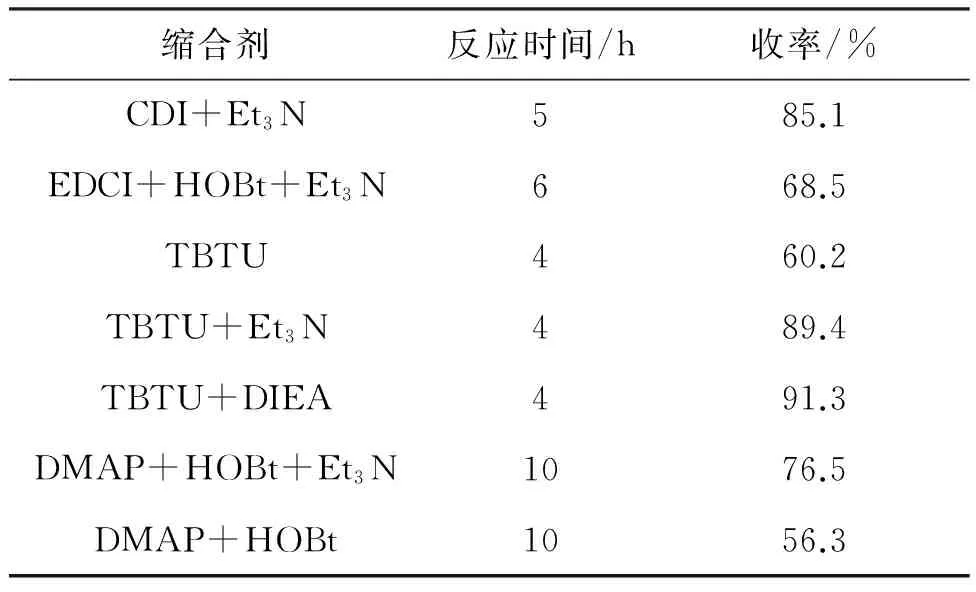
表2 缩合剂对1收率的影响
由表2可以看出,在EDCI+HOBt+Et3N体系中,由于活性相对较弱,反应时间适中(6 h),但收率较低(68.5%);单独以TBTU为缩合剂,效果并不理想,需配合叔胺碱才能达到较好效果,如TBTU与Et3N配合使用,收率可达89.4%,但考虑Et3N和DIEA的成本相差不大,从原子经济学角度考虑,选择TBTU和DIEA配合,效果更佳。在DMAP+HOBt体系中,无论是否添加缚酸剂,收率均较低(56.3%)。
综上所述,合成1的最佳条件为:氮气保护下,DMF为溶剂,TBTU为缩合剂,DIEA为碱,收率91.3%。
[1]田敏,王陆瑶,牛小玲,等. 环烷基取代苯并咪唑衍生物的合成及抑菌活性研究[J].应用化工,2013,42(7):1208-1212.
[2]Hauel N H, Nar H, Priepke H,etal. Structure-based design of novel potent nonpeptide thrombin inhibitors[J].Journal of Medicinal Chemistry,2002,45(9):1757-1766.
[3]Jirman J, Richter J, Lustig P. A method for the preparation of dabigatran:WO 2009 111 997[P].2009.
[4]蔡志强,马维英,候旭,等. 达比加群酯的合成工艺改进[J].精细化工,2015,32(3):308-311.
[5]刘晓君,陈国华. 达比加群酯的合成[J].应用化学,2013,30(4):373-377.
[6]蔡志强,侯旭,张波,等. 新型苯并咪唑衍生物的合成及抗凝血活性[J].合成化学,2015,23(10):908-912.
[7]汤传飞,黄安民,王彪. 达比加群酯制备路线[J].临床医药文献电子杂志,2015,33(2):6946-6947.
[8]郭雅俊,朱雪焱,黄雨,等. 达比加群酯的合成[J].合成化学,2014,22(2):262-264.
[9]刘晓君,陈国华. 达比加群酯的合成[J].应用化学,2013,30(4):373-377.
Synthesis of The Key Intermediate of Dabigatran Etexilate Ethyl 3-【2-[(4-Cyanophenyl)amino]methyl-1-methyl-N-(pyridin-2-yl)-1H-benzo[d]imidazole-5-carboxamido】propanoate
CAI Zhi-qiang1*,HOU Xu1,HOU Ling1,ZHANG Xiao-yan2,HU Zhi-quan1,JIN Zheng-sheng1
(1. School of Petrochemical Engineering, Shenyang University of Technology, Liaoyang 111003, China;2. Liaoning Provincal Nuclear and Radiation Monitoring Center, Shenyang 110161, China)
The key intermediate, ethyl 3-【2-{[(4-cyanophenyl)amino]methyl}-1-methyl-N-(pyridin-2-yl)-1H-benzo[d]imidazole-5-carboxamido】propanoate, in total yield of 79.6%, was synthesized by ammoniation reaction of 4-aminobenzonitrile, then amidation with ethyl 3-{[3-amino-4-(methylamino)benzoyl]-pyridin-2-ylamino}propanoate and ring-formation. The structure was confirmed by1H NMR and ESI-MS.
4-aminobenzonitrile; benzimidazole; Dabigatran etexilate; intermediate synthesis
2016-03-16
辽宁省教育厅科学研究一般项目(L2015383); 沈阳工业大学博士启动基金资助项目(521422)
蔡志强(1980-),男,汉族,辽宁阜新人,博士,硕士生导师,主要从事药物合成的研究。 E-mail: kahongzqc@163.com
O626.23; R914.5
A
10.15952/j.cnki.cjsc.1005-1511.2016.08.16072

