LC-MS/MS法测定比格犬血浆中丁酸氯维地平浓度
杨欣怡,陶春蕾,邵 凤,王 慧
(1.安徽中医药大学,安徽 合肥 230038;2.安徽万邦医药有限公司,安徽 合肥 230088)
LC-MS/MS法测定比格犬血浆中丁酸氯维地平浓度
杨欣怡1,2,陶春蕾1,2,邵凤1,2,王慧1,2
(1.安徽中医药大学,安徽 合肥230038;2.安徽万邦医药有限公司,安徽 合肥230088)
本研究建立了液相色谱-串联质谱(LC-MS/MS)法测定比格犬血浆中丁酸氯维地平浓度,用来研究自制的丁酸氯地平脂肪乳注射液与原研产品在比格犬体内的药代动力学参数,同时比较其生物等效性。实验以氨氯地平为内标,选取Phenomenex Luna C8色谱柱(2.0 mm×150 mm×5 μm),以甲醇-0.1%甲酸溶液(82∶18,V/V)为流动相,采用Waters Quattro Micro API的正离子检测方式,用MassLynx4.1软件进行数据处理。结果表明,丁酸氯维地平标准曲线的线性范围为0.4~100 μg/L。主要的药代动力学参数:参比制剂和试验制剂的Cmax平均值分别为(58.748±16.738) μg/L和(53.706±18.963) μg/L;Tmax分别为(2.938±0.678) μg/L和(2.875±0.991) μg/L;T1/2分别为(11.88±3.824) min和(11.587±3.634) min;AUC0→t分别为(1 883.821±647.882) μg·min/L和(1 856.541±590.653) μg·min/L;AUC0→∞分别为(1 889.834±649.135) μg·min/L和(1 863.485±592.039) μg·min/L。方差分析表明,这两种制剂的主要药动学参数之间无明显差异;双单侧t检验结果表明,两制剂在比格犬体内为生物等效制剂。
液相色谱-串联质谱(LC-MS/MS);丁酸氯维地平;药代动力学;生物等效性
围手术期急性高血压是手术治疗过程中常见的一种临床现象,是麻醉医生围手术期心电监测及治疗的重点。长期高血压会诱发患者其他脏器功能异常,严重者甚至会危及生命[1]。对于急性高血压的治疗,最好的方法是静脉内输注,这是因为注射液具有起效快、作用时间短、副作用较小、价格合理等特点[2]。丁酸氯维地平(cleviprex)是第3代新型短效二氢吡啶类钙通道拮抗剂,它不溶于水,结构中含有酯基,易发生水解反应,在血液和组织中酯酶的作用下能够迅速代谢成无活性的代谢产物,具有起效迅速、疗效可靠等特点,可以通过递增剂量准确地控制血压[3-4],2008年8月被FDA批准用于降低急性高血压。已有研究表明,与目前许多静脉注射后经肾和(或)肝代谢的抗高血压药不同,丁酸氯维地平在血液和组织中代谢,并不在体内蓄积,因此对急性及重度高血压疗效显著,但不得对豆类和鸡蛋过敏或脂质代谢异常的患者使用[5-6]。
本实验拟采用液相色谱-串联质谱(LC-MS/MS)法测定丁酸氯维地平在比格犬血浆中的浓度,用来研究自制的丁酸氯地平脂肪乳注射液与原研产品在比格犬体内的药代动力学参数,同时比较其生物等效性。
1 实验部分
1.1主要仪器与装置
Waters Quattro Micro API 三重四极杆串联质谱仪:美国Waters公司产品; GL-16G-Ⅱ型高速冷冻离心机,TDL-80-2B型低速台式离心机:上海安亭科学仪器厂产品;GL-88B型旋涡混合器:海门市其林贝尔仪器制造有限公司产品;BF-2000氮气吹干仪:北京八方世纪科技有限公司产品;AB135-S型电子分析天平:梅特勒-托利多仪器(上海)有限公司产品;GZX-9140MBE 数显鼓风干燥箱:上海博讯实业有限公司产品。
1.2主要材料与试剂
丁酸氯维地平对照品(批号1206629):含量99.98%,海南日中天制药有限公司产品;苯磺酸氨氯地平对照品(批号100374-201204):含量99.9%,由中国食品药品检定研究院提供。
甲醇:色谱纯,美国Sigma-Aldrich公司产品;甲酸:分析纯,天津市光复精细化工研究所产品;乙酸乙酯:分析纯,国药集团化学试剂有限公司产品;娃哈哈纯净水:分析纯,杭州娃哈哈集团有限公司产品。
8条比格犬:雌雄各半,由南京安立默科技有限公司提供。
1.3实验条件
1.3.1色谱条件色谱柱:Phenomenex Luna C8柱(2.0 mm×150 mm×5 μm);流动相:甲醇-0.1%甲酸溶液(82∶18,V/V);流速:0.2 mL/min;柱温:40 ℃;样品盘温度:4 ℃;进样量:20 μL。
1.3.2质谱条件离子源:ESI源;毛细管电压:3.5 kV;提取锥孔电压:3 V;射频透镜电压:0.3 V;源温度:130 ℃;溶剂温度:350 ℃;去溶剂气流速:600 L/h;锥孔气流速:60 L/h;正离子方式检测,选择反应监测(MRM)模式扫描;用于定量的离子分别为丁酸氯维地平的母离子m/z410.00和子离子m/z238.00;碰撞能量20 eV;锥孔电压20 V;内标:氨氯地平,母离子m/z479.08,子离子m/z361.00;碰撞能量20 eV;锥孔电压20 V。
1.4溶液的配制
1.4.1储备液的配制丁酸氯维地平储备液的配制:精确称取10.02 mg丁酸氯维地平对照品,置于10 mL棕色容量瓶中,用甲醇溶解并稀释至刻度,制得1 000 mg/L丁酸氯维地平储备液。先用甲醇将丁酸氯维地平储备液稀释至10 mg/L,再用甲醇依次稀释成浓度为1 000、500、250、100、50、25、10、4 μg/L的对照溶液,作为丁酸氯维地平标准曲线浓度点的储备液。另外,再取一定量的丁酸氯维地平储备液,用甲醇稀释成浓度为800、400、150、8 μg/L的溶液,作为质控样品的储备液;取一定量的丁酸氯维地平储备液,用甲醇稀释成浓度为3 200、1 500 μg/L的溶液,作为稀释准确度储备液。
内标氨氯地平储备液的配制:精确称取10.01 mg氨氯地平对照品,置于10 mL棕色容量瓶中,用甲醇溶解并稀释至刻度,得到1 000 mg/L氨氯地平储备液,再用甲醇稀释至500 μg/L,作为内标储备液。
1.4.2标准曲线的绘制分别量取20 μL不同标准曲线浓度的丁酸氯维地平储备液,依次配制成含待测物丁酸氯维地平血浆浓度为0.4、1、2.5、5、10、25、50、100 μg/L的样品,选择1.3.1节和1.3.2节条件进行测定,建立丁酸氯维地平的标准曲线。分别以待测物丁酸氯维地平浓度(x,μg/L)为横坐标,待测物丁酸氯维地平色谱峰面积(As)与内标氨氯地平色谱峰面积(Ai)的比值(y=As/Ai)为纵坐标,用加权(1/X2)最小二乘法进行线性回归运算,结果示于图1。
1.5比格犬血浆样品处理
采样时间点为0、0.5、1.0、1.5、2.0、3.0、4.0、5.0、10.0、20.0、30.0、45.0(给药结束),45.5、46.0、46.5、47.0、48.0、49.0、50.0、55.0、60.0、80.0、100.0、120.0 min,7天后采集交叉服药后比格犬的血浆。
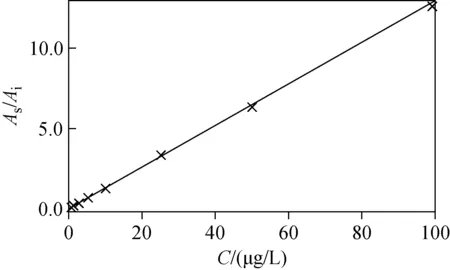
图1 丁酸氯维地平标准曲线Fig.1 Standard curve of clevidipine
精密量取200 μL 血浆样品,加入20 μL 2.5 mg/L 内标氨氯地平,混合均匀后加入500 μL水,再次混匀后加入4 mL乙酸乙酯,涡旋振荡1 min,以3 000 r/min离心10 min,定量移取3 mL上清液于试管中,用40 ℃氮气吹干;加入300 μL流动相复溶,涡旋振荡1 min,置于1.5 mL离心管中,以12 000 r/min离心5 min,取20 μL 上清液于进样瓶中,待测。
2 结果与讨论
2.1方法学考察
2.1.1专属性实验在ESI离子化方式下,丁酸氯维地平与内标氨氯地平主要生成[M+H]+母离子,分别为m/z479.08和m/z410。对母离子[M+H]+进行二级离子扫描,结果示于图2。丁酸氯维地平和内标氨氯地平生成的主要子离子分别为m/z361和m/z238,将它们作为定量分析时的监测离子。
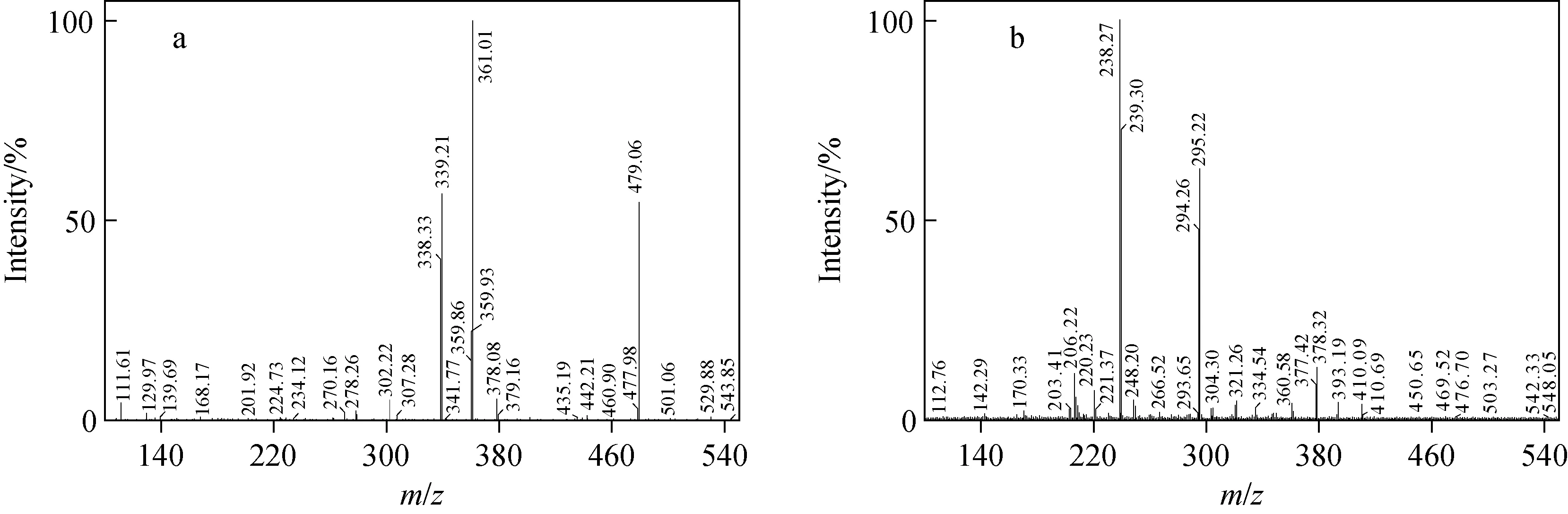
图2 丁酸氯维地平(a)与内标氨氯地平(b)[M+H]+的二级质谱图Fig.2 MS/MS spectra of [M+H]+ for clevidipine (a) and the internal standard amlodipine (b)
取200 μL 比格犬空白血浆,加入20 μL 标准工作液和内标溶液,然后向比格犬给药后的血浆样品中加入20 μL 内标,按1.5节方法处理,进样测定,其色谱图示于图3。

注:a.空白血浆;b.空白血浆+丁酸氯维地平;c.空白血浆+内标氨氯地平(500 μg/L);d.给药血浆+内标氨氯地平(500 μg/L)图3 比格犬血浆中丁酸氯维地平LC-MS/MS色谱图Fig.3 LC-MS/MS chromatograms of cleviprex in Beagle dogs plasma
可见,丁酸氯维地平的保留时间为2.98 min,氨氯地平的保留时间为1.55 min。这说明,比格犬血浆中的内源性物质不干扰丁酸氯维地平和内标氨氯地平的测定。
2.1.2最低检测限取20 μL 4 μg/L 的丁酸氯维地平储备液于具塞试管中,用40 ℃氮气吹干后,精密加入200 μL比格犬空白血浆,配制成0.4 μg/L 丁酸氯维地平血浆样品,按2.3节方法操作,进行6样本分析,定量下限(LLOQ)数据结果列于表1,其色谱图示于图4。
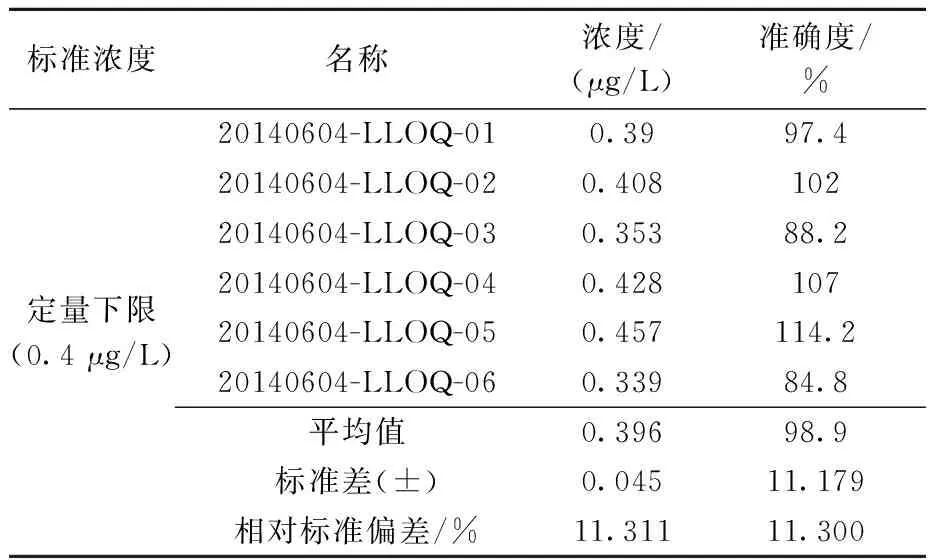
表1 丁酸氯维地平的定量下限准确度、均值及标准差
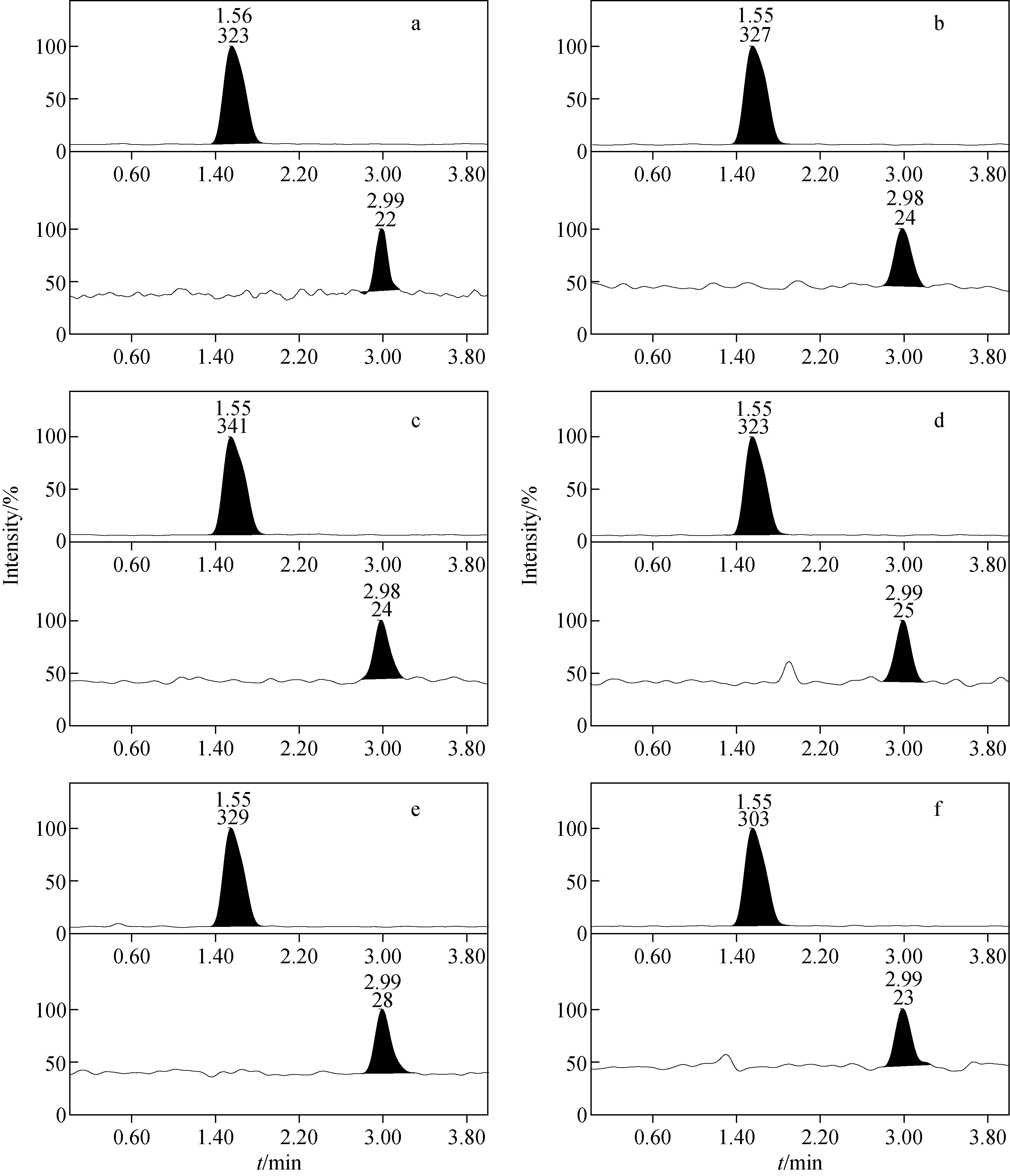
注:a.20140604-LLOQ-01;b.20140604-LLOQ-02;c.20140604-LLOQ-03;d.20140604-LLOQ-04;e.20140604-LLOQ-05;f.20140604-LLOQ-06图4 定量下限色谱图Fig.4 Chromatogram of LLOQ
由表1可以看出,丁酸氯维地平的准确度在真实浓度的80%~120%范围内,相对标准偏差(RSD)小于20%,说明丁酸氯维地平的定量下限为0.4 μg/L是精密可靠的。
2.1.3丁酸氯维地平随行质控样品的精密度和准确度为减少系统误差,在进行样品分析时,每天建立一条随行标准曲线计算血药浓度,并测定低、中1、中2、高4个浓度(丁酸氯维地平血药浓度分别为0.8、15、40、80 μg/L)的质控样品,确保所得到的药物浓度准确可靠,质控样品均匀分布在未知样品测试顺序中。质控样品数量及测定结果列于表2,其中丁酸氯维地平不合格的质控点为20140702-LQC-03和20140703-LQC-05,不合格率均为5%(不合格率为不合格点数占所分析批次质控点总数的比例)。本实验所得结果均符合《化学药物制剂人体生物利用度和生物等效性研究技术指导原则》中对质控样品数量、分布及结果的要求。
2.1.4精密度和准确度实验精密量取20 μL丁酸氯维地平低、中1、中2、高(8、150、400、800 μg/L)的质控对照溶液于具塞试管中,用40 ℃氮气吹干后,精密加入200 μL空白血浆,配制成丁酸氯维地平血浆浓度分别为0.8、15、40、80 μg/L的质量控制(QC)样品;按2.3节方法操作,每一浓度进行6样本分析,连续测定3天,根据当日的标准曲线,计算QC样品的测得浓度,根据其结果,计算本方法的精密度和准确度。结果表明,日内、日间相对标准偏差(RSD)均小于15%,准确度在85%~115%范围内(低浓度的准确度在80%~120%)。可见,血浆样品分析的精密度和准确度良好。
2.1.5提取回收率和基质效应实验分别精密加入20 μL浓度为8、150、400、800 μg/L丁酸氯维地平对照液和2.5 mg/L内标氨氯地平对照溶液于试管中,并精密量取200 μL比格犬空白血浆,加入500 μL纯净水,振荡涡旋10 s,再加入4 mL乙酸乙酯,振荡涡旋1 min,以3 000 r/min离心10 min,取3 mL上层清液于试管中,用40 ℃氮气吹干,加入300 μL流动相,涡旋混匀,以12 000 r/min离心5 min后,取20 μL上清液进样分析,得到丁酸氯维地平和内标氨氯地平的峰面积值APIT和ADIA。
精密量取200 μL比格犬空白血浆,加入500 μL纯净水,振荡涡旋10 s,再加入4 mL乙酸乙酯,振荡涡旋1 min,以3 000 r/min离心10 min,取3 mL上层清液于试管中,用40 ℃氮气吹干。分别精密加入20 μL浓度为8、150、400、800 μg/L丁酸氯维地平对照液和2.5 mg/L内标氨氯地平对照溶液于试管中,涡旋混匀,加入260 μL流动相,涡旋混匀,以12 000 r/min离心5 min后,取20 μL 上清液进样分析,得到丁酸氯维地平和内标氨氯地平的峰面积值BPIT和BDIA。
分别精密量取20 μL浓度为8、150、400、800 μg/L丁酸氯维地平对照液和2.5 mg/L内标氨氯地平对照溶液于试管中,用40 ℃氮气吹干,加入300 μL流动相,涡旋混匀,取20 μL上清液进样分析,得到丁酸氯维地平和内标氨氯地平的峰面积值CPIT和CDIA。
按:提取回收率/%=A/B×100%,基质效应/%=B/C×100%计算,得到丁酸氯维地平的提取回收率为89.553%~101.974%,内标氨氯地平的平均提取回收率为99.190%。丁酸氯维地平的基质效应范围为85.782%~89.656%,内标氨氯地平的平均基质效应为101.189%。
2.1.6稳定性实验取室温0 h、室温8 h和处理后放置20 h的丁酸氯维地平样品,反复冻融3次及长期冷冻20天,进行稳定性实验。结果表明:浓度为150、400、800 μg/L样品的RSD均小于15%,偏差小于15%,稳定性均在85%~115%之间;8 μg/L样品的RSD小于20%,偏差小于±20%,稳定性均在80%~120%之间。因此,可得出丁酸氯维地平含药血浆样品在室温放置8 h、处理后所得样品室温放置20 h,于-20 ℃冰箱中反复冻融3次,以及于-20 ℃长期冷冻20天条件下,样品稳定性较好。由于检测结果已表明,在-20 ℃条件下,丁酸氯维地平的血浆样品经反复冻融3次后,性质仍较为稳定,故本实验没有对冻融1、2次的样品(即1号、2号样)进行检测。
精密量取20 μL新鲜配制的低(8 μg/L)、中1(150 μg/L)、中2(400 μg/L)、高(800 μg/L)丁酸氯维地平对照储备液,与20 μL新鲜配制的500 μg/L内标氨氯地平储备液一同加入到试管中,然后加入260 μL流动相,混匀后取200 μL于进样瓶中,进样20 μL,得到相应的峰面积值。精密量取20 μL在-20 ℃条件下放置3天的低、中1、中2、高丁酸氯维地平对照储备液,与在-20 ℃条件下放置3天的20 μL内标氨氯地平储备液一起置于试管中,加入260 μL流动相,混匀,取200 μL于进样瓶中,进样20 μL,得到相应的峰面积值。将其与新鲜配制的结果相比较,考察储备液放置3天的稳定性。 结果表明,稳定性均在85%~115%之间,结果精密可靠。

2.2药动学结果
比格犬空腹口服受试制剂和参比制剂丁酸氯维地平脂肪乳注射液后,丁酸氯维地平的血药浓度C(μg/L)-时间t(min)曲线示于图5。
交叉给予8只比格犬两种制剂,注射过程比格犬血浆中丁酸氯维地平浓度结果列于表2。空腹静脉注射受试制剂(T)和参比制剂(R)后,丁酸氯维地平的ln(AUC(0-12))、ln(AUC(0-∞))、ln(Cmax)方差分析结果分别列于表3~6。

图5 给药后丁酸氯维地平受试制剂和参比制剂的血药浓度-时间曲线Fig.5 Plasma concentrations vs time curve of the test preparation and reference preparation for clevidipine after administration

药代参数实验制剂平均值实验制剂标准差变异系数参比制剂平均值参比制剂标准差变异系数Cmax/(μg/L)53.70618.9635.356.09815.57827.8tmax/min2.8750.99134.52.9380.67823.1t1/2/min11.5873.63431.411.883.82432.2AUC0→t/(μg·h/L)1856.54590.65331.81869.83639.95434.2AUC0→∞/(μg·h/L)1863.49592.03931.81875.84641.2534.2F104.130.429.2F为AUC0→t相对生物利用度F1104.330.529.2F1为AUC0→∞相对生物利用度
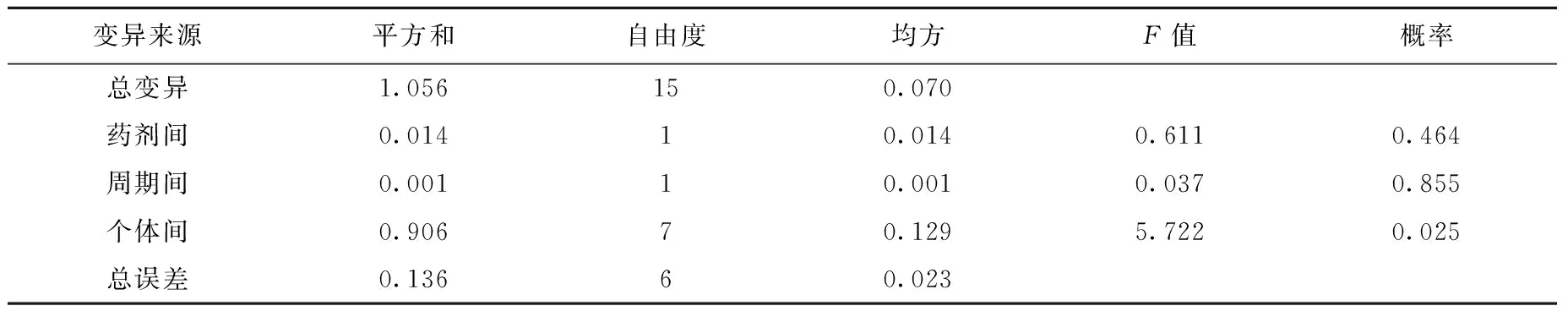
表4 丁酸氯维地平脂肪乳注射液和参比制剂lnCmax方差分析结果

表5 丁酸氯维地平脂肪乳注射液和参比制剂lnAUC0→t方差分析结果
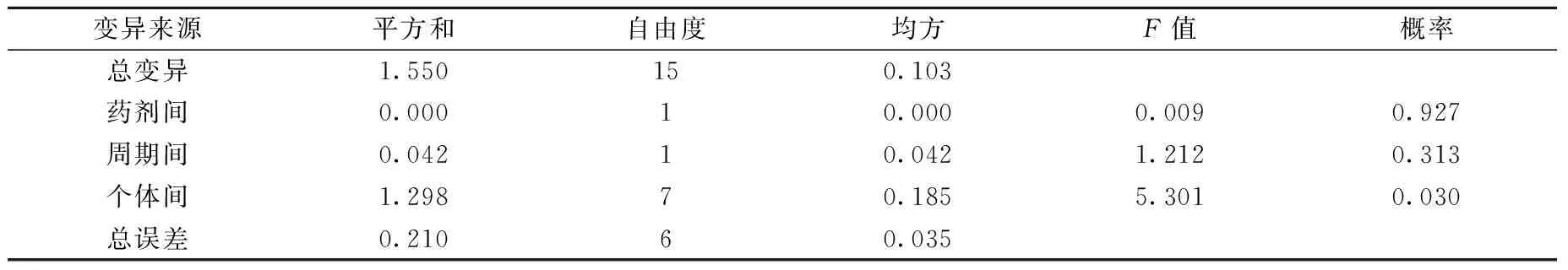
表6 丁酸氯维地平脂肪乳注射液和参比制剂lnAUC0→∞方差分析结果
以澳大利亚Medicines Company公司生产的丁酸氯维地平注射用乳剂(cleviprex)为参比制剂,自制的丁酸氯维地平脂肪乳注射液为受试制剂,对两者的AUC和Cmax(经对数转换)进行方差分析。结果表明,两制剂、两周期lnAUC0→t、lnAUC0→∞和lnCmax间无显著性差异。对两制剂lnAUC和lnCmax经双单侧t检验,计算得t1、t2均大于t(1-0.05)(6)=1.943,说明两制剂AUC和Cmax间等效。经Wilcoxon非参数检验证明两种制剂tmax等效。
2.3讨论
2.3.1流动相的选择最初,实验选用乙腈-0.1%甲酸溶液和甲醇-0.1%甲酸溶液作为流动相,发现甲醇-0.1%甲酸溶液作为流动相可以得到较好的峰形。之后,经调整甲醇与0.1%甲酸的比例,最终选用甲醇-0.1%甲酸溶液(82∶18,V/V)作为流动相。
2.3.2提取剂的选择分别考察了乙醚、正己烷、乙酸乙酯作为丁酸氯维地平的提取剂,其中乙酸乙酯的提取效果最好,提取回收率可达87.97%~95.10%,且峰形良好。
2.3.3定量下限的选择从本实验可以得出,LLOQ准确度在真实浓度的80%~120%范围内,相对标准偏差(RSD)小于20%,所以丁酸氯维地平的定量下限(LLOQ)为0.4 μg/L是精密可靠的。且本实验的LLOQ低于文献[7]中所提到的0.5 μg/L,更加精密准确。
3 结论
降低急性高血压的新制剂很少,许多药物虽然能够降低血压,然而,其中只有少数具有精确地控制急性高血压的能力。丁酸氯维地平具有独特的药效学和药代动力学性质,能够快速、安全和准确的降低高血压急症,具有独特的精确度,副作用小、用药剂量低。本实验验证了自制的丁酸氯维地平脂肪乳注射液与原研制剂在比格犬血浆内的主要药代动力学参数,发现二者无明显差异,在比格犬体内为生物等效制剂。
[1]贾新安. 围手术期高血压危险因素与防治[J]. 中外医疗,2012,31(6):107.
JIA Xin’an. The risk factors and prevention of hypertension in peri operation period[J]. China Foreign Medical Treatment, 2012, 31(6): 107(in Chinese).
[2]BERGESE S D, PUENTE E G. Clevidipine butyrate: A promising new drug for the management of acute hypertension[J]. Expert Opinion on Pharmacotherapy, 2010, 11(2): 281-295.
[3]NGUYEN H M, MA K D. Clevidipine for the treatment of severe hypertension in adults[J]. Clinical Therapeutics, 2010, 32(1): 11-23.
[4]KEATING G M. Clevidipine: A review of its use for managing blood pressure in perioperative and intensive care settings[J]. Drugs, 2014, 74(16): 1 947-1 960.
[5]王晓琳,栾瀚森,杨莉,等. 国外上市新型注射剂的研究进展[J]. 中国医药工业杂志,2012,43(1):60-67.
WANG Xiaolin, LUAN Hansen, YANG Li, et al. Progress in the research of the novel injections marketed abroad[J]. Chinese Journal of Pharmaceuticals, 2012, 43(1): 60-67(in Chinese).
[6]杨丽霞,全东琴,王涛. 丁酸氯维地平静脉脂肪乳剂的质量评价[J]. 现代生物医学进展,2013,13(7):1 272-1 277.
YANG Lixia, QUAN Dongqin, WANG Tao. Quality evaluation of clevidipine butyrate emulsion for intravenous injection[J]. Progress in Modern Biomedicine, 2013, 13(7): 1 272-1 277(in Chinese).
[7]WEI H, YUAN G, LIU Y, et al. Quantitation of clevidipine in dog blood by liquid chromatography tandem mass spectrometry: Application to a pharmacokinetic study[J]. Journal of Chromatography B, 2014, (971): 52-57.
Determination of the Concentrations of Butyric Acid Clevidipine in Beagle Dogs Plasma by LC-MS/MS
YANG Xin-yi1,2, TAO Chun-lei1,2, SHAO Feng1,2, WANG Hui1,2
(1.AnhuiUniversityofTraditionalChineseMedicine,Hefei230038,China;2.AnhuiWanBangMedicineCo.,Hefei230088,China)
Pharmacokinetic parameters of the cleviprex fat emulsion injection and original research products in beagle dogs plasma were identified by liquid chromatography-tandem mass spectrometry (LC-MS/MS). Taking amlodipine as internal standard, metabolites were separated on Phenomenex Luna C8(2.0 mm×150 mm×5 μm) column by the gradient elution with methanol-0.1% formic acid (82∶18,V/V) as mobile phase, and detected by positive ions electrospray ionization (ESI) mass spectrometry with fullscan-data dependent scan. Data was disposed through MassLynx4.1. The result shows that the linear range of cleviprex is 0.4-100 μg/L. The average values ofCmax,Tmax,T1/2, AUC0→tand AUC0→∞are (58.748±16.738) μg/L, (2.938±0.678) μg/L, (11.88±3.824) min, (1 883.821±647.882) μg·min/L, (1 889.834±649.135) μg·min/L for the reference preparation, respectively. While the average values ofCmax,Tmax,T1/2, AUC0→tand AUC0→∞are (53.706±18.963) μg/L, (2.875±0.991) μg/L, (11.587±3.634) min, (1 856.541±590.653) μg·min/L, (1 863.485±592.039) μg·min/L, for the test preparation, respectively. ANOVA and two one-sidedt-tests analysis show that there is no significant difference with the pharmacokinetic parameters of the two formulations, and they have bioequivalent in Beagle dogs plasma.
liquid chromatography-tandem mass spectrometry (LC-MS/MS); cleviprex; pharmacokinetics; bioequivalence
2015-07-13;
2015-10-06
杨欣怡(1992—),女(汉族),安徽蚌埠人,硕士研究生,药剂学专业。E-mail: lovejelly0111@gmail.com
陶春蕾(1971—),女(汉族),安徽灵璧人,副主任药师,从事新药研究与开发和药代动力学研究。
E-mail: 1225433686@qq.com
O657.63
A
1004-2997(2016)01-0147-09
10.7538/zpxb.youxian.2016.0008
网络出版时间:2016-01-19;网络出版地址:http:∥www.cnki.net/kcms/detail/11.2979.TH.20160119.0929.010.html

