辉瑞重磅新药palbociclib专利分析及其创新思考
冯超,杨德山,欧阳雪宇,孙海燕
·调查与研究·
辉瑞重磅新药palbociclib专利分析及其创新思考
冯超,杨德山,欧阳雪宇,孙海燕
Palbociclib(又名 PD-0332991),商品名 Ibrance,化学名 6-乙酰基-8-环戊基-5-甲基-2-((5-(哌嗪-1-基)吡啶-2-基)氨基)吡啶[2,3-d]嘧啶-7(8H)-酮,是一种口服的细胞周期蛋白依赖性激酶(CDK)4/6 抑制剂,主要通过抑制 CDK4/6活性来阻止细胞由生长期(G1期)进展到 DNA 复制期(S1期),进而阻断细胞 DNA 的合成,是美国辉瑞公司近来备受关注的最重要试验药物之一。2015 年 2 月 3 日,辉瑞公司宣布美国食品和药品管理局 (FDA)已经加速批准了 palbociclib 联合来曲唑作为以内分泌治疗为基础的一线疗法用于治疗未曾接受过系统治疗的雌激素受体阳性(ER+)、人表皮生长因子受体 2 阴性(HER2-)绝经期女性晚期乳腺癌,为 palbociclib 的最终上市扫清了障碍。一旦 palbociclib 获得批准上市,它将成为全球首个 CDK4/6激酶抑制剂,预计年销售值将达到 30 亿 ~ 50 亿美元,辉瑞公司也将借此率先撬开 CDK4/6 抑制剂市场[1-2]。本文通过对 palbociclib 在全球及中国的专利申请及保护情况进行分析,探寻辉瑞公司对 palbociclib 的专利申请策略,以及国内企业目前的研发方向,希望藉此能够为国内制药企业在 palbociclib 相关产品或同类药物的研发提供一些创新思路。
笔者以德温特世界专利索引数据库(WPI)、中国专利文摘数据库(CNABS)和国际联机检索系统(STN)数据库中涉及 palbociclib 的专利申请进行检索,并利用最早优先权日(OPD)、国际分类号(IPC)等字段对专利申请数据进行统计分析(将一个专利族视为一项专利申请)。
1 专利概况
1.1全球专利申请量趋势
截止到 2015 年 12 月 23 日,共检索得到涉及palbociclib 的专利申请 83项,首次申请出现在 2003 年(图 1)。从全球 palbociclib 专利申请量发展趋势可以看出,主要分为 2 个阶段:第 1 阶段为 2003 - 2010 年,这一阶段的专利申请量较少,且大部分涉及 palbociclib 的化合物相关专利。原研企业美国辉瑞公司作为沃尼尔·朗伯有限责任公司的母公司,是 palbociclib 原始专利申请的实际专利权人。在这一阶段辉瑞公司基本完成了 palbociclib核心基础专利在全球的布局,已在欧洲、日本、美国、中国、澳大利亚等国家和地区取得了关于化合物结构的专利权(表 1)。随着 palbociclib 在临床试验中治疗效果的突显,CDK4/6 抑制剂在乳腺癌治疗中的应用引起广泛关注,自2011 年起,涉及 palbociclib 的全球专利申请迅速高涨,进入了第 2 阶段发展期。
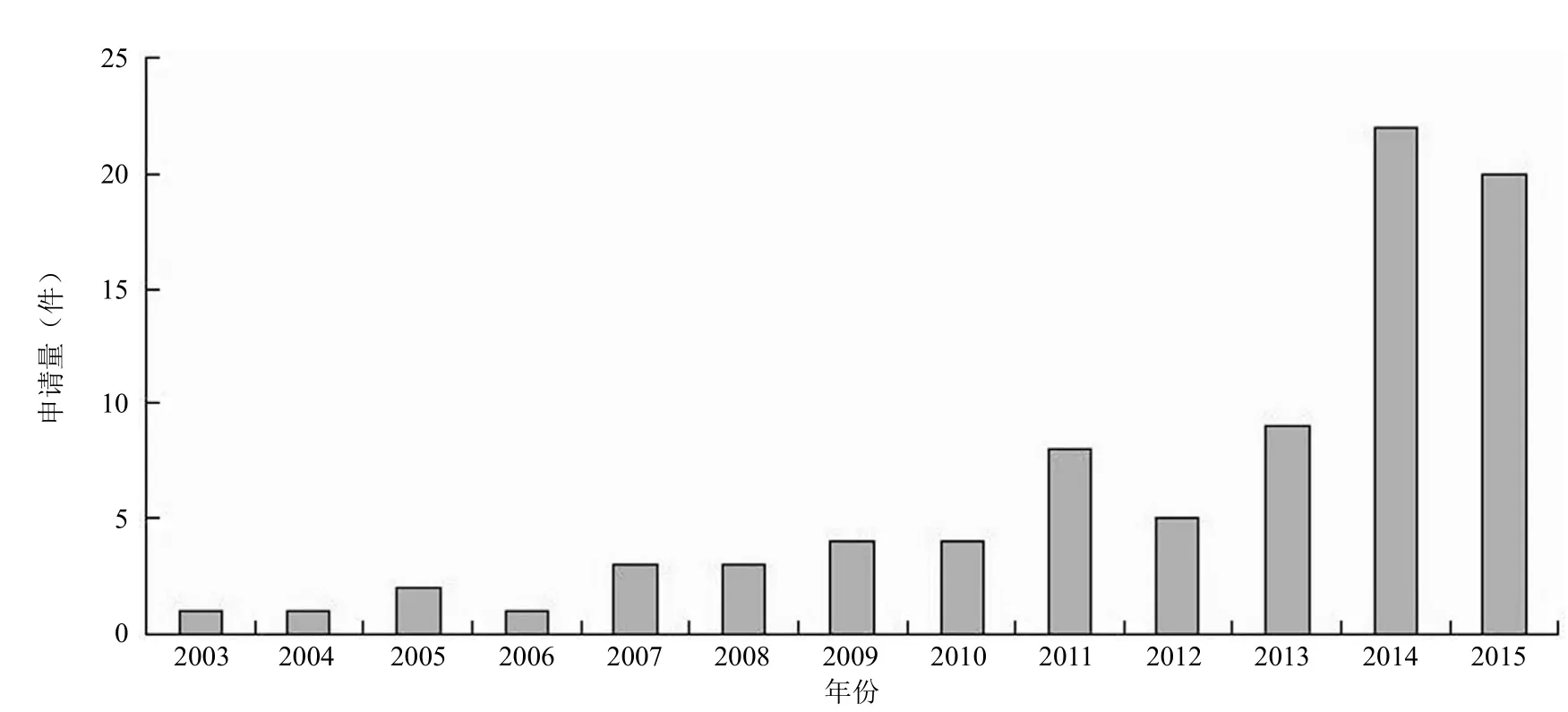
图1 Palbociclib 2003 - 2015 年的全球申请量
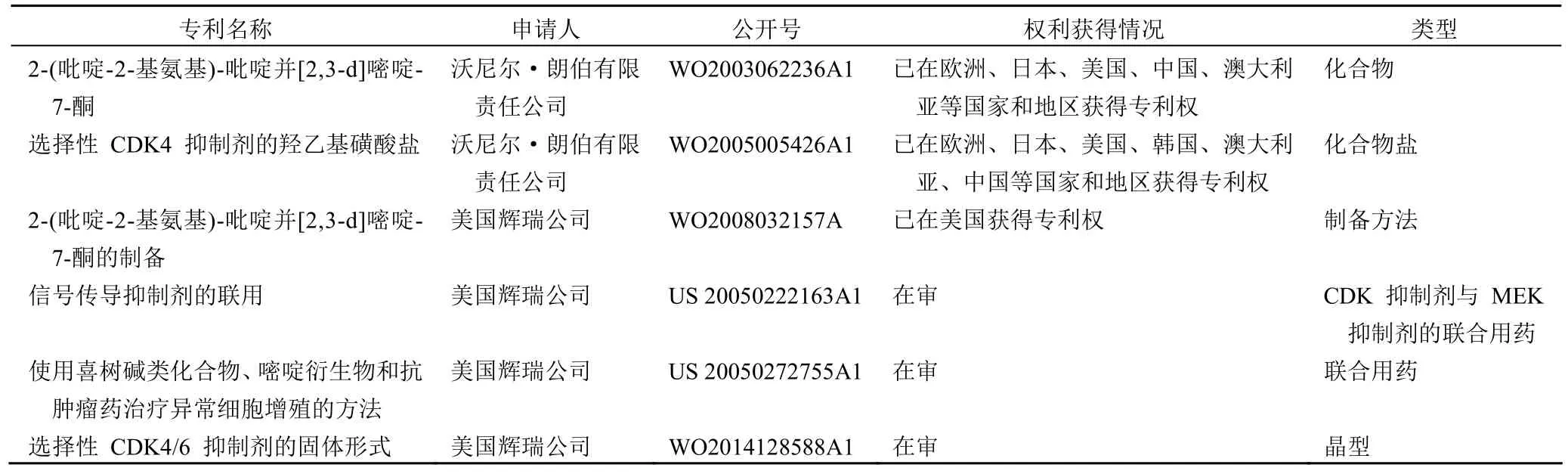
表1 辉瑞公司 palbociclib 的专利申请情况
1.2全球专利申请类型分布
除了原研企业在化合物、化合物盐、化合物制备方法以及晶型方面的专利申请之外,非原研企业,尤其是国外企业,则更倾向于以联合用药或组合物的形式将 palbociclib 作为抗癌药物的可选项纳入专利申请中或权利保护范围内,即,在技术主题涉及抗癌方法时,将 palbociclib 作为抗癌药物的一个具体种类限定到从属权利要求,与其他抗癌药构成组合物进行联合用药,这种方式可能实际投入的研究工作极少,仅仅是提及 palbociclib,并没有相应的试验予以验证联合用药产生的效果,但是这一举措却可能会对后续palbociclib 适应证或者组合物的扩展构成专利壁垒,对该专利布局的完整性产生巨大影响(图 2)。
1.3Palbociclib 基础专利在华分布
2004 年 7 月 22 日,palbociclib 化合物基础专利申请0380255.6 进入中国,开启了 palbociclib 基础专利在华的专利布局,该化合物基础专利申请已于 2011 年 2 月 12日被授予专利权,其保护范围主要包括 palbociclib在内的具有相同母核结构的近百个具体化合物及其在制备用于治疗哺乳动物由异常细胞增殖引起的障碍或病症的药物中的用途,以及包含上述具体化合物的药物组合物和 palbociclib药学上可接受的盐。Palbociclib 原研公司又分别于 2010 年8 月 16 日和 2011 年 4 月 27 日以 0380255.6 为母案提出分案申请 201010255766.6 和 201110115074.6,并已分别于 2013 年 4 月 25 日和 2013 年 9 月 3 日被授予专利权,其保护范围主要是具有 palbociclib 母核结构的马库什化合物及其在制备用于治疗哺乳动物由异常细胞增殖引起的障碍或病症的药物中的用途,以及包含上述马库什化合物的药物组合物。
Palbociclib 化合物基础专利申请进入中国国家阶段的同时,涉及 palbociclib 化合物盐的专利申请200480023494.X、涉及 palbociclib 制备方法的专利申请200780033416.1 以及涉及 palbociclib 晶型的专利申请201480009556.5 也陆续进入中国国家阶段,原研企业积极展开对 palbociclib 的在华专利布局。其中,涉及 palbociclib化合物盐的专利申请 200480023494.X 已于 2010 年 3 月24 日被授予专利权,其保护范围主要包括 palbociclib 的单-羟乙基磺酸盐及其制备方法,以及包含所述盐的药物制剂和该盐制备治疗哺乳动物中由异常细胞增殖、病毒或真菌感染引起的疾病或病症以及自身免疫疾病的药物的用途(表 2)。
由此可见,原研企业已取得 palbociclib 化合物及其单一衍生物盐在国内的专利权,虽然已授权专利中涉及了药物组合物、药物制剂和制药用途,但是保护范围宽泛,涉及与具体药物联用的药物组合物、涉及具体剂型的药物制剂、制备中间体、其他衍生物等的专利申请仍是空白,原研企业对palbociclib 的专利布局尚未完成。
1.4国内申请人对 palbociclib 的专利申请情况
与 palbociclib 化合物基础专利申请最早于 2011 年2 月 12 日获得专利权相比,直到 2014 年 palbociclib 才引起国内企业的广泛关注,自此以 palbociclib 为技术主题的专利申请不断涌现。从申请类型可以看出,与国外企业更倾向于以联合用药形式设立专利壁垒不同,国内企业提出的专利申请主要集中在 palbociclib 的制备方法方面,更注重对后续工业生产的研发和创新(表 3)。
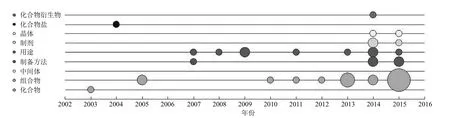
图2 Palbociclib 2003 - 2015 年的全球申请类型分布

表2 Palbociclib 原研公司 PCT 申请进入中国国家阶段的情况
2 创新思考
从以上对 palbociclib 专利情况的概述可以看出,对于palbociclib 的在华权利,目前,仅有原研企业涉及palbociclib 化合物及其羟乙基磺酸盐的专利授权,原研企业对 palbociclib 的制备方法没有获得专利权。其他涉及palbociclib 制备方法、制药用途、药物制剂以及晶型等的专利申请仍处于在审或者等待审查状态。因此,palbociclib 涉及制备方法、药物制剂、晶型、中间体、组合物等方面的在华专利权仍是空白。
对比化学药物从化合物到晶型、组合物的基础专利加上以新工艺和药物制剂为主的后续专利形成完整专利保护网的常见专利布局,palbociclib 专利布局还处于零星、松散的状态,尚且没有形成完整的保护网。由此,国内申请人可以从以下几个方面寻找创新入口:
2.1对已有结构的改造
对已有结构的改造,即开发所谓 me too 或 me better药物。自 palbociclib作为 CDK4/6 抑制剂引起业内巨大关注之后,诺华和礼来率先开发出了类似结构的 CDK4/6 抑制剂[3]。其中以诺华公司的 LEE011 与 palbociclib 结构最为接近,诺华通过变换酮基的位置、从吡啶环到吡咯环,以及从甲基到二甲氨基完成了对 palbociclib 的结构改造。对于礼来的 LY2835219 化合物来说,其改造位置也以吡啶环部分为主(图 3)。
诺华和礼来的做法为国内企业提供了一个不错的研发思路,即以相同作用机制或靶点为出发点,以 palbociclib 结构为模板进行结构改造。虽然可能在开发的过程中仍存在高投入和高风险的情况,但是经过结构改造的化合物最有可能绕开 palbociclib 的基础专利,后续的侵权风险最低。
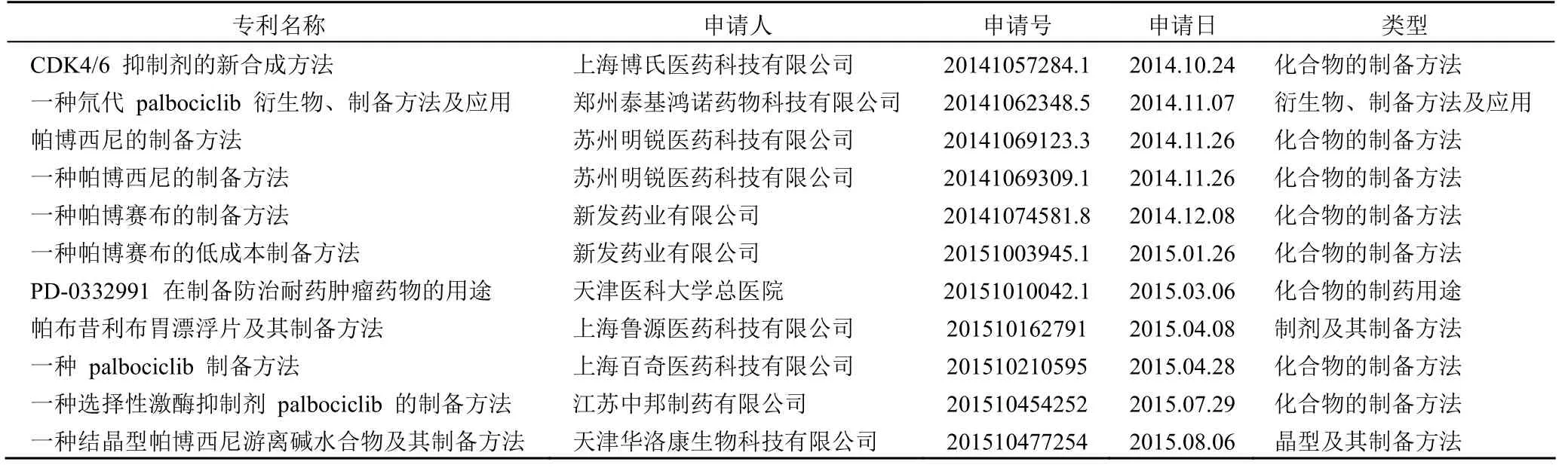
表3 国内企业 palbociclib 的专利申请情况
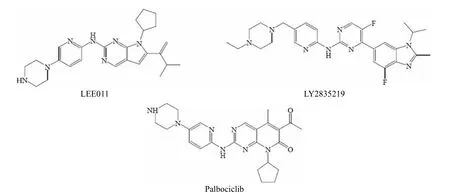
图3 Palbociclib、LEE011 和 LY2835219 的化学结构
2.2药物制剂的开发
以辉瑞另一重磅药物舍曲林为例,自上市销售到专利到期,涉及舍曲林的药物制剂专利从未停止过,从通过改进药物辅料提供常规制剂的稳定性等物理性质,到开发缓控释制剂,人们对药效的不断追求也为药物制剂的开发提供了源源不断的动力。从已授权的舍曲林化合物基础专利可以看出,辉瑞虽然在化合物基础专利中公开了一些常规制剂,但是,在后续专利布局中还会继续追加包括如口服制剂等常规制剂以及缓控释制剂在内的专利申请。
就 palbociclib 而言,在基础专利的说明书中记载了本发明还包含药物制剂,包括粉剂、片剂、丸剂等常规剂型,并且在实施例中制备得到了片剂和肠胃外制剂,但是尚且没有涉及 palbociclib 特定剂型的专利申请获得授权。目前,国内仅有上海鲁源医药科技有限公司于 2015 年 4 月8 日提出关于 palbociclib 胃漂浮片及其制备方法的专利申请,国内制药企业可以从改善稳定性、提高生物利用度、达到缓控释的释药特性等技术问题入手,通过开发新剂型、对药物辅料的筛选优化等方式获得新的药物制剂。由此可以大大降低研发风险和成本,弱化基础专利,在必要时可以与在先专利权人进行交叉许可或专利谈判,以有效地降低企业的许可和转让费用或者侵权风险。
2.3制备工艺的优化
Palbociclib 化合物基础专利 0380255.6 的说明书中公开了通式 I 化合物的合成路线,以及部分具体化合物的制备例,但是其权利要求书中并没有请求保护该制备方法。此后,辉瑞公司在 2007 年提出的制备方法专利申请中请求保护 2-(吡啶-2-基氨基)-吡啶并[2,3-d]嘧啶-7-酮的制备,但是其法律状态已为视为撤回。可见,palbociclib 的制备方法在华并未取得专利权。
由于多在确定活性化合物具有优异药效时提出相应的化合物专利申请,所以,化合物基础专利中公开的制备方法多数为仅在实验室规模上可合成该化合物的工艺路线。一旦药物上市销售,需要工业规模生产原料药时,基础专利中公开的制备方法往往不能胜任这一重要角色,那么此时,简化合成路线、提高终产品产率、降低生产成本,成为研发的重点以及专利申请的热点。对于 palbociclib,从首先提出申请的上海博氏医药科技有限公司,到新增的江苏中邦制药有限公司,都印证了这一研发思路。
2.4药用盐及其晶体
在药物原型化合物存在各种应用缺陷的情况下,开发可药用盐或各种晶型来改善各种理化性质或药代动力学性质是本领域技术人员常常采取的研发策略。以立普妥为例,立普妥在我国受保护的专利权是 1 晶型,但是辉瑞后续还申请了其他 20 多种晶型,这些晶体不一定是重点产品,但是却给国内企业的专利规避和仿制带来了很大的难度。
从辉瑞的申请情况可以看出,其专利申请策略从化合物基础专利到药用盐,再到制备方法和晶型,每一步都以化合物为基础向外延伸开,织成保护网将 palbociclib 多方面保护起来,在其他晶型和药用盐尚未有专利申请的情况下,国内企业还有机会打破辉瑞公司将来可能构建的专利网。例如,天津华洛康生物科技有限公司率先就结晶型 palbociclib游离碱水合物及其制备方法提出专利申请。
3 结语
基于上述分析可以看出,palbociclib 作为全球首个CDK4/6 抑制剂,其在全球以及国内的专利布局尚未完全建立起来。从专利申请策略上,国内企业在 palbociclib 已呈现出潜力巨大的市场前景之后才开始提出申请,其专利申请的速度远慢于国外企业,而且,专利申请的类型也呈现出较为单一的情况,主要集中在制备方法的开发和优化方面,这也从侧面反映出目前国内企业在研发策略和思路上的单一化。
随着 2015 年《国务院关于改革药品医疗器械审评审批制度的意见》的发布,提高仿制药质量、推进仿制药质量一致性评价将成为国内企业进行仿制药或改良型新药的研发所面临的巨大挑战。而研发质量与后续专利申请的质量以及最终专利权的稳定性又息息相关,研发质量的提高势必对专利申请的质量产生正向促进作用,从而提高授权的可能性,增强后续专利权的稳定性。为此,国内企业应当学习和借鉴国外企业成熟的研发策略和专利保护策略,从原研药的化学结构、作用机制、释药特性等方面出发,拓宽研发思路,例如,对已有结构进行改造获得疗效更显著的新药,与其他作用机制的药物联合用药达到协同增效作用,或者开发新型药物制剂提高生物利用度等,并以此展开外围专利布局,在研发的同时获得专利权,充分保护研发成果,以便在后续的市场竞争中占得一席之地。
[1] Ning CQ, Huang JS, Yu NF. A breackthrough: palbocilib. Anti-tumor Pharm, 2015, 5(2):81-82. (in Chinese)
宁澄清, 黄健升, 余聂芳. “突破性进展”药物Palbociclib. 肿瘤药学,2015, 5(2):81-82.
[2] Wang SS, Yu HY. Palbociclib in combination with letrozole versus letrozole alone as first-line treatment of oestrogen receptor positive,HER2-negative, advanced breast cancer significantly improve progression-free survivial. J Evid Based Med, 2015, 15(3):146-148. (in Chinese)
王树森, 余鸿雁. Palbociclib联合来曲唑一线治疗ER阳性、HER2阴性进展期乳腺癌能显著提高无进展生存期. 循证医学, 2015,15(3):146-148.
[3] Liu S, Xu J, Cui Y, et al. Palbociclib—a new drug approved for advanced breast cancer. Prog Pharm Sci, 2015, 39(8):634-640. (in Chinese)
刘恕, 徐军, 崔毅, 等. 抗乳腺癌新药palbociclib. 药学进展, 2015,39(8):634-640.
10.3969/j.issn.1673-713X.2016.04.018
100190 北京,国家知识产权局专利局专利审查协作北京中心医药部
冯超,Email:fengchao_3@sipo.gov.cn
2016-04-12

