基于4,8-双(TIPS)苯并二噻吩和异靛蓝交替共聚物的合成及表征*
徐兴华,王建龙,同军锋
(兰州交通大学光电技术与智能控制教育部重点实验室,甘肃 兰州 730070)
基于4,8-双(TIPS)苯并二噻吩和异靛蓝交替共聚物的合成及表征*
徐兴华,王建龙,同军锋
(兰州交通大学光电技术与智能控制教育部重点实验室,甘肃兰州730070)
通过Stille偶联法合成了窄带隙异靛蓝基交替共聚物:聚[4,8-双(三异丙基硅乙炔基)苯并[1,2-b:4,5-b′]二噻吩-2,6-二基-alt-N,N′-(2-己基癸基)异靛蓝-6,6′-二基] (PBDT-TIPS-IDC16)。其在300~730 nm范围内对太阳光有吸收,光学带宽约1.66 eV。用PBDT-TIPS-IDC16作给体、PC61BM作受体、Ca/Al为阴极制备了本体异质结聚合物太阳能电池。在AM 1.5 G,100 mW·cm-2光照条件下,当活性层给/受体质量比为1:2时,器件能量转化效率为0.03%,开路电压、短路电流密度和填充因子分别为0.63 V、0.14 mA·cm-2和29.38%。空间电荷限制电流法测得空穴和电子迁移率分别为1.2×10-7和6.4×10-5cm-2·V-1·s-1。
异靛蓝;窄带隙;共轭聚合物;光伏性能;空间限制电流法
本体异质结型聚合物太阳能电池(PSCs)倍受学术界和产业界的广泛关注,是因其具有可大面积卷对卷加工、质量轻、低成本和化学结构多样性等优势[1-2]。近年来,通过材料设计优化[3-4]和器件制备工艺的改进[5],PSCs发展非常迅速。研究表明,要进一步提高PSCs的能量转换效率(PCE),最重要的策略是通过在聚合物主链结构中引入给体-受体(D-A)交替单元,调节给体单元或受体单元来改善共聚物的光电性能。
异靛蓝(isoindigo, ID)拥有两个2-吲哚酮单元,构成了一个对称性的平面π共轭结构。其所拥有两个强吸电子的内酰胺基团,使得整个ID单元高度的缺电子和高的电子亲和势[6-8]。自从2010年,Mei等[9]首次将异靛蓝小分子用作给体光伏材料以来,异靛蓝被广泛用作电子受体单元构筑共轭聚合物。截至目前,用于太阳能电池的能量转化效率(PCE)已超过8%[10]。2011年,上海交通大学的Zhang等[11]报道三个含ID的D-A聚合物PTT-ID、PT-ID和PBDT-ID,通过改变给电子单元部分,实现了PCE为1.91%的光伏器件。瑞典查尔姆斯理工大学的Wang等[12]设计并合成了一个三联噻吩和ID的聚合物P3TI,其光学带隙仅为1.5 eV,基于P3T1和PC71BM的器件效率达到6.3%。2014年,国立台湾大学的Ho等[13]进一步研究齐聚噻吩单元nT与ID的聚合物PnTI,证实P6TI的PCE可达7.2%。接着中科院长春应化所Deng等[10]设计了二噻并咔唑(DTC)与氟代ID的共聚物,实现8.2%的倒置型光伏器件。
将具有大体积的三异丙基硅乙炔基(TIPS)接入到苯并二噻吩(BDT)骨架上不仅可增强聚合物的溶解性、结晶性能和氧化稳定性,还可促进相邻共轭分子的π-轨道重叠[14-15]。2012年韩国的Kim等将TIPS和4-辛基苯乙炔基作为侧链接入到BDT上制备了共聚物,发现引入TIPS可使聚合物HOMO能级降至-5.4 eV,实现了PCE为4.61%光伏器件[16]。我们课题组通过引入不同侧链到二噻并苯并二噻吩(DTBDT)上,发现引入TIPS可有效地降低HOMO能级从而提高开路电压,同时明显改善空穴迁移率,获得了6.4%电池器件[17]。
鉴于ID单元具有刚性的共平面结构、高的光吸收系数和高的迁移率等优良特性和BDT单元的小位阻、高电荷迁移率的优势以及TIPS单元可有效降低材料的HOMO能级和改善材料的溶解性和稳定性的特点,在前面研究基础上[18],选用BDT-TIPSSn与6,6′-二溴-N,N′-(2-己基癸基)异靛蓝(IDC16Br2)通过Stille法共聚,制备了窄带隙交替共聚物PBDT-TIPS-IDC6。其在300~730 nm范围对太阳光有吸收,光学带宽约1.66 eV,HOMO和LUMO能级分别为-5.74和-4.08 eV。当PBDT-TIPS-IDC16:PC61BM共混质量比为1:2(添加3%DIO)时,本体异质结太阳能电池PCE约0.03%,VOC为0.63 V,JSC为0.14 mA·cm-2。
1 实 验
1.1试剂与仪器
6-溴靛红和6-溴-吲哚-2-酮购自北京偶合科技有限公司。其它化学试剂除非特别说明,均购自百灵威、Aldrich、Acros和TCI。溶剂按照标准溶剂处理程序纯化。所有反应均在N2氛围下进行。单体2,6-双(三甲基锡)-4,8-双(三异丙基硅乙炔基)苯并[1,2-b:4,5-b′]二噻吩(BDT-TIPSSn)[18]、1-溴-2-己基癸烷[19]和6,6′-二溴异靛蓝(IDBr2)[9]按照相应的文献合成,且在使用前经1H NMR分析。
1H NMR在Bruker DRX 400核磁谱谱仪上测定,以四甲基硅烷(TMS)为内标物;分子量及分子量分布采用Waters 2410凝胶色谱仪测量,以线性聚苯乙烯为标准样,THF为洗脱剂;紫外-可见吸收光谱在岛津UV2500紫外分析仪上测量;电化学循环伏安曲线测定采用上海辰华CHI660电化学工作站和三电极体系,在0.1 mol·L-1的四丁基六氟磷酸铵(Bu4NPF6)的乙腈溶液中,将聚合物溶液滴到铂碳电极晾干成膜用作工作电极,铂丝作对电极,Ag/AgNO3为参比电极,且整个测试在室温环境下进行,扫描速度为50 mV/s。工作电极在使用前经氧化铝悬浮液抛光并用丙酮洗涤。
1.2光伏器件的制备与表征
本实验采用的器件结构是ITO/PEDOT:PSS(40 nm)/聚合物:PC61BM(80 nm)Ca/Al(100 nm),其中PEDOT:PSS为阳极修饰层,Polymer:PC61BM为活性层。器件的工艺过程为:将ITO玻璃依次用ITO清洗液、丙酮、去离子水,异丙醇各超声清洗10 min,最后用氮气吹干,然后将ITO基板进行臭氧等离子体处理10 min。处理完成后,在其上旋涂约40 nm厚的空穴传输层PEDOT:PSS,将旋涂好的基片在160 ℃条件下烘烤20 min。随后用旋涂仪将聚合物浓度为10 mg·mL-1的Polymer:PC61BM氯苯溶液(CB)在设备上制备约80 nm厚的Polymer:PC61BM光活性层,将旋涂好的基片在150 ℃条件下退火20 min。然后在真空度优于6×10-6Pa的条件下依次蒸镀Ca(8 nm)和Al(100 nm)电极。活性层的有效面积为10 mm2。光源采用日本SAN-EI生产的AAA模拟太阳光源,AM 1.5 G环境下白光,照射光强为100 mW·cm-2。薄膜厚度使用美国Bruker detakxt台阶仪测得。器件的电流-电压特性曲线(J-V曲线)由AM 1.5 G (100 mW·cm-2)模拟太阳光源和Keithley2400测量得到,外量子效率(IPCE)由北京赛凡光电XES-70S1测得。
1.3单体合成
(1) 6,6′-二溴-N,N′-(2-己基癸基)异靛蓝(IDC16Br2)[20]
称取IDBr2(1.00 g, 2.38 mmol)、无水K2CO3(1.64 g, 11.88 mmol)和25 mLN,N′-二甲基甲酰胺(DMF)加入到250 mL 三口烧瓶中,氩气下升温至100 ℃。反应2 h后,将10 mL DMF溶解的1-溴-2-己基癸烷(2.98 g, 9.77 mmol)用注射器缓慢滴加到反应体系中,反应约12 h。待反应液冷却到室温后,倾入到400 mL冰水中,氯仿萃取三次,水洗后无水Na2SO4干燥。蒸除溶剂后,粗产物用硅胶层析柱(200~300目)提纯,洗脱剂为石油醚:二氯甲烷=5:1(体积比),得红色固体(1.30 g,产率:62.8%)。1H NMR (CDCl3, 400 MHz), δ (ppm): 9.06 (d,3J=8.4 Hz, 2H), 7.14 (d,3J=8.4 Hz, 2H), 6.86 (s, 2H), 3.62 (d,3J=7.2 Hz, 4H), 1.88 (br, 2H), 1.31~1.25 (m, 48H), 0.89 (t,3J=5.2 Hz, 12H)。
(2)聚合物PBDT-TIPS-IDC16的合成
称取BDT-TIPSSn (200.0 mg, 0.228 mmol)、IDC16Br2(198.11 mg, 0.228 mmol)、Pd2(dba)3(1.5 mg)、P(o-tol)3(2.5 mg)加入到10 mL聚合瓶中,量取6 mL脱气甲苯和0.5 mL新蒸DMF加入聚合体系,用氩气给聚合溶液鼓泡约15 min。在氩气保护下,升温至105 ℃反应48 h。然后加入20 mg 2-三(正丁基锡基)噻吩、4 mg Pd(PPh3)4,105 ℃反应8 h后,接着再加入0.2 mL 2-溴噻吩、4 mg Pd(PPh3)4,105 ℃反应8 h。反应结束后,将反应瓶中的混合物滴入300 mL甲醇中,有沉淀析出。将抽滤得到的沉淀依次用乙醇、丙酮、正己烷、二氯甲烷、甲苯抽提。将甲苯抽提的溶液浓缩至8 mL,滴入200 mL 甲醇中,抽滤得褐色沉淀物,经真空干燥得到目标聚合物PBDT-TIPS-IDC16 (198 mg,产率69%)。Mn=17000 g/mol, (PDI=2.21)。1H NMR (CDCl3, 400 MHz), δ(ppm): 9.28~9.02 (m, 2H), 7.90~7.40 (d, 2H), 7.19~6.60 (m, 4H), 4.19~3.62 (m, 4H), 2.03~1.95 (br, 2H), 1.70~0.95 (m, 90H), 0.82 (br, 12H)。
2 结果与讨论
2.1聚合物的合成与表征
单体双锡BDT-TIPSSn[18]和二溴物IDC16Br2[20]按照相应的文献合成,如图1所示,PBDT-TIPS-IDC16则由BDT-TIPSSn和二溴物IDC16Br2在催化剂Pd2(dba)3、P(o-tol)3作用下通过Stille偶联反应制得。反应结束后依次加入2-三(正丁基锡基)噻吩、2-溴噻吩及催化剂Pd(PPh3)4反应,目的是为了除去反应体系中残留的端基溴和三甲基锡从而提高聚合物的稳定性[21]。聚合物在室温下溶解性都较好,室温下可溶于氯仿、THF、甲苯和氯苯等溶剂。经GPC测定的数均分子量(Mn)和分子量分布指数(PDI)分别为:17000 g/mol、2.21。其5%的失重温度为385 ℃(图2),说明该材料应用于聚合物太阳能电池具有足够的热稳定性。
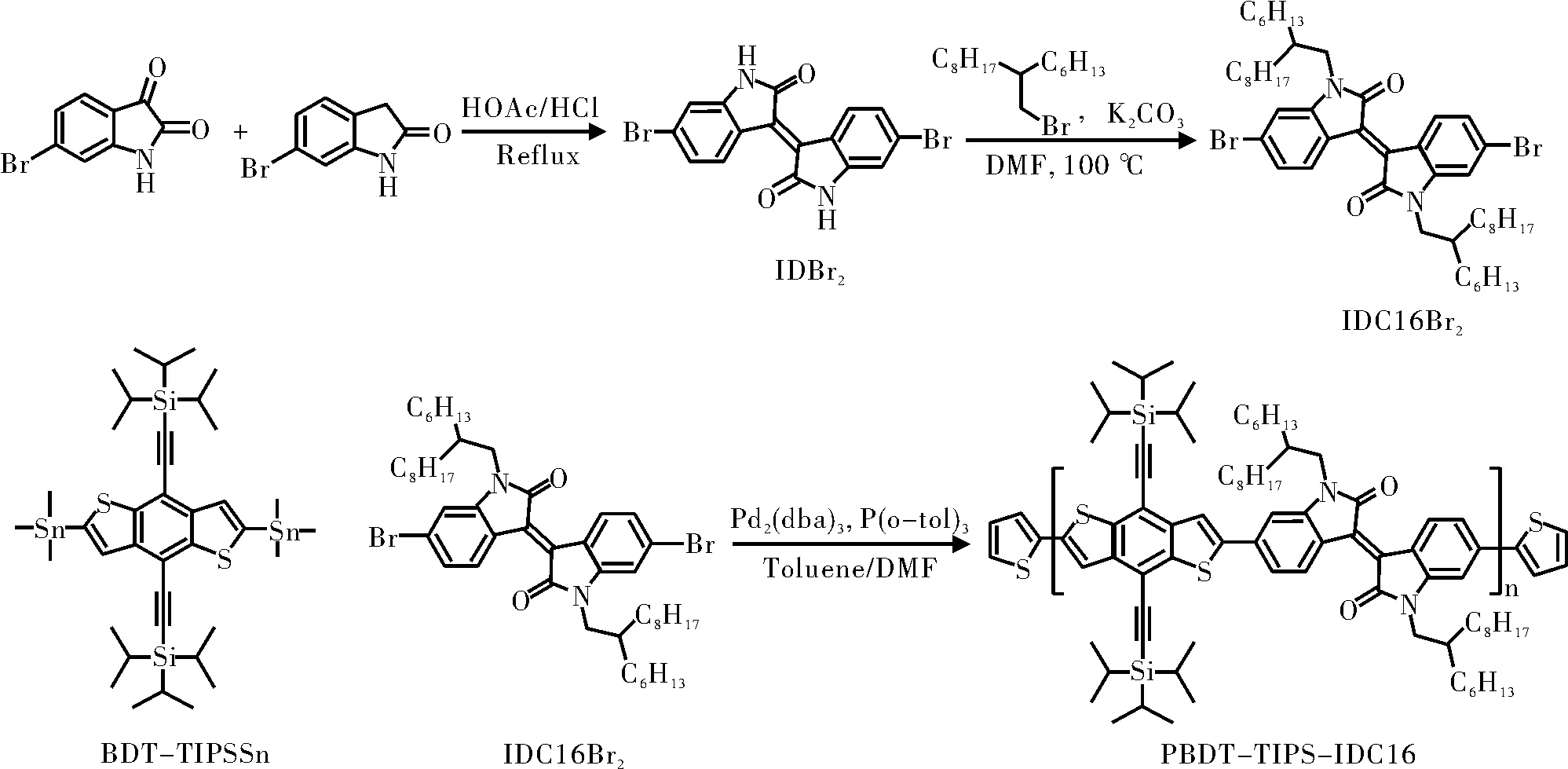
图1 聚合物PBDT-TIPS-IDC16的合成路线图
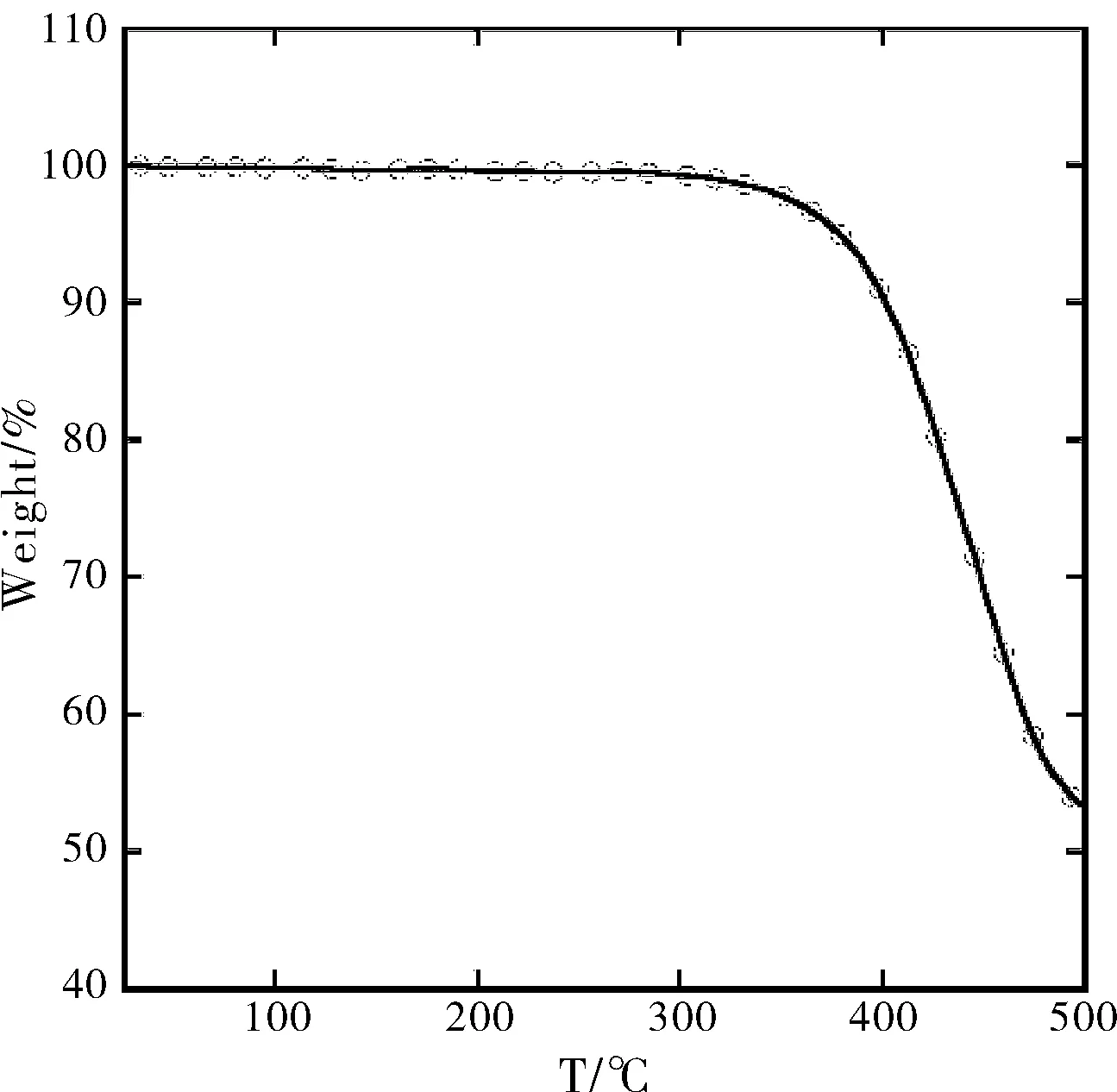
图2 聚合物PBDT-TIPS-IDC16的热重分析曲线
2.2聚合物的光学、电学性质
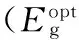
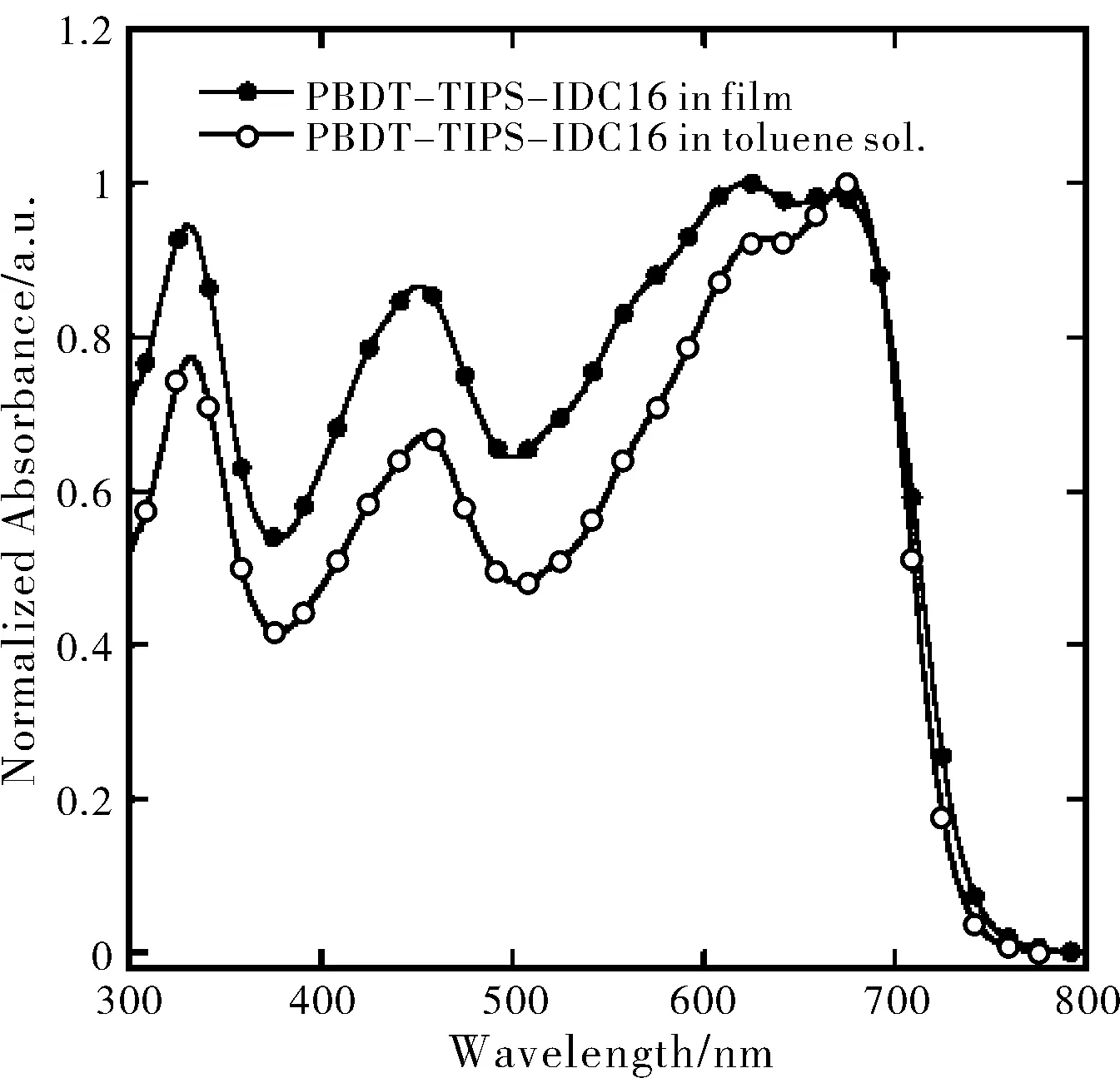
图3 聚合物PBDT-TIPS-IDC16的吸收光谱
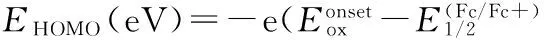
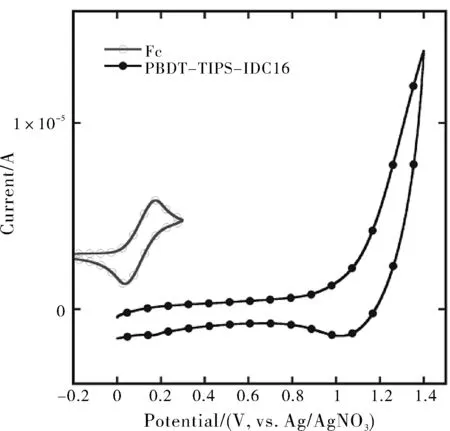
图4 聚合物PBDT-TIPS-IDC16的循环伏安曲线
2.3光伏性能研究
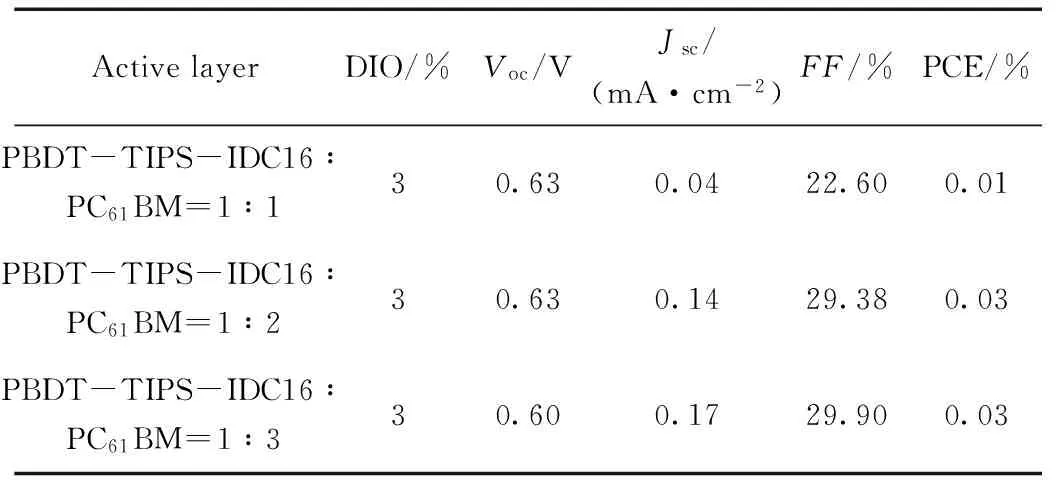
表1 聚合物PBDT-TIPS-IDC16的光伏特性
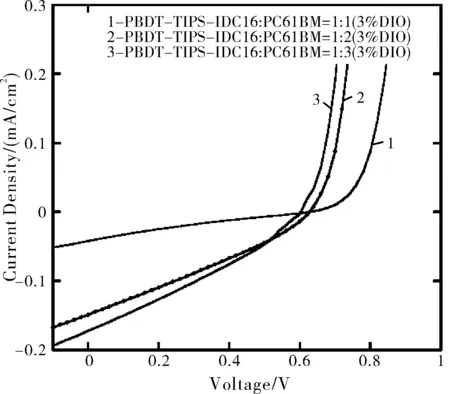
图5 基于聚合物PBDT-TIPS-IDC16的光伏电池J-V曲线
为了考察其光伏性能,我们用PBDT-TIPS-IDC16为给体、PC61BM为受体、给/受体质量比依次为1:1、1:2、1:3,Ca/Al为阴极制备了本体异质结光伏器件,基本结构为ITO/PEDOT:PSS/聚合物:PC61BM/Ca/Al,共混层薄膜的制备过程使用了3%(体积)的1,8-二碘辛烷(DIO)作添加剂。其J-V曲线如图3所示,器件数据列于表1。当共混活性层PBDT-TIPS-IDC16:PC61BM比例从1:1变化到1:2再到1:3时,开路电压(VOC)从0.63 V降至0.60 V;短路电流密度(JSC)从0.04 mA·cm-2升高到0.17 mA·cm-2;填充因子(FF)从22.60%升至29.90%;器件的PCE从0.01%升至0.03%。
2.4聚合物PBDT-TIPS-IDC16的载流子迁移率
聚合物PBDT-TIPS-IDC16的载流子(空穴、电子)迁移率采用空间电荷限制电流(SCLC)的方法测试。根据Mott-Gurney公式[23]计算出PBDT-TIPS-IDC16的空穴或电子迁移率。
(1)
式中:J是电流,μ表示零场下的载流子迁移率,ε0为真空介电常数(ε0=8.85×10-12F·m-1),εr为有机半导体相对介电常数(εr=3),d表示有机层厚度,V是聚合物层的有效电压,由器件的施加电压(Vappl)减去器件的内建电场电压(Vbi)和器件其它层电阻的电压降(Vs):V=Vappl-Vbi-Vs。器件的迁移率可由通过J1/2-V曲线的斜率计算求得。为了测试空穴迁移率(μh),制备空穴器件。结构为:ITO/PEDOT:PSS/polymer/MoO3/Al。图6为SCLC法测得空穴器件的J-V曲线和J1/2-V曲线。由式(1)和图6计算出PBDT-TIPS-IDC16的μh=1.2×10-7cm-2·V-1·s-1。
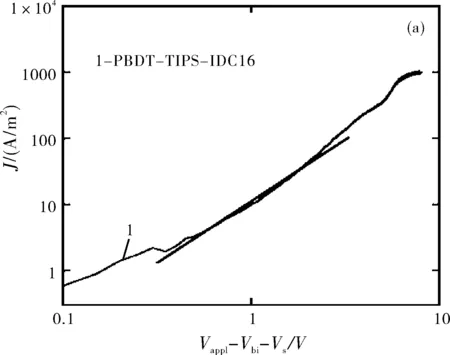

图6 SCLC法测量空穴器件的J-V曲线(a)和J1/2-V曲线(b)
为了测量电子迁移率(μe),制备电子器件。结构为:ITO/Al/polymer/Al。由式(1)和图7可得其μe=6.4×10-5cm-2·V-1·s-1。
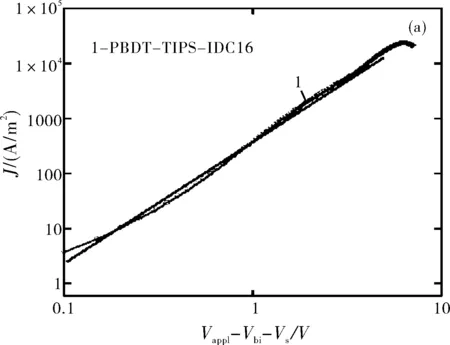
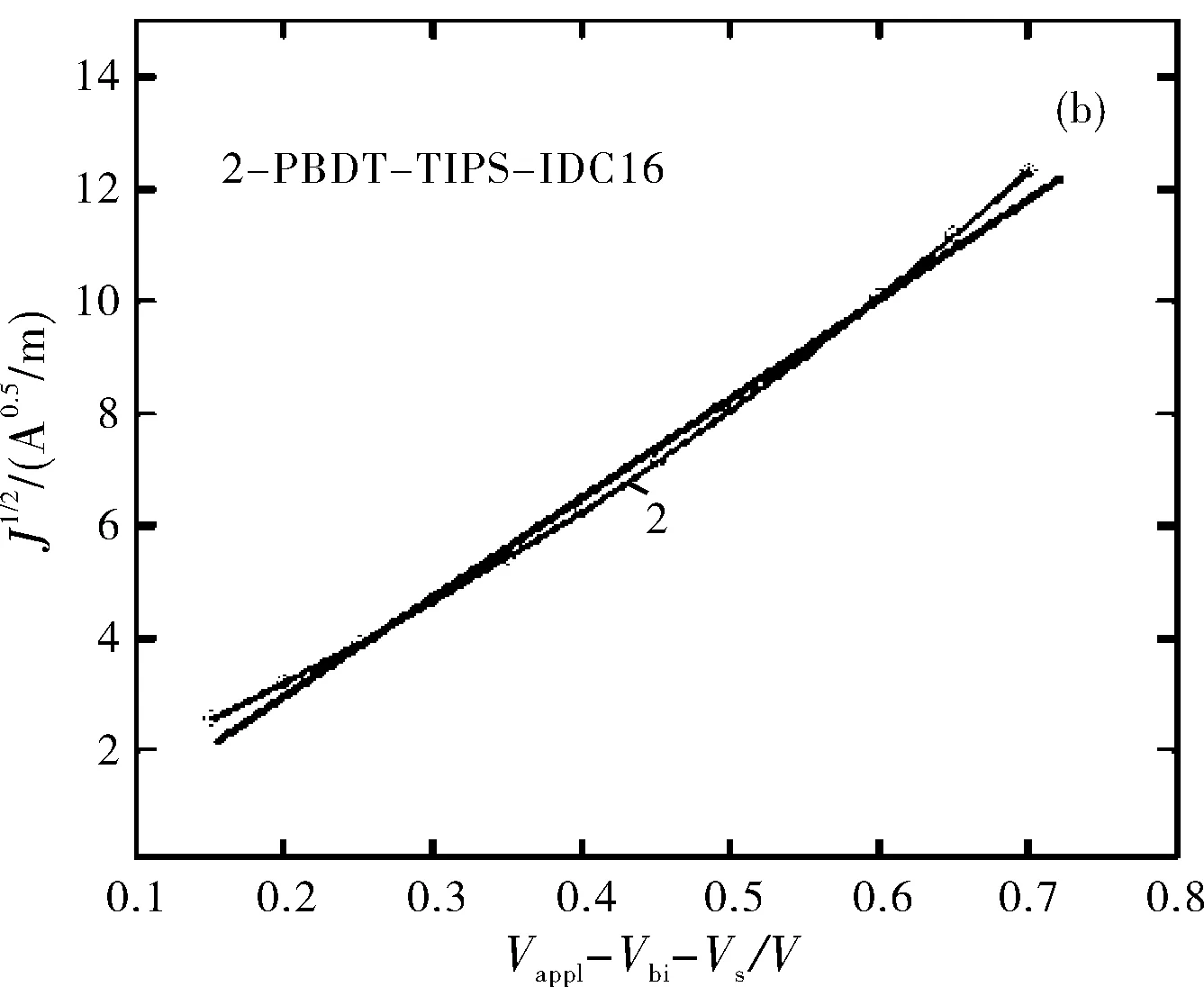
图7 SCLC法测量电子器件的J-V曲线(a)和J1/2-V曲线(b)
3 结 论
本文成功合成了窄带隙交替共聚物PBDT-TIPS-IDC16。其在300~730 nm范围对太阳光有吸收,光学带宽约1.7 eV,HOMO能级约-5.74 eV。在AM 1.5 G,100 mW·cm-2光照条件下,当活性层给/受体质量比为1:2时,PCE仅0.03%,VOC、JSC和FF依次为0.63 V、0.14 mA·cm-2和29.38%。SCLC法测得空穴和电子迁移率分别为1.2×10-7和6.4×10-5cm-2·V-1·s-1。
[1]Li G, Zhu R and Yang Y. Polymer solar cells[J]. Nat. Photonics, 2012(6):153-161.
[2]Li Y. Molecular design of photovoltaic materials for polymer solar cells: toward suitable electronic energy levels and broad absorption[J]. Acc. Chem. Res., 2012, 45(5):723-733.
[3]Liang Y, Feng D, Wu Y, et al. Highly efficient solar cell polymers developed via fine-tuning of structural and electronic properties[J]. J. Am. Chem. Soc., 2009, 131(22):7792-7799.
[4]Wang M, Hu X, Liu P, et al. Donor-acceptor conjugated polymer based on naphtho[1,2-c:5,6-c]-bis[1,2,5]thiadiazole for high-performance polymer solar cells[J]. J. Am. Chem. Soc., 2011, 133(25):9638-9641.
[5]Blouin N, Michaud A, Gendron D, et al. Toward a rational design of poly(2,7-carbazole) derivatives for solar cells[J]. J. Am. Chem. Soc., 2008, 130(2):732-742.
[6]Stalder R, Mei J, Graham, K R, et al. Isoindigo, a versatile electron-deficient unit for high-performance organic electronics[J]. Chem. Mater., 2014, 26:664-678.
[7]Wang E., Mammo W. and Andersson M. R. 25th Anniversary article: isoindigo-based polymers and small molecules for bulk heterojunction solar cells and field effect transistors[J]. Adv. Mater., 2014, 26:1801-1826.
[8]Deng P Zhang Q. Recent developments on isoindigo-based conjugated polymers[J]. Polym. Chem., 2014, 5:3298-3305.
[9]Mei J, Graham K R, Stalder R, et al. Synthesis of isoindigo-based oligothiophenes for molecular bulk heterojunction solar cells[J]. Org. Lett., 2010, 12:660-663.
[10]Deng Y, Liu J, Wang J, et al. Dithienocarbazole and isoindigo based amorphous low bandgap conjugated polymers for efficient polymer solar cells[J]. Adv. Mater., 2014, 26:1801-1826.
[11]Zhang G, Fu Y, Xie Z, et al. Synthesis and photovoltaic properties of new low bandgap isoindigo-based conjugated polymers [J]. Macromolecules, 2011, 44(6): 1414-1420.
[12]Wang E, Ma Z, Zhang Z, et al. An easily accessible isoindigo-based polymer for high-performance polymer solar cells[J]. J. Am. Chem. Soc., 2011, 133:14244-14247.
[13]Ho C C, Chen C A, Chang C Y, et al. Isoindigo-based copolymers for polymer solar cells with efficiency over 7%[J]. J. Mater. Chem. A, 2014, 2:8026-8032.
[14]Shi Q, Fan H, Liu Y, et al. A copolymer of benzodithiophene with TIPS side chains for enhanced photovoltaic performance[J]. Macromolecules, 2011, 44(23):9173-9179.
[15]Kim J H, Song C E, Shin N, et al. High-crystalline medium-band-gap polymers consisting of benzodithiophene and benzotriazole derivatives for organic photovoltaic cells[J]. ACS Appl. Mater. Interfaces, 2013, 5(24):12820-12831.
[16]Kim H. G, Jo S B, Shim C, et al. Synthesis and photovoltaic properties of benzo[1,2-b:4,5-b’]di-thiophene derivative-based polymers with deep HOMO levels[J]. J. Mater. Chem., 2012, 22(34):17709-17717.
[17]Sun S, Zhang P, Li J, et al. Synthetically controlling the optoelectronic properties of dithieno-[2,3-d:2′,3′-d′]benzo[1,2-b:4,5-b′]dithiophene-alt-diketopyrrolopyrrole-conjugated polymers for efficient solar cells[J]. J. Mater. Chem. A, 2014, 2(317):15316-15325.
[18]袁延华, 同军锋. 基于苯并二噻吩不同侧链共聚物的合成及光伏性能[J]. 广州化工, 2015, 43(9):42133.
[19]Guo X, Watson M D. Conjugated polymers from naphthalene bisimide[J]. Org. Lett., 2008, 10:5333-5336.
[20]Zhang G, Fu Y, Xie Z, et al. Synthesis and photovoltaic properties of new low bandgap isoindigo-based conjugated polymers[J]. Macromolecules, 2011, 44:1414-1420.
[21]Tong J, Guo P, Zhang H, et al. Synthesis of modified benzothiadiazole-thiophene-cored acceptor and carbazole/indolocarbazole alternating conjugated polymers and their photovoltaic applications[J]. Polym. Bull., 2015, 72(3):565-581.
[22]De Leeuw D M, Simenon M M, Brown J A R, et al. Stability of n-type doped conducting polymers and consequences for polymeric microelectronic devices[J]. Synth. Met., 1997, 87:53-59.
[23]Li J, Zhao C, Zhang P, et al. A New anthracene-based small molecule as cathode interlayer for efficient polymer solar cells[J]. Bull. Korean Chem. Soc., 2015, 36:1196-1202.
Synthesis and Characterization of Conjugated Polymer Containing 4,8-bis (triisopropylsilyl)ethynylyl)benzo[1,2-b:4,5-b′dithiophene-alt-isoindigo Unit*
XUXing-hua,WANGJian-long,TONGJun-feng
(Key Laboratory of Optoelectronic Technology and Intelligent Control of Education Ministry,Lanzhou Jiaotong University, Gansu Lanzhou 730070, China)
An isoindigo-based low band gap conjugated polymer, namely poly[(4,8-bis(triiso-propylsilyl)ethynylyl)benzo[1,2-b:4,5-b′]dithiophene-2,6-diyl-alt-N,N′-(2-hexyldecyl)isoindigo-6, 6′-diyl] (PBDT-TIPS-IDC16), was synthesized by the stille coupling reaction. The copolymer showed the broad absorption spectra in a range of 300~760 nm, with an optical band gap of approximately 1.66 eV. Bulk-heterojunction polymer solar cells (PSCs) were fabricated, based on PBDT-TIPS-IDC16 as donor, PC61BM as acceptor (D/A weight ratio 1:2) and Ca/Al as cathode electrode. Under the illumination of AM 1.5G, 100 mW·cm-2, the PSCs showed the best PCE of 0.03%, withVOCof 0.63 V,JSCof 0.14 mA·cm-2,FFof 29.38%. The hole and electron mobilities for PBDT-TIPS-IDC16 measured by the space-charge limited currents (SCLC) were 1.2×10-7and 6.4×10-5cm-2·V-1·s-1, respectively.
isoindigo; low band gap; conjugated polymer; photovoltaic property; space-charge limited current
国家自然科学基金(61264002, 61166002, 61404067)。
徐兴华,男,硕士,研究方向:聚合物太阳能电池材料的设计与合成。
同军锋,男,讲师,研究方向:光电材料与器件。
O631.3
A
1001-9677(2016)07-0055-05

