替诺福韦挽救治疗耐药复发的慢性乙型肝炎患者48周疗效初探
朱冬梅,叶春艳,钱梅云,徐天敏,柳龙根
替诺福韦挽救治疗耐药复发的慢性乙型肝炎患者48周疗效初探
朱冬梅,叶春艳,钱梅云,徐天敏,柳龙根
目的观察替诺福韦(TDF)单药或联合恩替卡韦(ETV)挽救治疗耐药复发的慢性乙型肝炎患者的疗效及安全性。方法回顾性分析11例耐药复发的慢性乙型肝炎患者的挽救治疗,其中6例患者单用TDF,5例患者采用TDF联合ETV。采用时间分辨免疫荧光法检测血清乙型肝炎病毒标志物,采用脱氧核糖核酸测序法检测与耐药相关的HBV P区169、173、180、181、184、202、204、233、236、250位耐药变异,采用PCR-荧光探针法检测血清HBV DNA载量,采用苦味酸法检测血清肌酐(Cr)水平。应用Kaplan-Meier分析血清HBV DNA累积不可检出率。结果挽救治疗前,1例患者检测到ADV基因型耐药,7例患者检测到LAM/ETV基因型耐药,3例患者检测到LAM/ETV/ADA基因型耐药;HBV DNA基线水平为(4.82±1.29)lg IU/ml,挽救治疗第4周降至(3.57±0.55)lg IU/ml,第12周降至(2.91±0.37)lg IU/ml,随访至第48周,仅1例患者可检测出HBV DNA。挽救治疗4、12、24和36周,血清HBV DNA累积不可检出率分别为36.4%(4/11)、63.6%(7/11)、81.8%(9/11)和90.9%(10/11);随访结束时,血清ALT水平由(64.36±34.55)U/L降至(37.7±24.49)U/L;治疗期间未发生肾功能异常或其他不良事件。结论TDF单药或联合ETV挽救治疗耐药复发的慢性乙型肝炎患者仍能较快速地抑制病毒复制,具有良好的疗效和安全性。
慢性乙型肝炎;替诺福韦;病毒耐药;挽救治疗
【Abstract】ObjectiveToevaluatetheefficacyandsafetyoftenofovirdisoproxilfummte(TDF)monotherapy or in combination with entecavir(ETV)for relapsed chronic hepatitis B patients with nucleos(t)ide resistance.MethodsEleven chronic hepatitis B patients with nucleos(t)ide resistance were treated with TDF. Out of them,six patients were treated with TDF monotherapy and five patients were treated with TDF in combination with ETV.The serum HBV DNA,ALT and serum creatinine(Cr)levels were detected at weeks 4,12,24,36 and 48 since the rescue treatment started.Cumulative probability of serum HBV DNA undetectable rate during the treatment period was calculated by using the Kaplan-Meier method.ResultsAll patients at presentation had nucleos(t)ide resistance mutations,including one patient with ADV-related mutations,seven patients with LAM/ETV-resistant mutations,and three patients with LAM/ETV/ADA-resistant mutations;After rescue therapy,serum HBV DNA level decreased from(4.82±1.29)lg IU/mL at onset to(3.57±0.55)lg IU/mL and to(2.91±0.37)lg IU/mL at 4 and 12 weeks,respectively;At 48 weeks of rescue treatment,serum HBV DNA was detectable in only one of 11 patients;Serum HBV DNA became undetectable in 36.4%(4/11),63.6%(7/11),81.8%(9/11)and 90.9%(10/11)of patients at 4,12,24 and 36 weeks of rescue treatment,respectively;Serum ALT levels decreased from(64.36±34.55)U/L at onset to(37.7±24.49)U/L at the end of follow-up;There were no renal dysfunction orotheradverse eventsobserved during treatment.ConclusionTDF monotherapy or in combination with ETV is effective in reducing serum HBV DNA levels and is safe for CHB patients with nucleos(t)ide resistance.
【Key words】Chronic hepatitis B;Nucleos(t)ide resistance;Tenofovir;Rescue therapy
有研究认为,替诺福韦酯(Tenofovir disoproxil fumarate,TDF)对既往一种或多种核苷(酸)类(NAs)抗病毒治疗不应答者仍有较好的疗效[1~7],但应用其治疗耐药复发患者的研究仍较少。我们回顾性分析了我院11例因出现耐药复发而应用TDF或TDF联合恩替卡韦(ETV)挽救治疗的慢性乙型肝炎患者,现将结果报告如下。
1 对象与方法
1.1研究对象回顾性分析2012年10月至2013年3月就诊于我院有完整记录,在应用NAs抗病毒治疗后出现耐药复发的11例慢性乙型肝炎患者,男性10例,女性1例;平均年龄为(43.82±8.05)岁。所有患者诊断均符合《慢性乙型肝炎防治指南》的标准[4]。排除其他肝炎病毒重叠感染、酒精性肝病、药物性肝损伤、自身免疫性肝病。
1.2挽救治疗和随访根据既往NAs用药史、基线耐药检测结果和患者个人意愿,给予以TDF为基础的抗病毒治疗。其中5例患者单用TDF(Viread,Gilead)300 mg口服,1次/d,1例曾行肾移植术患者血清肌酐清除率为50 ml/min,也给予TDF 300 mg/d治疗,另5例给予TDF 300 mg/d联合恩替卡韦(Entecavir,ETV,Baraclude,BMS)0.5 mg口服,1次/d治疗。
1.3检测方法采用时间分辨免疫荧光法检测血清乙型肝炎病毒标志物(广州市达瑞抗体有限公司);采用脱氧核糖核酸测序法检测与耐药相关的HBV P区169、173、180、181、184、202、204、233、236、250位耐药变异(上海艾迪康生物医学检测中心);采用PCR-荧光探针法检测血清HBV DNA载量(上海复星长征医学科学有限公司,检测下限为100 IU/ml);采用IFCC法检测血清谷丙转氨酶(ALT,日本和光纯药工业株式会社,参考值为9~50 U/L);采用苦味酸法检测血清肌酐(Cr)水平(日本和光纯药工业株式会社,参考值为36~144 μmol/L)。
1.4统计学方法应用SPSS 19.0软件进行统计分析。将血清HBV DNA水平进行对数转换,计量资料以()表示,采用t检验,采用Kaplan-Meier法分析HBV DNA累积不可检出率,采用Log-rank检验比较不同组间差异,以P<0.05为差异有统计学意义。
2 结果
2.1研究对象的一般特征本组所有患者均有较好的依从性。挽救治疗前,抗病毒治疗时间为(59.18 ±28.02)月,其中HBeAg阳性者6例,HBeAg阴性者5例;入组血清HBV DNA基线水平为(4.82± 1.29)lg IU/mL,ALT基线水平为(64.36±34.55)U/L。除1例肾移植患者外,10例患者血清肌酐(Cr)基线水平为(82.09±13.73)μmol/L。
2.2既往NAs用药史及耐药基因检测情况在11例CHB患者中,初始应用NAs情况为:3例为拉米夫定(Lamivudine,LAM),5例为阿德福韦酯(Adefovir dipivoxil,ADV),2例为ETV,1例为替比夫定(Telbivudine,LdT)。在挽救治疗前,9例(81.8%)患者单药序贯或联合使用过两种或两种以上NAs药物;4例(31.6%)患者经过2次换药或加药。在入组时,检测到的LAM基因型耐药变异为rtL180M、rtA181T/V/S、rtA184A、rtS202G、rtM204V、rtM204I和rtM250V,ADV基因型耐药变异为rtA181T/V/S、rtA181V和rtN236T,ETV基因型耐药变异为rtL180M、rtA181、rtA184A、rtS202G/C、rtM204V、rtM204I和rtM250V/I。1例患者检测到ADV基因型耐药,7例患者检测到LAM/ETV基因型耐药,3例患者检测到LAM/ETV/ADV基因型耐药。11例患者NAs用药史及基因型耐药情况见表1。
2.3挽救治疗后病毒学应答情况随挽救治疗时间的延长,11例患者血清HBV DNA水平逐步下降。HBV DNA基线水平为(4.82±1.29)lg IU/mL,第4 w时,降至(3.57±0.55)lg IU/mL,第12 w降至(2.91±0.37)lg IU/mL,随访至第48 w,仅9号患者可检测出血清HBV DNA,但较基线水平下降了2.32 lg IU/mL。挽救治疗4、12、24和36 w,分别有4、3、2、1例患者血清HBV DNA低于检测线,累积不可检出率分别为36.4%、63.6%、81.8%和90.9%。随访结束时,1例患者发生HBeAg血清学转换。对挽救治疗单用TDF的6例患者和TDF联合ETV的5例患者进一步行Log-rank检验,发现两组间HBV DNA不可检出率差异无统计学意义(P= 0.24)。有研究认为,ADV相关耐药变异(rtA181T/V、rtN236T)可降低TDF的敏感性。我们的研究中4例患者存在rt181T/V和/或rtN236T变异(表1),与无该变异的7例患者比较,血清HBV DNA不可检出率差异无统计学意义(P=0.86)。
2.4生化学应答情况挽救治疗时,11例患者血清ALT基线水平为(64.36±34.55)U/L,其中9例患者ALT水平高于正常值上限。在治疗过程中,血清ALT水平逐渐下降,至48 w时降至(37.7±24.49)U/L,但仍有2例患者高于正常值上限(分别为74 U/L和89 U/L)。11例CHB患者血清ALT变化情况见图1。2.5抗病毒治疗的安全性在治疗期间,11号肾移植患者血清Cr基线水平为184μmol/L,肌酐清除率为50 ml/min。第48 w时血清Cr水平降至148.2μmol/L,肌酐清除率升至63 ml/min。其余10例患者血清Cr变化情况见图2。未发生因肾功能异常或其他明显不适而停药事件。

表1 11例CHB患者NAs用药史和基因型耐药变异情况

图1 11例CHB患者血清ALT水平变化
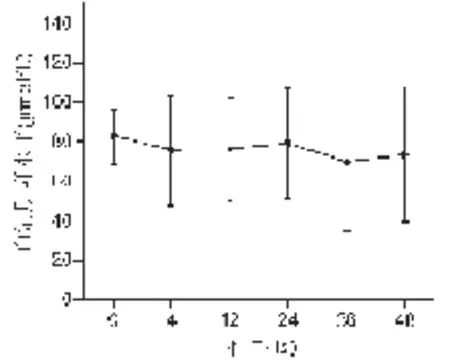
图2 10例患者血清Cr水平变化情况
3 讨论
挽救治疗是根据病毒对不同NAs耐药特点加用或换用无交叉耐药的NAs治疗[8~11]。本组11例患者中9例有挽救治疗史。挽救治疗虽可抑制耐药病毒株的复制,但也增加了多药耐药的风险[12,13]。11例患者均检测到耐药相关变异位点,其中1例为ADV耐药,7例为LAM/ETV耐药,3例为LAM/ETV/ADV耐药。此次挽救治疗后,11例患者HBV DNA水平快速下降,第48周累积不可检出率为90.9%,稍高于Kim et al[6]的研究结果,但低于杨丹红等[14]的研究结果。前者分析了韩国29例两种及以上NAs治疗失败的患者,使用以TDF为基础的挽救治疗,随访至12月时HBV DNA累积不可检出率为86.2%;后者观察了我国31例服用TDF挽救治疗的患者,至第12月时,HBV DNA累积不可检出率为96.77%。我们随访至第48周时,仅1例患者可检测到HBV DNA,但较基线水平下降了2.32 lg IU/ mL,该患者耐药变异位点为rtM204V+rtM250V,说明该耐药变异对TDF仍敏感[9]。
最近有研究认为,TDF单药与TDF联合ETV治疗ETV部分应答或者ETV耐药者病毒学应答率的差异无统计学意义[7,15]。黄明星等[8]研究发现TDF单药与TDF联合其他NAs挽救治疗,HBV DNA不可检出率差异无统计学意义。我们的研究也有类似的发现。但又有研究发现TDF单药治疗LAM/ADV耐药者的病毒学应答率显著低于仅有LAM或ADV耐药者[9]。因此,TDF单药与TDF联合ETV治疗多药耐药者病毒学应答是否有差异,尚需进一步研究。
TDF是一种无环核苷酸类似物,在分子结构上与ADV相似,两者存在一定程度的交叉耐药,携带ADV耐药株的患者对TDF的敏感性下降[12]。ADV相关耐药变异最常见的是rtA181T/V和rtN236T。体外研究显示,携带rtA181T/V和携带rtN236T的变异株对TDF的敏感性分别下降3.2和4倍[16]。有研究观察了113例TDF单药治疗的CHB患者,发现ADV耐药组HBV DNA阴转率(HBV DNA<400拷贝/毫升)为52%,明显低于非ADV耐药组的100%,认为ADV耐药者对TDF的敏感性下降[10]。然而,另一项研究分析了60例(其中21例ADV耐药)使用TDF挽救治疗的患者,认为病毒学应答不受ADV耐药的影响[11]。我们的研究中,4例ADV耐药者HBV DNA均降至检测线以下,与非ADV耐药者相比,HBV DNA阴转率差异无统计学意义。
TDF主要通过肾小球滤过和肾小管主动分泌排泄,可使近端肾小管损伤坏死,引起肾脏疾病[17]。有学者分析已发表的相关文献,发现TDF可增加HIV感染患者发生肾脏疾病的风险,但在CHB患者中并无相关发现[18]。本研究中,所有患者随访期间血清Cr维持于稳定水平,未发生TDF相关肾病及其他不良事件,与韩国两项研究结果类似[5,7],故TDF具有良好的耐受性和安全性。值得注意的是,一例肾移植患者初治服用LAM序贯ETV,耐药后单用TDF,HBV DNA快速下降,至12周时低于检测下限,血清Cr波动于184~148.2 μmol/L,与Shan et al的病例报道类似。另一项研究也认为,TDF可能是治疗伴LAM耐药肾移植患者的安全有效药物。因此,TDF可能有较好的疗效和安全性,对于肾移植患者亦如此。
[1]参加慢性乙型肝炎长期治疗讨论会专家.核苷和核苷酸类药物治疗慢性乙型肝炎的长期性.实用肝脏病杂志,2015,18(1):1-7.
[2]Deng L,Tang H.Hepatitis B virus drug resistance to current nucleos(t)ide analogs:Mechanisms and mutation sites.Hepatol Res,2011,41(11):1017-1024.
[3]常静霞,汪茂荣.乙型肝炎病毒基因耐药变异研究进展.实用肝脏病杂志,2013,16(5):467-470.
[4]中华医学会肝病学分会和感染病学分会.慢性乙型肝炎防治指南(2010年版).实用肝脏病杂志,2011,14(2):81-89.
[5]Lee CI,Kwon SY,Kim JH,et al.Efficacy and safety of tenofovir-based rescue therapy for chronic hepatitis B patients with previous nucleo(s/t)ide treatment failure.Gut Liver,2014,8(1): 64-69.
[6]Kim YJ,Sinn DH,Gwak GY,et al.Tenofovir rescue therapy for chronic hepatitis B patients after multiple treatment failures.World J Gastroenterol,2012,18(47):6996-7002.
[7]Lim YS,Byun KS,Yoo BC,et al.Tenofovir monotherapy versus tenofovir and entecavir combinationtherapy inpatients with entecavir-resistant chronic hepatitis B with multiple drug failure: results of a randomised trial.Gut,2015,Epub ahead of print.
[8]黄明星,李新华,吴元凯,等.替诺福韦单独与联合其他核苷类似物治疗慢性乙型肝炎患者72周疗效比较.中山大学学报,2014,35(4):250-254.
[9]Liu Y,Zhang Y,Yuan J,et al.Efficacy of tenofovir disoproxil fumarate therapy in Chinese chronic hepatitis B patients after multiple antiviral failures.Hepatol Res,2014,Epub ahead of print.
[10]van Bmmel F,de Man RA,Wedemeyer H,et al.Long-term efficacy of tenofovir monotherapy for hepatitis B virus-monoinfected patientsafterfailureofnucleoside/nucleotideanalogues. Hepatology,2010,51(1):73-80.
[11]Patterson SJ,George J,Strasser SI,et al.Tenofovir disoproxil fumarate rescue therapy following failure of both lamivudine and adefovirdipivoxilinchronichepatitisB.Gut,2011,60(2): 247-254.
[12]庄辉,翁心华.核苷和核苷酸类药物治疗慢性乙型肝炎的耐药及其管理.中华肝脏病杂志,2013,21(1):15-22.
[13]Duarte-Rojo A,Heathcote EJ.Efficacy and safety of tenofovir disoproxil fumarate in patients with chronic hepatitis B.Therap Adv Gastroenterol,2010,3(2):107-119.
[14]杨丹红,赵年丰,潘红英,等.替诺福韦酯挽救治疗核苷(酸)类药物多重耐药慢性乙型肝炎.中华肝脏病杂志,2015,23(1):75-76.
[15]Yip B,Chaung K,Wong CR,et al.Tenofovir monotherapy and tenofovirplusentecavircombinationasrescuetherapyfor entecavirpartialresponders.DigDisSci,2012,57(11): 3011-3016.
[16]Qi X,Xiong S,Yang H,et al.In vitro susceptibility of adefovir-associated hepatitis B virus polymerase mutations to other antiviral agents.Antivir Ther,2007,12(3):355-362.
[17]JafariA,KhaliliH,Dashti-KhavidakiS.Tenofovir-induced nephrotoxicity:incidence,mechanism,riskfactors,prognosisand proposed agents for prevention.Eur J Clin Pharmacol,2014,70(9):1029-1040.
[18]Hall AM.Update on tenofovir toxicity in the kidney.Pediatr Nephrol,2013,28(7):1011-1123.
(收稿:2015-06-29)
(本文编辑:陈从新)
Efficacy of 48-week tenofovir rescue therapy for relapsed chronic hepatitis B patients with nucleos(t)ide
ZhuDongmei,YeChunyan,QianMeiyun,etal.DepartmentofLiverDiseases,Third
People's Hospital,Changzhou 213001,JiangsuProvince,China
10.3969/j.issn.1672-5069.2016.01.010resistance
213000江苏省常州市第三人民医院肝病科(朱冬梅,叶春艳,钱梅云,柳龙根);感染病科(徐天敏)第一作者:朱冬梅,女,33岁,硕士研究生,住院医师。E-mail:zhudongmeido@126.com
柳龙根,E-mail:331608712@qq.com

